一种靶向APJ的抗体及其制备方法和应用与流程
一种靶向apj的抗体及其制备方法和应用
技术领域
1.本发明属于生物技术领域,具体涉及一种靶向apj的抗体及其制备方法和应用。
背景技术:
2.apj是一个g蛋白偶联受体,在内皮细胞、肌细胞、海马体、结肠、胰腺、骨组织均有表达,通过与其配体apelin-13结合,启动gi/o信号通路,从而在心血管系统发挥作用;另外,在癌症组织中,发现apj及其配体apelin表达上调,比如胃癌及胃癌细胞、胶质母细胞瘤、肺小细胞肺癌等,apj-apelin信号通路可能会诱导瘤内淋巴管生成和促进肿瘤的淋巴转移,有动物实验表明,apelin会促进小鼠胆管癌血管生成和癌细胞增殖,在静脉注射apj小分子抑制剂后,会抑制肿瘤生长。与小分子药物相比,抗体类的大分子药物具有特异性好、安全性高、代谢慢等诸多优势,因此开发可用于治疗癌症的apj抗体药物有显著的优势。
3.杂交瘤技术是制备高亲和力抗体的经典方法,目前上市的抗体药物大部分是通过杂交瘤技术获得的。该技术涉及到多个环节,包括制备免疫原、动物免疫、浆b细胞的融合、杂交瘤上清的筛选等,每个环节对于获得高质量的抗体都较为重要,特别是动物免疫部分。目前适合作为抗体药物的靶点众多,但是并非都可以获得具有治疗活性的抗体,比如离子通道、gpcr等多次跨膜蛋白,由于这些靶点暴露在胞外的区域有限、难以获得高纯度的蛋白、有些功能性表位的氨基酸序列人和免疫动物的同源性较高等原因,导致针对这些靶点的抗体发现很有挑战性。
4.apj是一个具有377个氨基酸、7次跨膜域的g蛋白偶联受体,人和小鼠的氨基酸序列同源性较高,作为多次跨膜蛋白,暴露在胞外区的氨基酸序列较短,无法制备纯度和产量较高的重组蛋白,蛋白可在哺乳动物表达并且定位于脂膜,但是表达量有限,因此很难在小鼠体内引起较强的免疫反应,从而获得高亲和力和具备生物学活性的抗体,且难以有效抑制apelin通路活性。cn110655577a公开了一种apj单克隆抗体,并将其与elabala融合施用。而现有技术中仍然缺乏对于apj抗原结合活性更高,并能够抑制apelin通路的高效抗体。
5.因此急需一种能够用于抑制apj/apelin信号通路,且对apj抗原结合活性更高的靶向apj抗体。
技术实现要素:
6.本发明所要解决的技术问题是为克服现有技术中缺乏高效且能抑制apelin通路的apj抗体的缺陷,提供一种靶向apj的抗体及其制备方法和应用。
7.为解决上述问题,本发明提供的技术方案之一为:一种靶向apj的抗体或其抗原结合片段,其包含重链可变区(vh)和轻链可变区(vl),所述重链可变区包含重链互补决定区hcdr1、hcdr2和hcdr3,所述轻链可变区包含轻链互补决定区lcdr1、lcdr2和lcdr3;
8.其中,所述hcdr1含有如seq id no:2或seq id no:10所示的序列或其变体1,所述hcdr2含有如seq id no:3或seq id no:11所示的序列或其变体2,所述hcdr3含有如seq id no:4或seq id no:12所示的序列;所述lcdr1含有如seq id no:6或seq id no:14所示的序
列或其变体3,所述lcdr2含有如seq id no:7或seq id no:15所示的序列或其变体4,所述lcdr3含有如seq id no:8或seq id no:16所示的序列或其变体5。
9.本发明所述变体1较佳地为对seq id no:10所示序列的第1或4位进行替换后获得;其中,第1位优选替换为a,第4位优选替换为f;更佳地,所述变体1的序列如seq id no:20所示。
10.本发明所述变体2较佳地为对seq id no:11所示序列的第9位氨基酸替换后获得,优选替换为a;更佳地,其序列如seq id no:24所示。
11.本发明所述变体3较佳地为对seq id no:14所示序列的第7位氨基酸替换后获得,优选替换为k;更佳地,其序列如seq id no:26所示。
12.本发明所述变体4较佳地为对seq id no:15所示序列的第1位氨基酸替换后获得,优选替换为a;更佳地,其序列如seq id no:27所示。
13.本发明所述变体5较佳地为对seq id no:16所示序列的第5位氨基酸替换后获得,优选替换为g;更佳地,其序列如seq id no:22所示。
14.在一较佳实施方案中,本发明所述hcdr1的氨基酸序列如seq id no:2所示,所述hcdr2的氨基酸序列如seq id no:3所示,所述hcdr3的氨基酸序列如seq id no:4所示,所述lcdr1的氨基酸序列如seq id no:6所示,所述hcdr2的氨基酸序列如seq id no:7所示,且所述hcdr3的氨基酸序列如seq id no:8所示。
15.在另一较佳实施方案中,本发明所述hcdr1的氨基酸序列如seq id no:10所示,所述hcdr2的氨基酸序列如seq id no:11所示,所述hcdr3的氨基酸序列如seq id no:12所示,所述lcdr1的氨基酸序列如seq id no:14所示,所述hcdr2的氨基酸序列如seq id no:15所示,且所述hcdr3的氨基酸序列如seq id no:16所示。
16.在另一较佳实施方案中,本发明所述hcdr1的氨基酸序列如seq id no:20所示,所述hcdr2的氨基酸序列如seq id no:11所示,所述hcdr3的氨基酸序列如seq id no:12所示,所述lcdr1的氨基酸序列如seq id no:14所示,所述hcdr2的氨基酸序列如seq id no:15所示,且所述hcdr3的氨基酸序列如seq id no:22所示。
17.在另一较佳实施方案中,本发明所述hcdr1的氨基酸序列如seq id no:10所示,所述hcdr2的氨基酸序列如seq id no:24所示,所述hcdr3的氨基酸序列如seq id no:12所示,所述lcdr1的氨基酸序列如seq id no:26所示,所述hcdr2的氨基酸序列如seq id no:27所示,且所述hcdr3的氨基酸序列如seq id no:16所示。
18.本发明中,所述重链可变区较佳地还包括重链框架区;所述重链框架区优选为鼠源框架区或者人源框架区;
19.更佳地,所述重链可变区序列包含如seq id no:1或9所示的氨基酸序列,或与其具有95%以上同源性的序列;
20.所述具有95%以上同源性的序列优选为如seq id no:17、19或23所示的序列。
21.本发明中,所述轻链可变区较佳地还包括轻链框架区;所述轻链框架区优选为鼠源框架区或者人源框架区;
22.更佳地,所述的轻链可变区包含如seq id no:5或13所示的氨基酸序列,或与其具有95%以上同源性的序列;
23.所述具有95%以上同源性的序列优选为如seq id no:18、21或25所示的序列。
24.本发明所述的抗体或其抗原结合片段,可以为包括igg、fab、fab’、f(ab’)2、fv,例如scfv或者其他任何保留抗体特异性结合抗原的部分能力的抗体形式。
25.本发明所述的抗体或其抗原结合片段,较佳地还包括鼠抗体的重链恒定区或人抗体的重链恒定区,所述鼠抗体的重链恒定区包括鼠igg1、igg2a、igg2b3或igg3的重链恒定区,所述人抗体的重链恒定区包括人igg1、igg2、igg3或igg4的重链恒定区。
26.本发明所提供的技术方案之二为:一种分离的核酸,其编码上述的抗体或其抗原结合片段。
27.所述核酸较佳地包含选自seq id no:28~32之一所示的序列,和选自seq id no:33~37之一所示的序列。
28.在本发明一较佳实施方案中,所述核酸包含如seq id no:28和seq id no:33所示的序列、如seq id no:29和seq id no:34所示的序列、如seq id no:30和seq id no:35所示的序列、如seq id no:31和seq id no:36所示的序列,或如seq id no:32和seq id no:37所示的序列。
29.本发明所提供的技术方案之三为:一种重组表达载体,其包含上述分离的核酸。
30.本发明所述重组表达载体较佳地包含真核细胞表达载体或原核细胞表达载体。
31.本发明所提供的技术方案之四为:一种转化体,其包含上述分离的核酸或上述的重组表达载体。
32.本发明所述转化体的宿主细胞较佳地为原核细胞或真核细胞;所述原核细胞优选e.coli细胞,所述真核细胞优选hek293细胞或cho细胞。
33.本发明所提供的技术方案之五为:一种靶向apj的抗体或其抗原结合片段的制备方法,其包含培养上述的转化体,从培养物中获得靶向apj的抗体或其抗原结合片段的步骤。
34.本发明所提供的技术方案之六为:一种嵌合抗原受体,所述嵌合抗原受体包含上述靶向apj的单克隆抗体或其抗原结合片段。
35.本发明所提供的技术方案之七为:一种抗体药物偶联物,其包含细胞毒性剂,以及上述的靶向apj的抗体或其抗原结合片段。
36.本发明所提供的技术方案之八为:一种药物组合物,其包含上述的靶向apj的单克隆抗体或其抗原结合片段,以及药学上可接受的载体;
37.所述药物组合物较佳地还包括其他抗肿瘤抗体作为活性成分。
38.本发明所提供的技术方案之九为:一种给药装置,其包括上述的靶向apj的抗体或其抗原结合片段、上述嵌合抗原受体、上述抗体药物偶联物和/或上述药物组合物;
39.所述给药装置较佳地还包括将上述靶向apj的抗体或其抗原结合片段、上述嵌合抗原受体、上述抗体药物偶联物和/或上述药物组合物施用于受试者的部件,例如注射器或输液装置。
40.本发明所提供的技术方案之十为:一种上述靶向apj的抗体或其抗原结合片段、上述嵌合抗原受体、上述抗体药物偶联物和/或上述药物组合物在制备诊断、预防和/或治疗apj过表达相关的疾病的药物中的应用。
41.本发明所提供的技术方案之十一为:一种治疗apj过表达相关的疾病的方法,所述方法包括将上述的靶向apj的单克隆抗体或其抗原结合片段、上述嵌合抗原受体、上述抗体
药物偶联物和/或上述药物组合物向有需要患者施用的过程。
42.本发明中,所述apj过表达相关的疾病或病症较佳地为apj/apelin介导的疾病;所述apj/apelin介导的疾病优选为为癌症;所述癌症进一步优选为胃癌、胶质母细胞瘤或者肺小细胞肺癌。
43.本发明的抗体编号采用kabat定义的编号。
44.在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
45.本发明所用试剂和原料均市售可得。
46.本发明的积极进步效果在于:本发明所提供的靶向apj抗体或其抗原结合片段具有高亲和力及高结合特异性;并且能够有效抑制apj-apelin信号通路,从而对于apj/apelin介导的疾病具有较高的治疗价值;此外,其除人apj抗原外,还能够与猴apj抗原有效结合,从而使得临床前安评研究中可以选择灵长类动物猕猴(cynomolgus,cyno)的疾病模型进行药理毒理实验,为临床前药理、毒理等研究带来极大的便利。
附图说明
47.图1为小鼠血清中免疫原的抗体效价和特异性。
48.图2为测试抗体与含人apj抗原细胞的结合活性。
49.图3为测试抗体与含猴apj抗原细胞的结合活性。
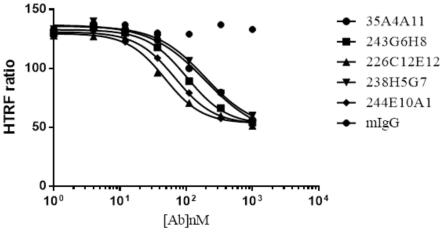
50.图4为测试抗体对camp生成影响的活性。
具体实施方式
51.下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
52.实施例1.apj抗体的制备
53.(一)免疫原的制备
54.apj是一个多次跨膜受体,本发明构建了重组表达apj的293细胞株,具体序列见表1。
55.表1免疫原序列
[0056][0057]
选择表达量最高的克隆,通过反复冻融的方式制备细胞裂解液,用以和小鼠树突状细胞(dc细胞)进行孵育,使树突状细胞能够摄取、加工并且提成抗原。
[0058]
(二)小鼠树突状细胞的制备、抗原摄取及成熟
[0059]
实验选择6~8周龄sjl小鼠(购于上海斯莱克公司),取大腿股骨和肱骨骨,提取骨髓细胞,反复吹打细胞团块,用70um的筛网过滤细胞悬液,在1500rpm的转速下离心5分钟,弃掉上清保留细胞沉淀,加入1ml红细胞裂解液,于4度静止5分钟,加入完全培养液终止裂解,300g离心5分钟,用dc分化培养液(含20ng/mll gm-csf)重悬细胞,将细胞密度调整到1e4个细胞每毫升,接种到10cm(10毫升每皿)或者15cm(25毫升每皿)的非组织培养皿中,然后置于二氧化碳培养箱培养13天使细胞进行分化和增殖,期间通过梯度换液来更新树突状细胞分化培养液(含20ng/mll gm-csf),第14和15天用含20ng/mll gm-csf和5ng/ml小鼠il4的分化培养液培养细胞,第16天,将抗原细胞裂解液和dc细胞(按照dc:抗原细胞为1:3的比例)混合孵育24小时,第17天,在前述分化培养液中添加1ug/ml lps和0.5ug/ml cpg诱导dc细胞成熟,过夜培养,第18天收集dc细胞计数,按照1e5个细胞每只小鼠的剂量进行免疫。
[0060]
(三)动物免疫
[0061]
免疫采用6~8周龄抗体sjl小鼠,小鼠在spf条件下饲养。初次免疫时,腹腔注射成熟的树突状细胞,每只小鼠注射10万个细胞。加强免疫时,腹腔注射表达apj的293细胞(293-apj细胞,可购自铂金埃尔默、金斯瑞等公司;也可自行构建:从uniprot获得apj基因编码序列,合成基因,将apj基因插入慢病毒表达载体,然后感染293母细胞,通过抗生素筛选获得稳定表达ajp的细胞株),每只小鼠注射50万个细胞。初次免疫与第一次加强免疫之间间隔2周,以后每次加强免疫之间间隔3周。每次加强免疫1周后采血,用facs检测(检测步骤同实施例3a)第二次加强免疫后第七天的小鼠血清中免疫原的抗体效价和特异性,结果如图1和表2所示。表2说明,经细胞免疫后的小鼠血清对免疫原均有不同程度的结合,呈现抗原抗体反应,其中最高稀释度在一千左右。其中空白对照为1%(w/w)bsa,其中批次指第二次加强免疫后第七天的小鼠血清,表中的数据为mfi值
[0062]
表2流式细胞术检测293-apj细胞免疫后小鼠血清抗体效价(mfi值)
[0063][0064]
(三)杂交瘤细胞的制备和抗体筛选
[0065]
免疫步骤完成后,将所选择的每只小鼠最后一次免疫腹腔注射50万293-apj细胞,3天后处死小鼠,收集脾细胞。加入nh4oh至终浓度1%(w/w),裂解脾细胞中参杂的红细胞,获得脾细胞悬液。用dmem基础培养基1000转每分钟离心清洗细胞3次,然后按活细胞数目5:1比率与小鼠骨髓瘤细胞sp2/0(购自atcc)混合,采用高效电融合方法(参见methods in enzymology,vol.220)进行细胞融合。融合后的细胞稀释到含20%胎牛血清、1
×
hat的dmem培养基中,所述百分比为质量百分比。然后按1
×
105/200微升每孔加入到96孔细胞培养板中,放入5%co2、37℃培养箱中,所述百分比为体积百分比。融合后的细胞稀释到含20%胎牛血清、1
×
hat的dmem培养基中,所述百分比为质量百分比。然后按1
×
105/200微升每孔加入到96孔细胞培养板中,放入5%co2、37℃培养箱中,所述百分比为体积百分比。10天后用acumen筛选细胞融合板上清,检测办同时接种了chok1空细胞和chok1-apj细胞,将acumen结果中阳性细胞对阴性细胞平均荧光强度比值大于3的阳性克隆扩增到24孔板,在含10%(w/w)ht胎牛血清,dmem(invitrogen)在37℃,5%(v/v)co2条件下扩大培养。培养3天后取24孔板中扩大培养的培养液进行离心,收集上清液,用流式细胞术确定对抗原的结合活性(结合活性的检测方法请分别参见实施例3a和实施例3b)。
[0066]
根据24孔板筛选结果,挑选facs实验中mfi比值》10的杂交瘤细胞为符合条件的阳性克隆,选择符合条件的杂交瘤细胞用有限稀释法在96孔板进行亚克隆,在含10%(w/w)fbs的dmem培养基中(购自invitrogen)37℃,5%(v/v)co2条件下培养。亚克隆后10天用acumen进行初步筛选,挑选单个阳性单克隆扩增到24孔板继续培养。3天后用facs确定抗原结合阳性,并用htrf camp实验评估生物活性(评估标准为htrf实验中htrf比值》2)。
[0067]
根据24孔板样品检测结果,挑选出最优的克隆,并于含10%(w/w)fbs的dmem培养基中(购自invitrogen)在37℃,5%(v/v)co2条件下将该最优的克隆进行扩大培养,液氮冻存即得本发明杂交瘤细胞,并可用于后续的抗体生产和纯化。
[0068]
实施例2.先导抗体的生产和纯化
[0069]
杂交瘤细胞产生的抗体浓度较低,大约仅1-10μg/毫升,浓度变化较大。且培养基中细胞培养所产生的多种蛋白和培养基所含胎牛血清成分对很多生物活性分析方法都有不同程度的干扰,因此需要进行小规模(1-5毫克)抗体生产纯化。
[0070]
将实施例1所得的杂交瘤细胞接种到t-75细胞培养瓶并用生产培养基(hybridoma serum free medium,购自invitrogen公司)驯化传代3代。待其生长状态良好,接种细胞培养转瓶。每个2升的培养转瓶中加入500毫升生产培养基,接种细胞密度为1.0
×
105/毫升。盖紧瓶盖,将转瓶置于37℃培养箱中的转瓶机上,转速3转/分钟。连续旋转培养14天后,收集细胞培养液,过滤去除细胞,并用0.45微米的滤膜过滤至培养上清液澄清。澄清的培养上清液可马上进行纯化或-30℃冻存。
[0071]
澄清的杂交瘤细胞的培养上清液(300ml)中的单克隆抗体用2ml蛋白a柱(购自ge healthcare)纯化。蛋白a柱先用平衡缓冲液(pbs磷酸缓冲液,ph7.2)平衡,然后将澄清的培养上清液上样到蛋白a柱,控制流速在3ml/分钟。上样完毕后用平衡缓冲液清洗蛋白a柱,平衡缓冲液的体积为4倍蛋白a柱柱床体积。用洗脱液(0.1m甘氨盐酸缓冲液,ph2.5)洗脱结合在蛋白a柱上的apj抗体,用紫外检测器监测洗脱情况(a280紫外吸收峰)。收集洗脱的抗体,加入10%1.0m tris-hcl缓冲液中和ph,所述百分比为体积百分比,然后立即用pbs磷酸缓冲液透析过夜,第二天换液1次并继续透析3小时。收集透析后的apj抗体,用0.22微米的滤器进行无菌过滤,无菌保存,即得纯化的apj抗体。
[0072]
将纯化的apj抗体进行蛋白浓度(a280/1.4)、纯度等检测分析。
[0073]
实施例3.先导抗体的检测
[0074]
a、流式细胞术实验(facs)检测抗原抗体结合
[0075]
对实施例2所得的纯化的apj抗体进行与过表达人和猴apj的细胞进行结合反应,以表征其与抗原的亲和性以结合特异性。
[0076]
(1)亲和性测定
[0077]
将293-apj细胞用tryple消化为单个细胞,300g离心,用封闭液[pbs+2%fbs]重悬细胞沉淀,配制为30万个细胞每毫升的细胞密度,然后以100μl每孔加到96孔facs检测板,室温封闭30分钟。离心弃掉封闭液,加入实施例2所得的纯化的apj抗体100μl每孔。室温孵育1小时后,用洗液[pbs]洗细胞3次,每次250μl每孔。加入alexa488标记的二抗(购自thermofisher),室温孵育1小时后,用洗液[pbs]洗细胞3次,每次250μl每孔。用can ii流式细胞检测仪读取alexa488的平均荧光强度mfi数值,与人apj细胞的结合活性如图2、表3和表4,与猴apj细胞的结合活性如图3和表5所示,其中igg对照为小鼠igg,表中的数据为mfi值。
[0078]
本发明所得抗体与含人和猴apj抗原的细胞分别具有良好的亲和性。
[0079]
表3 facs检测apj抗体与人apj抗原的结合
[0080][0081]
表4 apj抗体与含人apj的细胞的结合活性
[0082][0083][0084]
表5 facs检测apj抗体与含猴apj的细胞的结合
[0085][0086]
(2)特异性测定
[0087]
通过与(1)相同的步骤检测所得抗体与不含apj抗原的293空细胞(可常规购买)的结合,以表征其特异性,结果如表6所示:该抗体与不含apj抗原的细胞不结合,具有良好的抗原结合特异性。
[0088]
表6 facs检测apj抗体与hek293空细胞的结合
[0089]
[0090][0091]
b、htrf检测抗体对配体apelin13介导的camp生成的抑制
[0092]
对实施例2所得的纯化的apj抗体进行受体活性抑制实验检测。
[0093]
将chok1-apj细胞用tryple消化为单个细胞,400g离心,用含0.5mm ibmx的基本培养液配制成密度为2
×
106个细胞每毫升的细胞悬液,按照2μl每孔的体积将细胞接种到384-孔板,配制最高浓度为2500nm的抗体梯度稀释液,将抗体溶液以4μl/孔的体积加到孔板与细胞孵育1个小时,期间用含1%bsa的f12k溶液配制10nm的apelin-13溶液,取2μl加到微孔板,与细胞孵育30分钟,配制10um的forskolin溶液,取2μl加到微孔板与细胞孵育30分钟以刺激camp生成,先后加入camp-cryptate和camp-d2检测试剂,室温孵育1小时,用thermo varioskan lux检测htrf信号,抗体对camp生成影响的活性如图4和表7,其中igg对照为小鼠igg,表中的数据为htrf比率值。
[0094]
对实施例2所得的纯化的apj抗体进行camp生成影响活性的检测(见表7及表8)。
[0095]
表7.htrf方法检测抗体对apeline介导的apj细胞camp生成的影响
[0096][0097][0098]
表8.apj抗体对apeline介导的apj细胞camp生成的抑制活性
[0099]
抗体克隆号top htrf ratioec50,nm35a4a11136.9195243g6h8132.9102.1226c12e12129.647.76
238h5g7135.9194.4244e10a1130.968.16
[0100]
说明本发明的抗体能够有效抑制抑制apj-apelin信号通路。
[0101]
实施例4.抗体氨基酸序列测定
[0102]
总rna分离:将实施例1亚克隆培养所得的上清液检验过抗原结合后(即经过实施例2~3的检定和活性测定后),通过离心搜集5
×
107个杂交瘤细胞,加入1ml trizol混匀并转移到1.5ml离心管中,室温静置5分钟;加0.2ml氯仿,振荡15秒,静置2分钟后于4℃,12000g离心5分钟,取上清转移到新的1.5ml离心管中;加入0.5ml异丙醇,将管中液体轻轻混匀,室温静置10分钟后于4℃,12000g离心15分钟,弃上清;加入1ml 75%乙醇(所述百分比为体积百分比),轻轻洗涤沉淀,4℃,12000g离心5分钟后弃上清,将沉淀物晾干,加入depc处理过的h2o溶解(55℃水浴促进溶剂10分钟),即得总rna。
[0103]
逆转录与pcr:取1μg总rna,配制20μl体系,加入逆转录酶后于42℃反应60分钟,于7℃反应10分钟终止反应。配制50μlpcr体系,包括1μlcdna、每种引物25pmol、1μl dna聚合酶以及相配的缓冲体系、250μmol dntps;设置pcr程序,预变性95℃3分钟,变性95℃30秒,退火55℃30秒,延伸72℃35秒,35个循环后再额外于72℃延伸5分钟,得pcr产物。其中逆转录所用的试剂盒为primescript rt master mix,购自takara,货号rr036;pcr所用的试剂盒包括q5超保真酶,购自neb,货号m0492。
[0104]
克隆与测序:取5μl pcr产物进行琼脂糖凝胶电泳检测,将检测阳性样品使用柱回收试剂盒纯化,其中回收试剂盒为gel&pcr clean-up,购自macherey-nagel,货号740609。进行连接反应:样品50ng,t载体50ng,连接酶0.5μl,缓冲液1μl,反应体系10μl,于16℃反应半小时得连接产物,其中连接的试剂盒为t4 dna连接酶,购自neb,货号m0402;取5μl连接产物加入100μl的感受态细胞(ecos 101competent cells,购自yeastern,货号fye607)中,冰浴5分钟,而后于42℃水浴热激1分钟,放回冰上1分钟后加入650μl无抗生素soc培养基,于37℃摇床上以200rpm的速度复苏30分钟,取出200μl涂布于含抗生素的lb固体培养基上于37℃孵箱过夜培养;次日,使用t载体上引物m13f和m13r配制30μlpcr体系,进行菌落pcr,用移液器枪头蘸取菌落于pcr反应体系中吹吸,并吸出0.5μl点于另一块含100nm氨苄青霉素的lb固体培养皿上以保存菌株;pcr反应结束后,取出5μl进行琼脂糖凝胶电泳检测,将阳性样品进行测序和分析[参见kabat,“sequences of proteins of immunological interest,”national institutes of health,bethesda,md.(1991)]。测序结果如表9和表100所示。
[0105]
表9 apj抗体氨基酸序列编号
[0106]
[0107][0108]
其中,表9中的数字即为序列表中序列号,如35a4a11的重链蛋白可变区的氨基酸序列为seq id no:1,35a4a11的重链蛋白可变区中cdr1的氨基酸序列为seq id no:2。
[0109]
表10 apj抗体核苷酸(dna)序列编号
[0110]
克隆号重链可变区轻链可变区35a4a112833243g6h82934226c12e123035238h5g73136244e10a13237
[0111]
应理解,在阅读了本发明的上述内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1