一种猪用抗病型益生芽孢杆菌及其应用
本发明属于微生物领域,具体涉及一种猪用抗病型益生芽孢杆菌及其应用。
背景技术:
枯草芽孢杆菌是一类公认安全(gras)的可食用微生物,它早已被我国农业农村部确认为可以直接在动物饲料中添加的饲用微生物品种。枯草芽孢杆菌功能极其多样性,能生产包括多种消化酶类、维生素、寡糖,以及抗菌物质,如抗生素、抗菌肽、脂肽等。目前有关枯草芽孢杆菌在畜牧生产中的开发利用已经非常普遍,但纵观国内外,已经开发利用的芽孢杆菌菌株通常功能均比较单一,有生产消化酶的,有肠道定居后起到占位保健的,也有只在体外用于生产多种功能性畜禽饲料的。这些菌株大多来源于自然环境中,通常具有较强的耗氧量,饲喂进入到动物体消化道后,难以在动物消化道内定居,发挥长期稳定功效。
技术实现要素:
本发明的目的是解决现有技术的不足,提供一种猪用抗病型益生芽孢杆菌及其应用,具体采用以下的技术方案:
一种猪用抗病型益生芽孢杆菌,所述益生芽孢杆菌保藏于中国典型培养物保藏中心,保藏编号为cctccm2021657。
优选的,所述益生芽孢杆菌的制备方法为:以pca作为筛选培养基,以致病性大肠杆菌作为指示菌,在37℃下进行点种法筛选,从猪的十二指肠、空肠、回肠、盲肠、结肠和直肠中分离得到肠道内生菌若干株,经抑菌活性检测,排除产酸、产过氧化氢,并经蛋白酶类处理后,得到所述益生芽孢杆菌。
优选的,所述益生芽孢杆菌的活性产物为iturin、surfactin和fengycine三类分子构成的复合物。
根据发明人的实验探究发现,上述益生芽孢杆菌可应用在动物饲料、制备抑制革兰氏阳性菌药物和制备抑制革兰氏阴性菌药物中。
与现有技术相比,发明的有益效果为:
1、本发明的猪用抗病型益生芽孢杆菌不仅在有氧的条件下能生长迅速,并产生抑菌活性物质,同时在类似肠道的厌氧或兼性厌氧的条件下也能很好地生长,并同样产生抑菌活性产物。
2、本发明的猪用抗病型益生芽孢杆菌既可以在体外通过饲料发酵的方式来为动物提供抑菌防病促生长的生物活性饲料,同时还可以通过在动物肠道内的定植来达到长期保健,甚至终生防病的作用,具有很高的推广应用价值。
附图说明
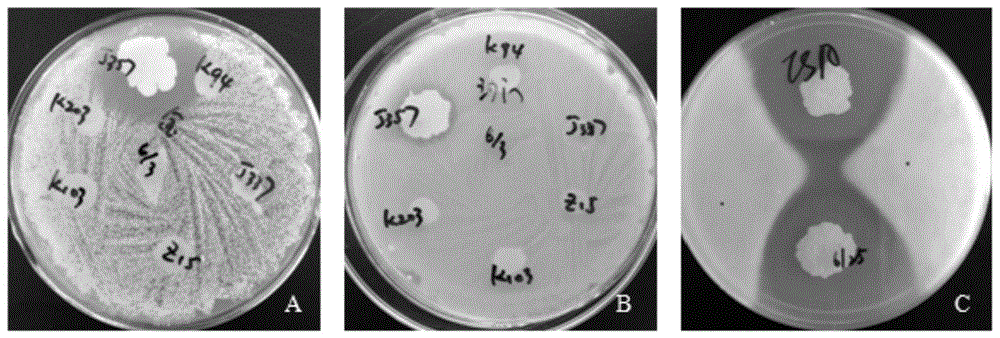
图1所示为对革兰氏阳性菌、革兰氏阴性菌及霉菌的抑菌活性结果图,a为对革兰氏阳性菌的抑菌活性情况图,b为对革兰氏阴性菌的抑菌活性情况图,c为对霉菌的抑菌活性情况图;
图2所示为对指示菌李斯特单胞菌的的抑菌活性检测结果图;
图3所示为本发明益生芽孢杆菌抑菌活性产物hplc分离结果图;
图4所示为本发明益生芽孢杆菌抑菌活性组份的maldi-tof-ms分析图谱;
图5所示为本发明益生芽孢杆菌抑菌活性产物hplc第25min馏分maldi-tof-ms图谱;
图6所示为本发明益生芽孢杆菌抑菌活性产物hplc第22min馏分maldi-tof-ms图谱。
具体实施方式
以下将结合实施例和附图对本发明的构思及产生的技术效果进行清楚、完整的描述,以充分地理解本发明的目的、方案和效果。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。
实施例1
菌株的制备
在菌株筛选时,以pca(platecountagar)成品培养基(胰蛋白胨0.5%,酵母浸粉0.25%,葡萄糖0.1%,琼脂1.5%)作为筛选培养基,以临床分离的致病性大肠杆菌作为指示菌,在37℃条件下,用平板进行点种法筛选。先后从猪的十二指肠、空肠、回肠、盲肠、结肠和直肠中分离得到肠道内生菌2300多株,经抑菌活性检测,有超过100株对指示菌具有抑菌活性,但经过排除产酸、产过氧化氢,以及经蛋白酶类处理后,最后得到该目标菌株。
如图1所示,a为对革兰氏阳性菌的抑菌活性,b为对革兰氏阴性菌的抑菌活性,c为对霉菌的抑菌活性,利用该目标菌株与金黄色葡萄球菌、沙门菌,以及从环境中分离得到的霉菌进行点种法对峙培养,结果表明该目标菌株对革兰氏阳性菌(g+)、革兰氏阴性菌(g-),以及真菌中的霉菌均显示出良好的抑菌活性。
实施例2
活性物质的分离及检测
通过固体培养的方法,收集菌体细胞后用有机溶剂提取,提取液经固相柱萃取后的50%乙腈洗脱组份具有很强的抑菌活性,用hplc分离后,发现活性组份分别出现在不同的馏份里,经modi-tof-ms分析,这些活性组份并非单一分子,而是由iturin、surfactin、fengycine等三类分子构成的复合物,这些复合物组份分开以后活性迅速减弱甚至消失。
利用pca平板,一次性接种20块,37℃培养48小时,收集全部菌体细胞,用70%异丙醇提取2小时,离心去菌体,上清即为提取液,经检测对指示菌李斯特单胞菌(listeriainnocua)具有微弱的抑菌活性,如图2所示。将活性提取液经sep-pakc18固相萃取,用乙腈梯度(25%、50%、75%、100%)洗脱,得到50%乙腈洗脱液活性组份。从抑菌活性强度看,该活性组份不仅去除了细胞提取液中绝大部分其他提取成分(杂质),同时也可对抑菌活性组分进行浓缩。
将50%的乙腈洗脱组份进行hplc分离纯化,用c18制备柱(250mm*10mm),以纯水和异丙醇-乙腈(2:1)为洗脱液,流速3.0ml/min,洗脱规程为:0-30min,有机溶剂从10%-100%梯度洗脱,30-35min为100%有机溶剂洗脱。每次上样100μl,在220nm波长下记录hplc的分离检测结果色谱图,结果如图3所示,按每1分钟间隔分别收集洗脱馏分,置通风橱中进行风干,适时检测各组份的抑菌活性,结果表明抑菌活性物质并非在某一集中时段被洗脱出来,而是广泛地分布在第20~28分钟馏分中。取hplc分离后抑菌活性最强的第22和25分钟馏分,以及50%乙腈洗脱液进行modi-tof-ms分析,结果表明50%乙腈洗脱液抑菌活性物中含有包括iturin、surfactin和fengycine三类不同的脂肽类物质,结果如图4所示,而第22和25分钟馏分中则只有iturin和surfactin两脂肽,结果如图5、图6所示。通过对3组样品中分子量的组成结构分析,推测样品50%乙腈洗脱液抑菌活性组分及其第22和25分钟hplc馏分的抑菌活性复合物组成分别见表1、表2和表3。
表1益生芽孢杆菌抑菌活性产物50%乙腈洗脱液组份的组成分成分析
表2益生芽孢杆菌抑菌活性产物第25分钟hplc馏分组成成分分析
表3益生芽孢杆菌抑菌活性产物第22分钟hplc馏分组成成分分析
通过相应的引物可以从益生芽孢杆菌中扩增出iturin、surfactin、fengycine三类产物生产的关键酶基因。根据iturin、surfactin、fengycine三类脂肽合成基因ituc、fend和srfaa序列设计相应的特异性扩增引物,itucf(5’-ggctgctgcagatgctttat)、itucr(5’-tcgcagataatcgcagtgag)、srfaf(5’-tcgggacaggaagacatcat)、srfar(5’-ccactcaaacggataatcctga)、fendf(5’-ggcccgttctctaaatccat)、fendr(5’-gtcatgctga。
- 还没有人留言评论。精彩留言会获得点赞!