一种抑制FOXO1基因表达的特异性siRNA(siFX1)及其应用
一种抑制foxo1基因表达的特异性sirna(sifx1)及其应用
技术领域
1.本发明涉及生物技术领域,具体涉及一种抑制foxo1基因表达的特异性sirna(sifx1)及其应用。
背景技术:
2.作为叉头(forkhead)蛋白o(foxo)家族中的一种重要转录因子,foxo1(fkhr)通过调节细胞的氧化应激、增殖及凋亡等多种生理过程,参与生物体的生长发育、代谢及肿瘤形成等。foxo1基因的表达具有时空差异,广泛表达于成人各组织器官中,包括心脏、脑组织、胎盘、食管、肺、肝脏、骨骼肌、肾脏、胰腺、脾脏、胸腺、前列腺、睾丸、卵巢、小肠、结肠、外周血白细胞等,参与涉及多种疾病基因的表达调控,可能对细胞的生长、分化、衰老等多种生理代谢功能起着重要的调节作用。因此,对foxo1基因的研究对各种相关疾病的研究和治疗具有促进作用,例如,对胰岛β细胞的调控作用可能使其成为治疗ⅱ型糖尿病新的靶基因;近年来已证实pax3
‑
foxo1融合蛋白作为高效转录因子可激活多个下游基因,也为腺泡型横纹肌肉瘤的治疗提供了更多的靶标。
3.通过短片段双链rna分子抑制目的基因正常表达的sirna(small interfering rna或short interfering rna)干扰技术,是一种在基因表达调控和功能研究中广泛使用的重要工具和方法。目前,已有各种不同的sirna双链核苷酸序列在多种蛋白基因的研究乃至疾病的治疗中得到验证和应用。然而,在这些研究和应用中,sirna双链干扰也具有一定的局限性,比如不稳定性、表达沉默的短时性、细胞膜的通透性及脱靶效应的存在等等。因此,针对同一目的基因的一种sirna不可能用于不同内容、目的和条件背景的研究中,因而有必要寻找和使用不同的干扰序列。
4.结合上述转录因子foxo1在生物体中的重要性,针对其设计筛选出了一条新的sirna双链短片段序列。我们发现,该序列对人foxo1基因的转录和翻译表达都具有强烈的敲降或抑制效应。它在腺泡型横纹肌肉瘤以及含有foxo1融合基因的细胞或疾病等的基础研究中具有重要的应用价值。此外,根据序列比对分析结果,该sifx1 sirna序列也适用于在诸如猕猴、大猩猩等灵长类动物中有关foxo1基因方面的基础研究工作。
技术实现要素:
5.本发明的目的在于克服现有技术中的缺陷,提供了一种新的抑制foxo1基因表达的特异性sirna(sifx1)及其应用。
6.为实现上述目的,本发明采用如下技术方案:
7.本发明的第一方面是提供一种抑制foxo1基因表达的特异性sirna,该特异性sirna为人foxo1 mrna序列中19个连续的核苷酸碱基对应的片段;该特异性sirna为sifx1,其序列如下:
8.sifx1
‑
s:5'
‑
gcgccgacuucaugagcaa dtdt
‑
3';
9.sifx1
‑
as:5'
‑
uugcucaugaagucggcgc dtdt
‑
3'。
10.进一步地,上述特异性sirna通过转染至含有foxo1基因的人源组织细胞中,抑制其中foxo1基因的转录表达。
11.进一步地,上述特异性sirna抑制人腺泡型横纹肌肉瘤细胞中foxo1基因的转录表达。
12.进一步地,通过序列比对分析,上述特异性sirna也能抑制非人源的灵长类动物如猕猴、猩猩等来源的foxo1基因的转录表达。
13.本发明的第二方面是提供上述特异性sirna在含有foxo1基因的组织细胞的基础研究中的应用。
14.本发明的第三方面是提供上述特异性sirna在含有foxo1融合基因的细胞或疾病的基础研究中的应用。
15.本发明的第四方面是提供上述特异性sirna在腺泡型横纹肌肉瘤的基础研究中的应用。
16.进一步地,上述特异性sirna通过转染至腺泡型横纹肌肉瘤细胞中抑制人foxo1基因的转录表达。
17.进一步地,上述转染至腺泡型横纹肌肉瘤细胞中的特异性sirna的终浓度为10~30nm。
18.进一步地,上述转染至腺泡型横纹肌肉瘤细胞中的特异性sirna的终浓度为20nm。
19.本发明的第五方面是提供包括上述特异性sirna的的抑制人foxo1基因转录或/及表达的试剂盒或其它以此sirna为基础的任何改良、优化而产生的方法、工具及研究系统。
20.本发明采用以上技术方案,与现有技术相比,具有如下技术效果:
21.本发明提供的抑制foxo1基因表达的特异性sirna具有极强的特异性,不存在脱靶效应,且具有更强的抑制、敲降效应;同时,该特异性sifx1几乎对细胞形态和生长没有什么影响,因此,该序列在有关foxo1基因的研究,特别是在腺泡型横纹肌肉瘤以及含有foxo1融合基因的细胞或疾病的基础研究中具有重要的应用价值;此外,根据序列比对分析,该sifx1序列同样适用于人源之外的其它包括猕猴、猩猩等灵长类动物中有关foxo1基因转录表达的基础研究。
附图说明
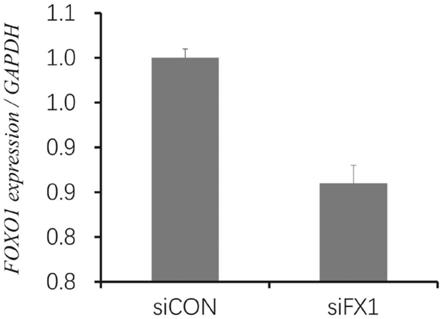
22.图1为本发明一实施例中腺泡型横纹肌肉瘤细胞rh4转染sifx1后,人foxo1基因的定量pcr(qrt
‑
pcr)分析结果;其中,gapdh为内参基因;
23.图2为本发明一实施例中腺泡型横纹肌肉瘤细胞rh4转染sifx1后,foxo1及pax3
‑
foxo1基因的蛋白表达的通过western blot结果(图a)及其相对定量分析结果(图b);其中,α
‑
tubulin为内参蛋白。
24.图3为本发明一实施例中腺泡型横纹肌肉瘤细胞rh4转染sifx4后,foxo1及pax3
‑
foxo1基因的蛋白表达的通过western blot结果(图a)及其相对定量分析结果(图b);其中,α
‑
tubulin为内参蛋白;
25.图4显示了本发明一实施例中不同sirna干扰序列转染腺泡型横纹肌肉瘤细胞rh4细胞后细胞形态的变化。
具体实施方式
26.本发明提供了一种抑制foxo1基因表达的特异性sirna,对腺泡型横纹肌肉瘤以及含有foxo1融合基因的细胞或疾病的基础研究具有重要意义,具体地,该特异性sirna,即sifx1为人foxo1 mrna序列中的19个连续的核苷酸碱基序列,并且3’'端垂悬有dtdt。具体地,该sifx1的核苷酸序列如下:
27.sifx1
‑
s:5'
‑
gcgccgacuucaugagcaa dtdt
‑
3'(seq id no.1);
28.sifx1
‑
as:5'
‑
uugcucaugaagucggcgc dtdt
‑
3'(seq id no.2)。
29.下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
30.下面结合具体实施例和附图对本发明作进一步说明,但不作为本发明的限定。
31.实施例1
32.本实施例验证了sifx1对foxo1基因在腺泡型横纹肌肉瘤细胞株中的转录水平的抑制效应,具体的实验步骤和结果如下:
33.接种腺泡型横纹肌肉瘤细胞的代表细胞株rh4(sj
‑
rh4)于6
‑
孔板或60mm的细胞培养皿中,在含有10%fbs(胎牛血清)、但无抗生素的dmem培养液中,37℃、5%二氧化碳条件下,过夜生长至60
‑
80%的细胞密度。利用lipofectamine 2000试剂分别转染sifx1及sicon(对照sirna,sicon
‑
s(正义链):5'
‑
cuauagcgaaccgugaucudtdt
‑
3'(seq id no.3),sicon
‑
as(反义链):5'
‑
agaucacgguucgcuauagdtdt
‑
3'(seq id no.4))序列至细胞中(sirna终浓度为20nm),6
‑
8小时后,将培养液替换为含有0.3%fbs、1%抗生素的dmem培养液,37℃、5%二氧化碳条件下,培养72小时。收集细胞,提取并测定总rna浓度。取1μg总rna反转录成cdna,利用以下人源的特异性引物进行定量pcr反应,检测foxo1基因在转录水平上的变化情况,分析sifx1序列对foxo1基因转录的影响,结果如图1所示。
34.用于人foxo1基因qrt pcr反应的引物序列:
35.正向引物:5
’‑
gacaccagttgatcctgggg
‑3’
(seq id no.5)
36.反向引物:5
’‑
ctggctgccataggttgaca
‑3’
;(seq id no.6)
37.用于q rt pcr反应的人gapdh基因内参序列:
38.正向引物:5
’‑
ctgggctacactgagcacc
‑3’
(seq id no.7)
39.反向引物r:5
’‑
aagtggtcgttgagggcaatg
‑3’
(seq id no.8)。
40.由图1可知,腺泡型横纹肌肉瘤细胞rh4转染sifx1后,人foxo1基因在转录水平上明显下降。
41.实施例2
42.本实施例验证了在腺泡型横纹肌肉瘤细胞株中,sifx1和已知特异性foxo1 sirna序列(sifx4,sifx4
‑
s(正义链):5'
‑
ggagguaugagucaguauadtdt
‑
3'(seq id no.9),sifx4
‑
as(反义链):5'
‑
uauacugacucauaccuccdtdt
‑3’
(seq id no.10);参考“foxo1 inhibits the invasion and metastasis of hepatocellular carcinoma by reversing zeb2
‑
induced epithelial
‑
mesenchymal transition”,tianxiu dong et al,oncotarget,第8卷第1期,第1703
‑
1713页,20170103)对foxo1基因在蛋白水平上的抑制效应,具体的实验步
骤和结果如下:
43.同实施例1,将sifx1或sicon转染至rh4细胞中,在无血清或低浓度胎牛血清(0.3%)条件下培养72小时后,收集细胞,提取总蛋白。取30
‑
50μg总蛋白进行sds
‑
page胶电泳,转pvdf膜,用foxo1、α
‑
tubulin等的抗体孵育,检测sifx1sirna对细胞中foxo1表达的影响,结果如图2所示。
44.由图2可知,sifx1只抑制腺泡型横纹肌肉瘤细胞的foxo1的转录和蛋白表达,不抑制融合基因pax3
‑
foxo1的表达,不存在脱靶效应。且对比图3可知,相对于已知sirna序列,sifx1比已存在的foxo1 sirna的干扰效率高,特异性强。
45.同时发现,转染sifx1 sirna后,细胞中pax3
‑
foxo1表达有所增加,但这并非脱靶效应,而是foxo1与pax3
‑
foxo1之间本身存在着的一种互作关系的反映。
46.实施例3
47.本实施例验证sifx1与已知阳性对照sifx4对细胞形态的影响,具体的实验操作和结果如下:
48.同实施例1,将sifx1、sifx4 sirna和sicon分别转染至rh4细胞中,在低浓度胎牛血清(0.3%fbs)条件下培养至60
‑
72小时,选取不同时间点,在显微镜下观察细胞形态的变化差异,并拍照记录,结果如图4所示。
49.由图4可知,sifx1干扰序列与已知对照sifx4干扰序列对细胞形态的影响存在着差异。通过转染sirna序列敲降foxo1表达后,在低浓度血清培养条件下,sifx1几乎对细胞形态和生长没有什么影响,而sifx4则严重影响其形态和胞细生长,导致细胞最后变成细丝状,乃至细胞死亡。可见,sifx4等已知对照干扰序列可能对细胞具有脱靶效应或其它还未完全弄清楚的作用。
50.以上对本发明的具体实施例进行了详细描述,但其只作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明精神和范围下所做的均等变换、修改和包括shrna(short hairpin rna)等技术方面的应用,都应涵盖在本发明的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1