1,4,6-三羟基-8-支链-9,10-蒽醌类化合物及在制备抑菌剂中的应用的制作方法
1.本发明属于药物化学技术领域,具体涉及1,4,6-三羟基-8-支链-9,10-蒽醌类化合物及在制备抑菌剂中的应用。
背景技术:
2.细菌性传染病一直是人类和动物健康的重要威胁。猪链球菌(streptococcus suis)是一种重要的细菌性传染病病原,具有流行广、致病力强的特点,是一种重要的人兽共患传染病病原,能引起包括人和猪在内的多种动物的多种疾病,造成感染甚至死亡,严重影响养猪业的发展和人类健康。猪丹毒杆菌(erysipelothrixrhusiopathiae)为猪丹毒的病原菌,偶然可使人、鸟类和羔羊等感染,人感染后可发生“类丹毒”。抗生素在控制细菌感染中发挥着重要作用,临床多重耐药菌株、超级耐药细菌的出现,均提示现有抗细菌感染的药物已不能满足动物和人类防控细菌感染的需求,此迫切需要研究新的抗细菌药物。
3.申请人前期获得了8个1,4,6-三羟基-8-支链蒽醌化合物(化合物1-8),发现该系列化合物具有较好的抗肿瘤活性[吴兆圆等,anthraquinone analogues from a soil actinomycetestreptomyces sp.ws-13394and their bioactivities.natural product research,2018,32(4):412-417;吴兆圆等,new cytotoxic alkylated anthraquinone analogues from a soil actinomycetestreptomyces sp.ws-13394.chemical&pharmaceutical bulletin,2014,62(1):118-121.]。
[0004]
本发明在化合物1-8的结构基础上,申请人进一步获得了化合物9-11,发现化合物1-11对细菌,特别是金黄色葡萄球菌、猪丹毒杆菌和猪链球菌具有明显的生长抑制作用,在国内外文献均未见报道。
技术实现要素:
[0005]
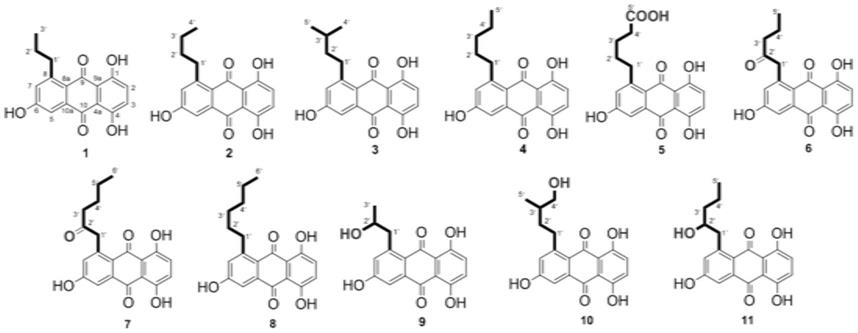
本发明目的在于提供1,4,6-三羟基-8-支链-9,10-蒽醌类化合物,所述化合物的结构式如下:
[0006][0007]
其中,r为:丙基、丁基、异戊基、戊基、戊羧基、2
′‑
羰基戊基、2
′‑
羰基己基、己基、2
′‑
羟基丙基、4
′‑
羟基异戊基或2
′‑
羟基戊基。
[0008]
本发明的另一个目的在于提供1,4,6-三羟基-8-支链-9,10-蒽醌类化合物在制备细菌抑菌剂中的应用。
[0009]
为了达到上述目的,本发明采取以下技术措施:
[0010]
1,4,6-三羟基-8-支链-9,10-蒽醌类化合物,所述化合物的结构式如下:
[0011][0012]
其中,r为:丙基、丁基、异戊基、戊基、戊羧基、2
′‑
羰基戊基、2
′‑
羰基己基、己基、2
′‑
羟基丙基、4
′‑
羟基异戊基或2
′‑
羟基戊基。
[0013]
当上述r为不同基团时,依次命名为化合物1-11,具体的,化合物1-11的结构式如下:
[0014][0015]
本发明的保护范围还包括:上述1,4,6-三羟基-8-支链-9,10-蒽醌类化合物在制备细菌抑制剂中的应用。
[0016]
以上所述的应用中,优选的,所述的细菌为金黄色葡萄球菌(staphylococcus aureus)、猪丹毒杆菌(erysipelothrixrhusiopathiae)和/或猪链球菌(streptococcus suis)。
[0017]
本发明与现有技术相比,具有以下优点和有益效果:
[0018]
1、目前临床使用的抗细菌药物主要是环肽类、大环内酯类和青霉素类。本发明所涉及结构与目前临床使用的抗细菌药物的骨架类型完全不同,它们是一种1,4,6-三羟基-8-支链-9,10-蒽醌类化合物。基于此类化合物进一步开发成的抗细菌药物可完全避开现有上市药物专利,为市场提供更多选择。
[0019]
2、本发明发现新化合物9-11,并首次发现1,4,6-三羟基-8-支链-9,10-蒽醌类化合物具有抗金黄色葡萄球菌、猪链球菌和猪丹毒杆菌活性。
[0020]
3、抗菌实验结果表明,化合物1、2、4、5、8和10对金黄色葡萄球菌有显著的抗菌活性(mic《0.78μg/ml),化合物3、6、9和11对金黄色葡萄球菌也具有较强的抗菌活性(mic分别为6.25、1.56、0.78和1.56μg/ml);化合物3、9和10对猪丹毒杆菌具有较强的抗菌活性(mic分别为3.125、6.25和3.125μg/ml);化合物1、2、3、4和8对猪链球菌具有较强的抗菌活性(mic分别为6.25、3.125、6.25、3.125和1.56μg/ml)。因此,1,4,6-三羟基-8-支链-9,10-蒽醌类化合物具有制备作为新型抗细菌药物的潜在用途。
具体实施方式
[0021]
下面结合具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本
发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
[0022]
实施例1:
[0023]
1,4,6-三羟基-8-支链-9,10-蒽醌类化合物,所述化合物的结构式如下:
[0024][0025]
其中,r为:丙基、丁基、异戊基、戊基、戊羧基、2
′‑
羰基戊基、2
′‑
羰基己基、己基、2
′‑
羟基丙基、4
′‑
羟基异戊基或2
′‑
羟基戊基。
[0026]
当上述r为不同基团时,依次命名为化合物1-11,具体的,化合物1-11的结构式如下:
[0027][0028]
其中,化合物1-8申请人已报道过,化合物9-11的结构鉴定的uv、hr-esi-ms以及nmr谱数据如下:
[0029]
化合物9-11均为红色粉末,共同的uv吸收紫外吸收光谱(466,277,225nm)表明这些化合物都具有共同的1,4,6,8-取代蒽醌的骨架。
[0030]
hr-esi-ms数据:化合物9(m/z337.0688,[m+na]
+
)推断其分子式为c
17h14
o6。化合物10(m/z365.0994,[m+na]
+
),推断其分子式为c
19h18
o6;化合物11(m/z365.0994,[m+na]
+
),推断其分子式为c
19h18
o6。
[0031]
nmr数据如下:
[0032]
表1.化合物9-11(dmso-d6)的1h-nmr(500mhz)数据(δh,j hz)
[0033][0034]
表2化合物9-11(dmso-d6)的
13
c-nmr数据(125mhz)数据
[0035][0036]
实施例2:
[0037]
化合物1-11抗菌活性测试:
[0038]
选取金黄色葡萄球菌(staphylococcus aureus)、猪丹毒杆菌(erysipelothrixrhusiopathiae)和猪链球菌(streptococcus suis)、大肠杆菌(escherichia coli)以及绿脓杆菌(pseudomonas aeruginosa)菌种在营养琼脂斜面培养基上传代培养1次,再将其接种至营养肉汤培养基中37℃培养6~12h,放置于冰箱备用。取待测样品及阳性对照(链霉素和青霉素),用培养液依次进行稀释至100μg/ml、50μg/ml、25μ
g/ml、12.5μg/ml、6.25μg/ml、3.125μg/ml、1.56μg/ml和0.78μg/ml,振荡混合后取1ml转移至96孔板,以培养基为空白对照,空白及每个浓度均选择3个重复,实验重复3次,37℃培养12~18h,用酶标仪630nm测定吸光度,确定mic值。
[0039]
结果:化合物1、2、4、5、8和10对金黄色葡萄球菌有显著的抗菌活性(mic《0.78μg/ml),化合物3、6、9和11对金黄色葡萄球菌也具有较强的抗菌活性(mic分别为6.25、1.56、0.78和1.56μg/ml);化合物3、9和10对猪丹毒杆菌具有较强的抗菌活性(mic分别为3.125、6.25和3.125μg/ml);化合物1、2、3、4和8对猪链球菌具有较强的抗菌活性(mic分别为6.25、3.125、6.25、3.125和1.56μg/ml)。
[0040]
表3化合物1-11对三种细菌的抑制作用(micμg/ml)
[0041][0042]
“‑”
代表药物浓度为100μg/ml以下均无抗菌活性
[0043]
上述实施例仅用于说明而不用于限制本发明的保护范围。本领域技术人员可以对本发明做各种改动或修改,这些等效变化同样为本发明权力要求所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1