一种制备4-羟基喹啉-2(1H)-酮类化合物的方法
一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法
技术领域
1.本发明属于有机合成领域,具体涉及一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法。
背景技术:
2.二氧化碳是主要的温室气体,同时也是一种很有应用前景的c1合成子,在有机合成领域中引起了广泛的关注。由于二氧化碳的热力学稳定性和动力学惰性,开发有效的二氧化碳活化及后续转化策略至关重要。离子液体具有高可调节性、高稳定性、低蒸气压、高极性和低熔点的特点,在吸收和活化二氧化碳方面显示出巨大的潜力,成为二氧化碳转化中理想的有机溶剂和催化剂。
[0003]4‑
羟基
‑
2(1h)喹啉酮类衍生物是一类具有杀菌、抗真菌、抗疟疾和抗艾滋病毒等多种生物活性的化合物,开发其合成方法具有重要意义。常规的合成方法有:1)取代苯胺与丙二酸酯衍生物在二苯醚溶剂中高温下缩合反应得到4
‑
羟基
‑
2(1h)喹啉酮(j.med.chem.;1992,35(18):3423
‑
3425);2)邻硝基苯甲酸先制备苯甲酰乙酸乙酯衍生物,再还原环化生成4
‑
羟基
‑
2(1h)喹啉酮(european j.med.chem.;2017,138:491
‑
500.);3)n
‑
(2
‑
氯乙酰基)
‑
n
‑
甲基邻氨基苯甲酸甲酯在碲化钠(na2te)催化下合成4
‑
羟基
‑
2(1h)喹啉酮(j.org.chem.;2005,70(12):4682
‑
4686.);4)苯胺与丙二酸在氯化锌和三氯氧磷中缩合生成4
‑
羟基
‑
2(1h)喹啉酮(j.hetero.chem.;2001,38(1):61
‑
67.)。这些常规方法存在反应温度高,使用腐蚀性酸性化合物,原料难得等缺点,需要进一步改进。
[0004]
近年来,利用二氧化碳与邻氨基苯乙炔衍生物合成4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物成为该领域新的研究热点,此方法利用碘化亚铜或硝酸银为催化剂,实现了4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的高效合成,且兼具原子经济性高的特点。yamada等报道了邻氨基苯乙炔衍生物与二氧化碳在dbu存在下,dmso为溶剂,常压、60℃下反应24小时,合成4
‑
羟基
‑
2(1h)喹啉酮的产率可达到99%(org.lett.;2013,15(14):3710
‑
3713.)。zhang等发现用碘化亚铜替换硝酸银后,在类似条件下也可以实现4
‑
羟基
‑
2(1h)喹啉酮,此时二氧化碳的需增压到1mpa,产率中等(catal.sci.tech.;2014,4(6):1570.)。politanskaya等将yamada报道的方法进行优化,使用乙腈作为溶剂,应用于一系列多氟取代的4
‑
羟基
‑
2(1h)喹啉酮衍生物的合成,取得了良好的效果(j.fluoro.chem.;2021,242:1
‑
10.)。以上这些方法为4
‑
羟基
‑
2(1h)喹啉酮的合成提供了新的途径,但是依然存在反应时间长,银或铜催化剂使用量过多,需要使用有机溶剂的缺点,需要进一步优化。
技术实现要素:
[0005]
针对现有技术中4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物制备过程中存在的上述技术问题,本发明提出一种使用离子液体和银盐催化剂,在常压下实现以二氧化碳和2
‑
乙炔基苯胺为原料合成该类化合物的方法。
[0006]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,式(1)所示
的2
‑
乙炔基苯胺类化合物和二氧化碳为原料,在银盐催化剂存在作用下,一并在离子液体中反应得到式(ii)所示的4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物,其反应式如下:
[0007][0008]
式(1)和式(ii)中,x表示苯环上的取代基r的数量,x=1~4;苯环上不同取代位置的取代基r1相同或不同;取代基r1选自h、c1
‑
c4烷基、卤素、c1
‑
c4烷氧基或硝基。
[0009]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
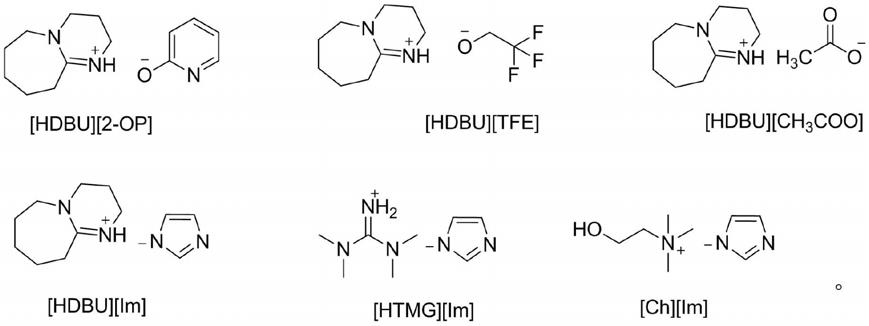
酮类化合物的方法,其特征在于,所述离子液体的结构式选自下列之一:
[0010][0011]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,所述银盐催化剂为硝酸银或乙酸银。
[0012]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,所述银盐催化剂与2
‑
乙炔基苯胺类化合物的摩尔比为1:5~100,优选为1:10~50。
[0013]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,式(1)所示的2
‑
乙炔基苯胺类化合物与离子液体的摩尔比为1:1~10,优选为1:2~4。
[0014]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,反应温度为30℃~120℃,反应时间为2小时~48小时。
[0015]
所述的一种制备4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的方法,其特征在于,反应时的co2压力为0.1mpa~2mpa。
[0016]
相对于现有技术,本发明取得的优点是:本发明使用的离子液体合成方法较为简单,采用相应的有机碱和酸在乙醇溶剂中室温搅拌即可制得。本发明的离子液体在应用于4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的反应中时,反应条件较为温和,产物的分离纯化过程较为简单,产物产率高,底物适用范围广。
具体实施方式
[0017]
下面结合具体实施例对本发明作进一步说明,但本发明的保护范围并不限于此。
[0018]
实施例1,本发明使用的离子液体均是采用相应有机酸和有机碱在乙醇搅拌后制得,具体步骤如下:
[0019]
实验一:称取2
‑
羟基吡啶(5mmol)和1,8
‑
二氮杂二环十一碳
‑7‑
烯(dbu,5mmol)加
入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂,即得到[hdbu][2
‑
op],黄色液体,产率100%。
[0020]
实验二:称取三氟乙醇(5mmol)和1,8
‑
二氮杂二环十一碳
‑7‑
烯(dbu,5mmol)加入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂,即得到[hdbu][tfe],无色液体,产率100%。
[0021]
实验三:称取咪唑(5mmol)和四甲基胍(5mmol)加入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂,即得到[htmg][im],淡黄色液体,产率100%。
[0022]
实验四:称取咪唑(5mmol)和胆碱(48
‑
50%水溶液,5mmol)加入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂和水分,得到[ch][im],黄色液体,产率100%。
[0023]
实验五:称取咪唑(5mmol)和1,8
‑
二氮杂二环十一碳
‑7‑
烯(dbu,5mmol)加入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂,得到[hdbu][im],黄色液体,产率100%。
[0024]
实验六:称取乙酸(5mmol)和1,8
‑
二氮杂二环十一碳
‑7‑
烯(dbu,5mmol)加入到50ml烧瓶中,加入20ml无水乙醇,室温搅拌24小时后,蒸发浓缩脱除乙醇溶剂,得到[hdbu][ch3coo],黄色液体,产率100%。
[0025]
实施例2:
[0026]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0027]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[hdbu][2
‑
op](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率69%,1h nmr(500mhz,dmso
‑
d6)δ:11.36(br s,1h,oh),11.20(s,1h,nh),7.78(d,1h,ar
‑
h),7.49(t,1h,ar
‑
h),7.26(d,1h,ar
‑
h),7.14(t,1h,ar
‑
h),5.74(s,1h,ch)。
[0028]
实施例3:
[0029]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0030]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[hdbu][ch3coo](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率67%。
[0031]
实施例4:
[0032]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0033]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[hdbu][tfe](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4
小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率46%。
[0034]
实施例5:
[0035]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0036]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[hdbu][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率78%。
[0037]
实施例6:
[0038]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0039]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[ch][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率86%。
[0040]
实施例7:
[0041]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0042]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应4小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率87%。
[0043]
实施例8:
[0044]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0045]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应6小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率90%。
[0046]
实施例9:
[0047]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0048]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧
化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率88%。
[0049]
实施例10:
[0050]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0051]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),80℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率30%。
[0052]
实施例11:
[0053]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0054]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),30℃下搅拌反应18小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率80%。
[0055]
实施例12:
[0056]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0057]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率89%。
[0058]
实施例13:
[0059]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0060]
称取2
‑
乙炔基苯胺(1mmol)、醋酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率86%。
[0061]
实施例14:
[0062]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0063]
称取2
‑
乙炔基苯胺(1mmol)、硝酸银(0.01mmol)和[htmg][im](3mmol)到20ml反应
管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基喹啉
‑
2(1h)
‑
酮,产率83%。
[0064]
实施例15:
[0065]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0066]
称取2
‑
乙炔基苯胺(1mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,没有析出白色固体,薄层色谱显示原料未反应。
[0067]
实施例16:
[0068]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0069]
称取2
‑
乙炔基
‑4‑
甲基苯胺(1mmol)、硝酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基
‑6‑
甲基喹啉
‑
2(1h)
‑
酮,产率91%。1h nmr(500mhz,dmso
‑
d6)δ:10.94(s,1h,nh),7.58(s,1h,ar
‑
h),7.28(d,1h,ar
‑
h),7.13(d,1h,ar
‑
h),5.65(s,1h,ch),2.33(s,3h,ch3)。
[0070]
实施例17:
[0071]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0072]
称取2
‑
乙炔基
‑4‑
甲氧基苯胺(1mmol)、硝酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基
‑6‑
甲氧基喹啉
‑
2(1h)
‑
酮,产率94%。1h nmr(500mhz,dmso
‑
d6)δ:10.93(s,1h,nh),7.24(1h,ar
‑
h),7.18(1h,ar
‑
h),7.11(dd,1h,ar
‑
h),5.66(s,1h,ch),3.77(s,3h,och3)。
[0073]
实施例18:
[0074]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0075]
称取2
‑
乙炔基
‑4‑
氯苯胺(1mmol)、硝酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出白色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基
‑6‑
氯喹啉
‑
2(1h)
‑
酮,产率90%。1h nmr(500mhz,dmso
‑
d6)δ:11.54(s,1h,oh),11.34(s,1h,nh),7.72(d,1h,ar
‑
h),7.53(dd,1h,ar
‑
h),7.27(d,1h,ar
‑
h),5.76(s,1h,ch)。
[0076]
实施例19:
[0077]
本实施例提供一种4
‑
羟基喹啉
‑
2(1h)
‑
酮类化合物的制备方法,具体步骤如下:
[0078]
称取2
‑
乙炔基
‑4‑
硝基苯胺(1mmol)、硝酸银(0.02mmol)和[htmg][im](3mmol)到20ml反应管中,反应管中装入有搅拌子,且反应管放置于磁力搅拌器上,反应管的管口连接装有二氧化碳的气袋,在二氧化碳气袋保护下(反应过程中co2压力约为0.1mpa),60℃下搅拌反应2小时。反应结束后冷却到室温,加入10ml水,1mol/l稀硝酸调节ph到6~7,析出黄色固体,过滤,水洗(10ml
×
3),甲基叔丁基醚洗涤(10ml
×
3),干燥得到目标产物4
‑
羟基
‑6‑
硝基喹啉
‑
2(1h)
‑
酮,产率80%。1h nmr(500mhz,dmso
‑
d6)δ:12.23(brs,1h,oh),11.74(s,1h,nh),8.58(d,1h,ar
‑
h),8.32(dd,1h,ar
‑
h),7.39(d,1h,ar
‑
h),5.79(s,1h,ch)。
[0079]
实施例2~19描述的反应物和反应产物的结构式如下表所示:
[0080][0081]
本说明书所述的内容仅仅是对发明构思实现形式的列举,本发明的保护范围不应当被视为仅限于实施例所陈述的具体形式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1