一种结合新冠病毒RBD位点的环肽及其制备方法和用途
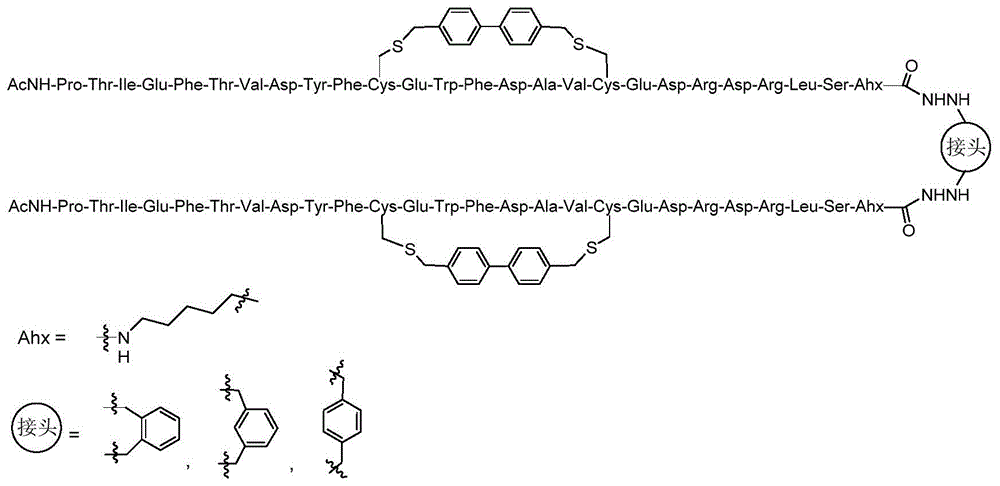
本发明涉及一种纳摩尔级别结合新冠病毒rbd位点的环肽及其制备方法。
背景技术:
:抑制sars-cov-2感染的有效途径是阻断sars-cov-2spikerbd与ace2受体之间的相互作用。市面上靶向新冠病毒的抗体药物绝大多数均能高亲和力结合sars-cov-2表面的rbd位点。然而,抗体药物分子体积大,其保存需要低温,同时制备成本极为昂贵。相对抗体药物,多肽药物分子体积小,可以常温保存,且易于低成本化学合成与改造。最近的ace2与rbd蛋白质复合物结构表明ace2主要通过一段螺旋结构的多肽序列与病毒的rbd结合。基于此,国际上多个课题组提出使用ace2的一段螺旋结构多肽来抑制新冠病毒。但是,研究表明ace2天然序列多肽并不能与sars-cov-2的rbd位点结合,无法抑制新冠病毒对人细胞的感染。因此,发展能够以高亲和力结合新冠病毒rbd位点的ace2肽模拟物仍是新冠病毒药物研发的重要方向。技术实现要素:早期ace2多肽模拟物不具备高亲和力结合新冠病毒rbd位点,不能产生所需的抗病毒活性。基于ace2的一段螺旋结构多肽的序列,本发明通过氨基酸的点突变,侧链-侧链交联,和多肽酰肼与苯二甲醛的共价二聚化,得到一种具备纳摩尔级别结合新冠病毒rbd位点的环肽。相比于原有的ace2模拟物,本发明环肽具有纳摩尔级别亲和力,有望为sars-cov-2的治疗和检测提供具有商业价值的生物活性先导分子。本发明环肽是通过制备线性酰肼肽、线性酰肼肽的侧链环化和酰肼肽的二聚化改造后获得的,其结构如下所示:本发明结合新冠病毒rbd位点的环肽的制备方法,包括如下步骤:步骤1:合成肼-2-cl-trt树脂将2-ci-trt-cl树脂用dmf溶胀,再加入5%水合肼的dmf溶液重复处理两次,接着加入dcm、meoh对树脂进行封闭处理,得到肼-2-cl-trt树脂;步骤2:fmoc法固相合成线性酰肼肽将步骤1获得的树脂转移到固相合成管中,dmf溶胀后采用fmoc法依肽序进行氨基酸的固相拼接;肽序列拼接结束后,外加切割试剂反应2小时,冰乙醚沉淀得到线性酰肼肽:acnh-pro-thr-ile-glu-phe-thr-val-asp-tyr-phe-cys-glu-trp-phe-asp-ala-val-cys-glu-asp-arg-asp-arg-leu-ser-ahx-conhnh2(ahx=6-氨基己酸);步骤3:线性酰肼肽的侧链环化将步骤2得到的线性酰肼肽粗品经液相色谱纯化,纯化后的线性酰肼肽溶解在dmf/h2o/nh4hco3混合溶剂中,在4,4-二溴甲基联苯作用下,形成侧链环化的酰肼肽;步骤4:制备侧链环化酰肼肽的二聚体将步骤3得到的产物纯化冻干,溶解到hoac/meoh溶液中,在1,3-苯二甲醛、1,2-苯二甲醛或1,4苯二甲醛中的一种以及氰基硼氢化钠的作用下,形成目标环肽。具体制备过程如下:步骤1:合成肼-2-cl-trt树脂称量268mg2-ci-trt-cl树脂(载量0.56mmol/g,150μmol)于固相合成管中,加入3mldmf溶胀20分钟;树脂依次被dcm清洗三次,dmf清洗两次;加入3.5ml5%水合肼(125μl水合肼+3.33mldmf),常温震荡30min,弃废液,重复一次;再加入2.5ml20%meoh/dmf(2mldmf+0.5mlmeoh)常温震荡封闭反应20min,dmf洗涤5次即得肼-2-cl-trt树脂。步骤2:fmoc法固相合成线性酰肼肽将步骤1获得的树脂转移到固相合成管中,加入现配制的dic/oxyma/6-氨基己酸的dmf混合液(10eqdic:10eqoxyma:10eq6-氨基己酸,2mldmf),于55℃反应40分钟;dmf洗涤树脂后,加入2ml封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89)封闭未连接的胺基,2min后,dmf清洗树脂三次;再加入20%哌啶的dmf溶液,常温震荡8min,弃反应液;重复20%哌啶处理步骤;dmf清洗树脂三次后,加入现配制的dic/oxyma/fmoc-ser(tbu)-oh的dmf混合液(10eqdic:10eqoxyma:10eqfmoc-ser(tbu)-oh,2mldmf),于55℃反应40min。接下来氨基酸缩合重复上面的操作,依肽序缩合fmoc保护的氨基酸leu、arg、asp、arg、asp、glu、cys、val、ala、asp、phe、trp、glu、cys、phe、tyr、asp、val、thr、phe、glu、ile、thr、pro缩合完成后,再加入2ml封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89)封闭n末端胺基。当线性肽固相合成完成后,树脂用大量dmf、dcm洗涤,自然干燥后,外加6ml切割试剂(tfa:间甲酚:水:tips=88:5:5:2,v/v)处理2小时。收集切割试剂,加入10倍以上体积当量的冰乙醚沉淀,离心粉末状粗肽,半制备hplc纯化多肽;真空冷冻干燥得到纯化线性酰肼肽:acnh-pro-thr-ile-glu-phe-thr-val-asp-tyr-phe-cys-glu-trp-phe-asp-ala-val-cys-glu-asp-arg-asp-arg-leu-ser-ahx-conhnh2(ahx=6-氨基己酸)。步骤3:线性酰肼肽的侧链环化将10mg线性肽溶解于2.0mldmf:h2o混合物(2:1,v:v)中,将1.4mg4,4-二溴甲基联苯加入到0.1mldmf中溶解,并加入到混合物中,使用1.0mnh4hco3将反应混合物的ph值调节至8.0。在震荡混合器中常温反应2h后,加入3ml乙腈:h2o混合物(1:1,v:v,0.1%tfa)以淬灭反应。环化肽通过制备型hplc纯化并且冷冻抽干后,获得白色粉末(~3mg,30%)。侧链环化酰肼多肽序列如下:步骤4:制备侧链环化酰肼肽的二聚体将3mg侧链环化酰肼多肽(~0.9μmol)溶解在600μl乙酸:甲醇混合物(1:1,v:v)中;然后制备1,3-苯二甲醛或者1,2-苯二甲醛或1,4-苯二甲醛(4.1mg1,3-苯二甲醛苯在1.0ml乙酸:甲醇混合物中);将10μl新制备的1,3-苯二甲醛添加到线性环化酰肼多肽溶液中,室温震荡反应1h,将在300μlh2o中的3.0mgnabh3cn添加到反应混合物中,再常温震荡反应1h,加入4ml乙腈:h2o混合物(1:1,v:v,0.1%tfa)以淬灭反应;用制备型hplc纯化产物并且冷冻抽干后,获得所需的抗新冠病毒肽,为白色粉末(0.6mg,20%)。已经公开报道的ace2模拟多肽几乎不能结合新冠病毒的受体结合位点。本发明涉及的ace2肽模拟物能以高达16nm的结合力结合新冠病毒rbd位点。与市面上的抗体药物相比,本发明涉及的多肽具有潜在更高的热稳定性,免疫反应性较低,且易于大规模生产。附图说明图1是抗新冠病毒肽结构示意图。图2是本发明的合成路线示意图。图3是线性酰肼肽的hplc谱图。图4是侧链环化酰肼肽的hplc谱图和ms图。图5是抗新冠病毒肽的hplc和ms图。图6是抗新冠病毒肽与sars-cov-2spikerbd结合力测试。具体实施方法以下结合具体的实施例对本发明技术方案做进一步的说明。本发明所使用的缩写的含义列于下表:英文缩写中文含义fmoc9-芴甲氧羰基tbu叔丁基trt三苯甲基dcm二氯甲烷dmfn,-n二甲基甲酰胺hoac乙酸tfa三氟乙酸dicn,n-二异丙基碳化二亚胺oxyma2-肟氰乙酸乙酯tips三异丙基硅烷tris三羟甲基氨基甲烷hplc高效液相色谱esi-ms电喷雾离子源液相质谱实施例1:合成肼-2-cl-trt树脂称量268mg2-ci-trt-cl树脂(载量0.56mmol/g,150umol)于固相合成管中,加入3mldmf溶胀20分钟。树脂依次被dcm清洗三次,dmf清洗两次。加入3.5ml5%水合肼(125μl水合肼+3.33mldmf),常温震荡30min,弃废液,重复一次。再加入2.5ml20%meoh/dmf(2mldmf+0.5mlmeoh)常温震荡封闭反应20min,dmf洗涤5次即得肼-2-cl-trt树脂。实施例2:fmoc固相合成线性酰肼肽将实施例1制备的树脂转移到固相合成管中,加入现配制的dic/oxyma/6-氨基己酸的dmf混合液(10eqdic:10eqoxyma:10eq6-氨基己酸,2mldmf),于55℃反应40分钟。dmf洗涤树脂后,加入2ml封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89)封闭未连接的胺基。2min后,dmf清洗树脂三次。再加入20%哌啶的dmf溶液,常温震荡8min,弃反应液。重复20%哌啶处理步骤。dmf清洗树脂三次后,加入现配制的dic/oxyma/fmoc-ser(tbu)-oh的dmf混合液(10eqdic:10eqoxyma:10eqfmoc-ser(tbu)-oh,2mldmf),于55℃反应40分钟。接下来氨基酸缩合重复上面的操作,依肽序缩合fmoc保护的氨基酸leu、arg、asp、arg、asp、glu、cys、val、ala、asp、phe、trp、glu、cys、phe、tyr、asp、val、thr、phe、glu、ile、thr、pro缩合完成后,再加入2ml封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89)封闭n末端胺基。当线性肽固相合成完成后,树脂用大量dmf、dcm洗涤,自然干燥后,外加6ml切割试剂(tfa:间甲酚:水:tips=88:5:5:2,v/v)处理2小时。收集切割试剂,加入10倍以上体积当量的冰乙醚沉淀,离心粉末状粗肽,半制备hplc纯化多肽;真空冷冻干燥得到纯化线性酰肼肽:acnh-pro-thr-ile-glu-phe-thr-val-asp-tyr-phe-cys-glu-trp-phe-asp-ala-val-cys-glu-asp-arg-asp-arg-leu-ser-ahx-conhnh2(ahx=6-氨基己酸)。实施例3:线性酰肼肽的侧链环化将10mg线性肽溶解于2.0mldmf:h2o混合物(2:1,v:v)中,将1.4mg4,4-二溴甲基联苯加入到0.1mldmf中溶解,并加入到混合物中,使用1.0mnh4hco3将反应混合物的ph值调节至8.0。在震荡混合器中常温反应2h后,加入3ml乙腈:h2o混合物(1:1,v:v,0.1%tfa)以淬灭反应。环化肽通过制备型hplc纯化并且冷冻抽干后,获得白色粉末(~3mg,30%),如图4所示。侧链环化酰肼多肽序列如下:实施例4:制备侧链环化酰肼肽的二聚体将3mg侧链环化酰肼多肽(~0.9μmol)溶解在600μl乙酸:甲醇混合物(1:1,v:v)中。然后制备1,3-苯二甲醛(4.1mg1,3-苯二甲醛苯在1.0ml乙酸:甲醇混合物中)。将10μl新制备的1,3-苯二甲醛添加到线性环化酰肼多肽溶液中,室温震荡反应1h。将在300μlh2o中的3.0mgnabh3cn添加到反应混合物中,再常温震荡反应1h。加入4ml乙腈:h2o混合物(1:1,v:v,0.1%tfa)以淬灭反应。用制备型hplc纯化产物并且冷冻抽干后,获得所需的抗新冠病毒肽,为白色粉末(0.6mg,20%),如图5所示。实施例5:抗新冠病毒肽与sars-cov-2spikerbd结合力测试将sars-cov-2spikerbd-his加载到基于链霉亲和素的sa传感器上。将100μlhepes缓冲液(20mmhepes、100mmnacl、0.02%tween20,ph7.5)和2μldmso(0.5%,v/v)添加到300μl生物素化sars-cov-2spikerbd-his。使缓冲液中sars-cov-2spikerbd-his的浓度为75μg/ml。将400μlsars-cov-2spikerbd-his溶液等分为两个室,用于装载六个sa传感器。sa传感器的平衡时间设置为5分钟,加载时间设置为10分钟。然后,我们通过fortebiooctetred96测量了抗新冠病毒肽与sars-cov-2spikerbd的结合。使用基于双参考的方法进行实验。上述六个sars-cov-2尖峰rbd修饰的sa探针用作配体传感器,六个未经处理的sa探针用作参考传感器。测试的ace2肽模拟物22的浓度分别设置为0nm、125nm、250nm、500nm、1000nm和2000nm。我们使用的缓冲液由20mmhepes,100mmnacl,0.02%tween20,ph7.5和0.5%dmso组成。每个传感器将首先在缓冲液中平衡5分钟(基线),然后转移到样品中7分钟(结合),最后在缓冲液中解离7分钟(解离)。通过从0nm样品和未处理的sa传感器中减去背景信号,获得每个浓度的数据。最后测得抗新冠病毒肽与sars-cov-2spikerbd具有16nm,如图6所示。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1