一种高稳定强碱性多孔离子交换材料的制备方法
1.本发明属于高分子离子交换材料技术领域,具体涉及一种高稳定强碱性多孔离子交换材料的制备方法。
背景技术:
2.离子交换材料应用于水处理、电力行业、生物及化学药剂的分离纯化以及催化合成等领域。其中,阴离子交换树脂的应用尤为广泛。
3.阴离子交换树脂颗粒是由交联的具有三维空间立体网络结构的骨架构成,连接有许多较为活拨的不能自由移动的功能基团。这种功能基团能离解出离子,在使用或再生时可以与周围同电荷其它离子相互交换。因具有处理容量大,适用范围广,工作寿命长,运行费用低等诸多优点而被广泛应用于工业生产。
4.传统方法制备阴离子交换树脂,主要是将共聚物进行氯甲基化,再通过胺化反应获得。但是,在氯甲基化过程中使用的氯甲醚、二氯甲醚等试剂具有较强的致癌性,因此该方法在一定程度上受到限制。而且,由于阴离子交换树脂热稳定性较低,普通商业通用的强碱性阴离子交换树脂特别是氢氧型阴离子交换树脂的使用温度仅限于60℃以下,限制了强碱性阴离子交换树脂的应用范围。近年来以科学家们试图改变季铵基团与树脂骨架的连接方式以提高季铵基团的热稳定性。然而该方法并未从根本上改善材料的热稳定性。这些耐高温强碱性阴离子交换树脂的制备仍存在合成路线长、工艺复杂、操作条件苟刻、单体分离且收率低提纯困难、生产成本高等缺点,难以推广应用。同时,由于传统离子交换树脂的聚合链间会由于缠绕而形成离子位包夹,影响其离子交换容量;而且其缺乏永久孔道会导致吸附速率较为缓慢。
技术实现要素:
5.针对现有技术的缺陷和不足,本发明目的在于提供一种高稳定强碱性多孔离子交换材料的制备方法。
6.为实现上述发明目的,本发明提供以下技术方案:
7.一种高稳定强碱性多孔离子交换材料,以三氨基胍盐和2,5
‑
二甲氧基
‑
1,4
‑
苯二甲醛为反应单体,以酸为催化剂,用乙醇、1,4
‑
二氧六环等为溶剂反应得到目标材料。
8.本发明所述的一种高稳定强碱性多孔离子交换材料,其制备反应方程式如下:
[0009][0010]
本发明离子交换材料的结构式如下所示:
[0011][0012]
采用的聚合反应为酸催化的席夫碱形成反应。
[0013]
本发明所述的一种高比表面积、高稳定、强碱性多孔离子交换材料,其是由如下步骤所述方法制备得到:
[0014]
(1)将三氨基胍盐与醛基配体加入到装反应容器中,后依次向容器中加入反应溶剂和催化剂;
[0015]
(2)将步骤(1)中的反应液超声5~20min,保证溶液混合均匀,然后在氮气或氩气氛围和液氮下(77k)进行冷冻
‑
抽真空
‑
解冻操作,循环2~5次,在真空条件下将反应容器密封;
[0016]
(3)将步骤(2)密封的反应容器在80~150℃条件下反应2~7天;
[0017]
(4)将步骤(3)的反应容器(底部有棕黄色沉淀)冷却至室温后打开,真空过滤得到
红色固体。将红色固体用dmf,水,无水甲醇多次洗涤;随后用甲醇索氏提取数天,提取产物在80~200℃真空下干燥4~40小时,得到橙色固体。
[0018]
(5)将步骤(4)所得固体用1~5m koh溶液(或其他强碱溶液)进行离子交换1~10天,得到本发明所述的高稳定强碱性多孔离子交换材料。
[0019]
优选的,按摩尔比,三氨基胍盐:醛基配体=2:3。
[0020]
优选的,所述的洗涤方法为:将所得产物抽滤后,依次用二甲基甲酰胺(20~90℃)、水(20~100℃)、甲醇(20~50℃)分别洗涤3~5次。
[0021]
优选的,所述的纯化方法为:将洗涤后的所得物依次用四氢呋喃、二氯甲烷、甲醇索氏提取3~5次。
[0022]
优选的,所述的三氨基胍盐为三氨基胍盐酸盐。
[0023]
测试表明,本发明所得材料具有良好的稳定性和多孔性质,材料可以稳定在近200℃,孔道具有强碱性离子,bet比表面积可达到645.8m2/g。本发明材料可以在吸附、分离、催化等众多领域中得到应用。
[0024]
与现有离子交换树脂相比,本发明的有益效果是:
[0025]
(1)相比于普通商用强碱性阴离子交换树脂,本发明材料具有高热稳定性以及高化学稳定性。普通商用强碱性阴离子交换树脂特别是氢氧型阴离子交换树脂的使用温度仅限于60℃以下,限制了强碱性阴离子交换树脂的应用范围。而本发明所得材料可以在将近200℃的高温环境下使用,同时高的酸碱稳定性使得本发明材料可以在各种极端条件下使用而不会影响本产品性能,实现循环使用。
[0026]
(3)本发明相比于普通商用强碱性阴离子交换树脂,本发明材料为多孔材料,具有高比表面积,快速孔道传质,高离子容量等优势,使其在催化、吸附、分离、离子交换等领域有更好的工业化应用潜力。
[0027]
(2)值得一提的是,本发明采用廉价单体,获取方便,反应操作简单,可以一步获得,具有明显经济优势以及工业应用潜力。
附图说明
[0028]
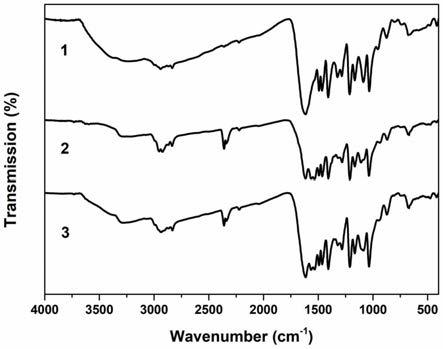
图1:本发明合成的高稳定强碱性多孔离子交换材料(图中曲线1)和12m氢氧化钠浸泡搅拌一周(图中曲线2)以及12m盐酸浸泡搅拌一周(图中曲线3)的红外谱图;
[0029]
图2:本发明合成的高稳定强碱多孔离子交换材料的碳固体核磁图;
[0030]
图3:本发明合成的高稳定强碱多孔离子交换材料的热重图;
[0031]
图4:本发明合成的高稳定强碱多孔离子交换材料(图中曲线1)和12m氢氧化钠浸泡搅拌一周(图中曲线2)以及12m盐酸浸泡搅拌一周(图中曲线3)的粉末衍射谱图;
[0032]
图5:本发明合成的高稳定强碱多孔离子交换材料的氮气吸附
‑
脱附等温线;
[0033]
图6:本发明合成的高稳定强碱多孔离子交换材料经12m盐酸处理一周的氮气吸附
‑
脱附等温线;
[0034]
图7:本发明合成的高稳定强碱多孔离子交换材料经12m氢氧化钠处理一周的氮气吸附
‑
脱附等温线;
[0035]
图8:本发明合成的高稳定强碱多孔离子交换材料的孔径分布图;
具体实施方式
[0036]
以下结合实施例,对本发明做进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不限定于本发明。
[0037]
实施例1
[0038]
首先将14.8mg(0.1mmol)三氨基胍盐酸盐、29.1mg(0.15mmol)2,5
‑
二甲氧基
‑
1,4
‑
苯二甲醛加入至10ml安瓶中;随后在安瓶中依次加入0.2ml三甲苯、0.2ml水、0.3ml乙醇以及0.2ml冰醋酸;将混合溶液超声10min;在氩气氛围和液氮下进行冷冻
‑
抽真空
‑
解冻操作,循环三次后,在真空条件下将安瓶密封;将密封安瓶放在120℃烘箱中反应3天。将混合物真空过滤得到红色固体,并依次用二甲基甲酰胺、水、甲醇多次洗涤。然后将固体粉末索氏提取,所得产物在120℃真空干燥12小时后,将其用koh或其他碱性溶液离子交换4天,洗涤后得到本发明产品。
[0039]
图1所示为本发明高稳定强碱性多孔离子交换材料与12m酸碱处理一周的红外谱图对比,1620cm
‑1位置的峰是席夫碱反应生成的
‑
c=n
‑
特征吸收峰,图中无反应单体
‑
nh2和
‑
cho特征吸收峰,证明聚合反应非常彻底。且酸碱处理一周后红外谱图均无变化,证明本发明产品具有高酸碱稳定性能。
[0040]
图2所示为本发明高稳定强碱多孔离子交换材料的碳固体核磁图,2,5
‑
二甲氧基
‑
1,4
‑
苯二甲醛中的
‑
cho碳峰位于190ppm,然而本发明材料在190ppm没有碳峰出现,证明聚合反应彻底。
[0041]
图3所示为本发明高稳定强碱多孔离子交换材料的热重图,热重分析表明本发明材料的热分解温度近200℃,表明其具有高稳定性。
[0042]
图4所示为本发明高稳定强碱性多孔离子交换材料以及12m酸碱处理一周的粉末衍射图,均有明显的衍射峰,酸碱处理一周后衍射峰无明显变化。
[0043]
图8所示为本发明高稳定强碱多孔离子交换材料的孔径分布图,本发明材料的主孔径在0.661nm处。
[0044]
实施例2
[0045]
改变上述实施例1中的反应溶剂,在实施例2中反应溶剂为1,4
‑
二氧六环,其它不
[0046]
变,获得与实施例1中所述相同材料,与实施例1所得到产品各性能基本一致。
[0047]
综上所述,本发明以三氨基胍盐和2,5
‑
二甲氧基
‑
1,4
‑
苯二甲醛为反应单体,在酸催化下合成了高稳定强碱性多孔离子交换材料。热重分析表明本发明材料具有良好热稳定性。通过氮气吸附和脱附曲线,得到本发明材料的bet比表面积达到645.8m2/g。通过粉末衍射仪测试酸碱浸泡搅拌一周的产品,发现本发明材料具有极高酸碱稳定性。
[0048]
图5所示为本发明高稳定强碱多孔离子交换材料的氮气吸附
‑
脱附等温线,计算得到本发明材料的bet比表面积为645.8m2/g。
[0049]
图6所示为本发明合成的高稳定强碱多孔离子交换材料经12m盐酸处理一周的氮气吸附
‑
脱附等温线,计算得到本发明材料的bet比表面积为454.4m2/g。
[0050]
图7所示为本发明合成的高稳定强碱多孔离子交换材料经12m氢氧化钠处理一周的氮气吸附
‑
脱附等温线,计算得到本发明材料的bet比表面积为310.5m2/g。
[0051]
以上所述,对于本领域的技术人员来说,可以根据本发明的技术方案和技术构思做出其它各种相应的改变和变形,而所有这些改变和变形均属于本发明后附的权利要求的
保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1