一种检测产毒微囊藻菌型的探针组合、芯片、试剂盒及方法与流程
1.本发明属于微生物检测技术领域,具体地,涉及一种检测产毒微囊藻菌型的探针组合、芯片、试剂盒及方法。
背景技术:
2.随着人类工业活动和社会经济的持续发展,湖泊因为富营养化而导致的藻类污染已经成为全球性的重大环境问题。水体富营养化主要指的是源于水中营养物质氮和磷的积累而导致的水体浮游生物迅速繁殖,水中溶解氧下降的现象。水体富营养化主要会带来三个方面的危害。首先是影响水体生态系统,当水体中营养物质过于丰富,引起藻类的过度繁殖,水面被藻类覆盖,从而影响下层水中生物的光合作用,同时死亡藻类被微生物分解也会消耗氧气,最终会导致水体缺氧,而影响水中其它生物的自然生长,破坏生态系统稳定,严重阻碍湖泊水产养殖业的发展。另一方面,水体富营养化后通常会伴随藻类的爆发,湖泊被覆盖上一层厚厚的绿膜,死去的水体生物又会发出难闻的气味,这一系列的变化会导致湖泊观赏程度降低,影响附近居民生活,阻碍社会旅游经济发展。最后,也是最重要的一点,富营养化的水体中使得大量可以产生毒素的藻类爆发生长,而被藻毒素污染的水源无论是直接作为饮用水,还是通过间接的水中水产食用,都可能会对人类生命健康造成巨大威胁。
3.在已知的富营养化水体中最为常见的产毒素藻类是微囊藻。微囊藻(microcystis),广泛分布于富营养湖泊,如滇池、太湖和巢湖等。微囊藻属产生的微囊藻毒素会造成人体的肝脏、神经系统和皮肤疾病,因而世界卫生组织明确规定饮用水中的微囊藻毒素不能超过1μg/l。微囊藻属是典型的有害藻属之一,该属菌株多样性很高,目前该属内已发现上百种菌株分属十个物种,不同菌株生活特性,是否产毒素也有所差别,因此对水体湖泊中的产毒微囊藻进行菌株水平长期精准检测对于藻毒素危害的监测和预警意义重大。
4.目前微囊藻的检测主要分为两种检测策略。一种是利用质谱仪根据微囊藻毒素特性直接检测水体中微囊藻毒素含量,从而判断水体是否被微囊藻污染。这种检测策略主要的劣势在于,只有当水体中已经被微囊藻严重污染且进入毒素释放阶段之后才能检测出,而早期微囊藻休眠阶段很难检出微囊藻污染。第二种策略是通过对微囊藻特定dna片段扩增测序的方式检测水体中是否含有微囊藻,包括针对微囊藻16s rrna片段和藻毒素功能基因片段的定量pcr检测方法。这种策略具有较好的早期微囊藻预警效果,但是对于微囊藻检出的分辨率不够,通常只能鉴定到属的水平,从而混淆了不同微囊藻菌株的产毒素差异。
5.基因芯片是由密集固定于玻片上的寡核苷酸探针组成,利用探针与荧光标记的样本dna进行碱基互补配对杂交,通过对杂交信号强弱的判读,可以完成对探针目标序列的检测。因为基因芯片的高通量,高敏感性特点,目前已经广泛应用于人类病原微生物检测中,但是将基因芯片技术应用于产毒微囊藻的检测,目前还未有报道。
技术实现要素:
6.为了解决上述技术问题中的至少一个,本发明采用的技术方案如下:
7.本发明第一方面提供本发明检测产毒微囊藻菌型的探针组合,所述探针组合包括检测产毒微囊藻菌型组合中各个产毒微囊藻菌型的探针,其中,所述检测产毒微囊藻菌型组合包括microcystis wesenbergii fachb
‑
929、microcystis aeruginosa fachb
‑
909、microcystis aeruginosa fachb
‑
911、microcystis aeruginosa fachb
‑
925、microcystis aeruginosa fachb
‑
975、microcystis aeruginosa fachb
‑
978、microcystis sp.fachb
‑
1005、microcystis sp.fachb
‑
1023、microcystis sp.fachb
‑
1026、microcystis sp.fachb
‑
1027和microcystis elabens fachb
‑
917中的至少两种。
8.微囊藻属(microcystis)是蓝藻门(cyanophyta)、色球藻纲(chroococcophyceae)、色球藻目(chroococcales)、色球藻科(chrococcaceae)的一属。又名多胞藻属。细胞呈球形,由多数细胞包在胶质物中形成不规则群体。微囊藻属大量繁殖时引起湖靛,并产生毒素,有害于水产养殖。
9.在本发明中,产毒微囊藻菌型是指同一种微囊藻菌的不同微囊藻菌产毒类型,在产毒方面存在较小差异的为同一菌型。在本发明中,定义上述11种菌型,若检测其中一种菌型的探针检测结果为阳性,则待测样本中存在该菌型的产毒微囊藻菌。
10.在本发明的一些实施方案中,所述检测产毒微囊藻菌型组合包括所述11种菌型中的3种、4种、5种、6种、7种、8种、9种、10种或全部11种。
11.在本发明的一些具体实施方案中,检测microcystis wesenbergii fachb
‑
929菌型的探针选自seq id no.1~47所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
909菌型的探针选自seq id no.48~87所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
911菌型的探针选自seq id no.88~132所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
925菌型的探针选自seq id no.133
‑
161所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
975菌型的探针选自seq id no.162~205所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
978菌型的探针选自seq id no.206~241所示探针中的至少一个;检测microcystis sp.fachb
‑
1005菌型的探针选自seq id no.242~283所示探针中的至少一个;检测microcystis sp.fachb
‑
1023菌型的探针选自seq id no.284~327所示探针中的至少一个;检测microcystis sp.fachb
‑
1026菌型的探针选自seq id no.328~387所示探针中的至少一个;检测microcystis sp.fachb
‑
1027菌型的探针选自seq id no.388~451所示探针中的至少一个;检测microcystis elabens fachb
‑
917菌型的探针选自seq id no.452~504所示探针中的至少一个。
12.本发明第二方面提供本发明第一方面任一所述的探针组合在制备用于检测产毒微囊藻菌型的基因芯片或试剂盒中的应用。
13.本发明第三方面提供一种检测产毒微囊藻菌型的基因芯片,所述基因芯片包括权利要求1所述的探针组合。
14.进一步地,所述基因芯片还包括有阴性对照探针。在本发明的一些优选实施方案中,所述阴性对照探针的核苷酸序列如seq id no.506所示。
15.进一步地,所述基因芯片还包括全局质控探针。在本发明的一些优选实施方案中,所述全局质控探针的核苷酸序列如seq id no.507所示。
16.进一步地,所述基因芯片还包括阳性对照探针。在本发明的一些优选实施方案中,所述阳性对照探针的核苷酸序列如seq id no.505所示。
17.本发明第四方面提供一种检测产毒微囊藻菌型的试剂盒,其特征在于,所述试剂盒包括本发明第一方面任一所述的探针组合或本发明第三方面任一所述的基因芯片。
18.进一步地,所述试剂盒还包括待测样本基因组dna提取试剂。
19.更进一步地,所述试剂盒还包括核酸扩增试剂和荧光标记试剂。
20.更进一步地,所述试剂盒还包括纯化试剂。
21.本发明第五方面提供一种检测产毒微囊藻菌型的方法,包括以下步骤:
22.s1,获取待测样本的基因组dna;
23.s2,对获取的基因组dna进行核酸扩增、荧光标记并进行纯化;
24.s3,利用本发明第三方面任一所述的基因芯片进行杂交检测;
25.s4,根据检测到的探针信号判断检测结果。
26.在本发明的一些实施方案如此,步骤s1中,可使用本领域常规方法进行核酸提取,进行所述获取待测样本的基因组dna。
27.在本发明的一些实施方案中,步骤s2中,所述核酸扩增为非特异性随机扩增;使用cyanine3
‑
dutp进行荧光标记。
28.在本发明的一些实施方案中,步骤s3的基因芯片包括检测microcystis wesenbergii fachb
‑
929、microcystis aeruginosa fachb
‑
909、microcystis aeruginosa fachb
‑
911、microcystis aeruginosa fachb
‑
925、microcystis aeruginosa fachb
‑
975、microcystis aeruginosa fachb
‑
978、microcystis sp.fachb
‑
1005、microcystis sp.fachb
‑
1023、microcystis sp.fachb
‑
1026、microcystis sp.fachb
‑
1027和microcystis elabens fachb
‑
917中的至少两种产毒微囊藻菌型的探针,还包括阴性对照探针、全局质控探针和阳性对照探针。
29.在本发明的一些实施方案中,检测microcystis wesenbergii fachb
‑
929菌型的探针选自seq id no.1~47所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
909菌型的探针选自seq id no.48~87所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
911菌型的探针选自seq id no.88~132所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
925菌型的探针选自seq id no.133
‑
161所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
975菌型的探针选自seq id no.162~205所示探针中的至少一个;检测microcystis aeruginosa fachb
‑
978菌型的探针选自seq id no.206~241所示探针中的至少一个;检测microcystis sp.fachb
‑
1005菌型的探针选自seq id no.242~283所示探针中的至少一个;检测microcystis sp.fachb
‑
1023菌型的探针选自seq id no.284~327所示探针中的至少一个;检测microcystis sp.fachb
‑
1026菌型的探针选自seq id no.328~387所示探针中的至少一个;检测microcystis sp.fachb
‑
1027菌型的探针选自seq id no.388~451所示探针中的至少一个;检测microcystis elabens fachb
‑
917菌型的探针选自seq id no.452~504所示探针中的至少一个。
30.任选地,所述阴性对照探针的核苷酸序列如seq id no.506所示,任选地,所述全局质控探针的核苷酸序列如seq id no.507所示,任选地,所述阳性对照探针的核苷酸序列如seq id no.505所示。
31.进一步地,步骤s4的步骤为:
32.s41,扫描及特征提取:清洗后的芯片使用安捷伦芯片扫描仪在multi
‑
tiff模式下进行扫描,得到芯片特征数据,接着使用特征提取软件提取信号特征,得到探针信号特征数据;
33.s42,数据质检:对上一步的探针信号特征数据进行质检,设置信号检出阈值为100,若:a)所有阴性对照探针均未检出(荧光信号值均低于阈值);b)检出了50%以上的阳性对照探针;c)所有全局质控探针均检出,且均未出现信号过饱和,则本次检测数据质检合格;
34.s43,探针信号判断:首先对所有探针的探针信号值进行杂交置信度筛选,将置信度较低的探针杂交荧光信号删除,得到具有合格信号值的探针数目或比例;对于某一种菌型在待测样本中被检出的检测标准为:检测该菌型的探针中具有合格信号值的探针至少有一个或检测该菌型的全部探针中具有合格信号值的探针的比例高于阈值。
35.在本发明的一些实施方案中,而判断一个探针是否具有合格信号值,主要通过对杂交位点图像内全部包含的像素点荧光值进行统计分析判断得出。
36.在本发明的一些具体实施方案中,探针信号值是否合格的判断步骤包括:
37.①
探针信号信噪比筛选:信噪比大于2,单个探针信号值减去背景值,再除以背景值的标准差,结果大于2的探针信号判断为合格信号;
38.②
探针信号信倍比筛选:信背比大于2,单个探针信号值除以背景信号值,结果大于2的探针信号判断为合格信号。
39.在本发明的一些优选实施方案中,所述阈值为50%、60%、70%或80%。
40.在本发明中,所述待测样本可以来源为任意水源,包括但不限于江、河、溪、海、湖、泊、水库、池塘等任意流动的或不流动的水源。
41.本发明的有益效果
42.相对于现有技术,本发明具有以下有益效果:
43.1.现有的产毒微囊藻分子检测技术大都将检测目标区域限定在16s rrna核糖体基因,或者微囊藻毒素基因区域,因为目标检测区域较小因此分辨率较低,无法鉴定到种以及以下水平。本发明通过基因芯片技术,利用全基因组范围内菌株特异探针,可以对菌株水平的产毒微囊藻进行检测,弥补了现有检测技术分辨率不够的缺陷。
44.2.本发明利用基因芯片技术,可以同时对11种常见产毒微囊藻菌株在水体中的存在进行检测。且该检测方法操作方法简单,相比较于基于测序的检测方法省去了目标区域pcr和测序的步骤,同时数据处理更为简单便捷。这种高通量,高分辨率的便捷产毒微囊藻菌株检测方法对于水体危害蓝藻污染的长期动态监测具有重要应用价值,可指导藻华控制和水生态修复。
附图说明
45.图1示出了目标菌株与非目标菌株在模拟样本中的显著荧光探针比率分布,图中虚线代表菌株判定标准,比率高于60%的菌株可被判定为检出。
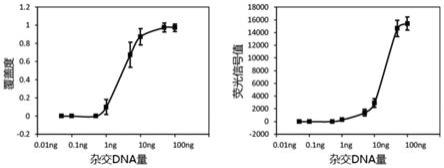
46.图2示出了不同杂交dna总量梯度下目标产毒微囊藻的检出效果。
具体实施方式
47.除非另有说明、从上下文暗示或属于现有技术的惯例,否则本技术中所有的份数和百分比都基于重量,且所用的测试和表征方法都是与本技术的提交日期同步的。在适用的情况下,本技术中涉及的任何专利、专利申请或公开的内容全部结合于此作为参考,且其等价的同族专利也引入作为参考,特别这些文献所披露的关于本领域中的合成技术、产物和加工设计、聚合物、共聚单体、引发剂或催化剂等的定义。如果现有技术中披露的具体术语的定义与本技术中提供的任何定义不一致,则以本技术中提供的术语定义为准。
48.本技术中的数字范围是近似值,因此除非另有说明,否则其可包括范围以外的数值。数值范围包括以1个单位增加的从下限值到上限值的所有数值,条件是在任意较低值与任意较高值之间存在至少2个单位的间隔。例如,如果记载组分、物理或其它性质(如分子量,熔体指数等)是100至1000,意味着明确列举了所有的单个数值,例如100,101,102等,以及所有的子范围,例如100到166,155到170,198到200等。对于包含小于1的数值或者包含大于1的分数(例如1.1,1.5等)的范围,则适当地将1个单位看作0.0001,0.001,0.01或者0.1。对于包含小于10(例如1到5)的个位数的范围,通常将1个单位看作0.1。这些仅仅是想要表达的内容的具体示例,并且所列举的最低值与最高值之间的数值的所有可能的组合都被认为清楚记载在本技术中。
49.关于化学化合物使用时,除非明确地说明,否则单数包括所有的异构形式,反之亦然(例如,“己烷”单独地或共同地包括己烷的全部异构体)。另外,除非明确地说明,否则用“一个”,“一种”或“该”形容的名词也包括其复数形式。
50.术语“包含”,“包括”,“具有”以及它们的派生词不排除任何其它的组分、步骤或过程的存在,且与这些其它的组分、步骤或过程是否在本技术中披露无关。为消除任何疑问,除非明确说明,否则本技术中所有使用术语“包含”,“包括”,或“具有”的组合物可以包含任何附加的添加剂、辅料或化合物。相反,出来对操作性能所必要的那些,术语“基本上由
……
组成”将任何其他组分、步骤或过程排除在任何该术语下文叙述的范围之外。术语“由
……
组成”不包括未具体描述或列出的任何组分、步骤或过程。除非明确说明,否则术语“或”指列出的单独成员或其任何组合。
51.为了使本发明所解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。
52.实施例
53.以下例子在此用于示范本发明的优选实施方案。本领域内的技术人员会明白,下述例子中披露的技术代表发明人发现的可以用于实施本发明的技术,因此可以视为实施本发明的优选方案。但是本领域内的技术人员根据本说明书应该明白,这里所公开的特定实施例可以做很多修改,仍然能得到相同的或者类似的结果,而非背离本发明的精神或范围。
54.除非另有定义,所有在此使用的技术和科学的术语,和本发明所属领域内的技术人员所通常理解的意思相同,在此公开引用及他们引用的材料都将以引用的方式被并入。
55.那些本领域内的技术人员将意识到或者通过常规试验就能了解许多这里所描述的发明的特定实施方案的许多等同技术。这些等同将被包含在权利要求书中。
56.下述实施例中未作具体说明的分子生物学实验方法,均按照《分子克隆实验指南》(第四版)(j.萨姆布鲁克、m.r.格林,2017)一书中所列的具体方法进行,或者按照试剂盒和
产品说明书进行。其他实验方法,如无特殊说明,均为常规方法。下述实施例中所用的仪器设备,如无特殊说明,均为实验室常规仪器设备;下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。
57.实施例1产毒微囊藻菌型特异性检测探针筛选
58.本实施例利用11种菌株的基因组序列进行探针设计。11种菌株包括microcystis wesenbergii fachb
‑
929、microcystis aeruginosa fachb
‑
909、microcystis aeruginosa fachb
‑
911、microcystis aeruginosa fachb
‑
925、microcystis aeruginosa fachb
‑
975、microcystis aeruginosa fachb
‑
978、microcystis sp.fachb
‑
1005、microcystis sp.fachb
‑
1023、microcystis sp.fachb
‑
1026、microcystis sp.fachb
‑
1027和microcystis elabens fachb
‑
917。11种菌株均来源于中国科学院淡水藻种库(freshwater algae culture collection at the institute of hydrobiology,fachb),全部获得了基因组序列。
59.下面为利用产毒微囊藻菌株microcystis wesenbergii fachb
‑
929的基因组序列(gca_014698625.1)设计microcystis wesenbergii fachb
‑
929产毒菌型的特异性检测探针的过程。
60.1.数据集收集:
61.为设计microcystis wesenbergii fachb
‑
929产毒菌型的特异性探针,准备的数据主要包括两个部分,产毒微囊藻菌株microcystis wesenbergii fachb
‑
929的基因组序列和背景基因组序列。
62.在本实施例中,以ncbi数据库中全部的2531个其它(截止到2021年3月12日的数据)的蓝藻基因组序列被设定为背景序列。
63.2.特异性探针初步挑选:
64.将2531个蓝藻基因组序列全部打断成50mer长度的kmer片段,并建立背景序列kmer片段hash库,记录kmer的出现频率和所归属菌株信息。再建立微囊藻菌株microcystis wesenbergii fachb
‑
929基因组序列的kmer片段(50mer长度)hash库。将目标序列kmer库与背景序列的kmer库进行比较分析,将只存在于目标序列kmer库中而没有出现在背景序列kmer库中的kmer挑选出来,作为该菌株的备选特异探针库。
65.3.备选特异探针中潜在非特异结合探针的剔除:
66.如果探针与非目标序列有超过20个碱基的连续匹配,可能发生潜在的非特异结合。利用ncbi的blast程序,将备选特异探针与背景kmer库进行序列比对,根据比对结果,将备选特异探针中与背景kmer有超过20个碱基连续匹配的探针剔除。
67.4.探针理化性质筛选:
68.上步结束后共得到253条microcystis wesenbergii fachb
‑
929菌株特异探针,这些探针序列唯一的存在于该菌株基因组中,且与其它的菌株基因组没有超过20个连续碱基的匹配。随后对剩余特异探针进行理化性质筛选,主要条件包括:
69.(1)探针序列与目标序列的核酸自由能(free energy,单位kcal/mol),如核酸自由能小于
‑
30,则去除该探针序列。
70.(2)若探针的连续相同碱基出现5次,那么该探针的复杂度太低,去除该探针序列。
71.(3)根据熔解温度tm值(65<tm<95)和gc含量(0.2<gc含量<0.8)进行菌株特异探针
的最后筛选。
72.最终,设计得到47个分布于microcystis wesenbergii fachb
‑
929全基因组范围内的特异探针。如表1所示:
73.表1 microcystis wesenbergii fachb
‑
929产毒菌型特异性探针
[0074][0075]
实施例2产毒微囊藻特异检测基因芯片制备
[0076]
利用实施例的方法,分别利用microcystis aeruginosa fachb
‑
909、microcystis aeruginosa fachb
‑
911、microcystis aeruginosa fachb
‑
925、microcystis aeruginosa fachb
‑
975、microcystis aeruginosa fachb
‑
978、microcystis sp.fachb
‑
1005、microcystis sp.fachb
‑
1023、microcystis sp.fachb
‑
1026、microcystis sp.fachb
‑
1027和microcystis elabens fachb
‑
917的基因组序列设计探针,结果如表2所示。
[0077]
表2 10种产毒菌型的特异性探针
[0078]
[0079]
[0080]
[0081]
[0082]
[0083]
[0084]
[0085]
[0086]
[0087][0088]
由此,设计出的探针数目如表3:
[0089]
表3各产毒菌型对应的探针
[0090]
产毒菌型探针数目seq id no.microcystis wesenbergii fachb
‑
929471~47microcystis aeruginosa fachb
‑
9094048~87microcystis aeruginosa fachb
‑
9114588~132microcystis aeruginosa fachb
‑
92529133~161microcystis aeruginosa fachb
‑
97544162~205microcystis aeruginosa fachb
‑
97836206~241microcystis sp.fachb
‑
100542242~283microcystis sp.fachb
‑
102344284~327microcystis sp.fachb
‑
102660328~387microcystis sp.fachb
‑
102764388~451microcystis elabens fachb
‑
91753452~504
[0091]
阳性和阴性对照探针及全局质控探针的设计:
[0092]
阳性探针序列(seq id no.505):
[0093]
gcgctcgttgcgggacttaacccaacacctcacggcacgagctgacgaca
[0094]
阴性对照探针序列(seq id no.506):
[0095]
gacctgataaagcgcaaccgataactaaagagggcagatataatatctgt
[0096]
全局质控探针序列(seq id no.507):
[0097]
tgagcatgaggtcgcgttgattaatcccgaaggtcaactggcggatttct
[0098]
探针序列设计方法:均为人工合成序列,且这三个探针与目前已知微生物序列无杂交亲和性。
[0099]
将设计的全部特异性探针委托安捷伦(agilent)公司合成。
[0100]
同时,将上述特异性探针进行不同组合制备成不同基因芯片,例如选择11种菌型中的甚至一种或几种,根据选择出来的菌型,再分别对应选择一种或多种探针,并制成基因芯片。如此,可以制备大量不同的基因芯片。
[0101]
对照探针和全局质控探针排布方式:随机分布于检测探针之间;
[0102]
对照探针和全局质控探针数量:对照探针与质控探针为40条重复探针随机排布在芯片上。
[0103]
在本实施例中,制备如下基因芯片:
[0104]
基因芯片#1,包括的探针如表4所示:
[0105]
表4基因芯片#1探针信息
[0106]
产毒菌型探针数目seq id no.microcystis aeruginosa fachb
‑
9111089、91、93、95、102、104、110、115、119、123microcystis sp.fachb
‑
102310286、289、290、296、299、301、308、314、319、323microcystis elabens fachb
‑
91710455、459、462、468、473、481、485、489、493、500
[0107]
基因芯片#2,包括的探针如表5所示:
[0108]
表5基因芯片#2探针信息
[0109]
产毒菌型探针数目seq id no.microcystis wesenbergii fachb
‑
92953、8、14、29、38microcystis aeruginosa fachb
‑
9755168、171、174、188、194microcystis sp.fachb
‑
10055245、254、253、278、281microcystis sp.fachb
‑
10235288、291、298、305、314microcystis sp.fachb
‑
10265328、330、343、356、377
[0110]
基因芯片#3,包括的探针如表6所示:
[0111]
表6基因芯片#3探针信息
[0112]
产毒菌型探针数目seq id no.microcystis wesenbergii fachb
‑
929471~47microcystis aeruginosa fachb
‑
9114588~132microcystis aeruginosa fachb
‑
97544162~205microcystis aeruginosa fachb
‑
97836206~241microcystis sp.fachb
‑
102660328~387microcystis elabens fachb
‑
91753452~504
[0113]
基因芯片#4,包括的探针如表7所示:
[0114]
表7基因芯片#4探针信息
[0115][0116]
基因芯片#5,包括的探针如表8所示:
[0117]
表8基因芯片#5探针信息
[0118][0119][0120]
实施例3利用实施例2制备的基因芯片快速检测常见水体产毒微囊藻产毒菌型的方法
[0121]
1.目标样本dna提取
[0122]
采集湖泊或者河流中的水体并通过滤膜过滤对蓝藻进行富集,以富集物作为待测样本,随后,使用agilent cgh microarray的dna提取试剂盒进行待测样本核酸提取,也可以使用其他本领域常规方法进行待测样本核酸提取。
[0123]
2.dna纯化
[0124]
dna纯化主要步骤为:
[0125]
(1)取500ng提取得到的dna样品于打断管中,补足h2o至50μl。设置打断时间为90s;
[0126]
(2)预先室温平衡onepure magbeads 30min,并充分振荡混匀,确保无明显磁珠沉淀;
[0127]
(3)向低吸附管/八联管中加入60μl onepure magbeads(1.2
×
),再加入步骤(1)的打断产物,涡旋混匀,瞬离收集管壁液体,室温静置5min;
[0128]
(4)将低吸附管或八联管放在磁力架上,待管中溶液澄清,弃去上清液;
[0129]
(5)向1.5ml低吸附管或八联管中加入200μl 80%新鲜配制的乙醇,静置30s后弃去上清液,重复操作步骤,直至上清去除较为干净;
[0130]
(6)将低吸附管或八联管置于磁力架上,室温静置1到2min至磁珠干裂或将管子开
盖放于45℃金属浴上,待磁珠表面无水光干裂,管底无乙醇残留;
[0131]
(7)将离心管从磁力架上移开,并加入15μl温育好的nuclease
‑
free water重悬磁珠,涡旋或吹打混匀后,瞬离收集管壁液体,室温放置3min;
[0132]
(8)将低吸附管或八联管放在磁力架上,待管中溶液澄清,转移13μl上清液到新的pcr管中,用于下一步标记。
[0133]
3.dna荧光标记
[0134]
本实施例使用agilent suretag complete dna labeling kit试剂盒,包括以下步骤:
[0135]
(1)向打断后纯化好的gdna中加入2.5μl random primer mix,混匀后,进行如下变性反应:98℃3min、4℃hold;
[0136]
(2)向上述变性反应体系(13μl gdna和2.5μl random primer mix)中直接加入以下试剂:5μl 5
×
reaction buffer、2.5μl 10
×
dntp、1.5μl cyanine 3
‑
dutp、0.5μl exo(
‑
)klenow,共25μl;
[0137]
(3)使用移液枪吹打或涡旋振荡混匀后,快速离心收集管壁上的液体,去除气泡;
[0138]
(4)将反应体系置于pcr仪上,设置热盖温度为75℃,并运行以下程序:37℃2h、65℃10min、4℃hold。
[0139]
4.目标样本荧光dna与实施例3制备的基因芯片进行杂交
[0140]
本实施例使用agilent oligo acgh/chip
‑
on
‑
chip hybridization kit试剂盒,包括以下步骤:
[0141]
(1)将纯化后的样品提及浓缩至14.3μl,并按表9配置杂交体系好后,用枪吹打混匀,瞬离后将反应体系置于pcr仪上,设置热盖温度为105℃,并运行以下程序:98℃3min、37℃30min、37℃hold;
[0142]
(2)杂交:
[0143]
a.首先将一个干净的垫片放入安捷伦chamber里面,垫片标签朝上,与chamber底部的矩形部分对准,确保垫圈与腔室底座齐平;
[0144]
b.然后吸取上一步37℃的样品55μl到垫片上的橡胶圈中间,避免产生气泡,将芯片倒扣在垫片上;
[0145]
c.接着将chamber盖子盖上去,拧紧旋钮;
[0146]
d.将每个组装好的装置装入恒温箱旋转架,取一个配平的chamber,垂直旋转杂交室,使载玻片湿润,并评估气泡的流动性。
[0147]
e.设置杂交旋转器旋转速度为20rpm,67℃杂交4h。
[0148]
(3)芯片清洗:杂交后在室温下取出芯片,放在洗液1(agilent试剂盒的试剂)中,设置250rpm,在室温下震荡清洗5min;接着再用洗液2(agilent试剂盒的试剂),设置200rpm,在39℃下震荡清洗1min,最后去除芯片表面的液体,并在4h内扫描。
[0149]
表9实施例3中的杂交体系表
[0150]
[0151][0152]
5.荧光结果扫描与信号分析
[0153]
(1)扫描及特征提取:清洗后的芯片使用安捷芯片扫描仪在multi
‑
tiff模式下进行扫描,得到芯片特征数据(tiff图片格式),接着使用特征提取软件(agilent feature extraction)v12.1从tiff文件中提取信号特征,得到探针信号特征数据;
[0154]
(2)数据质检:对上一步的探针信号特征数据进行质检,设置信号检出阈值为100,若a)所有阴性对照探针均未检出(荧光信号值均低于阈值);b)检出了50%以上的阳性对照探针;c)所有全局质控探针均检出,且均未出现信号过饱和,则本次实验数据质检合格。
[0155]
(3)信号解读:为了避免杂交实验中一些非特异探针信号的干扰,利用以下步骤实现对芯片探针信号的解读。首先对所有的探针信号进行杂交置信度筛选,将置信度较低的探针杂交荧光信号删除。而判断一个杂交位点的信号是否合格,主要通过对杂交位点图像内全部包含的像素点荧光值进行统计分析判断得出。随后,对于某一种菌型检出的检测标准为,检测该菌型的全部特异探针中至少有1个具有合格信号值。探针信号分析步骤主要包括:
[0156]
①
探针信号信噪比筛选。信噪比(单个探针管道中荧光目标信号与荧光噪音信号的比值)大于2,单个探针信号值减去背景值,再除以背景值的标准差,结果大于2的探针信号判断为合格信号。
[0157]
②
探针信号信倍比筛选。信背比(单个探针管道中荧光目标信号与荧光背景信号的比值)大于2,单个探针信号值除以背景信号值,结果大于2的探针信号判断为合格信号。
[0158]
③
探针信号合格率筛选。统计某一种菌型具有合格探针信号的个数或比例。
[0159]
④
检测结果判定:对于某一种菌型检出的检测标准为:如果针对该菌型的特性性探针有至少1个探针具有合格探针信号值或具有合格探针信号值的比例大于某个阈值,如50%、60%、70%或80%,那么该产毒微囊藻菌型被检测存在于目标水体中。
[0160]
实施例4检测产毒微囊藻产毒菌型的基因芯片的特异性测试
[0161]
特异性指的是,对于目标的菌株可以针对性的检测在水体样本中的有无。为了测试发明人设计的探针与基因芯片的特异检出效果,发明人产毒微囊藻菌株进行多组合混合,利用本发明方法对混合菌液进行检测,比较检测结果与实验选定组合设计之间的一致性,并分析检测结果的假阳性和假阴性比率。
[0162]
发明人从中国科学院淡水藻种库(freshwater algae culture collection at the institute of hydrobiology,fachb)获得11种微囊藻产毒菌株,将11种菌株的菌液进
行多种组合混合(混合所用每一种单菌的dna总量为30ng),一共设计出6种模拟样本,每种模拟样本包含三个重复(表10)。
[0163]
表10模拟样本的纯菌组合
[0164]
产毒微囊藻菌株模拟样本1模拟样本2模拟样本3模拟样本4模拟样本5模拟样本6microcystis aeruginosa fachb
‑
909√
×××××
microcystis aeruginosa fachb
‑
911√√
××××
microcystis aeruginosa fachb
‑
925√√√
×××
microcystis aeruginosa fachb
‑
975√√√√
××
microcystis aeruginosa fachb
‑
978√√√√√
×
microcystis sp.fachb
‑
1005
×
√√√√√microcystis sp.fachb
‑
1023
××
√√√√microcystis sp.fachb
‑
1026
×××
√√√microcystis sp.fachb
‑
1027
××××
√√microcystis elabens fachb
‑
917
×××××
√microcystis wesenbergii fachb
‑
929
×××××
√
[0165]
发明人利用实施例2制备的基因芯片#5通过实施例3的方法对上述6个模拟样本进行检测。
[0166]
检测结果显示,所有6个模拟样本中的目标菌株的探针组中具有显著荧光信号的探针比例都大于60%,而非目标菌株的该比例都小于60%(图1)。以探针组点亮探针比例大于60%作为菌株检出标准,所有模拟样本检出微囊藻菌株与实际添加的菌株相吻合,假阳性和假阴性的比例都为0(表11)。
[0167]
表11模拟样本检出结果
[0168]
产毒微囊藻菌株模拟样本1模拟样本2模拟样本3模拟样本4模拟样本5模拟样本6microcystis aeruginosa fachb
‑
909+
‑‑‑‑‑
microcystis aeruginosa fachb
‑
911++
‑‑‑‑
microcystis aeruginosa fachb
‑
925+++
‑‑‑
microcystis aeruginosa fachb
‑
975++++
‑‑
microcystis aeruginosa fachb
‑
978+++++
‑
microcystis sp.fachb
‑
1005
‑
+++++microcystis sp.fachb
‑
1023
‑‑
++++microcystis sp.fachb
‑
1026
‑‑‑
+++microcystis sp.fachb
‑
1027
‑‑‑‑
++microcystis elabens fachb
‑
917
‑‑‑‑‑
+microcystis wesenbergii fachb
‑
929
‑‑‑‑‑
+样本检测准确率100%100%100%100%100%100%样本检测假阴性0%0%0%0%0%0%样本检测假阳性0%0%0%0%0%0%
[0169]
以上结果证实了本发明的探针和基因芯片以及检测方法具有可靠的微囊藻菌株水平检测效果。
[0170]
实施例5对目标产毒微囊藻的最低检测限度
[0171]
为了检验本发明检测方法对于环境中极低浓度的微囊藻菌株是否具有检出能力,设计了浓度梯度检出试验。具体的方案为,选择随机挑选三种微囊藻菌株,每一种菌株分别提取dna,并选取总量为0.1、0.5、1、5、10、50和100ng的dna与实施例2基因芯片#5进行荧光杂交实验,实验步骤与实施例3相同。比较在不同的dna总量下,目标菌型具有显著荧光信号
探针占据该菌型探针组比例以及对应的探针荧光信号均值。
[0172]
如图2,结果表明,当体系中的目标菌株dna总量达到5ng以及以上,菌株特异探针组中的阳性探针结果就会大于60%,可以通过判定条件,被判定为成功检出。
[0173]
以上结果证实,利用本发明的探针和基因芯片以及检测方法,在水体中含有微量目标产毒微囊藻时,依然具有良好的检出能力。
[0174]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1