一种莫那比拉韦的制备工艺的制作方法
1.本发明具体涉及一种改进的莫那比拉韦(mk-4482,以前称为eidd-2801)制备工艺。莫那比拉韦是一种口服活性抗病毒剂,目前正在进行其治疗新冠肺炎感染方面的研究。
背景技术:
2.莫那比拉韦的化学名是[(2r,3s,4r,5r)-3,4-二羟基-5-[4-(羟氨基)-2-氧代嘧啶-1-基]氧代-2-基]甲基2-甲基丙酸甲酯,具有式i所示结构:
[0003][0004]
莫那比拉韦由埃默里大学发现,目前该大学正与ridgeback biotherapeutics公司和merck&co.公司合作进行临床研发。
[0005]
据报道,莫那比拉韦的第一条合成路线使用尿苷作为起始物料,这种材料价格昂贵且供应有限[wo2019113462;wo2019173602]。此外,该路线所得产率较低。与尿苷相比,胞苷的价格较低,而且胞苷与羟胺能直接转氨。因此,已经报道了基于胞苷的新路线(方案1和2)。
[0006][0007]
方案1公开了使用novozyme 435(固定化南极假丝酵母脂肪酶b)选择性地将胞苷的伯醇与异丁酰基丙酮肟酯进行酯化。然后,胞苷酯与硫酸羟胺反应,得到莫那比拉韦(chem.commun.,2020年,第56期,13363-13364)。由于使用固定化酶,该方案成本非常高。此外,尽管使用了酶,在第一阶段还是会产生一定量的二酯和三酯杂质,在第二阶段则观察到部分脱氨。这两个阶段均需要通过柱色谱法进行纯化。
[0008]
方案2采用化学方法选择性酯化胞苷的伯醇,以替代酶系统。
[0009][0010]
胞苷与丙酮、硫酸和2,2-二甲氧基丙烷反应,得到2',3'-o-异亚丙基胞苷硫酸盐。加入1.8-二氮杂双环[5.4.0]十一碳-7-烯(dbu)和催化量的4-二甲基氨基吡啶(dmap),在乙腈中与异丁酸酐反应。所得胞苷缩丙酮酯与硫酸羟胺在70%ipa(kf滴定24%的水)中反应,随后用甲酸将缩丙酮脱保护,得到莫那比拉韦。用柱纯化法分离最终产物,产率为64%。或者,可通过用硫酸羟胺在40%的ipa(60%的水)中处理更长时间,一步完成羟胺化和缩丙酮脱保护,将胞苷缩丙酮酯直接转化为莫那比拉韦。然而,这使得大量酯被水解,形成约20%的n-羟基胞苷副产物(synlett.,2021年,第32(3)期,326-328)。
[0011]
方案2的另一个主要缺点是,我们观察到在采用甲酸进行缩丙酮脱保护时,反应过程中会释放出一氧化碳。一些使用甲酸进行缩丙酮的脱保护的文献中(wo2019113462;wo2019173602;wo2016/106050a1)也明确提到,甲酸是一氧化碳的来源,仅将其储存较长时间就会释放一氧化碳(容器需经常通风)。
[0012]
因此,这两种基于胞苷的方案都有一定的缺点,需要一种更安全的替代工艺。
技术实现要素:
[0013]
本发明在研究通过加入碱使2',3'-o-异亚丙基胞苷硫酸盐(ii)与丁酸酐酯化时,发现除了5'-异丁酰基胞苷缩丙酮(式iii)外,由于胞苷的氨基发生交叉反应,还形成了约8%的酰胺副产物(杂质-1)(方案3)。
[0014]
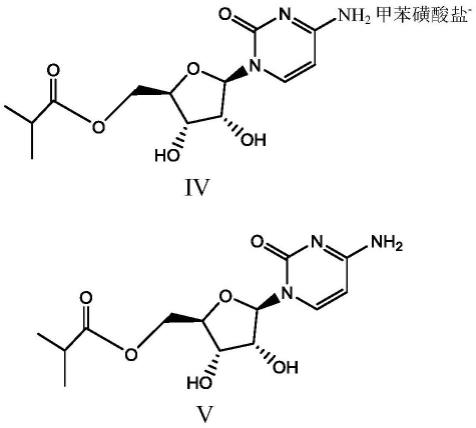
在不使用柱色谱法的情况下,本发明研究了各种酸的成盐,获得了一种纯化方法。当使用作为一水合物的对甲苯磺酸(ptsa)进行成盐时,除了获得不含酰胺杂质的纯盐外,还观察到缩丙酮基团的脱保护,并直接获得了5'-异丁酰基胞苷对甲苯磺酸盐(式iv)(方案3)。
[0015]
而采用共沸ptsa虽然能形成甲苯磺酸盐,但不能水解缩丙酮基团,这一事实进一步证明了结晶水的重要性。
[0016]
同样令人惊喜的是,酸中存在的结晶水只水解缩丙酮基团,而不影响分子中存在的异丁烯酯基团。
[0017]
然后,将对甲苯磺酸盐(式iv)转化为5-异丁酰基胞苷游离碱(式v),再与羟胺反应后得到莫那比拉韦(式i)。
[0018][0019]
本发明的有益效果:
[0020]
本工艺的主要优点在于避免了采用作为一氧化碳来源的甲酸进行缩丙酮脱保护,并且不使用柱色谱法就能实现纯化。
具体实施方式
[0021]
本发明提供了一种制备莫那比拉韦的新工艺,包括以下步骤:
[0022]
a、加入非亲核碱,使具有式ii结构的2',3'-o-异亚丙基胞苷硫酸盐在室温下与溶剂中的异丁酸酐反应,得到式iii结构的5-异丁酸酯和作为杂质-1的n-异丁酸酰胺;
[0023]
[0024][0025]
b、将步骤a得到的反应产物与对甲苯磺酸一水合物反应,得到5'-异丁酰基胞苷酸对甲苯磺酸盐(式iv),该盐不含n-异丁酸酰胺杂质;
[0026][0027]
c、将5'-异丁酰基胞苷酸盐(式iv)转化为其游离碱(式v),再使游离碱与羟胺反应,得到莫那比拉韦(式i)。
[0028]
所需起始物料,即式(ii)的2',3'-o-异亚丙基胞苷硫酸盐,可通过synlett(2021),32(3),326-328中所述的方法制备。
[0029]
加入非亲核碱,通过2',3'-o-异亚丙基胞苷硫酸盐(式ii)与异丁酸酐的酯化反应得到异丁酸酯(式iii)。该反应可在室温下在乙腈中进行。可使用的非亲核碱有:三乙胺、二异丙基乙胺(dipea)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(dbu)、n-甲基吗啉(nmm)和1,4-二氮杂双环-[2.2.2]辛烷(dabco)。加入催化量的4-二甲基氨基吡啶可促进反应。反应完成需要约18-24小时,之后浓缩,残渣用水和二氯甲烷的混合物搅拌约5分钟。分层后,干燥并浓缩有机层,得到含有约90%产率(式iii)的泡沫状固体。残渣中还含有约8%的杂质-1(一种酰胺衍生物)以及经hplc分析含量约为0.5%的未知杂质-2。
[0030]
用对甲苯磺酸一水合物处理残渣,得到5'-异丁酰基胞苷甲苯磺酸盐和缩丙酮水解物。该反应可在乙酯乙酸或乙腈中进行。在室温下,只形成甲苯磺酸盐。然而,在75-80℃下反应约24小时后,缩丙酮部分水解形成(式iv),hplc纯度为98%。它完全不含杂质-1,杂质-2含量减少到约低于0.05%。缩丙酮水解由对甲苯磺酸一水合物中的结晶水引起,结晶
水约为12%。在二甲苯中共沸后的ptsa不能引起缩丙酮水解。在干燥器中干燥ptsa一水合物不会降低含水量。将乙腈用作溶剂时,观察到约5%的酯水解。对甲苯磺酸盐(式iv)与碱反应得到5'-异丁酰基胞苷(式v)。虽然可使用各种有机碱,但使用二环己基胺(dcha)可获得最佳结果。在室温下以1-1.5当量dcha在丙酮中处理式iv约1小时,产生ptsa.dcha盐的沉淀,过滤除去即可。浓缩滤液,用水和二氯甲烷处理残渣,以除去残留的ptsa-dcha盐和剩余的游离dcha。
[0031]
自1965年以来,便已知通过胞苷衍生物与羟胺反应得到n-羟基胞苷(biochemical&biophysical research communications,第18(4)期,1965年,617-622)。
[0032]
胞苷丁酸酯(v)的游离碱可通过与羟胺反应转化为莫那比拉韦。该反应可使用市售羟胺盐,如盐酸或硫酸盐来进行。完成反应需要3~5摩尔当量羟胺,并在70~80℃下加热15至20小时。
[0033]
下文进一步描述了本发明的实施例,这些实施例不以任何方式限制本发明的范围。
[0034]
实施例1:制备5-异丁酰胞苷对甲苯磺酸盐(iv)
[0035]
将缩丙酮硫酸盐胞苷(ii)(22g,57.69mmol)、4-二甲基氨基吡啶(1.41g,0.2当量)、1.4-二氮杂双环[5.4.0]十一碳-7-烯(27.23g,3.1当量)溶于乙腈(220ml)中,在15分钟内加入异丁酸酐(14.6g,1.6当量)。将溶液搅拌20小时。浓缩反应混合物,残渣用水(100ml)和二氯甲烷(100ml)处理。搅拌5分钟后,分离成两层,有机层用无水硫酸钠干燥并浓缩,得到20.9g泡沫状固体,其中含有89.7%的iii、8.54%的杂质-1和0.54%的未知杂质-2。
[0036]
将上述固体溶解在乙酸乙酯(100ml)中,加入对甲苯磺酸一水合物(10.98g,1.0当量)与乙酸乙酯(100ml)的溶液。将反应混合物加热至75-80℃,并搅拌24小时。冷却至室温后,过滤沉淀的固体,用乙酸乙酯(100ml)洗涤,真空干燥4小时,得到21.5g(76.7%)iv。hplc纯度:98.53%,iii的对甲苯磺酸盐:0.24%,杂质-1:无,杂质-2:0.03%。
[0037]
ft-ir(kbr,cm-1
):3481,3415,3282,3137,2923,1724,1690,1542,1497,1453,1420,1397,1331,1280,1243,1198,1172,1138,1126,1099,1035,1010,919,875,830,814,765,683,622,585,567,527.1h-nmr(300mhz,dmso-d6):δ9.50(s,1h),8.44(s,1h),7.95-7.93(d,1h),7.50-7.46(d,2h,ar-h),7.13-7.10(d,2h,ar-h),6.12-6.09(d,1h),5.71-5.69(d,1h),4.33-4.20(m,2h),4.12-4.04(m,2h),3.93-3.89(m,1h),2.64-2.54(m,1h),2.29(s,3h),1.11-1.05(d,6h).
13
c-nmr(75mhz,dmso-d6):δ176.40,159.64,147.65,145.05,144.87,138.82,128.76,125.93,94.65,90.99,81.64,73.73,69.71,63.90,33.60,21.25,19.24,19.19.esi-ms:314.18[m+h]
+
(游离碱m.w.:313.31)。
[0038]
实施例2:分两步制备5-异丁酰胞苷对甲苯磺酸盐(iv)
[0039]
将缩丙酮硫酸盐胞苷(ii)(30.3g)、4-二甲基氨基吡啶(1.94g,0.2当量)、1,4-二氮杂双环[5.4.0]十一碳-7-烯(37.5g,3.1当量)溶于乙腈(300ml)中,滴加异丁酸酐(20.1g,1.6当量),并按实施例-1所述完成反应,得到29.1g泡沫状固体,经hplc分析含有88.17%的(iii)、7.31%的杂质-1和0.43%的未知杂质-2。
[0040]
将上述固体溶于乙酸乙酯(150ml)中,加入对甲苯磺酸一水合物(17.23g,1.1当量)与乙酸乙酯(100ml)的溶液。在25~30℃下搅拌反应混合物一小时,过滤沉淀的固体,用
乙酸乙酯(100ml)洗涤,真空干燥4小时,得到32.8g(78.54%)iii的对甲苯磺酸盐。hplc纯度:97.4%,iv:1.98%,杂质-1:无,m.r:160-169℃。
[0041]
ft-ir(kbr,cm-1
):3256,3059,2987,2941,2786,1731,1702,1660,1543,1496,1458,1409,1388,1373,1352,1326,1265,1252,1233,1205,1191,1166,1154,1124,1111,1092,1072,1034,1009,970,899,868,817,755,681,623,593,577,564,1h-nmr(300mhz,dmso-d6):δ9.51(s,1h),8.42(s,1h),8.00-7.98(d,1h),7.49-7.47(d,2h,ar-h),7.13-7.10(d,2h,ar-h),6.08-6.06(d,1h),5.80-5.79(d,1h),5.07-5.04(dd,1h),4.80-4.77(dd,1h),4.36-4.32(m,1h),4.28-4.17(m,2h),2.54-2.47(m,1h和dmso),2.29(s,3h),1.49(s,3h),1.29(s,3h),1.08-1.05(d,6h).
13
c-nmr(75mhz,dmso-d6):δ176.27,159.93,147.68,146.80,145.46,138.55,128.68,125.93,113.63,94.44,85.48,84.38,81.12,64.21,33.51,27.32,25.54,21.25,19.19,19.10.esi-ms:354.12[m+h]
+
(游离碱m.w.:353.37)。
[0042]
将上述固体,即iii的对甲苯磺酸盐(32.7g),悬浮在乙酸乙酯(300ml)中,加热至75-80℃,搅拌20-24小时。冷却至室温后,过滤固体,用乙酸乙酯(100ml)和丙酮(100ml)洗涤,真空干燥3-4小时,得到21.5g iv。hplc纯度:98.8%,o-异亚丙基胞苷-5-异丁酸酯(iii):0.16%。
[0043]
实施例3:制备5-异丁酰胞苷对甲苯磺酸盐(iv)
[0044]
按照实施例-1所述进行实验,只是将溶剂乙酸乙酯换成了乙腈(产率:80.6%;hplc纯度:98.6%)。
[0045]
实施例4:制备2',3'-o-异亚丙基胞苷-5'-异丁酸酯(iii)
[0046]
将缩丙酮硫酸盐胞苷(ii)(3g)、4-二甲基氨基吡啶(0.19g,0.2当量)、二异丙基乙胺(dipea)(3.15g,3.1当量)溶于乙腈(30ml),在15分钟内加入异丁酸酐(3.15g,1.6当量)。将溶液搅拌16小时。浓缩反应混合物,用水(100ml)和二氯甲烷(100ml)处理残渣;搅拌5分钟后,分离成两层,有机层用无水硫酸钠上干燥并浓缩,得到2.6g(95%)(iii)。hplc纯度:83.15%,杂质-1:9.04%,未知杂质-2:0.31%。
[0047]
实施例5:制备胞苷-5-异丁酸酯游离碱(v)
[0048]
将胞苷-5'-异丁酸酯对甲苯磺酸盐(iv)(15g,0.031mol)悬浮在丙酮(300ml)中并进行搅拌。向悬浮液中加入二环己基胺(6.72g,0.037mol),并继续搅拌2小时;过滤除去沉淀的甲苯磺酸二环己基铵盐。用丙酮(50ml)洗涤固体;聚合丙酮滤液,并减压浓缩;残渣溶于水(100ml),并用二氯甲烷(2x 100ml)洗涤。水溶液减压浓缩,所得固体残渣与丙酮共沸,得到8.3g(85%y)泡沫状固体(v)。hplc纯度:99.5%。
[0049]
实施例6:制备胞苷-5-异丁酸酯游离碱(v)
[0050]
除了用1,4-二氧六环代替丙酮外,按实施例-4所述进行实验,得到7.8g(80.6%y)v,hplc纯度:98.6%。
[0051]
实施例7:制备莫那比拉韦(i)
[0052]
将异丁酰基胞苷(v)(5.0g,0.15mmol)悬浮在70%异丙醇中,并加入硫酸羟胺(8.4g,0.51mmol)。将反应混合物加热至75-80℃,持续16小时。分离异丙醇层,并减压浓缩。将残渣溶解在异丙醇(60ml)中,过滤除去不溶物质,浓缩滤液,再次在50℃下将残渣溶解在异丙醇中。冷却澄清溶液,过滤固体,得到3.7g(71%)(i)无色固体,hplc:99.29。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1