一种靶向成纤维细胞活化蛋白的治疗药物及其制备方法与流程
1.本发明涉及核医学与分子影像学领域,具体地涉及一种靶向成纤维细胞活化蛋白的治疗药物及其制备标记。
背景技术:
2.成纤维细胞活化蛋白(fibroblast activation protein,fap)是一种膜丝氨酸肽酶,表达于肿瘤间质活化的成纤维细胞表面。研究表明,超过90%的上皮恶性肿瘤的基质成纤维细胞表面检测到成纤维细胞活化蛋白的高表达。因此,fap已成为肿瘤显像和治疗的重要靶点。
3.目前,放射性核素标记的以喹啉酸衍生物为代表的成纤维细胞活化蛋白抑制剂(fapi)已在肿瘤精准成像领域取得了重要进展。例如,金属核素
68
ga标记的fapi已实现30余种不同类型的肿瘤特异性pet显像。由于
68
ga
3+
由发生器产生,一次产量低,且半衰期短(仅为68min),无法实现量产和配送,极大的限制其诊断应用在临床推广。另外,由于fapi快速代谢和洗脱导致肿瘤部位有效剂量较低、保留时间过短,不能满足治疗用途的需要。因此,需要开发新的fapi治疗药物,使其具有适宜的代谢动力学、较高的肿瘤摄取剂量和较长的肿瘤保留时间,以满足核素治疗需求。
技术实现要素:
4.基于上述背景,本发明的首要目的在于开发一种靶向成纤维细胞活化蛋白的治疗核素药物。
5.为实现上述目的,本发明基于以下构思进行研发:采用体内原位白蛋白结合策略,通过截短型伊文思蓝修饰fapi,实现白蛋白作为fapi递送载体,从而延长其在外周血中的半衰期,提高在肿瘤中的摄取富集和保留时间。
6.本发明首先提出一种靶向成纤维细胞活化蛋白的治疗药物前体化合物,其结构如下式(i)所示:
[0007][0008]
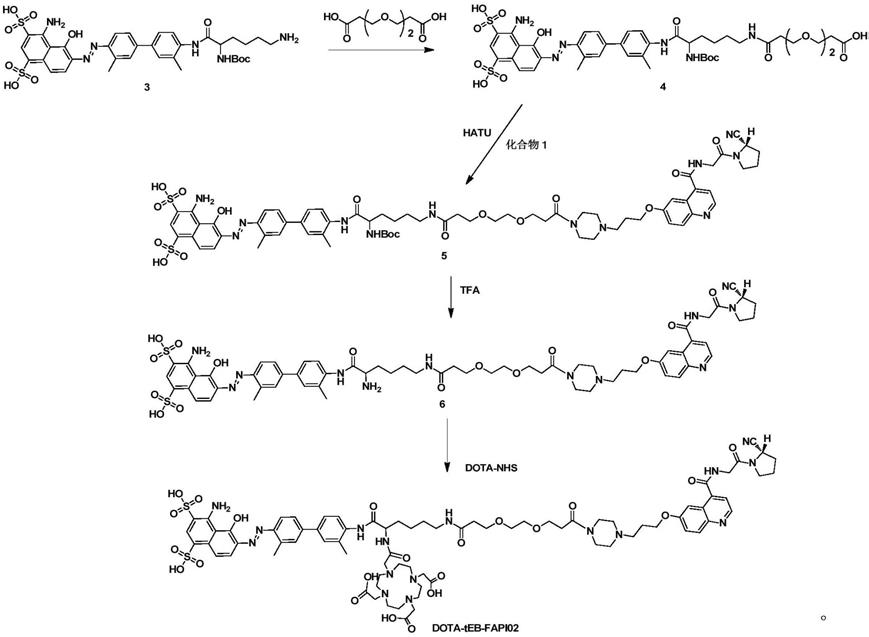
在此基础上,本发明进一步提供制备式(i)所示前体化合物的方法,包括以下步骤:
[0009]
teb衍生物与聚乙二醇
‑
2cooh在缩合试剂hatu作用下反应;接着与fapi小分子抑制剂在hatu作用下发生缩合反应;接着用tfa脱除boc保护;最后与dota
‑
nhs反应,得到式
(i)所示化合物,记作“dota
‑
teb
‑
fapi02”。
[0010]
上述步骤合成路线如下:
[0011][0012]
本发明进一步提供一种靶向成纤维细胞活化蛋白的治疗药物,所述的治疗药物是放射性标记的所述dota
‑
teb
‑
fapi02的配合物,即以本发明所述的式(i)化合物dota
‑
teb
‑
fapi02为配体,经治疗性核素标记得到配合物,可以作为放射性核素治疗探针。
[0013]
所述的治疗性核素可以选择
177
lu、
90
y、
213
bi、
211
at、
223
ra或
225
ac的任意一种。
[0014]
本发明优选的所述治疗药物,是以本发明所述的式(i)化合物dota
‑
teb
‑
fapi02为配体,经治疗性核素
177
lu标记得到配合物,其结构如式(ii)所示:
[0015][0016]
本发明还提供所述治疗药物的制备方法,包括将所述前体化合物溶于缓冲溶液或去离子水中;在所得溶液中加入放射性核素溶液,密闭反应5
‑
40min,即生成放射性核素标记的配合物。
[0017]
本发明优选的方案中,所述的制备方法具体包括以下步骤:将50微克式(i)化合物溶于20微升dmso中,加入200μl缓冲溶液(ph=5.5),震荡使之完全溶解,加入5mci左右
177
lucl3。混合物摇匀后95摄氏度加热反应30min。反应结束后冷却至室温。取一c18分离小
柱,先用10ml无水乙醇缓慢淋洗,再用10ml水淋洗。用10ml水将标记液稀释后,上样到分离柱上,先用10ml水除去未标记的
177
lu离子,再用0.3ml 10mm hcl的乙醇溶液淋洗得到产品。该淋洗液经生理盐水稀释,并经无菌过滤后即得式(ii)所示治疗药物注射液。
[0018]
所述缓冲溶液为稳定反应液ph值的物质,可以为醋酸盐、乳酸盐、酒石酸盐、苹果酸盐、马来酸盐、琥珀酸盐、抗坏血酸盐、碳酸盐和磷酸盐,以及它们的混合物等。
[0019]
上述合成步骤中的所使用的其它化学物质为市售商品。
[0020]
再一个方面,本发明还提供式(i)或(ii)所示化合物或其药学上可接受的盐在制备fap蛋白高表达肿瘤的治疗药物中的应用。
[0021]
本发明优选的所述应用中,所述的式(ii)配合物被制备成注射剂,通过静脉注射给药,用于fap蛋白高表达肿瘤患者。
[0022]
本发明所述的应用中,所述的fap蛋白高表达肿瘤包括但不限于乳腺癌、结直肠癌、卵巢癌、肺癌、胃癌或胰腺癌。
[0023]
本发明所述的靶向成纤维细胞活化蛋白的治疗核素药物结构中,利用截短型伊文思蓝的修饰的成纤维活化蛋白抑制剂能够显著延长其循环半衰期,并且能够增强肿瘤摄取富集和保留时间。此外,通过将本发明所述的靶向成纤维细胞活化蛋白的治疗药物与某些靶向成纤维细胞活化蛋白的诊断药物配合使用,有望提升成纤维细胞活化蛋白阳性肿瘤的诊疗效果。所述的靶向成纤维细胞活化蛋白的诊断药物可以是如下式(iii)所示的放射性标记配合物:
[0024]
附图说明
[0025]
图1为本发明实施例1的化合物3的质谱图。
[0026]
图2为本发明实施例1的化合物5的质谱图。
[0027]
图3本发明实施例1的化合物dota
‑
teb
‑
fapi02的质谱图。
[0028]
图4本发明实施例2中hplc质控结果示意图。
[0029]
图5本发明实施例2中制备的
177
lu
‑
dota
‑
teb
‑
fapi02在正常小鼠体内分布实验结果。
[0030]
图6本发明实施例2中制备的
177
lu
‑
dota
‑
teb
‑
fapi02在u87荷瘤鼠不同时间点的spect显像。
具体实施方式
[0031]
以下通过具体实施方式结合附图对本发明的技术方案进行进一步的说明和描述。
[0032]
实施例1:化合物dota
‑
teb
‑
fapi02的制备
[0033]
化合物4的合成:
[0034]
向化合物3(1.0mmol)的n,n
‑
二甲基甲酰胺中分别加入cooh
‑
peg2‑
cooh
(1.50mmol)、hatu(1.0mmol)和n,n
‑
二异丙基乙胺(3.0mmol),室温搅拌过夜,通过hplc监测反应完成。减压蒸馏除去溶剂,得到粗产物。将粗产物经反相柱化,冷冻干燥得到纯的化合4,产率67%。其中,化合物3的质谱图见图1。
[0035]
化合物5的合成:
[0036]
在50ml烧瓶中分别投入化合物4(0.1mmol)、hatu(0.1mmol)和n,n
‑
二异丙基乙胺(0.3mmol)、fapi小分子抑制剂化合物1(0.1mmol)以及5ml n,n
‑
二甲基甲酰胺,室温反应,通过hplc监测反应完成。减压蒸馏除去溶剂,得到粗产物。将粗产物经反相柱化,冷冻干燥得到纯的化合5,产率54%。图2为化合物5的质谱图。其中fapi小分子抑制剂化合物1结构如下式(iv)所示:
[0037][0038]
化合物dota
‑
teb
‑
fapi02的合成:
[0039]
在25ml烧瓶中,将化合物5(0.1mmol)溶解在tfa/二氯甲烷(体积比1:9)溶液中脱除boc保护,通过hplc监测脱保护进程至反应结束,氮气吹干溶剂,加入dota
‑
nhs(0.05g,0.1mmol)以及n,n
‑
二异丙基乙胺(0.04g,0.3mmol)依次投入至5ml n,n
‑
二甲基甲酰胺。反应体系室温搅拌反应,通过hplc监测脱至反应结束,减压蒸馏除去溶剂,得到粗产物。将粗产物经反相柱化,冷冻干燥得到纯的化合物dota
‑
teb
‑
fapi02,产率55%。图3为化合物dota
‑
teb
‑
fapi02的质谱图。
[0040]
上述步骤合成路线如下:
[0041]
[0042]
实施例2. 177lu
‑
dota
‑
teb
‑
fapi02配合物的制备:
[0043]
将50微克实施例1方法制备的化合物dota
‑
teb
‑
fapi02溶于20微升dmso中,加入200μl缓冲溶液(ph=5.5),震荡使之完全溶解,加入5mci左右
177
lucl3。混合物摇匀后95摄氏度加热反应30min。反应结束后冷却至室温。取一c18分离小柱,先用10ml无水乙醇缓慢淋洗,再用10ml水淋洗。用10ml水将标记液稀释后,上样到分离柱上,先用10ml水除去未标记的
177
lu离子,再用0.3ml 10mm hcl的乙醇溶液淋洗得到产品。该淋洗液经生理盐水稀释,并经无菌过滤后即得
177
lu
‑
dota
‑
teb
‑
fapi02的注射液。hplc质控结果如图4所示。
[0044]
实验例.分析及应用效果
[0045]
1、hplc分析鉴定
[0046]
hplc体系如下:shimadzulc
‑
20a;c18色谱柱(ymc,3μm,4.6
×
150mm)用于分析。检测波长254nm,流速为1ml/min,淋洗梯度:0~3分钟:10%乙腈(0.1%tfa)和90%水(0.1%tfa)保持不变;3
‑
16分钟:增加到90%乙腈(0.1%tfa)和10%水(0.1%tfa);16
‑
18min:降低到10%(0.1%tfa)和90%水(0.1%tfa);18
‑
20min:保持10%乙腈(0.1%tfa)和90%水(0.1%tfa)。
[0047]
2、
177
lu
‑
dota
‑
teb
‑
fapi02配合物在正常小鼠和u87荷瘤模型小鼠中的实验。
[0048]
按实施例2的方法制备好纯度大于95%的
177
lu
‑
dota
‑
teb
‑
fapi02,在正常小鼠和u87荷瘤模型小鼠中,经尾静脉注射1.3mbq的
177
lu
‑
teb
‑
fapi。在注射后不同时间点测试药代动力学及进行spect显像,结果见图5和图6。结果显示,
177
lu
‑
dota
‑
teb
‑
fapi02在正常小鼠体内具有良好的药代动力学,在u87荷瘤模型小鼠中能够持续被肿瘤组织摄取并维持超过48h,表明
177
lu
‑
dota
‑
teb
‑
fapi02具有显著增强的肿瘤摄取和保留时间,可以用作肿瘤治疗剂。
[0049]
综上所述,本发明提供的方案中,利用截短型伊文思蓝的修饰的成纤维活化蛋白抑制剂能够显著延长其循环半衰期,并且能够增强肿瘤摄取富集和保留时间。
[0050]
此外,将本发明所述的靶向成纤维细胞活化蛋白的治疗药物与某些靶向成纤维细胞活化蛋白的诊断药物配合使用,有望提升成纤维细胞活化蛋白阳性肿瘤的诊疗效果。
[0051]
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1