一种磷酸奥司他韦干混悬剂杂质的制备方法
1.本发明属于医药化工领域,尤其涉及化学合成,具体涉及一种磷酸奥司他韦干混悬制剂中两个杂质的制备方法。
背景技术:
2.磷酸奥司他韦是一种神经氨酸酶抑制剂,主要通过干扰病毒从被感染宿主细胞表面的释放减少病毒的传播,临床用于治疗和预防甲型和乙型病毒性流感以及h5n1型禽流感。已成为who推荐的基本药物,被美国和欧洲的疾控中心推荐为主要的抗流感病毒药物。同时,在中国也被卫计委(nhfpc)推荐为治疗h1n1和h7n9流感的首选药物,并被《儿童流感诊断与治疗专家共识(2015年版)》推荐用于儿童流感的治疗和预防。
3.目前,原研磷酸奥司他韦的剂型只有胶囊剂和干混悬剂两种,国内截止2020年只有胶囊剂和颗粒剂上市销售。2021年印度生产的干混悬剂在国内获批进口上市销售,商品名为奥唯平,国内多个厂家的干混悬剂正在进行be研究或者即将获批上市。干混悬剂由于口感好,比较适合儿童服用,磷酸奥司他韦干混悬剂极具开发潜力。
4.原研磷酸奥司他韦干混悬剂的处方中含有辅料柠檬酸单钠,稳定性研究表明,该辅料会和主成分——磷酸奥司他韦的氨基发生反应,形成两个同分异构体杂质,杂质ⅰ和杂质ⅱ,因此制备这两个杂质并建立相应的质量标准有利于提高制剂产品的质量水平。目前常用的获得这两种杂质的方法均是通过采用制备液相将这两种杂质分离出来,然后通过冷冻干燥分别获得两个杂质,尚没有通过合成的方法进行制备的报道。
技术实现要素:
5.为了克服现有技术的问题,本发明的目的在于提供一种磷酸奥司他韦干混悬制剂中两个杂质的人工合成方法,本发明的目的是通过以下技术方案实现的:
6.一种磷酸奥司他韦干混悬剂杂质的制备方法,包括以下两个步骤:
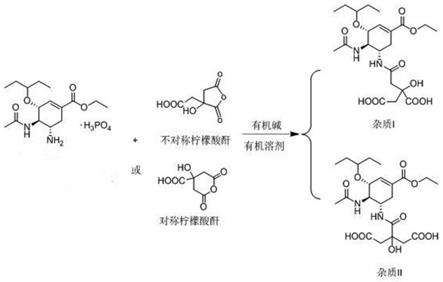
7.步骤1:以磷酸奥司他韦为起始原料与不对称柠檬酸酐或对称柠檬酸酐在有机碱存在的条件下,在非极性溶剂中反应,反应完毕将溶剂减压蒸干;当选择不对称柠檬酸酐时得到杂质ⅰ和杂质ⅱ两个杂质的混合物粗品,当选择对称柠檬酸酐时得到杂质ⅱ的粗品;
8.步骤2:将两个杂质的混合物粗品或杂质ⅱ的粗品进行分离纯化分别得到杂质ⅰ和杂质ⅱ或者单独的杂质ⅱ;
9.杂质ⅰ的结构如式(1)所示,杂质ⅱ的结构如式(2)所示:
[0010][0011]
磷酸奥司他韦与对称柠檬酸酐发生酸酐的氨解开环反应生成杂质ⅰ;磷酸奥司他韦与不对称柠檬酸酐发生酸酐的氨解开环反应生成杂质ⅰ和杂质ⅱ的混合物。两个杂质系磷酸奥司他韦干混悬剂中主成分磷酸奥司他韦与辅料柠檬酸单钠在高温下产生的杂质,应定入质量标准中加以控制。
[0012]
进一步的,步骤2中通过制备液相色谱或柱层析进行分离纯化。
[0013]
进一步的,步骤1中有机碱采用三乙胺、吡啶、三正丁胺中任意一种;有机碱与磷酸奥司他韦的物质的量(摩尔)投料比为1.0:1.0~10.0:1.0。
[0014]
进一步的,步骤1中非极性溶剂采用二氯甲烷、二氯乙烷、苯、甲苯、甲基叔丁基醚、乙醚、异丙醚、乙腈、四氢呋喃中任意一种;非极性溶剂与磷酸奥司他韦的投料重量比为5:1~30:1。
[0015]
进一步的,步骤1中的反应温度为0℃~40℃。
[0016]
进一步的,步骤1中的反应温度为18~30℃,反应时间为8~20h。
[0017]
本发明的有益效果:
[0018]
通过设计工艺路线,采用合成的方法制备已知结构的杂质,可以规避采用制备液相分离获得杂质的缺点,如:杂质浓度低需要大量的含杂质的样品进行反复富集,耗时且成本极高,从而可以方便的获得奥司他韦干混悬剂的两个关键杂质,有利处方工艺的优化、反析方法的开发、提高产品的质量水平。
[0019]
本发明通过设计完成了对两个杂质的制备,不仅可以大量获得研究用的杂质对照品,而且大大缩短了获得杂质的时间,是药厂或者研究单位切实可行的获得这两个杂质对照品的途径,有利于国内制剂厂家优化处方工艺,提高制剂的质量水平。
附图说明
[0020]
下面结合附图和实施例对本发明作进一步说明。
[0021]
图1是本发明合成路线图;
[0022]
图2是为杂质ⅰ质谱;
[0023]
图3为杂质ⅰ氢谱;
[0024]
图4为杂质ⅰ碳谱;
[0025]
图5是为杂质ⅱ质谱;
[0026]
图6为杂质ⅱ氢谱;
[0027]
图7为杂质ⅱ碳谱。
具体实施方式
[0028]
本发明为一种磷酸奥司他韦干混悬剂杂质的制备方法,包括以下两个步骤,合成路线如图1所示。
[0029]
步骤1:以磷酸奥司他韦为起始原料与不对称柠檬酸酐或对称柠檬酸酐在有机碱存在的条件下,在非极性溶剂中反应,反应完毕将溶剂减压蒸干;当选择不对称柠檬酸酐时得到杂质ⅰ和杂质ⅱ两个杂质的混合物粗品,当选择对称柠檬酸酐时得到杂质ⅱ的粗品;
[0030]
步骤2:将两个杂质的混合物粗品或杂质ⅱ的粗品进行分离纯化分别得到杂质ⅰ和杂质ⅱ或者单独的杂质ⅱ。
[0031]
以上两个杂质均为磷酸奥司他韦制剂高温降解杂质。这两个杂质为主成分奥司他韦与辅料枸橼酸在高温下产生。本实施方式中,以枸橼酸为原料,先制备枸橼酸酐,然后将其与磷酸奥司他韦的氨基反应产生两个同分异构的杂质,杂质ⅰ和杂质ⅱ,通过制备液相分离纯化得到两个两个杂质,为磷酸奥司他韦制剂的质量控制提供有效的手段。具体实施例如下:
[0032]
实施例1
[0033]
0.87克不对称柠檬酸酐(5mmol)与2.05克磷酸奥司他韦(5mmol)以及20毫升二氯甲烷混合,搅拌下加入3.04克三乙胺(30mmol),20~30℃反应12~16小时反应完全,然后将反应液减压浓缩至干,残留物通过制备液相进行纯化处理得到杂质ⅰ共0.78克,摩尔收率32.1%和杂质ⅱ共0.73克,收率30.0%。杂质ⅰ和杂质ⅱ的质谱及核磁氢谱、核磁碳谱图见图2~7。
[0034]
液相方法:
[0035]
色谱条件:
[0036]
色谱柱:辛烷基硅烷键合硅胶为填充剂(kromasil c8,4.6
×
250mm,5μm)
[0037]
流动相a:0.05m磷酸二氢钾溶液(用1mol/l氢氧化钾溶液调节ph值至5.8
±
0.1)
[0038]
流动相b:甲醇
‑
乙腈(1:1)
[0039][0040]
柱温:50℃
[0041]
检测波长:207nm
[0042]
流速:1.5ml/min
[0043]
进样量:10μl
[0044]
运行时间:60min
[0045]
溶剂:水
‑
甲醇
‑
乙腈(70:15:15)
[0046]
杂质ⅰ:1h
‑
nmr(500mhz,dmso
‑
d6)δ(ppm):0.75~0.85(6h,m)、1.21~1.23(3h,t)、1.34~1.46(2h+2h,m)、1.78(3h,s)、2.17(1h,m)、2.44(1h,m)、2.56~2.72(2h+2h)、3.34
(1h,s)、3.39(1h,oh)、3.73~3.75(1h,m)、3.89~3.91(1h,m)、4.08~4.10(2h,m)、4.14~4.15(1h,d)、6.64(1h,d)、7.75~7.81(2h,酰胺两个nh)、12.40(2h,两个羧基上的氢)。
13
c
‑
nmr(125mhz,dmso
‑
d6)δ(ppm):9.44(ch3)、9.88(ch3)、14.54(ch3)、23.26(ch3)、25.66(ch2)、26.19(ch2)、30.70(ch2)、43.11(ch2)、43.49(ch2)、47.85(ch)、53.88(ch)、60.92(ch)、73.08(c)、75.49(ch)、81.60(ch)、128.88(烯基c)、138.88(烯基ch)、165.94(羰基碳)、169.58(羰基碳)、170.13(羰基碳)、171.73(羰基碳)、175.29(羰基碳)。
[0047]
质谱(esi
‑
负离子):485.2(m
‑
h)
‑
[0048]
杂质ⅱ:1h
‑
nmr(500mhz,dmso
‑
d6)δ(ppm):0.78~0.85(6h,m)、1.21~1.23(3h,t)、1.39~1.46(2h+2h,m)、1.82(3h,s)、2.2(1h,m)、2.55(1h,m)、2.56~2.75(2h+2h)、3.41~3.43(1h+oh,m)、3.84~3.87(1h+1h,m)、4.08~4.10(2h,m)、4.13~4.16(1h+2h,m)、6.66(1h,s)、7.63~7.64(1h,酰胺nh)、7.87~7.89(1h,酰胺nh)。
[0049]
13
c
‑
nmr(125mhz,dmso
‑
d6)δ(ppm):9.53(ch3)、9.84(ch3)、14.56(ch3)、23.19(ch3)、25.72(ch2)、26.19(ch2)、30.09(ch2)、42.98(ch2)、48.38(ch)、52.76(ch)、60.89(ch)、73.74(c)、74.96(ch)、81.60(ch)、129.14(烯基c)、138.11(烯基ch)、166.07(羰基碳)、169.58(羰基碳)、171.83(羰基碳)、172.00(羰基碳)、173.81(羰基碳)。
[0050]
质谱(esi
‑
负离子):485.2(m
‑
h)
‑
[0051]
实施例2
[0052]
0.87克对称柠檬酸酐(5mmol)与2.05克磷酸奥司他韦(5mmol)以及20毫升二氯甲烷混合,搅拌下加入3.04克三乙胺(30mmol),室温下反应过夜,反应完全,然后将反应液减压浓缩至干,残留物通过柱层析纯化(洗脱液:甲醇/二氯甲烷=1:3)得到杂质ⅱ共1.3克,摩尔收率53.5%。
[0053]
实施例3
[0054]
0.87克不对称柠檬酸酐(5mmol)与2.05克磷酸奥司他韦(5mmol)以及20毫升二氯乙烷混合,搅拌下加入3.04克三乙胺(30mmol),室温下反应过夜,反应完全,然后将反应液减压浓缩至干,残留物通过制备液相进行纯化处理得到杂质ⅰ共0.75克,摩尔收率30.9%和杂质ⅱ共0.71克,摩尔收率29.2%。
[0055]
实施例4
[0056]
0.87克不对称柠檬酸酐(5mmol)与2.05克磷酸奥司他韦(5mmol)以及20毫升二氯乙烷混合,搅拌下加入2.4克吡啶(30mmol),室温下反应过夜,反应完全,然后将反应液减压浓缩至干,残留物通过制备液相进行纯化处理得到杂质ⅰ共0.74克,摩尔收率30.4%和杂质ⅱ共0.72克,摩尔收率29.6%。
[0057]
实施例5
[0058]
1.74克对称柠檬酸酐(10mmol)与4.1克磷酸奥司他韦(10mmol)以及30毫升甲基叔丁基醚混合,搅拌下加入3.04克三乙胺(30mmol),30℃反应3小时,反应完全,然后将反应液减压浓缩至干,残留物通过柱层析纯化(洗脱液:甲醇/二氯甲烷=1:3)得到杂质ⅱ共2.67克,摩尔收率55%。
[0059]
最后应说明的是,以上仅用以说明本发明的技术方案而非限制,尽管参照较佳布置方案对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1