一种顺(反)-8-十二碳烯醇乙酸酯的合成方法与流程
一种顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法
技术领域
1.本发明涉及昆虫性信息素的人工合成技术领域。具体地说是一种顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法。
背景技术:
2.梨小食心虫(grapholithamolesta)是世界性害虫,又名梨小蛀果蛾、东方果蠹蛾,简称梨小,属鳞翅目小卷蛾科。梨小食心虫在国内分布较广,除西藏外,华北、华中、华南、东北发生普遍,为害梨、苹果、桃、山楂、杏、樱桃等果树。梨小食心虫的幼虫蛀食果实和嫩梢,且近几年来发生量较大,为害日趋严重。一般年份梨果受害率达到10%左右,个别果园达20%~30%,不喷药果园虫果率可达80%以上。
3.多年来,梨小食心虫的防治主要是以化学药剂为主。大量化学农药的使用不仅没有控制住害虫,反而由于破坏了生物链的良性循环导致害虫产生抗药性,以致于形成了“药年年打,虫年年多”的局面,同时大量化学农药的使用也带来了生态环境失衡及农残等诸多问题。
4.随着经济的发展,国家对生态环境的重视日益提高,民众对果品无公害无农残的要求日趋强烈,传统的防治观念和防治手段已经远远不能满足当前生态建设和林果业可持续发展的需要。
5.因此,将梨小食心虫信息素迷向新技术产品引入我国,利用高科技生物防治手段来防控梨小食心虫,不仅能确保果品安全无公害,大量减少化学农药的使用,逐步取代传统的化学防治手段,而且可以保护日益恶化的生态环境,逐渐恢复生态平衡。该方法符合国家政策和行业发展规划,可以全面贯彻落实“预防为主,科学防控,依法治理,促进健康”的林业有害生物防治方针,进一步促进农、林业有害生物的无公害防治水平,保护生态环境和生物的多样性,促进林果业的可持续、健康发展;同时为此类产品在国内害虫防控大面积应用和推广创造条件,具有广阔的发展前景和划时代的意义。
6.目前关于梨小食心虫性信息素类似物的合成主要包括以下两种途径:
7.1、从炔烃出发的合成路线。该合成路线的特点是:利用含炔键的原料合成梨小食心虫性信息素类似物,然后经部分还原得顺式和反式梨小食心虫性信息素,其末端基团的获得是由原料直接带入或是通过官能团转化。1973年holan g提出的合成路线是通过对合成的含炔键的中间体,经过硼烷部分还原及末端基团的转化合成。1977年中国科学院北京动物研究所杀虫剂组参照这类化合物的合成方法加以改进,提出了两条合成顺式梨小食心虫性信息素类似物的路线;第一路线的特点在于对中间体炔键的还原上采用了pd
‑
caco3催化加氢还原。其中第二路线与第一路线类似,只是在对炔键的还原上采用pd
‑
caco3催化加氢还原。上述合成路线存在较长链的端炔不易获得的缺陷。1982年,仲同生等提出一条含炔烃多位异构化的合成路线,1986年,mithran s等和1995年yuan,gu提出的合成方法与上面的方法类似,只是原料选择上略有变化,但仍是使用含炔键的原料。
8.2、从醛出发的合成路线。该路线的合成特点是:以合适的醛为原料,经wittig反
应,羰基成烯直接建立梨小食心虫性信息素中所需的双键。其末端基团一般由原料直接引入。1985年schaub b等提出的顺式和反式合成路线是属于这类性信息素合成中较典型的方法,他们以ω
‑
hydroxyalkylphosphonium salt和合适的醛出发,合成顺式和反式梨小食心虫性信息素,有关这一类方法的合成报道还有很多,且合成方法相似,只是在原料的选择上有差异。诸如:李森等以环辛酮为原料经8步合成(z/e)
‑8‑
十二碳烯
‑1‑
醇醋酸酯;vinczer,peter等以1,8
‑
辛二醛和ph3p=chpr为原料合成(z/e)
‑8‑
dodecen
‑1‑
ol混合物;以及1995年yuan,gu以ho(ch2)
n
oh和ch3(ch2)mcho为原料合成(z/e)
‑8‑
十二碳烯
‑1‑
醇醋酸酯(n=8,m=2)。
9.近三十多年来,有机化学专家们在梨小食心虫性信息素的合成上做了大量的工作,由多种原料合成了目标产物;但实现的操作较繁琐,或者还存在原料不易获得等问题。因此,如何提供一种操作简单安全、价格低廉的合成方法是本领域技术人员亟需解决的问题。
技术实现要素:
10.为此,本发明所要解决的技术问题在于提供一种顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,以解决当前梨小食心虫性信息素的合成上存在的原料不易获得、操作流程繁琐以及合成成本较高等问题。
11.为解决上述技术问题,本发明提供如下技术方案:
12.一种顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,包括如下步骤:
13.(1)常温下,将1,8
‑
辛二醇置于乙酸水溶液中,以硫酸为催化剂,不断搅拌使1,8
‑
辛二醇和乙酸发生反应,生成8
‑
乙酰氧基
‑1‑
辛醇;将生成的8
‑
乙酰氧基
‑1‑
辛醇在离心萃取机中用石油醚连续萃取,萃取得到石油醚相,蒸馏回收石油醚相中的石油醚,即得到8
‑
乙酰氧基
‑1‑
辛醇;
14.(2)向8
‑
乙酰氧基
‑1‑
辛醇中加入水、乙酸乙酯、溴化钠和三水合醋酸钠,搅拌使溴化钠和三水合醋酸钠溶解,然后加入四甲基哌啶氧化物,继续滴加次氯酸钠溶液,反应生成8
‑
乙酰氧基
‑1‑
辛醛;
15.(3)向四氢呋喃中加入丁基三苯基溴化膦,边搅拌边滴加有机碱,反应后生成磷叶立德;向磷叶立德中滴加8
‑
乙酰氧基
‑1‑
辛醛,使磷叶立德和8
‑
乙酰氧基
‑1‑
辛醛进行wittig反应,生成顺(反)
‑8‑
十二碳烯醇乙酸酯。
16.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(1)中,1,8
‑
辛二醇、硫酸和乙酸的摩尔比为1:(0.5~5):(5~15);乙酸水溶液中,乙酸的质量浓度为10wt%~25wt%;硫酸的浓度为1.5wt%~14wt%。
17.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(1)中,使用连续离心萃取机,不断用石油醚萃取出反应生成的8
‑
乙酰氧基
‑1‑
辛醇,连续萃取10~24h后,得到石油醚相,蒸馏石油醚相中的石油醚,待石油醚蒸干后即得到8
‑
乙酰氧基
‑1‑
辛醇;连续离心萃取机的转速为1450r/min,蒸出的石油醚继续进入连续离心萃取机,石油醚循环套用使用。室温下,在强酸的催化作用下,10wt%~25wt%乙酸水溶液中的乙酸对1,8
‑
辛二醇进行选择性单边酯化反应;反应生成的8
‑
乙酰氧基
‑1‑
辛醇采用石油醚连续萃取,1,8
‑
辛二醇几乎不溶于石油醚,而反应体系中由于存在大量的水,可使得8
‑
乙酰氧基
‑1‑
辛醇比较容易被石油
醚萃取,同时大大阻碍辛二醇二乙酸酯生成,从而使得8
‑
乙酰氧基
‑1‑
辛醇具有更高的收率。
18.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(2)中,8
‑
乙酰氧基
‑1‑
辛醇、水、乙酸乙酯、溴化钠、三水合醋酸钠、四甲基哌啶氧化物和次氯酸钠的摩尔比为1:(15~30):(10~25):(0.5~1.5):(0.5~3):(0.005~0.01):(1~2),其中,次氯酸钠溶液的有效氯为7wt%~11wt%;步骤(2)的反应温度控制在0~10℃。在步骤(2)中,水,乙酸乙酯是反应溶剂,溴化钠和和次氯酸钠转化生成次溴酸钠作为氧化剂,三水合醋酸钠是两相催化剂。
19.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,步骤(2)的具体操作方法为:
20.步骤(2
‑
1):向8
‑
乙酰氧基
‑1‑
辛醇中加入水、乙酸乙酯、溴化钠和三水合醋酸钠,搅拌使溴化钠和三水合醋酸钠溶解,然后加入四甲基哌啶氧化物,得到反应体系a;
21.步骤(2
‑
2):将所述反应体系a的温度降至0℃,滴加次氯酸钠溶液,并控制所述反应体系a的温度在0~10℃之间,待次氯酸钠溶液滴加完成后,在0~10℃温度下保温反应1h,得到反应体系b;
22.步骤(2
‑
3):取样检测反应体系b中8
‑
乙酰氧基
‑1‑
辛醇的含量,若其含量小于初始含量的3%,向所述反应体系b中加亚硫酸钠进行灭活,并静置分层,所述反应体系b分层后得到水相层和有机相层;亚硫酸钠的加入量为8
‑
乙酰氧基
‑1‑
辛醇摩尔质量的1%;本发明没有使用氯铬酸吡啶进行氧化的原因在于:
①
六价铬毒性大;
①
后处理困难麻,
③
成本高;本发明选用便宜易得的次氯酸钠和溴化钠为原料使其转化成次溴酸钠,以四甲基哌啶氧化物tempo作为催化剂,在较温和的反应条件下反应即可将8
‑
乙酰氧基
‑1‑
辛醇氧化成8
‑
乙酰氧基
‑1‑
辛醇;该方法学操作简单,安全,后处理简便,且收率高。
23.步骤(2
‑
4):将所述水相层用乙酸乙酯萃取3次,每次萃取时乙酸乙酯与8
‑
乙酰氧基
‑1‑
辛醇的体积之比为2:1,合并3次萃取后的乙酸乙酯相,得到有机相a;将所述有机相层合并后用质量分数为20wt%
‑
25wt%的氯化铵溶液洗涤3次,每次洗涤时氯化铵溶液与8
‑
乙酰氧基
‑1‑
辛醇的体积比为1:1,洗涤后的所述有机相层记为有机相b;将洗涤后的氯化铵溶液相用乙酸乙酯萃取2次,每次萃取时乙酸乙酯与8
‑
乙酰氧基
‑1‑
辛醇的体积之比为2:1,合并2次萃取后的乙酸乙酯相,得到有机相c;
24.步骤(2
‑
5):将所述有机相a、所述有机相b和所述有机相c合并干燥,干燥完成后进行抽滤,对抽滤得到的滤液蒸馏回收乙酸乙酯,即得到8
‑
乙酰氧基
‑1‑
辛醛。
25.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(3)中,所述有机碱的制备方法为:在惰性气体保护下,将四氢呋喃,氢化钠和二甲基亚砜搅拌混合,然后加热到50~70℃,保温反应2小时,待反应液澄清即制备得到有机碱二甲基亚砜钠。在本发明中,没有使用价格高昂、操作危险的正丁基锂和六甲基二硅氨基钠作为有机碱原料,而是采用上述方法自制得到二甲基亚砜钠作为有机碱,不仅成本廉价且安全性较好。在本发明中,先制备得到有机碱,然后再将制备得到的液体有机碱用于磷叶立德反应,这主要是由于丁基三苯基溴化膦在四氢呋喃中不溶解,此步骤制备的二甲基亚砜钠在四氢呋喃中形成液体有机碱,从而使有机碱更容易与丁基三苯基溴化膦反应。
26.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,氢化钠、四氢呋喃和二甲基亚砜的摩尔比为1:(1~5):(2~10)。
27.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(3)中,有机碱、丁基三苯基溴化膦和8
‑
乙酰氧基
‑1‑
辛醛的摩尔比为(1~2.5):1:(0.5~1);步骤(3)的反应温度控制在(
‑
10)℃~(
‑
50)℃。
28.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,步骤(3)的具体操作方法为:
29.步骤(3
‑
1):依次向反应釜中投入四氢呋喃和丁基三苯基溴化膦,将四氢呋喃和丁基三苯基溴化膦混合体系的温度降至(
‑
10)~(
‑
50)℃,然后将有机碱缓慢滴加到反应釜中,反应1h,得到反应体系c;
30.步骤(3
‑
2):控制所述反应体系c的温度为(
‑
10)~(
‑
50)℃,将8
‑
乙酰氧基
‑1‑
辛醛用四氢呋喃稀释后滴加到反应釜中,8
‑
乙酰氧基
‑1‑
辛醛和四氢呋喃体积比为1:1,滴加完成后反应1h,得到反应体系d;
31.步骤(3
‑
3):取样检测反应体系d中8
‑
乙酰氧基
‑1‑
辛醛的含量,若其含量小于初始含量的1%,向所述反应体系d中加入饱和氯化铵水溶液进行灭活;灭活后蒸馏回收四氢呋喃,得到浓缩料液a;
32.步骤(3
‑
4):将所述浓缩料液a用石油醚萃取3次,每次萃取时石油醚与8
‑
乙酰氧基
‑1‑
辛醛的体积之比为2:1,将3次萃取后的石油醚相合并,得到有机相d;
33.步骤(3
‑
5):将所述有机相d用无水硫酸钠干燥,干燥完成后进行抽滤,对抽滤得到的滤液蒸馏回收石油醚,得到浓缩料液b;将所述浓缩料液b进行精馏,即制得顺(反)
‑8‑
十二碳烯醇乙酸酯。
34.上述顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,在步骤(3)中,四氢呋喃和丁基三苯基溴化膦的摩尔比为1:18。
35.本发明的技术方案取得了如下有益的技术效果:
36.(1)本发明所使用的合成原料廉价且来源广泛,易于获得;采用本发明中提供的合成方法具有周期短、步骤少、收率高、后处理简单等优点,适合大规模工业化生产。
37.(2)本发明以1,8
‑
辛二醇和乙酸水溶液为原料,先进行单边乙酰化得到8
‑
乙酰氧基
‑1‑
辛醇;然后将8
‑
乙酰氧基
‑1‑
辛醇用次氯酸钠水溶液氧化得到8
‑
乙酰氧基
‑1‑
辛醛;接着以丁基三苯基溴化膦为原料与有机碱反应生成磷叶立德,然后将生成的磷叶立德与8
‑
乙酰氧基
‑1‑
辛醛进行wittig反应,即可生成顺(反)
‑8‑
十二碳烯醇乙酸酯。本发明的合成方法仅需三步即可合成顺(反)
‑8‑
十二碳烯醇乙酸酯。
38.(3)采用本发明的合成方法,8
‑
乙酰氧基
‑1‑
辛醇的收率可达75%以上;8
‑
乙酰氧基
‑1‑
辛醛的收率可达94%以上;顺(反)
‑8‑
十二碳烯醇乙酸酯的收率可达75%以上。本发明原料易得,生产流程简单,而且工业生产可操作性强,生产成本低廉,适合工业化应用。
附图说明
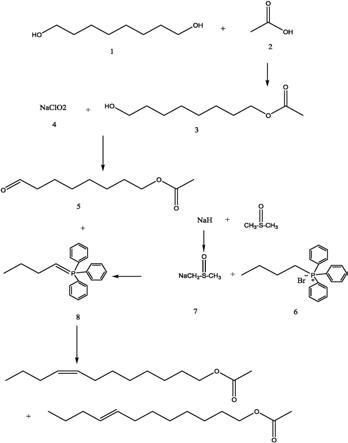
39.图1本发明顺(反)
‑8‑
十二碳烯醇乙酸酯合成方法的流程图;
40.图2本发明顺(反)
‑8‑
十二碳烯醇乙酸酯标准品的核磁图谱(碳谱);
41.图3本发明顺(反)
‑8‑
十二碳烯醇乙酸酯标准品的核磁图谱(氢谱);
42.图4本发明实施例1中顺(反)
‑8‑
十二碳烯醇乙酸酯合成产物的核磁图谱(碳谱);
43.图5本发明实施例1中顺(反)
‑8‑
十二碳烯醇乙酸酯合成产物的核磁图谱(氢谱)。
44.图中附图标记表示为:1
‑
1,8
‑
辛二醇;2
‑
乙酸;3
‑8‑
乙酰氧基
‑1‑
辛醇;4
‑
次氯酸
钠;5
‑8‑
乙酰氧基
‑1‑
辛醛;6
‑
丁基三苯基溴化膦;7
‑
二甲基亚砜钠;8
‑
磷叶立德。
具体实施方式
45.本发明顺(反)
‑8‑
十二碳烯醇乙酸酯合成方法的流程图如图1所示,下面结合图1通过实施例对本发明的合成方法做进一步说明。
46.实施例1
47.一种顺(反)
‑8‑
十二碳烯醇乙酸酯的合成方法,包括如下步骤:
48.(1)常温下,将1,8
‑
辛二醇置于乙酸水溶液中,以硫酸为催化剂,不断搅拌使1,8
‑
辛二醇和乙酸发生反应,生成8
‑
乙酰氧基
‑1‑
辛醇;使用连续离心萃取机,不断用石油醚萃取出反应生成的8
‑
乙酰氧基
‑1‑
辛醇,连续萃取20h后,得到石油醚相,蒸馏石油醚相中的石油醚,待石油醚蒸干后即得到8
‑
乙酰氧基
‑1‑
辛醇;连续离心萃取机的转速为1450r/min,蒸出的石油醚继续进入连续离心萃取机,石油醚循环套用使用;
49.(2)向8
‑
乙酰氧基
‑1‑
辛醇中加入水、乙酸乙酯、溴化钠和三水合醋酸钠,搅拌使溴化钠和三水合醋酸钠溶解,然后加入四甲基哌啶氧化物,继续滴加次氯酸钠溶液,反应生成8
‑
乙酰氧基
‑1‑
辛醛;
50.(3)向四氢呋喃中加入丁基三苯基溴化膦,边搅拌边滴加有机碱,反应后生成磷叶立德;向磷叶立德中滴加8
‑
乙酰氧基
‑1‑
辛醛,使磷叶立德和8
‑
乙酰氧基
‑1‑
辛醛进行wittig反应,生成顺(反)
‑8‑
十二碳烯醇乙酸酯。
51.在步骤(1)中,1,8
‑
辛二醇、硫酸和乙酸的摩尔比为1:5:15;乙酸水溶液中,乙酸的质量浓度为10wt%;硫酸的浓度为14wt%。
52.在步骤(2)中,8
‑
乙酰氧基
‑1‑
辛醇、水、乙酸乙酯、溴化钠、三水合醋酸钠、四甲基哌啶氧化物和次氯酸钠的摩尔比为1:30:25:1.5:3:0.01:2,其中,所述次氯酸钠溶液中有效氯为11wt%;
53.步骤(2)的具体操作方法为:
54.步骤(2
‑
1):向8
‑
乙酰氧基
‑1‑
辛醇中加入水、乙酸乙酯、溴化钠和三水合醋酸钠,搅拌使溴化钠和三水合醋酸钠溶解,然后加入四甲基哌啶氧化物,得到反应体系a;
55.步骤(2
‑
2):将所述反应体系a的温度降至0℃,滴加次氯酸钠溶液,并控制所述反应体系a的温度在0℃之间,待次氯酸钠溶液滴加完成后,在0℃温度下保温反应1h,得到反应体系b;
56.步骤(2
‑
3):取样检测反应体系b中8
‑
乙酰氧基
‑1‑
辛醇的含量,其含量为初始含量的1.88%,小于初始含量的3%,向所述反应体系b中加亚硫酸钠进行灭活,并静置分层,所述反应体系b分层后得到水相层和有机相层;亚硫酸钠的加入量为8
‑
乙酰氧基
‑1‑
辛醇摩尔质量的1%。
57.步骤(2
‑
4):将所述水相层用乙酸乙酯萃取3次,每次萃取时乙酸乙酯与8
‑
乙酰氧基
‑1‑
辛醇的体积之比为2:1,合并3次萃取后的乙酸乙酯相,得到有机相a;将所述有机相层合并后用质量分数为25wt%的氯化铵溶液洗涤3次,每次洗涤时氯化铵溶液与8
‑
乙酰氧基
‑1‑
辛醇的体积比为1:1,洗涤后的所述有机相层记为有机相b;将洗涤后的氯化铵溶液相用乙酸乙酯萃取2次,每次萃取时乙酸乙酯与8
‑
乙酰氧基
‑1‑
辛醇的体积之比为2:1,合并2次萃取后的乙酸乙酯相,得到有机相c;
58.步骤(2
‑
5):将所述有机相a、所述有机相b和所述有机相c合并干燥,干燥完成后进行抽滤,对抽滤得到的滤液蒸馏回收乙酸乙酯,即得到8
‑
乙酰氧基
‑1‑
辛醛。
59.在步骤(3)中,有机碱的制备方法为:在惰性气体保护下,将四氢呋喃,氢化钠和二甲基亚砜搅拌混合,然后加热到70℃,保温反应2小时,待反应液澄清即制备得到有机碱二甲基亚砜钠;氢化钠、四氢呋喃和二甲基亚砜的摩尔比为1:5:10。
60.在步骤(3)中,有机碱、丁基三苯基溴化膦和8
‑
乙酰氧基
‑1‑
辛醛的摩尔比为1:1:0.5;
61.步骤(3)的具体操作方法为:
62.步骤(3
‑
1):向反应釜中投入丁基三苯基溴化膦和四氢呋喃,四氢呋喃和丁基三苯基溴化膦摩尔比为1:18,将丁基三苯基溴化膦和四氢呋喃混合体系的温度降至
‑
10℃,然后将有机碱缓慢滴加到反应釜中,控制反应温度在
‑
10℃,反应1h,得到反应体系c;
63.步骤(3
‑
2):控制所述反应体系c的温度为
‑
10℃,将8
‑
乙酰氧基
‑1‑
辛醛用四氢呋喃稀释后滴加到反应釜中,8
‑
乙酰氧基
‑1‑
辛醛和四氢呋喃体积比为1:1;滴加完成后反应1h,得到反应体系d;
64.步骤(3
‑
3):取样检测反应体系d中8
‑
乙酰氧基
‑1‑
辛醛的含量,其含量为初始含量的0.27%,小于初始含量的1%,向所述反应体系d中加入饱和氯化铵水溶液进行灭活,饱和氯化铵水溶液的加入体积与步骤(3)中制备有机碱时使用的二甲基亚砜体积相等;灭活后蒸馏回收四氢呋喃,得到浓缩料液a;
65.步骤(3
‑
4):将所述浓缩料液a用石油醚萃取3次,每次萃取时石油醚与8
‑
乙酰氧基
‑1‑
辛醛的体积之比为2:1,将3次萃取后的石油醚相合并,得到有机相d;
66.步骤(3
‑
5):将所述有机相d用无水硫酸钠干燥,干燥完成后进行抽滤,对抽滤得到的滤液蒸馏回收石油醚,得到浓缩料液b;将所述浓缩料液b进行精馏,即制得顺(反)
‑8‑
十二碳烯醇乙酸酯。
67.在本实施例中,步骤(1)制备得到的8
‑
乙酰氧基
‑1‑
辛醇的收率76%,步骤(2)制备得到的8
‑
乙酰氧基
‑1‑
辛醛的收率98%;步骤(3)制备得到的顺(反)
‑8‑
十二碳烯醇乙酸酯的收率为79%。
68.图2和图3分别为顺(反)
‑8‑
十二碳烯醇乙酸酯标准品的碳谱和氢谱图;图4和图5分别为本实施例制备的顺(反)
‑8‑
十二碳烯醇乙酸酯的碳谱和氢谱图;对照图2和图4以及图3和图5可知,本实施例制备产物的碳谱和氢谱与顺(反)
‑8‑
十二碳烯醇乙酸酯标准品的碳谱和氢谱一致,说明本实施例制备得到了目标产物顺(反)
‑8‑
十二碳烯醇乙酸酯。
69.实施例2
70.本实施例与实施例1的方法相似,两者的区别如下:
71.在步骤(1)中,1,8
‑
辛二醇、硫酸和乙酸的摩尔比为1:0.5:5;乙酸水溶液中,乙酸的质量浓度为25wt%;
72.在步骤(2)中,8
‑
乙酰氧基
‑1‑
辛醇、水、乙酸乙酯、溴化钠、三水合醋酸钠、四甲基哌啶氧化物和次氯酸钠的摩尔比为1:15:10:0.5:0.5:0.005:1;
73.在步骤(3)中,有机碱的制备方法中:氢化钠、四氢呋喃和二甲基亚砜的摩尔比为1:1:2;在步骤(3)中,有机碱、丁基三苯基溴化膦和8
‑
乙酰氧基
‑1‑
辛醛的摩尔比为2.5:1:1。
74.在本实施例中,步骤(1)制备得到的8
‑
乙酰氧基
‑1‑
辛醇的收率80%,步骤(2)制备得到的8
‑
乙酰氧基
‑1‑
辛醛的收率98%;步骤(3)制备得到的顺(反)
‑8‑
十二碳烯醇乙酸酯的收率为78%。
75.实施例3
76.本实施例与实施例1的方法相似,两者的区别如下:
77.步骤(1)中,萃取时间为10h;
78.在步骤(2
‑
2)中,将所述反应体系a的温度降至0℃,滴加次氯酸钠溶液,并控制所述反应体系a的温度在10℃之间,待次氯酸钠溶液滴加完成后,在10℃温度下保温反应1h,得到反应体系b;
79.在步骤(3
‑
1)和步骤(3
‑
2)中,控制反应温度在
‑
50℃。
80.在本实施例中,步骤(1)制备得到的8
‑
乙酰氧基
‑1‑
辛醇的收率75%,步骤(2)制备得到的8
‑
乙酰氧基
‑1‑
辛醛的收率94%;步骤(3)制备得到的顺(反)
‑8‑
十二碳烯醇乙酸酯的收率为75%。
81.显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本专利申请权利要求的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1