一种基于非洲猪瘟病毒P30、P72蛋白的病毒样颗粒的制备与应用
一种基于非洲猪瘟病毒p30、p72蛋白的病毒样颗粒的制备与应用
技术领域
1.本发明属于生物技术领域,涉及一种表面展示非洲猪瘟病毒p30、p72蛋白的病毒样颗粒(vlp)颗粒的制备及其应用。
背景技术:
2.非洲猪瘟(infection with african swine fever virus,asf)是由非洲猪瘟病毒(african swine fever virus,asfv)感染家猪和野猪而引起的一种急性、出血性的烈性传染病。急性型非洲猪瘟起病快,病程短,以高热、食欲不振、发紫、内脏大出血、病死率近100%为特征
1.。世界动物卫生组织(oie)将其列为法定报告动物疫病,我国将其列为一类动物疫病和重点防范的外来动物疫病之一。我国自2018年8月暴发首例asf以来,截止2019年6月6日,已有32个省份累计暴发137起疫情(oie和农业农村部统计数据),几乎席卷我国所有省份和地区。我国作为世界猪肉产量最大国(约占世界总产量的50%),这场突如其来的asf疫情对我国的养猪业构成巨大威胁
2.。
3.asfv为有囊膜的双链dna病毒,是非洲猪瘟相关病毒科(asfarviridae)非洲猪瘟病毒属(asfivirus)的唯一成员,也是迄今发现的唯一dna虫媒病毒。胞外病毒粒子直径约为200nm,由内核(internal core)、内核心壳(core shell)、内膜(inner envelope)、衣壳(capsid)、囊膜(external envelope)形成的同心多层20面体对称结构组成
3.。asfv基因组为170
‑
190kb的线性双链dna,含有约150
‑
181个开放阅读框,编码约150
‑
200种蛋白
4.。内核心壳由pp220、pp62等多聚蛋白构成。内膜在电子显微镜下为单脂膜
5.,主要来源于内质网膜,包含p54、p17、p12蛋白。衣壳由2 000多个六边形壳粒组成,主要为p72蛋白,占病毒粒子总量的33%,衣壳蛋白p72、pe120r介导成熟病毒粒子从病毒工厂到细胞膜转运、出芽排出,p72具有促进病毒蛋白折叠/降解的伴侣分子样作用,可募集hsp70促进病毒蛋白的折叠。p54和p30蛋白参与病毒附着的两个不同步骤,介导asfv病毒与细胞受体之间的特异性相互作用,并且都有助于抗体介导的保护性免疫应答
6.,其中p30蛋白在病毒感染细胞的内化过程中起作用
7.。由于asfv生物学特性的复杂性,迄今未能研制出安全有效的疫苗
8.。p30、p72蛋白在病毒感染过程中的重要作用,使其成为疫苗开发、抗体治疗和基于抗原的诊断检测的重要靶点。
4.噬菌体展示技术经过20年的发展完善,已被广泛应用于抗原抗体库的建立、药物设计、疫苗研究、病原检测、基因治疗、抗原表位研究及细胞信号转导研究等
9.。由于噬菌体展示技术实现了基因型和表型的有效转换,因此人们可以在基因分子克隆基础上实现蛋白质构象体外控制,从而为获取具有良好生物学活性的表达产物提供了强有力手段。t7噬菌体展示技术具有稳定性高、特异性强、表达量高、操作简单、易于富集等优势
10.。利用t7噬菌体展示技术将外源蛋白展示于噬菌体表面,可制备重组vlp颗粒。通过vlp制备的新型基因工程疫苗,具有免疫保护效果突出、安全性好、抗原纯度高等特点。同时,还能为机体提供多重保护,有效刺激动物机体产生细胞免疫、体液免疫、粘膜免疫,为机体打造全方位免疫
保护,具有良好的应用前景。
技术实现要素:
5.为了解决现有技术中的问题,本发明提供一种基于非洲猪瘟病毒p30、p72蛋白的病毒样颗粒的制备与应用,解决现有技术中asfv迄今未能研制出安全有效的疫苗的问题。
6.本发明目的是通过如下技术方案实现的:
7.表达asfv病毒p30
‑
spycatcher融合蛋白的pet
‑
28a原核表达载体pet
‑
28a
‑
p30
‑
sc,序列特征为seq id no.4。
8.表达asfv病毒p72
‑
spycatcher融合蛋白的pet
‑
28a原核表达载体pet
‑
28a
‑
p72
‑
sc,序列特征为seq id no.5。
9.表达蛋白
‑
spycatcher融合蛋白的基因,包含asfv p30、p72蛋白和spycatcher标签蛋白,蛋白与标签之间以一段柔性肽连接,p30
‑
sc氨基酸序列特征为seq id no.6,p72
‑
sc氨基酸序列特征为seq id no.7。
10.一种基于非洲猪瘟病毒p30、p72蛋白的病毒样颗粒的制备方法,构建表达载体pet
‑
28a
‑
p30
‑
sc和pet
‑
28a
‑
p72
‑
sc并表达纯化融合蛋白,将大肠杆菌原核表达系统纯化的p30
‑
sc、p72
‑
sc融合蛋白在缓冲液中,分别与表面展示st标签蛋白的重组t7噬菌体颗粒t7
‑
st共同孵育,验证结合情况,通过板式化学发光实验对制备的病毒样颗粒颗粒的免疫原性进行评估。
11.所述构建表达载体pet
‑
28a
‑
p30
‑
sc和pet
‑
28a
‑
p72
‑
sc并表达纯化融合蛋白,具体包括以下步骤:
12.(1)asfv p30、p72基因的pcr扩增:以实验室现存基因所在质粒为模板,设计无缝克隆引物扩增p30、p72蛋白编码基因用于pet
‑
28a
‑
spycatcher原核载体连接;
13.(2)spycatcher基因的合成:将spycatcher基因序列合成于pet
‑
28a原核表达载体之上,在序列n段加上一段柔性肽序列,得到pet
‑
28a
‑
spycatcher表达载体,核苷酸序列为seq id no.8;
14.(3)表达p30
‑
sc、p72
‑
sc原核表达载体的构建及蛋白纯化:通过无缝克隆,将p30、p72基因序列分别克隆至pet
‑
28a
‑
spycatcher原核表达载体上,得到pet
‑
28a
‑
p30
‑
sc重组质粒,序列特征为seq no.4和pet
‑
28a
‑
p72
‑
sc重组质粒,序列特征为seq no.5;重组质粒转化大肠杆菌bl21表达菌株,经过蛋白纯化获得p30
‑
sc、p72
‑
sc融合蛋白。
15.所述表面展示st标签蛋白的重组t7噬菌体的构建方法为:通过t7噬菌体展示技术,将外源spytag蛋白基因片段插入到t7噬菌体基因组中,通过体外包装,获得表面展示st蛋白的t7噬菌体。具体包括以下步骤:
16.(1)首先通过基因合成获得st基因,基因n段加入一段柔性肽,合成序列两端加入ecor i和hind iii限制性酶切位点序列及相应的保护性碱基,序列特征为seq id no.1;
17.(2)重组噬菌体基因的构建:通过ecor i和hind iii两种限制性内切酶双酶切合成的st基因,之后通过t4连接酶将酶切产物与t7载体臂相连接,从而获得重组噬菌体基因组;
18.(3)体外包装:将步骤(2)中连接产物与t7包装提取物混合孵育,获得完整的含有重组基因组的t7噬菌体颗粒;
19.(4)噬菌斑分析:通过双层琼脂培养法,对包装产物进行噬菌斑计数,从而计算噬菌体滴度;
20.(5)文库鉴定:蛋白酶k法提取t7 dna,然后用t7通用引物进行pcr鉴定,最终得到所需要的噬菌体;
21.(6)文库扩增:使用液体裂解液法对噬菌斑进行扩增,待菌液变澄清后,离心将细胞碎片去除;通过peg/nacl沉淀法,对上清中的噬菌体进行浓缩,之后通过噬菌斑计数测定浓缩后的噬菌体滴度。
22.利用上述方法制备的病毒样颗粒在制备用于抗非洲猪瘟病毒药物中的应用。
23.本发明有益效果:本发明基于在非洲猪瘟病毒感染细胞及内化过程中起重要作用的p30蛋白以及asfv主要衣壳蛋白p72,利用spycatcher与spytag之间异肽键的特异性相互作用,制成了表面展示病毒致病相关p30、p72蛋白的vlp颗粒。与新型的腺病毒疫苗、mrna疫苗相比,通过vlp制备的新型基因工程疫苗,具有免疫保护效果突出、安全性好、抗原纯度高等特点。同时,还能为机体提供多重保护,有效刺激动物机体产生细胞免疫、体液免疫、粘膜免疫,为机体打造全方位免疫保护,具有良好的应用前景,为非洲猪瘟病毒的免疫防控提供选择。表面展示st的工程化t7噬菌体展示文库的构建具有一定的创新性,在为asfv的防控提供新思路与制剂的同时,也为其他疾病免疫防控制剂的制备奠定了基础。
附图说明
24.图1:包装产物噬菌斑分析结果;
25.图2:噬菌体重组率鉴定;
26.图3:文库扩增后噬菌斑分析测定噬菌体滴度;
27.图4:p30、p72基因无缝克隆pcr扩增结果;
28.图5:pet
‑
28a
‑
p30
‑
sc和pet
‑
28a
‑
p72
‑
sc重组质粒转化大肠杆菌后的转化子检测,1
‑
3泳道分别代表p30
‑
sc大肠杆菌转化子菌落pcr检测结果;4
‑
6泳道分别代表p72
‑
sc大肠杆菌转化子菌落pcr检测结果;
29.图6:p30
‑
sc融合蛋白预表达结果;
30.图7:p30
‑
sc融合蛋白大规模表达纯化结果;
31.图8:p72
‑
sc融合蛋白预表达结果;
32.图9:p72
‑
sc融合蛋白大规模表达纯化结果;
33.图10:p30
‑
sc展示在t7
‑
st表面示意图;
34.图11:sds
‑
page验证p30
‑
sc、p72
‑
sc与t7
‑
st结合情况;
35.图12:western blot验证p30
‑
sc、p72
‑
sc与t7
‑
st结合情况;
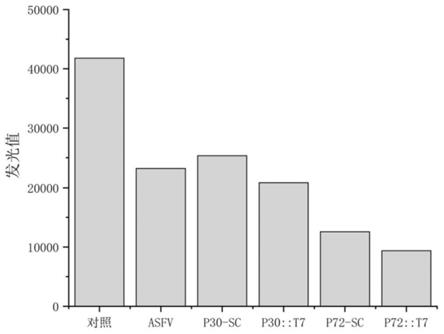
36.图13:化学发光实验验证vlp免疫原性结果。
具体实施方式
37.以下结合实例进一步阐述本发明,其中的内容不应理解为限定该发明的范围。实施例中所述试剂除特别说明,均为商业化试剂。
38.实施例1.表面展示spytag的工程化噬菌体的构建
39.(1)spytag片段的获得
40.将带有柔性肽和ecor i/hind iii酶切位点序列(带保护性碱基)的spytag片段,设计单链互补引物,退火合成双链基因片段,序列特征为seq no.1。
41.连接反应需要的目的基因片段为0.06pmol,合成的的基因总量为5nmol/管,因此加入50μl的ddh2o溶解后,浓度为0.1nmol,即100pmol,故需将片段再100倍稀释至1pmol后,取1μl进行双酶切。将上述合成基因片段经ecor i/hind iii双酶切,酶切体系如下:
[0042][0043]
37℃,酶切2h后,65℃,10min,使酶灭活,这样就得到终浓度为0.1pmol的插入基因片段。
[0044]
(2)spytag片段与t7载体臂的连接
[0045]
为了获得最大的克隆效率,优化每种插入物制备的插入物:载体比率是有必要的。最佳比例将根据插入片段的性质和质量而变化,但是通常在1:1至3:1的摩尔比(插入片段:载体)下可获得最高的克隆效率。插入制剂应不含干扰物质(盐,引物,核苷酸等)。通过使纯化的寡核苷酸退火而制备的插入物无需进一步处理即可使用。
[0046]
连接体系如下:
[0047][0048][0049]
将连接体系置于金属浴上,25℃连接3h。
[0050]
(3)体外包装
[0051]
1、让t7 select包装提取物在冰上解冻(提取物的体积为25μl,可包装高达1μg的载体dna而不会降低效率);
[0052]
2、每25μl提取物加入5μl连接反应。用吸管顶端轻轻搅拌,不要旋转;
[0053]
3、在室温(22℃)下孵化反应2小时;
[0054]
4、加入270μl无菌lb培养基停止反应。(如果包装产物在扩增前储存超过24小时,加入20μl氯仿并通过倒置轻轻混合。包装反应可在4℃保存长达一周,滴度没有明显损失。为了长期储存,包装后的噬菌体必须用平板或液体培养的方法进行扩增。)
[0055]
5、进行如下所述的空斑分析以确定产生的重组子的数量。
[0056]
(4)噬菌斑分析
[0057]
1、在平板划线的宿主菌株中,挑取单菌落接种在无抗无菌lb培养基中,在37℃摇动培养至od600=1.0。不要使用储存时间超过48小时的宿主细胞。
[0058]
2、融化上层琼脂培养基,分装至试管中,每管4ml,将其转移到45℃水浴中。
[0059]
3、使用无菌lb培养基作为稀释剂,准备一系列样品稀释液。通常,重组噬菌体的适当稀释度为103‑
106。
[0060]
4、吸取500μl对数期菌液至ep管中,每个ep管中加入5μl的包装产物(t7噬菌体),吸附5
‑
10min。
[0061]
6、将上述ep管中的混合物加入到预热的含上层琼脂培养基的试管中,混合均匀后倒入预热(37℃)的无抗无菌lb琼脂平板上。立即(轻轻地)旋转平板,使琼脂均匀分布。
[0062]
7、让平板静置几分钟,直到顶部琼脂变硬,然后倒置并在37℃孵育3
‑
4小时,或在室温下过夜。
[0063]
8、计数噬菌斑并计算噬菌体滴度.
[0064]
菌斑测定结果如图1所示,最终平板上噬菌斑数为2,经计算,噬菌体滴度为200pfu。
[0065]
(5)噬菌体文库重组率鉴定
[0066]
1、蛋白酶k法提取病毒dna。挑取噬菌斑至5ml对数期bl21菌液中,
[0067]
37℃培养至菌液澄清;取500μl裂解后菌液,5000rpm离心20min后,取250μl上清,加入100μl te缓冲液,75μl 10%sds和25μl蛋白酶k,58℃裂解2h;加入500μl氯仿,13000rpm,4℃,离心5min;取上层水相,加入无水乙醇至终浓度为70%,于4℃中过夜醇沉;13000rpm,4℃,离心15min,弃上清,室温下晾干;加入200μl ddh2o溶解。
[0068]
2、使用t7通用检测引物t7
‑
f(seq id no.9:
[0069]
ggagctgtcgtattccagtc)和t7
‑
r(seq id no.10:
[0070]
aacccctcaagacccgttta)进行噬菌体基因组pcr验证,结果如图2所示,pcr产物大小为176bp,两个噬菌斑所提取的基因组均验证正确,说明噬菌体文库重组率为100%。
[0071]
(6)文库扩增
[0072]
1、液体裂解液法扩增噬菌体文库。宿主菌大肠杆菌37℃培养od600=0.8左右时,加入噬菌体继续培养;
[0073]
2、待培养物开始变澄清时,终止培养,8000rpm离心10min,收集上清即为扩增后的噬菌体文库;
[0074]
3、浓缩纯化噬菌体。慢慢搅动并加入nacl至终浓度为0.5mol/l,这有利于病毒的沉淀,再等量加入10%peg;
[0075]
4、4℃过夜或放置一段时间;
[0076]
5、8000rpm离心30分钟,收集病毒沉淀;
[0077]
6、将病毒沉淀加入适量的1
×
pbs中,4℃过夜;
[0078]
7、10000r/min离心1小时,沉淀即为浓缩的病毒。还可以用梯度离心或其他方法进一步纯化。
[0079]
8、对扩增后文库进行噬菌斑测定。
[0080]
结果如图3所示,108倍稀释的平板上,噬菌斑数量为325,经计算,扩增后噬菌体文库滴度为3.25
×
10
12
pfu。
[0081]
实施例2.p30
‑
sc融合蛋白的原核表达纯化
[0082]
(1)p30、p72基因的扩增
[0083]
p30基因序列参考asfv病毒p30基因序列(genbank号:jq764967.1),以实验室现存质粒为模板,设计无缝克隆引物p30
‑
f(seq id no.11:cagcaaatgggtcgcggatccatgaaaatggaggtcatcttcaaaa)和p30
‑
r(seq id no.12:accggaattcgagtcggatccttttttttttaaaagtttaataaccatgag)扩增asfv p30蛋白编码基因p30用于原核载体连接。
[0084]
p72基因序列参考asfv病毒p72基因序列(genbank号:ay578708.1),以实验室现存质粒为模板,设计无缝克隆引物p72
‑
f(seq id no.13:cagcaaatgggtcgcggatcc atggcatcaggaggagctttttgtc)和p72
‑
r(seq id no.14:accggaattcgagtcggatccggtatggctacacgttcgctgcgta)扩增asfv p72蛋白编码基因p72用于原核载体连接。
[0085]
pcr体系为:
[0086][0087]
使用以下pcr程序进行扩增:
[0088][0089]
p30 pcr扩增产物大小为603bp,p72 pcr扩增产物大小为854bp,结果图如图4所示。
[0090]
(2)pet
‑
28a
‑
p30
‑
sc、pet
‑
28a
‑
p72
‑
sc表达载体的构建
[0091]
将p30、p72基因连接到pet
‑
28a
‑
spycatcher表达载体上(公司合成,序列特征为seq no.8)。pet
‑
28a
‑
spycatcher载体经bamh i酶切线性化后与无缝引物pcr扩增后的p30、p72基因连接,利用无缝克隆试剂盒(c112
‑
01,vazyme)获得连接产物,并转化e.coli dh5α。大肠杆菌转化子经卡那霉素抗性平板筛选,并用p30无缝克隆引物(p30
‑
f:
[0092]
cagcaaatgggtcgcggatccatgaaaatggaggtcatcttcaaaa(seq id no.11)和p30
‑
r:accggaattcgagtcggatccttttttttttaaaagtttaataaccatgag(seq id no.12))和p72无缝克隆引物(p72
‑
f:cagcaaatgggtcgcggatccatggcatcaggaggagctttttgtc(seq id no.13)和p72
‑
r:accggaattcgagtcggatcc ggtatggctacacgttcgctgcgta(seq id no.14))进行pcr验证及测序。
[0093]
结果如图5所示,p30菌落pcr扩增产物大小在603bp,阳性转化子为no.1号,p72菌落pcr扩增产物大小在854bp,阳性转化子为no.5号,测序结果表明,与预期结果一致,表明pet
‑
28a
‑
p30
‑
sc与pet
‑
28a
‑
p72
‑
sc表达载体构建成功。
[0094]
(3)p30
‑
sc、p72
‑
sc融合蛋白的表达纯化
[0095]
1、p30
‑
sc、p72
‑
sc融合蛋白的试表达。
[0096]
转化重组质粒:
[0097]
1.从
‑
80℃冰箱中取出bl21感受态(100μl/tube)置于冰上化冻约5min;
[0098]
2.取1μl质粒加至感受态细胞中,轻弹ep管壁数下后冰上放置30min;
[0099]
3.热击:将细胞置于42℃水中热击45sec后即刻插在冰上2min;
[0100]
4.在ep管中加入600μl无抗lb,在37℃摇床上培育45min;
[0101]
5.铺细胞:吸取100μl细胞至平板中用涂布棒涂匀;
[0102]
6.将铺好细胞的平板静置2min后,37℃倒置培养14小时。
[0103]
诱导试表达:
[0104]
1.挑取1个典型单菌落至5ml卡那霉素抗性lb培养基中,分别编号,将试管至于37℃摇床中震荡培养5h。
[0105]
2.取出试管,此时菌体od600≈1.2
[0106]
①
保种:分别取800μl菌液至保种管中,再加入800μl 50%甘油,混匀,并分别标明蛋白名称、载体名称、菌株名称、抗性、日期、编号,存放于
‑
80℃冰箱;
[0107]
②
对照取样:分别取800μl菌液至ep管中,分别记录编号;
[0108]
③
诱导:在剩下的菌液中分别加入1.5μl 1m iptg,将试管至于16℃摇床继续诱导培养5h;
[0109]
3.取出试管,分别取800μl菌液至ep管中,剩下的菌液超声破碎菌体后12000rpm,4℃离心10min,将上清和沉淀分开,分别记录编号;
[0110]
4.制样:分别将对照样品、诱导后样品和沉淀样品离心,弃上清,用100μl无菌水重悬菌液后加入20μl 6
×
sds loading buffer,在100μl上清样品中同样加入20μl 6
×
sds loading buffer,涡旋震荡混匀后置于100℃金属煮样器中煮10分钟;
[0111]
5.跑电泳:将煮好的样品离心,点样时尽量吸取上层样品5μl,电压:150v,时常:50min。
[0112]
6.染色:将胶从胶板中取出用清水清洗后,置于染色盒内加入清水,微波炉高火煮5min,弃水,再加入染色液,微波炉高火煮1min,取出后静置5min,回收染色液,最后用水再煮5min,此时可见条带。
[0113]
7.鉴定:根据marker大小,对比未诱导组鉴定是否有表达,如果有表达,则可准备下一步大规模生产。
[0114]
蛋白试表达结果如图6、图8所示,在诱导后的条带中可见目的蛋白成功表达,分子量符合预测大小,为可溶性蛋白。
[0115]
大规模表达纯化:
[0116]
提前一天挑取保存的p30 bl21甘油菌至5ml卡那霉素抗性的lb培养基中,活化菌株;第二天将5ml菌液平均转移至两个900ml的卡那霉素抗性lb培养基中,37℃,220rpm培养5h至od600=1.2左右;将摇床温度设置为16℃降温1h,然后在培养基中2加入360μl iptg,16℃,220rpm过夜培养16
‑
17h;收菌:将诱导后的菌液倒至离心瓶中(倒三分之二,不要倒满),秤好并对称放至离心机中,4000g离心20分钟;上清倒掉,用勺将细菌抠下来,转移至烧杯中,悬菌buffer重悬菌液;菌液中按照1:100加入1m的pmsf,然后使用高压破菌仪破碎菌体;将破碎后菌液转移至超速离心管中,18000rpm,4℃离心30min;将上清进行镍柱亲和层
析,20mm咪唑洗杂,300mm咪唑洗脱蛋白,洗脱是分8次,每次1ml;制样:取每管洗脱蛋白20μl,加入4μl 6
×
sds loading buffer,沸水煮10min后上样。
[0117]
将所制样品进行sds
‑
page电泳,结果如图7、图9所示,成功得到p30
‑
sc和p72
‑
sc融合蛋白,p30
‑
sc分子量在37kda左右,p72
‑
sc分子量在45kda左右。
[0118]
实施例3.表面展示p30
‑
sc、p72
‑
sc的t7噬菌体vlp颗粒的制备
[0119]
使用实施例2中纯化方法得到的蛋白溶于高浓度的咪唑中,因此需要通过透析,将蛋白缓冲液置换为1
×
pbs。将透析后的蛋白通过浓缩管浓缩后,取20μl蛋白与先前纯化的等体积的t7
‑
st噬菌体共同孵育,4℃过夜即得到所制备的vlp颗粒(p30
‑
sc::t7
‑
st,简称p30::t7;p72
‑
sc::t7
‑
st,简称p72::t7)。结合后得到的vlp结构如图10所示,每个t7
‑
st噬菌体表面原则上可展示高达415个拷贝的融合蛋白。
[0120]
实施例4.p30::t7与p72::t7 vlp颗粒的表征
[0121]
1、sds
‑
page验证。分别取t7
‑
st、p30
‑
sc、p30::t7和p72::t7各20μl,加入5μl 5
×
sds loading buffer,沸水浴煮样10min,12000rpm离心10min,吸取8μl上清用于12%sds
‑
page电泳。
[0122]
图11结果表明,p30
‑
sc蛋白结合t7
‑
st噬菌体后,分子量为77kda,大小正确,表明p30
‑
sc成功结合并展示在t7
‑
st噬菌体表面;p72
‑
sc蛋白结合t7
‑
st噬菌体后,分子量为85kda,大小正确,表明p72
‑
sc成功结合并展示在t7
‑
st噬菌体表面。
[0123]
2、western blot验证。由于t7
‑
st本身不带有his标签,所以分别取t7
‑
st、p30
‑
sc、p30::t7、p72::t7样品各20μl,加入5μl 5
×
sds loading buffer,沸水浴煮样10min,12000rpm离心10min,吸取5μl上清用于12%sds
‑
page电泳。
[0124]
通过湿转法将蛋白分离胶转移至与其同等大小的pvdf膜上,在300ma 100min条件下转膜;室温下用5%脱脂牛奶封闭1小时;将膜完全浸没在用5%bsa 1:2000稀释的鼠抗his单克隆抗体(ht501,transgene)中,4℃置于摇床上孵育过夜;回收一抗,用1
×
tbst缓冲液漂洗pvdf膜3次,每次10min;用5%bsa 1:5000稀释的羊抗鼠hrp标记二抗(lk2003,sungene biotech)室温孵育1h;用1
×
tbst缓冲液漂洗pvdf膜3次,每次10min;避光向pvdf膜正面滴加化学发光显色底物(34075,thermofisher),通过bio
‑
rad化学发光成像仪曝光,观察蛋白展示情况。
[0125]
结果如图12所示,结合后的p30::t7分子量在77kda,p72::t7分子量在85kda,大小正确。western blot结果表明p30
‑
sc与p72
‑
sc成功结合并展示在t7
‑
st噬菌体表面。
[0126]
3、化学发光实验。
[0127]
通过酶联抗体竞争吸附板式化学发光实验,来对制备的p30::t7、p72::t7vlp颗粒的免疫原性进行初步的评估。具体步骤如下:
[0128]
1、包被(优化包被液与包被浓度)
[0129]
(1)将待包被蛋白稀释2μg/ml浓度,准备发光板,按照100μl每孔包被,4℃包被过夜;
[0130]
(2)包被过夜后,洗涤液洗涤两次,并拍干;
[0131]
2、封闭
[0132]
(1)上述拍干后的发光板,每孔加入350μl封闭液,置于37℃,封闭1小时;
[0133]
(2)封闭结束后,甩出封闭液,拍干,完成封闭;
response[j].1998,243(2):461
‑
71.
[0153]
[8]rock,d.l.,challenges for african swine fever vaccine development
‑
"...perhaps the end of the beginning".veterinary microbiology,2017.206:p.52
‑
58.
[0154]
[9]sheehan,jared,and wayne a marasco.“phage and yeast display.”microbiology spectrum vol.3,1(2015):aid
‑
0028
‑
2014.
[0155]
[10]piggott,andrew m,and peter karuso.“identifying the cellular targets of natural products using t7 phage display.”natural product reports vol.33,5(2016):626
‑
36.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1