维吾尔药材中二萜及其制备方法和作为制备预防或/和治疗炎症的抗炎、抗菌药物中的应用与流程
1.本发明涉及大苞荆芥分离纯化技术领域,是一种维吾尔药材中二萜及其制备方法和作为制备预防或/和治疗炎症的抗炎、抗菌药物中的应用,维吾尔药材中二萜成分为所述3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthre n-9-ol(nepetabrate c)的简称。
背景技术:
2.大苞荆芥nepeta bracteata benth为唇形科labiatae荆芥属nepeta植物,主要分布于巴基斯坦,尼泊尔,伊朗等国家,维吾尔名为“祖发”,习称神香草,临床用药广泛,主要以进口为主。其全草入药,气微清香,味淡、性微湿,入肺、肝经,具有镇咳平喘、清热利湿的作用,临床上用于治疗气管炎症,咳嗽气喘、感冒发烧、小便不利等症状。此外,大苞荆芥还具有来源容易、成本低廉、临床疗效可靠、毒副作用小等特点。迄今为止,对大苞荆芥进行探究的重点以及基础理论研究还不多见,现代药理学表明,其提取物具有显著的抗炎、抑菌活性,但尚未对化学成分进行相关研究,大苞荆芥可能是一味治疗呼吸系统疾病很好的物种,因此,近年来备受人们的关注。
3.大苞荆芥的药效主要来源于其中的萜类化合物,包括单萜类和二萜类化合物,其中优势成分二萜类成分抗炎、抑菌活性较好,因此,开发和利用大苞荆芥的二萜类单体化合物,进一步挖掘其潜在的药用价值,并对其单体化合物的结构和理化性质进行确定和表征,对于开发利用大苞荆芥具有重要意义。
技术实现要素:
4.本发明提供了一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)及其制备方法和应用,克服了上述现有技术之不足,其首次公开了3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isoprop yl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)及其作为制备预防炎症及抑菌药物或/和制备抗炎、抗菌药物或/和制备防治炎症及抑菌保健品的应用。
5.本发明的技术方案之一是通过以下措施来实现的:一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),化学结构式为
[0006][0007]
下面是对上述发明技术方案之一的进一步优化或/和改进:
[0008]
上述按照下述方法制备得到:第一步,将大苞荆芥粉碎并加入乙醇,在室温下浸泡3小时至4小时后,在50℃至60℃条件下加热回流提取3次,每次1小时至3小时,合并每次回流提取液并减压回收、浓缩,得大苞荆芥总浸膏;第二步,将大苞荆芥总浸膏用水分散,依次用石油醚和二氯甲烷萃取,得到石油醚部位和二氯甲烷部位;第三步,取石油醚部位浸膏用硅胶柱色谱梯度洗脱分离后得到8个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为1:0、100:1、50:1、25:1、8:1、5:1、1:1、1:0;第四步,将得到的8个馏分中第6个馏分再经硅胶柱色谱梯度洗脱分离后得到5个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为20:1、10:1、3:1、1:1、0:1;第五步,再将得到的5个馏分中第3个馏分再经硅胶柱色谱梯度洗脱分离后得到3个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为10:1、5:1、3:1;第六步,再将得到的3个馏分中第3个馏分再经高效液相色谱梯度洗脱纯化分离,并收集洗脱物,在第28.6分钟处得到3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)。
[0009]
上述第一步中,每1g大苞荆芥加入8ml至10ml乙醇。
[0010]
上述第六步中,高效液相色谱梯度洗脱的洗脱液为甲醇和水的混合液,其中,甲醇和水的体积比为85:15。
[0011]
本发明的技术方案之二是通过以下措施来实现的:一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的制备方法,按照下述步骤进行:第一步,将大苞荆芥粉碎并加入乙醇,在室温下浸泡3小时至4小时后,在50℃至60℃条件下加热回流提取3次,每次1小时至3小时,合并每次回流提取液并减压回收、浓缩,得大苞荆芥总浸膏;第二步,将大苞荆芥总浸膏用水分散,依次用石油醚和二氯甲烷萃取,得到石油醚部位和二氯甲烷部位;第三步,取石油醚部位浸膏用硅胶柱色谱梯度洗脱分离后得到8个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为1:0、100:1、50:1、25:1、8:1、5:1、1:1、1:0;第四步,将得到的8个馏分中第6个馏分再经硅胶柱色谱梯度洗脱分离后得到5个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为20:1、10:1、3:1、1:1、0:1;第五步,再将得到的5个馏分中第3个馏分再经硅胶柱色谱梯度洗脱分离后得到3个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为10:1、5:1、3:1;第六步,再将得到的3个馏分中第3个馏分再经高效液相色谱梯度洗脱纯化分离,并收集洗脱物,在第28.6分钟处得到3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)。
[0012]
下面是对上述发明技术方案之二的进一步优化或/和改进:
[0013]
上述第一步中,每1g大苞荆芥加入8ml至10ml乙醇。
[0014]
上述第六步中,高效液相色谱梯度洗脱的洗脱液为甲醇和水的混合液,其中,甲醇和水的体积比为85:15。
[0015]
本发明的技术方案之三是通过以下措施来实现的:一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备预防炎症及抑菌药物的应用。
[0016]
本发明的技术方案之四是通过以下措施来实现的:一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备抗炎及抗菌药物的应用。
[0017]
本发明的技术方案之五是通过以下措施来实现的:一种3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备防治炎症及抑菌保健品的应用。
[0018]
本发明首次公开了化合物3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopr opyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),并将该化合物进行了体外抗炎及抗菌药效学实验,实验明显可以看出该化合物对raw 264.7细胞和金黄色葡萄球菌及大肠杆菌具有较强的抑制作用,从而使该化合物能够作为制备预防炎症及抑菌药物或/和制备抗炎、抗菌药物或/和制备防治炎症及抑菌保健品的应用。
附图说明
[0019]
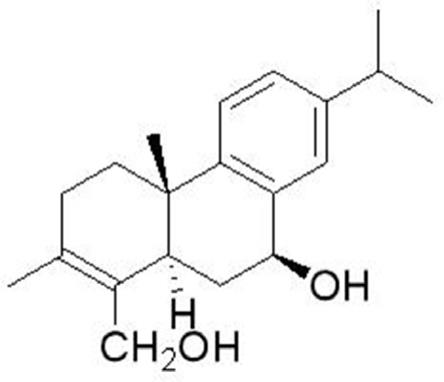
附图1为本发明所述3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的化学结构图。
[0020]
附图2为本发明所述3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的1h-nmr谱图。
[0021]
附图3为本发明所述3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的
13
c-apt谱图。
具体实施方式
[0022]
本发明不受下述实施例的限制,可根据本发明的技术方案与实际情况来确定具体的实施方式。本发明中所提到各种化学试剂和化学用品如无特殊说明,均为现有技术中公知公用的化学试剂和化学用品;本发明中的百分数如没有特殊说明,均为质量百分数;本发明中的溶液若没有特殊说明,均为溶剂为水的水溶液,例如,盐酸溶液即为盐酸水溶液;本发明中的常温、室温一般指15℃到25℃的温度,一般定义为25℃。
[0023]
下面结合实施例对本发明作进一步描述:
[0024]
实施例1:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),其特征在于化学结构式为
[0025][0026]
将本发明实施例1所述的3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopr opyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)进行核磁共振氢谱(1h-nmr)和核磁共振碳谱(
13
c-apt)分析。
[0027]
本实施例所述的3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的1h-nmr谱图如图2所示。
[0028]
本实施例所述的该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的
13
c-apt谱图如图3所示。
[0029]
对图2和图3进行图谱解析,并将图2和图3各峰进行归属,图2和图3的各峰归属如表1所示,通过表1的数据可知,本实施例所述的3,4,4a,9,10,10a-hexahydro-1-(hy droxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)的化学结构式如图1所示,易溶于氯仿、甲醇。
[0030]
实施例2:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),按照下述方法制备得到:第一步,将大苞荆芥粉碎并加入乙醇,在室温下浸泡3小时至4小时后,在50℃至60℃条件下加热回流提取3次,每次1小时至3小时,合并每次回流提取液并减压回收、浓缩,得大苞荆芥总浸膏;第二步,将大苞荆芥总浸膏用水分散,依次用石油醚和二氯甲烷萃取,得到石油醚部位和二氯甲烷部位;第三步,取石油醚部位浸膏用硅胶柱色谱梯度洗脱分离后得到8个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为1:0、100:1、50:1、25:1、8:1、5:1、1:1、1:0;第四步,将得到的8个馏分中第6个馏分再经硅胶柱色谱梯度洗脱分离后得到5个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为20:1、10:1、3:1、1:1、0:1;第五步,再将得到的5个馏分中第3个馏分再经硅胶柱色谱梯度洗脱分离后得到3个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为10:1、5:1、3:1;第六步,再将得到的3个馏分中第3个馏分再经高效液相色谱梯度洗脱纯化分离,并收集洗脱物,在第28.6分钟处得到3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)。
[0031]
实施例3:作为上述实施例的优化,该3,4,4a,9,10,10a-hexahydro-1-(hydroxymet hyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),按照下述方法制备得到:第一步,将大苞荆芥粉碎并加入乙醇,在室温下浸泡3小时或4小时后,在50℃或60℃条件下加热回流提取3次,每次1小时或3小时,合并每次回流提取液并减压回收、浓缩,得大苞荆芥总浸膏;第二步,将大苞荆芥总浸膏用水分散,依次用石油醚和二氯甲烷萃取,得到石油醚部位和二氯甲烷部位;第三步,取石油醚部位浸膏用硅胶柱色谱梯度洗脱分离后得到8个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为1:0、100:1、50:1、25:1、8:1、5:1、1:1、1:0;第四步,将得到的8个馏分中第6个馏分再经硅胶柱色谱梯度洗脱分离后得到5个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为20:1、10:1、3:1、1:1、0:1;第五步,再将得到的5个馏分中第3个馏分再经硅胶柱色谱梯度洗脱分离后得到3个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为10:1、5:1、3:1;第六步,再将得到的3个馏分中第3个馏分再经高效液相色谱梯度洗脱纯化分离,并收集洗脱物,在第28.6分钟处得到3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)。
[0032]
实施例4:作为上述实施例的优化,第一步中,每1g大苞荆芥加入8ml至10ml乙醇。
[0033]
实施例5:作为上述实施例的优化,第六步中,高效液相色谱梯度洗脱的洗脱液为甲醇和水的混合液,其中,甲醇和水的体积比为85:15。
[0034]
实施例6:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备预防炎症及抑菌药物的应用。
[0035]
实施例7:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备抗炎及抗菌药物的应用。
[0036]
实施例8:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)作为制备防治炎症及抑菌保健品的应用。
[0037]
实施例9:该3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)按照下述方法得到:第一步,将大苞荆芥粉碎并加入乙醇,在室温下浸泡3小时后,在50℃条件下加热回流提取3次,每次2小时,合并每次回流提取液并减压回收、浓缩,得大苞荆芥总浸膏;第二步,将大苞荆芥总浸膏用水分散,依次用石油醚和二氯甲烷萃取,得到石油醚部位和二氯甲烷部位;第三步,取石油醚部位浸膏用硅胶柱色谱梯度洗脱分离后得到8个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为1:0、100:1、50:1、25:1、8:1、5:1、1:1、1:0;第四步,将得到的8个馏分中第6个馏分再经硅胶柱色谱梯度洗脱分离后得到5个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为20:1、10:1、3:1、1:1、0:1;第五步,再将得到的5个馏分中第3个馏分再经硅胶柱色谱梯度洗脱分离后得到3个馏分,其中,硅胶柱色谱梯度洗脱液包括石油醚和乙酸乙酯,石油醚和乙酸乙酯的体积比依次为10:1、5:1、3:1;第六步,再将得到的3个馏分中第3个馏分再经高效液相色谱梯度洗脱纯化分离,并收集洗脱物,在第28.6分钟处得到3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropy l-2,4a-dimethylphenanthren-9-ol(nepetabrate c)。
[0038]
将本发明实施例9得到的3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopr opyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)进行体外抗炎及抗菌药效学实验,体外抗炎及抗菌药效学实验利用mtt比色法。
[0039]
以3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylph enanthren-9-ol(nepetabrate c)为实验组,以aspinin(阿司匹林,抗炎药物)为对照组,同时设立空白组,实验组、对照组和空白组选取raw 264.7细胞为实验对象,培养基稀释后,以6
×
104/ml的密度接种于96孔板,每孔100μl,培养箱中正常培养24小时后,各组加入相对应的药物,使各组药物的最终浓度分别为2.5μg/ml(1组),5μg/ml(2组),10μg/ml(3组),20μg/ml(4组),40μg/ml(5组),共设5个浓度,每个浓度3个复孔;培养48小时后,于每孔加mtt 10μl染色;继续培养四小时后,吸弃原培养液,每孔加入dmso 150μl,置摇床上低速振荡10min,使结晶物充分溶解,并于酶联免疫检测仪570nm波长处检测光密度值,根据光密度值计算50%抑制浓度(ic
50
,μm),光密度值计算ic
50
的计算方法为现有公知技术。实验组、对照组对raw 264.7细胞的ic
50
如表2所示。表2数据可以看出,本发明所述的3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)对raw264.7细胞均具有一定的抑制作用。
[0040]
以3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylph enanthren-9-ol(nepetabrate c)为实验组,以penicillin(阿莫西林,抗菌药物)为对照组,同时设立空白组,实验组、对照组和空白组选取金黄色葡萄球菌和大肠杆菌
为实验对象,将样品以无菌水或dmso稀释一定倍数后,离心取100μl加入指示菌平板的孔内,做为抑菌实验孔,取新鲜培养的指示菌株,将菌悬液浓度调至0.5mcfarland并均匀涂布在上述平板上,放置相应温度下培养24h或48h,观察各平皿的菌落生长情况。向孔中加入100μl新鲜培养基做为阴性对照孔,阿莫西林溶液做为阳性对照。培养基稀释后,以6
×
104/ml的密度接种于96孔板,每孔100μl,培养箱中正常培养24小时后,各组加入相对应的药物,使各组药物的最终浓度分别为2.5μg/ml(1组),5μg/ml(2组),10μg/ml(3组),20μg/ml(4组),40μg/ml(5组),共设5个浓度,每个浓度3个复孔;培养48小时后,于每孔加mtt 10μl染色;继续培养四小时后,吸弃原培养液,每孔加入dmso 150μl,置摇床上低速振荡10min,使结晶物充分溶解,并于酶联免疫检测仪570nm波长处检测光密度值,根据光密度值计算50%抑制浓度(ic
50
,μm),光密度值计算ic
50
的计算方法为现有公知技术。实验组、对照组对金黄色葡萄球菌和大肠杆菌的ic
50
如表3所示。表3数据可以看出,本发明所述的3,4,4a,9,10,10a-hexahydro-1-(hydroxymethyl)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c)对金黄色葡萄球菌和大肠杆菌均具有一定的抑制作用。
[0041]
综上所述,本发明首次公开了化合物3,4,4a,9,10,10a-hexahydro-1-(hydroxymethy l)-7-isopropyl-2,4a-dimethylphenanthren-9-ol(nepetabrate c),并将该化合物进行了体外抗炎及抗菌药效学实验,实验明显可以看出该化合物对raw 264.7细胞和金黄色葡萄球菌及大肠杆菌具有较强的抑制作用,从而使该化合物能够作为制备预防炎症及抑菌药物或/和制备抗炎、抗菌药物或/和制备防治炎症及抑菌保健品的应用。
[0042]
以上技术特征构成了本发明的实施例,其具有较强的适应性和实施效果,可根据实际需要增减非必要的技术特征,来满足不同情况的需求。
[0043]
表1
[0044][0045]
表2
[0046][0047]
表3
[0048]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1