一类含酰胺亚结构的二唑硫醚类化合物及其制备方法和应用
1.本技术涉及药物化学技术领域,尤其是一种含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物及其制备方法与应用。
背景技术:
2.无论是经济作物还是农业作物,都易受到各种病原体(细菌、真菌和病毒)的攻击,并引起严重的病害。植物病害已成为所有园艺系统或农业系统中作物生产的主要制约因素。据统计,每年因植物疾病造成的作物损失占世界作物产量的四分之一甚至更多。而且植物病害的爆发是不固定的,在某些情况下可能会造成颗粒无收。传统上,处理农业生态系统疾病的方法包括培育作物品种的抗性,防止污染土壤或种子传播的卫生措施,以及长时间施用单一的杀菌或抗病毒剂(如噻菌铜、噻唑锌、叶枯唑、井冈霉素、春雷霉素、宁南霉素和病毒唑等)。这些措施不仅成本高而且会显著增加了植物病原体的抗药性。同时越来越多的高毒性杀菌剂残留在环境中及人们的食品中,已导致一些杀菌剂取消注册。因此,迫切需要开发具有高活性、高选择性的新型绿色农药。
3.据文献报道,三氮唑或噁二唑类衍生物展示出了广谱生物活性,比如:抗炎、抗肿瘤、抗菌、抗真菌、抗病毒、除草、杀虫及调节植物生长等。本技术以三氮唑硫醇或噁二唑硫醇为母体,用酰胺结构将不同的活性官能团引入到此体系中,合成了一系列含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物,并考察了其生物活性,为新农药的研发和创制提供重要的科学基础。
4.2014年,liu等[liu,y.x.;song,h.j.;huang,y.q.;li,j.r.;zhao,s.;song,y.c.;yang,p.w.;xiao,z.x.;liu,y.x.;li,y.q.;shang,h.;wang,q.m.design,synthesis,and antiviral,fungicidal,and insecticidal activities of tetrahydro
‑
β
‑
carboline
‑3‑
carbohydrazide derivatives[j].j.agric.food chem.,2014,62,9987
‑
9999.]设计并合成了一系列1,2,3,4
‑
四氢
‑
β
‑
咔啉
‑3‑
羧酸衍生物,并评估了所有目标分子的生物活性。研究结果表明,不管在离体,还是活体条件下,大部分化合物对烟草花叶病毒(tmv)病毒都表现出比对照药剂病毒星更为优异的活性,田间试验结果证明了此类化合物的实践应用前景。同时,还发现此类化合物对黄瓜尖刀镰孢菌(fusarium oxysporum sp.cucumeris)等14种植物病原真菌表现出较好的生长抑制活性,对粘虫(mythimna separata)等4种害虫也有一定的杀伤作用。
[0005]
2010年,wang等[wang,b.l.;shi,y.x.;ma,y.;liu,x.h.;li,y.h.;song,h.b.;li,b.j.;li,z.m.synthesis and biological activity of some novel trifluoromethyl
‑
substituted 1,2,4
‑
triazole and bis(1,2,4
‑
triazole)mannich bases containing piperazine rings.j.agric.food chem.2010,58,5515
‑
5522.]通过曼尼希反应合成了一系列含嘧啶基哌嗪环的三氟甲基取代的1,2,4
‑
三唑曼尼希碱和双(1,2,4
‑
三唑)曼尼希碱。杀菌试验表明,大部分化合物对corynespora cassiicola,pseudomonas syringae pv.lachrymans,ascochyta citrallina smith,pseudoperonospora cubensis和
sclerotinia sclerotiorum具有很好的杀菌活性。在19个新化合物中,部分化合物表现出优于市售杀菌剂的优势。
[0006]
2017年,zhang等[zhang,j.p.;li,x.y.;dong,y.w.;qin,y.g.;li,x.l.;song,b.a.;yang,x.l.synthesis and biological evaluation of 4
‑
methyl
‑
1,2,3
‑
thiadiazole
‑5‑
carboxaldehyde benzoyl hydrazone derivatives.chinese chem.lett.2017,28,1238
‑
1242.]为寻找具有较高生物活性的新型先导化合物,设计合成了一系列新型4
‑
甲基
‑
1,2,3
‑
噻二唑
‑5‑
羧醛苯甲酰腙衍生物。初步生物活性测定表明,化合物在50μg/ml浓度下对6种真菌(valsa mali,botrytis cinerea,pythium aphanidermatum,rhizoctonia solani,fusarium moniliforme和alternaria solani)均有中等至较强的杀菌活性。部分化合物在500μg/ml时对tmv有较好的体内治疗活性(41.0%
‑
49.9%,略低于对照药宁南霉素)。化合物的构效关系分析表明,苯对位含卤素的化合物活性最好。其中某个化合物对腐烂病菌、灰霉病菌、花生腐霉、番茄丝核菌、念珠镰刀菌和番茄早疫病菌表现出广谱杀菌活性,ec
50
值分别为8.20、24.42、15.80、40.53、41.48和34.16μg/ml。
[0007]
2020年,soukhyarani gopal等[soukhyarani gopal,n.;boja,p.design,synthesis,in silico docking studies,and antibacterial activity of some thiadiazines and 1,2,4
‑
triazole
‑3‑
thiones bearing pyrazole moiety.russ.j.bioorg.chem.2020,46,97
‑
106.]设计了一系列6
‑
(substituted
‑
phenyl)
‑3‑
(5
‑
methyl
‑1‑
phenyl
‑
1h
‑
pyrazol
‑4‑
yl)
‑
7h
‑
[1,2,4]triazolo[3,4
‑
b][1,3,4]thiadiazines和4
‑
[(substituted
‑
benzylidene)amino]
‑5‑
(5
‑
methyl
‑1‑
phenyl
‑
1h
‑
pyrazol
‑4‑
yl)
‑
2,4
‑
dihydro
‑
3h
‑
1,2,4
‑
triazole
‑3‑
thiones类化合物。两类化合物对金黄色葡萄球菌、粪肠球菌、大肠杆菌和铜绿假单胞菌均有较好的抗菌活性。部分化合物的测试结果(mic)达到1.56
‑
6.25μg/ml。
[0008]
2007年,chen等[chen,c.j.;song,b.a.;yang,s.;xu,f.g.;bhadury,p.s.;jin,l.h.;hu,d.y.;li,q.z.;liu,f.;xue,w.;lu,p.;chen,z.synthesis and antifungal activities of 5
‑
(3,4,5
‑
trimethoxyphenyl)
‑2‑
sulfonyl
‑
1,3,4
‑
tthiadiazoleand 5
‑
(3,4,5
‑
trimethoxyphenyl)
‑2‑
sulfonyl
‑
1,3,4
‑
oxadiazole derivatives[j].bioorg.med.chem.2007,15,3981
‑
3989.]报道了一系列5
‑
(3,4,5
‑
三甲氧基苯基)
‑
1,3,4
‑
噁二唑
‑
砜类化合物,其中抗真菌活性测试结果显示:化合物在质量浓度为50μg/ml时对小麦赤霉病菌、黄瓜灰霉病菌和油菜菌核病菌的抑制率分别为:55.8%、100.0%、100.0%均优于对照药剂恶霉灵(52.9%、75.4%、77.5%)对该三种真菌的抑制活性。
[0009]
2016年,wang等[wang,p.y.;zhou,l.;zhou,j.;wu,z.b.;xue,w.;song,b.a.;yang,s.synthesis and antibacterial activity of pyridinium
‑
tailored 2,5
‑
substituted
‑
1,3,4
‑
oxadiazole thioether/sulfoxide/sulfone derivatives[j].bioorg.med.chem.lett.2016,26,1214
‑
1217.]报道了一系列含1,3,4
‑
噁二唑硫醚/亚砜/砜的吡啶盐类化合物,其中离体抗水稻白叶枯病菌活性测试结果显示:部分化合物的ec50值的范围达到了0.54~12.14μg/ml,而对照药剂叶枯唑对水稻白叶枯病菌ec
50
测试结果则为92.61μg/ml。
[0010]
2021年,he等[he,f.;wei,p.p.;yu,g.;guo,s.x.;zheng,z.g.;chen,s.h.;dai,
a.;zhang,r.f.;wu,z.x.;wu,j.synthesis of trans
‑
methyl ferulate bearing an oxadiazole ether as potential activators for controlling plant virus[j].bioorg.chem.2021,115,105248.]通过醚键将恶二唑结构引入反式阿魏酸中,合成了一系列含恶二唑醚的新型阿魏酸衍生物。对合成的目标化合物进行了体内抗烟草花叶病毒(tmv)活性评价,结果表明部分化合物对烟草花叶病毒(tmv)具有较强的控制活性。部分化合物在质量浓度为500mg/l时保护活性可达65.0%
‑
69.8%,优于对照药宁南霉素(64.7%)。部分化合物在质量浓度为500mg/l时治疗活性可达54.5%
‑
65.5%,优于对照药宁南霉素(54.5%)。
技术实现要素:
[0011]
本技术的目的之一提供了一种含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物或其立体异构体、或其盐或其溶剂化物。
[0012]
本技术的另一目的是提供了制备上述化合物或其立体异构体、或其盐或其溶剂化物的中间体化合物及其制备方法。
[0013]
本技术还有一目的是提供了一种含有上述化合物或其立体异构体、或其盐或其溶剂化物的组合物。
[0014]
本技术还有一目的是提供了上述化合物或其立体异构体、或其盐或其溶剂化物,或所述组合物的用途。
[0015]
本技术另一目的是提供了利用上述化合物或其立体异构体、或其盐或其溶剂化物,或所述组合物防治农业病虫害的方法。
[0016]
为实现上述目的,本技术采用了下述技术方案:
[0017]
一种含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
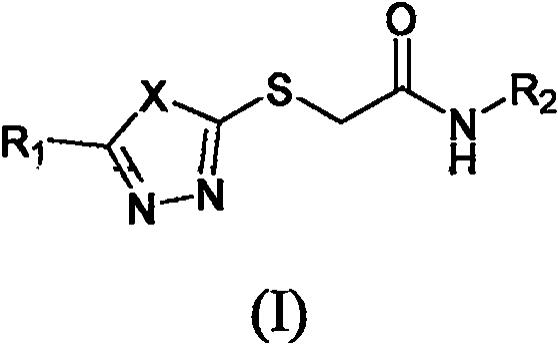
噻/噁二唑硫醚类化合物或其立体异构体、或其盐或其溶剂化物,该化合物具有如通式(i)所示的结构:
[0018][0019]
x为o,s或n
‑
nh2[0020]
r1选自氢、取代或未取代的烷基、任意取代或未取代的芳基、任意取代或未取代的苄基、任意取代或未取代的杂芳基中的一个或多个;
[0021]
r2选自氢、任意取代或未取代的烷基、任意取代或未取代的芳基、任意取代或未取代的苄基、任意取代或未取代的杂芳基中的一个或个。
[0022]
优选地,r1和r2各自独立的选自氢、氘、任意取代或未取代的烷基、任意取代或未取代的烷氧基、任意取代或未取代的环烷基、任意取代或未取代的芳基、任意取代或未取代的杂芳基中的一个或多个;更优选地,r1和r2各自独立的选自氢、任意取代或未取代的c1‑
c5烷基、任意取代或未取代的c5‑
c
10
环烷基、任意取代或未取代的c5‑
c
10
芳基、任意取代或未取代的c5‑
c
10
杂芳基、任意取代或未取代的苄基、22种常见的氨基酸甲酯;最优选地,r1和r2各自独立的选自氢、氘、甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异
戊基、新戊基、甲氧基、乙氧基、丙氧基、丁氧基、苯基、氯苯基、溴苯基、氟苯基、甲苯基、胺苯基、羟苯基、苄基、邻氟苄基、间氟苄基、对氟苄基、邻氯苄基、间氯苄基、对氯苄基、邻溴苄基、间溴苄基、对溴苄基、萘基、菲基、吡啶基、邻氟吡啶基、间氟吡啶基、邻溴吡啶基、间溴吡啶基、邻氯吡啶基、间氯吡啶基、邻氟噻吩基、间氟噻吩基、邻氟呋喃基、邻氟四氢呋喃基、间氟呋喃基、间氟四氢呋喃基、邻溴噻吩基、间溴噻吩基、邻溴呋喃基、间溴呋喃基、邻溴四氢呋喃基、间溴四氢呋喃基、邻氯噻吩基、间氯噻吩基、邻氯呋喃基、间氯呋喃基、邻氯四氢呋喃基、间氯四氢呋喃基、邻羟基苄基、间羟基苄基、对羟基苄基、邻氨基苄基、间氨基苄基、对氨基苄基、邻甲基苄基、间甲基苄基、对甲基苄基、邻羟基吡啶、间羟基吡啶基、对羟基吡啶基、邻氨基噻吩基、间氨基噻吩基、邻羟基呋喃基、间羟基呋喃基、邻羟基四氢呋喃基、间羟基四氢呋喃基、邻甲基呋喃基、间甲基呋喃基、邻甲基四氢呋喃基、间甲基四氢呋喃基、邻呋喃亚甲基、间呋喃亚甲基、邻四氢呋喃亚甲基、间四氢呋喃亚甲基中的一个或多个、甘氨酸甲酯、丙氨酸甲酯、缬氨酸甲酯、亮氨酸甲酯、异亮氨酸甲酯、甲硫氨酸甲酯、脯氨酸甲酯、色氨酸甲酯、丝氨酸甲酯、酪氨酸甲酯、半胱氨酸甲酯、苯丙氨酸甲酯、天冬酰胺甲酯、谷氨酰胺甲酯、苏氨酸甲酯、天冬氨酸甲酯、谷氨酸甲酯、赖氨酸甲酯、精氨酸甲酯、组氨酸甲酯、硒半胱氨酸甲酯和吡咯赖氨酸甲酯。
[0023]
本技术还提供了一种制备所述的含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物或其立体异构体、或其盐或其溶剂化物的中间体化合物,如下所示:
[0024][0025]
本技术还提供了所述的含异含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物或其立体异构体、或其盐或其溶剂化物的制备方法,其包括下述步骤:
[0026][0027]
其中r1和r2如上所述。
[0028]
本技术还提供了一种组合物,其含有所述的化合物或其立体异构体、或其盐或其溶剂化物,以及农业上可用的助剂或杀菌剂、杀虫剂或除草剂;优选地,所述组合物的剂型选自乳油(ec)、粉剂(dp)、可湿性粉剂(wp)、颗粒剂(gr)、水剂(as)、悬浮剂(sc)、超低容量喷雾剂(ulv)、可溶性粉剂(sp)、微胶囊剂(mc)、烟剂(fu)、水乳剂(ew)、水分散性粒剂(wg)。
[0029]
任一所述的化合物或其立体异构体、或其盐或其溶剂化物,或所述的组合物在防治农业病虫害方面的用途,优选地,所述农业病虫害为植物细菌性病害、真菌性病害或病毒性病害;更优选地,所述农业病虫害为植物叶枯病、植物溃疡病和植物病毒病;最优选地,所述农业病虫害为水稻白叶枯病、黄瓜白叶枯病、魔芋白叶枯病、烟草青枯病、柑橘溃疡病、猕猴桃溃疡病、葡萄溃疡病、番茄溃疡病、苹果溃疡病、黄瓜灰霉病、辣椒枯萎病原、油菜菌核病、小麦赤霉病、马铃薯晚疫病、烟草花叶病、番茄花叶病、水稻矮缩病。
[0030]
所述的化合物或其立体异构体、或其盐或其溶剂化物,或所述的组合物作用于有害物或其生活环境;优选地,所述农业病虫害为植物细菌性病害、真菌性病害或病毒性病害;更优选地,所述农业病虫害为植物叶枯病、植物溃疡病和植物病毒病;最优选地,所述农业病虫害为水稻白叶枯病、烟草青枯病菌、黄瓜白叶枯病、魔芋白叶枯病、柑橘溃疡病、猕猴桃溃疡病、葡萄溃疡病、番茄溃疡病、苹果溃疡病、黄瓜灰霉病、辣椒枯萎病原、油菜菌核病、小麦赤霉病、马铃薯晚疫病、烟草花叶病、番茄花叶病、水稻矮缩病。
[0031]
本技术还提供了一种用于保护植物免受农业病虫害侵害的方法,其包括其中使植物与所述的化合物或其立体异构体、或其盐或其溶剂化物,或所述的组合物接触的方法步骤。
[0032]
此处用到的术语“烷基”是包括具有特定数目碳原子的支链和直链饱和烃基。例如“c1‑
c5烷基”(或亚烷基)目的是c1、c2、c3、c4和c5烷基。另外,例如“c1‑
c6烷基”表示具有1到6个碳原子的烷基。烷基可为非取代或取代的,以使一个或多个其氢原子被其它化学基团取代。烷基的实施例包括但不限于甲基(me)、乙基(et)、丙基(如正丙基和异丙基)、丁基(如正丁基、异丁基、叔丁基)、戊基(如正戊基、异戊基、新戊基)及其类似物。
[0033]
此处用到的术语“取代的”指的是在指定原子或基团上的任意一个或多个氢原子以选择的指定基团取代,前提是不超过指定原子的一般化合价。如果没有其它说明,取代基命名至中心结构。例如,可以理解的是当(环烷基)烷基是可能的取代基,该取代基至中心结构的连接点是在烷基部分中。此处使用的环双键是形成于两个临近环原子之间的双键(如c=c、c=n或n=n)。
[0034]
取代基和变量的组合是允许的,仅当这些组合产生稳定的化合物或有用的合成中间体。稳定的化合物或稳定结构暗示所述化合物以有用的纯度从反应混合物分离出来时是足够稳定的,随之配制形成有效的治疗试剂。
[0035]
术语“环烷基”指的是环烷基,包括单
‑
、双
‑
或多环体系。c4‑
c
10
环烷基目的是包括c4、c4、c5、c6、c7、c8、c9和c
10
环烷基。环烷基实例包括但不限于环丙基、还丁基、环戊基、环已基、降冰片基及其类似物。此处用到的“碳环”或“碳环残余”指的是任何稳定3、4、5、6或7
‑
元单环或双环或7、8、9、10、11、12或13
‑
元双或三环,其可为饱和、部分不饱和、不饱和或芳香性的。这些碳环实例包括但不限于环丙基、环丁基、环丁烯基、环戊基、戊烯基、环己基、环己烯基、环庚基、环庚烯基、金刚烷基、环辛基、环辛烯基、环辛二烯、[3.3.0]双环辛烷、[4.3.0]双环壬烷、[4.4.0]双环癸烷、[2.2.2]双环辛烷、芴基、苯基、萘基、茚满基、金刚烷基、蒽基和四氢萘基(萘满)。如上所述,桥环也包含于碳环(如[2.2.2]双环辛烷)的定义中。如果没有其它说明,优选的碳环是环丙基、环丁基、环戊基、环已基和苯基。当使用术语“碳环”,目的是包括“芳基”。当一个或多个碳原子连接两个非临近碳原子出现桥环。优选的桥是一个或两个碳原子。指出的是桥总是将单环转化为双环。当环是桥连的,环的取代基也存
在于桥上。
[0036]
术语“杂芳基”指的是取代和非取代芳香5或6元单环基团,9
‑
或10
‑
元双环基团,和11到14元三环基团,在至少一个环中具有至少一个杂原子(o,s或n),所述含杂原子的环优选具有1、2或3个选自o、s和n中的杂原子。含杂原子的杂芳基的每个环可含一个或两个氧或硫原子和/或由1到4个氮原子,前提是每个环中杂原子的总数是4或更少,且每个环具有至少一个碳原子。完成双环和三环基团的稠合环可仅含有碳原子,并可以是饱和、部分饱和或不饱和。氮可任选被氧化及被季铵化。双环或三环的杂芳基必须包括至少一个全芳香环,氮其它稠合环可为芳香性或非芳香性的。杂芳基可在任何环的任何可利用氮或碳原子上连接。
[0037]
示例性单环杂芳基包括吡咯基、吡唑基、吡唑啉基、咪唑基、噁唑基、异噁唑基、噻唑基、噻二唑基、呋喃基、噻吩基、噁二唑基、吡啶基、吡嗪基、嘧啶基、哒嗪基、三嗪基及其类似物。
[0038]
示例性双环杂芳基包括吲哚基、苯并噻唑基、苯并二氧杂环戊烯基、苯并噁唑基、苯并噻吩基、喹啉基、四氢异喹啉基、异喹啉基、苯并咪唑基、苯并呋喃基、吲哚嗪基、苯并呋喃基、色酮基、香豆素基、苯并呋喃基、噌啉基、喹喔啉基、吲唑基、吡咯并吡啶基、氟代吡啶基、二氢异吲哚基、四氢喹啉基及其类似物。
[0039]
术语“卤素”或“卤素原子”指的是氯、溴、氟和碘。
[0040]
如果没有其它说明,本技术的化合物理解为包括游离态和其盐。术语“盐”表示以无机和/或有机酸和碱形成酸式和/或碱式盐。另外,术语“盐可包括两性离子(内盐),如当式i化合物含有碱性片段如胺或吡啶或咪唑环,和酸式片段如羧酸。药物上可接受的(即非毒性、生理学上可接受的)盐是优选的,如可接受的金属和胺盐,其中阳离子没有显著贡献毒性或盐的生物活性。然而,其它盐可是有用的,如在制备过程中采用分离或纯化步骤,因此也包含于本技术范围中。
[0041]
当提到取代基为烯基、炔基、烷基、卤素、芳基、杂芳基、烷氧基、环烷基、羟基、氨基、巯基、膦基时,或这些取代基具体的为某个具体的烯基、炔基、烷基、卤素、芳基、杂芳基、烷氧基、环烷基、羟基、氨基、巯基、膦基时,指的是一个到三个上述取代基。如甲基苯基指的是一个到三个甲基取代的苯基。
[0042]
通过采用上述技术方案,本技术以乙酰肼或异烟肼为起始原料,合成一系列含酰胺亚结构的1,2,4
‑
三唑硫醚及1,3,4
‑
噻/噁二唑硫醚类化合物,且发现该化合物对致病植物病原细菌和烟草花叶病毒具有良好的抑制作用,针对病原细菌[如水稻白叶枯病菌(xanthomonas oryzae pv.oryzae,xoo)、柑橘溃疡病菌(xanthomonas axonopodis pv.citri,xac)和烟草青枯菌(ralstonia solanacearum r.s.)等]及烟草花叶病毒(tobacco mosaic virus)均具有良好的抑制效果,为新农药的研发和创制提供重要的科学基础。
实施例
[0043]
下面通过实施例对本技术作进一步说明。应该理解的是,本技术实施例所述方法仅仅是用于说明本技术,而不是对本技术的限制,在本技术的构思前提下对本技术制备方法的简单改进都属于本技术要求保护的范围。实施例中用到的所有原料和溶剂均为市售产
品。
[0044]
实施例1:中间体4
‑
氨基
‑5‑
甲基
‑
4h
‑
1,2,4
‑
三唑
‑3‑
硫醇的制备
[0045]
在0
‑
4℃下,将乙酰肼(0.10mol)溶解在50ml含0.20mol koh的无水乙醇中。同时将0.15mol二硫化碳溶解在20ml无水乙醇中,然后缓慢将二硫化碳溶液缓慢滴加至上述溶液中。将反应混合物搅拌过夜后可得到黄色沉淀物。将沉淀物过滤后用石油醚洗涤,并在真空下干燥。得到的沉淀用50ml无水乙醇重新悬浮,然后加入水合肼(80%,0.15mol),将反应混合物回流12小时后冷却到室温。之后,在减压下除去溶剂,再加入30毫升蒸馏水。通过使用浓盐酸调节ph值至2
‑
3,过滤后得到浅黄色沉淀物(4
‑
氨基
‑5‑
甲基
‑
4h
‑
1,2,4
‑
三唑
‑3‑
硫醇),用冷水洗涤,并从无水乙醇中重新结晶,产率为58.3%。
[0046]
其核磁数据为:1h nmr(400mhz,dmso
‑
d6)δ13.41(s,1h),5.53(s,2h),2.24(s,3h).
13
c nmr(101mhz,dmso
‑
d6)δ165.85,149.61,10.88.
[0047]
同时,其余1,2,4
‑
三氮唑中间体,实验步骤及投料比例与实施例1一致,仅替换为相应的原料。
[0048]
实施例2:中间体5
‑
甲基
‑
1,3,4
‑
噁二唑
‑2‑
硫醇的制备
[0049]
在0
‑
4℃下,将乙酰肼(0.10mol)溶解在50ml含0.20mol koh的无水乙醇中。同时将0.15mol二硫化碳溶解在20ml无水乙醇中,然后缓慢将二硫化碳溶液缓慢滴加至上述溶液中。将反应混合物搅拌过夜后可得到黄色沉淀物。然后,将反应混合物回流12小时后冷却到室温。之后,在减压下除去溶剂,再加入30毫升蒸馏水。通过使用浓盐酸调节ph值至2
‑
3,过滤后得到浅黄色沉淀物(5
‑
甲基
‑
1,3,4
‑
噁二唑
‑2‑
硫醇),用冷水洗涤,并从无水乙醇中重新结晶,产率为62.4%。
[0050]
同时,其余1,3,4
‑
噁二唑中间体,实验步骤及投料比例与实施例2一致,仅替换为相应的原料。
[0051]
实施例3:2
‑
((4
‑
氨基
‑5‑
甲基
‑
4h
‑
1,2,4
‑
三唑
‑3‑
基)硫)
‑
n
‑
(叔丁基)乙酰胺
[0052]
将4
‑
氨基
‑5‑
甲基
‑
4h
‑
1,2,4
‑
三唑
‑3‑
硫醇(1mmol)和k2co3(1.2mmol)的混合物溶于3ml二甲基甲酰胺中。然后,将相应的n
‑
叔丁基
‑2‑
氯乙酰氨(1.2mmol)加入该混合物中。在室温下反应过夜后,将15毫升水倒入烧瓶,得到沉淀物。沉淀物被过滤,用冷水洗净,并在真空下干燥。最后,通过硅胶柱色谱法,以二氯甲烷/甲醇(20/1:v/v)为洗脱剂,纯化产品,得到目标化合物。
[0053]
以上述实施例类似的步骤,仅替换相应的原料制备得到下述化合物。所述化合物的结构及核磁共振氢谱和碳谱数据如表1所示,物化性质如表2所示。
[0054]
表1化合物的核磁共振氢谱和碳谱数据
[0055]
[0056]
[0057]
[0058]
[0059]
[0060]
[0061]
[0062]
[0063]
[0064]
[0065][0066]
表2目标化合物的理化性质
[0067]
[0068][0069]
药理实施例1:
[0070]
采用浊度法测试目标化合物对植物病原菌的抑制率,试验对象为水稻白叶枯病菌(xoo)、柑橘溃疡病菌(xac)、烟草青枯病菌和柑橘溃疡病菌(r.s.)。dmso溶解在培养基中作为空白对照。将水稻白叶枯病菌(水稻白叶枯病原菌在m210固体培养基)放到nb培养基中,在28℃、180rpm恒温摇床中振荡培养到对数生长期备用;将烟草青枯病菌(在m210固体培养基上)放到nb培养基中,在28℃、180rpm恒温摇床中振荡培养到对数生长期备用;将柑橘溃疡病菌(在m210固体培养基上)放到nb培养基中,在28℃、180rpm恒温摇床中振荡培养到对数生长期备用。将药剂(化合物)配置成不同浓度(例:100,50μg/ml)的含毒nb液体培养基5ml加入到试管中,分别加入40μl含有植病细菌的nb液体培养基,在28
‑
30℃、180rpm恒温摇床中振荡,其水稻白叶枯病原菌培养48h,烟草青枯病菌和柑橘溃疡病菌培养24
‑
36h。将各
个浓度的菌液在分光光度计上测定od
595
值,并且另外测定对应浓度的含毒无菌nb液体培养基的od
595
值。
[0071]
校正od值=含菌培养基od值
‑
无菌培养基od值
[0072]
抑制率%=[(校正后对照培养基菌液od值
‑
校正含毒培养基od值)/校正后对照培养基菌液od值]
×
100
[0073]
采用半叶枯斑法测试目标化合物对烟草花叶病毒(tmv)的抑制率。选取接种3周以上,tmv系统侵染寄主普通烟(nicotiana tabacum)k326植株上部叶片,去脉后进行提纯。治疗活性:选长势一致的5~6叶期心叶烟,用排笔蘸取病毒汁液磨擦接种于撒有金刚砂的叶片上,全叶接种病毒后30min,用清水冲洗。待叶片干后,在左半叶涂施药剂,右半叶涂施对应剂量的溶剂作对照。随后在光照培养箱中培养,控制温度23
±
1℃,光照10000lux,2~3d后观察并记录产生枯斑的数目。每处理3株,每株3~4片叶。保护活性:选长势一致的5~6叶期心叶烟,用毛笔轻轻在左半叶涂施药剂,右半叶涂施对应剂量的溶剂作对照。在光照培养箱中培养,控制温度23
±
1℃,光照10000lux,24h后,用毛笔蘸病毒汁液人工摩擦接种于撒有金刚砂的叶片上,接种30min后用清水冲洗叶片。并于光照培养箱中继续培养,控制温度23
±
1℃,光照10000lux,2~3d后观察并记录产生枯斑的数目。每处理3株,每株3~4片叶。
[0074]
抑制率(%)=[(空白对照枯斑数
‑
药剂处理枯斑数)/空白对照枯斑数]
×
100%
[0075]
目标化合物活性实验结果如表3
‑
6所示。
[0076]
表3本技术化合物对植物病原细菌的抑制活性
[0077]
[0078][0079]
表4本技术化合物对植物病原细菌的ec
50
[0080][0081]
表5本技术化合物对tmv的抑制率
[0082]
[0083][0084]
表6本技术部分化合物对tmv的ec
50
[0085][0086]
从表3
‑
4中可以看出,在离体试验中,目标化合物对植物致病病原菌(如水稻白叶枯病菌、柑橘溃疡病菌和烟草青枯病菌菌)表现出了良好的抑制活性。其中化合物10,11和35对水稻白叶枯病菌具有极为优异的活性,ec
50
分别为5.01、15.6和8.4μg/ml同时,化合物6、8、10、12、14、18、19、21、22、27、28、30、31、36、37、41和45对tmv也表现出优异的抑制活性,ec
50
为105.3、172.7、97.4、116.6、176.2、200.9、206.5、124.3、193.3、195.5、183.3、240.8、312.6、167.1、231.1、176.0和278.5μg/ml。由此,可知此类化合物极具研究前景,可用于制
备抗植物致病病原微生物农药。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1