荧光化合物及在检测尿素酶中的应用和体外诊断试剂
1.本发明涉及一种具有荧光特性的化合物,尤其涉及一种与尿素具有类似结构的化合物,作为尿素酶的底物,利用其荧光特性用于检测尿素酶的含量,及其在检测尿素酶的医疗器械中的应用。
背景技术:
2.尿素酶是一种能水解尿素产生二氧化碳和氨的含镍金属寡聚酶,广泛存在于植物种子、动物尿液及血液中,很多微生物也可合成分泌尿素酶。如在人体的上消化道口腔及胃寄生的唾液链球菌、幽门螺杆菌、內氏放线菌等微生物可产生尿素酶,这些微生物产生的尿素酶与其致病性有关,常见的相关性疾病包括龋齿、牙周炎、萎缩性胃炎和消化道溃疡等。与其他产尿素酶微生物相比,幽门螺杆菌的尿素酶含量大、活性高,其尿素酶含量占细胞总蛋白的5%-10%,其尿素酶活性是奇异变形杆菌的2倍,肠道菌的7倍。因此,临床上尿素酶活性测定可作为幽门螺杆菌感染的快速诊断依据。
3.尿素酶的检测方法主要包括酚红指示剂法、纳氏试剂显色法、胶乳凝集试验法、免疫印迹、酶联免疫吸附法。以上检测方法的原理可分为两种,其一是基于尿素酶水解底物尿素产生氨使指示剂酚红或纳氏试剂出现颜色变化;另外一种则是利用尿素酶抗体特异性识别尿素酶抗原的免疫反应。这些检测分析方法存在一些缺点,比如:通过抗原-抗体结合反应的方法特异性较好,但检测耗时较长,而利用反应体系ph值变化的方法对反应条件要求较苛刻。因此发展更高效、简便、快速、可靠的尿素酶检测方法具有重要的社会意义。
技术实现要素:
4.本发明的一个目的在于提供一种荧光化合物,具有类似尿素的分子结构,以其作为尿素酶的底物,并利用该化合物在尿素酶水解作用下产生特定波长的荧光特性,实现对尿素酶的定性或定量检测。
5.本发明的另一个目的在于提供一种荧光化合物的制备方法,取得具有类似尿素的分子结构,以其作为底物应用于尿素酶的定性和定量检测。
6.本发明的再一个目的在于提供一种荧光化合物用于尿素酶的检测,使得尿素酶检测更高效、更简便和更可靠。
7.本发明的又一个目的在于提供一种荧光化合物在制造检测尿素酶医疗器械中的应用,使得尿素酶检测更高效、更简便和更可靠。
8.本发明的第五个目的在于提供一种荧光化合物在制造检测尿素酶体外诊断试剂中应用。
9.为实现上述目的,本发明采用以下技术方案:
10.一种荧光化合物,其具有如下结构式i所示的结构,
[0011][0012]
其中,r1和r2独立地选自于荧光基团或淬灭基团。比如:r1和r2选自于相同的荧光基团;另如:r1选自于荧光基团,r2选自于淬灭基团;又如:r1选自于淬灭基团,r2选自于荧光基团;又如:r1和r2选自于荧光基团,但两种基团的激发波长不同,且其中一个荧光基团的发射波长位于另一个荧光基团的激发波长范围内。
[0013]
本发明的荧光化合物,荧光基团如:但不限于甲苯胺蓝、香豆素或荧光素。
[0014]
本发明的荧光化合物,淬灭基团如:但不限于黑洞淬灭剂(black hole quencher,bhq。
[0015]
荧光化合物未接触尿素酶时,因荧光能量共振转移(fluorescence resonance energy transfer,fret)的机制作用,荧光受到抑制。当其为底物与尿素酶接触后,在尿素酶水解作用下,使得反应液产生荧光特性,产生荧光或使荧光增强的特性,通过测定荧光强度值的改变,即可对尿素酶的活性进行检测,如:定性或定量检测。
[0016]
与现有技术相比,本发明检测尿素酶的检测原理不同。本发明通过检测尿素酶水解产物荧光量的变化直接计算尿素酶,检测快速而简便。现有技术则通过测定尿素酶反应后的溶液ph值变化间接计算尿素酶活性或者通过反应条件苛刻、时间缓慢的抗原-抗体结合检测分析,检测慢而复杂。
[0017]
将本发明的荧光化合物作为底物,制成尿素酶医疗器械,如:体外诊断试剂,以实现对尿素酶的快速定量和定性检测。
[0018]
一种制取本发明提供的荧光化合物的方法,包括如下步骤:
[0019]
以含有两个反应官能团的脲,与荧光分子(如:甲苯胺蓝)为反应原料以摩尔比1∶2的比例混合,溶解在有机溶剂(如:三乙胺和二甲基甲酰胺)中,在室温、避光条件下进行反应;反应结束后去除溶剂得到固体,再溶解在甲醇中。采用甲醇∶二氯甲烷20∶1(体积比)进行层析纯化即可制得荧光化合物。
[0020]
另一种制取本发明提供的荧光化合物的方法,包括如下步骤:
[0021]
以含有两个反应官能团的脲,与荧光分子(如:甲苯胺蓝)和淬灭分子(如:bhq3)为反应原料以摩尔比1∶1∶1的比例混合,溶解在有机溶剂中,在室温、避光条件下进行反应;反应结束后去除溶剂得到固体,再溶解在甲醇中。采用甲醇∶二氯甲烷20∶1(体积比)进行层析纯化即可制得荧光化合物。
[0022]
另一种制取本发明提供的荧光化合物的方法,包括如下步骤:
[0023]
以含有两个反应官能团的脲,与两个不同的荧光分子,如:香豆素和荧光素,为反应原料以摩尔比1∶1∶1的比例混合,溶解在有机溶剂中,在室温、避光条件下进行反应;反应结束后去除溶剂得到固体,再溶解在甲醇中。采用甲醇∶二氯甲烷20∶1(体积比)进行层析纯化即可制得荧光化合物。
附图说明
[0024]
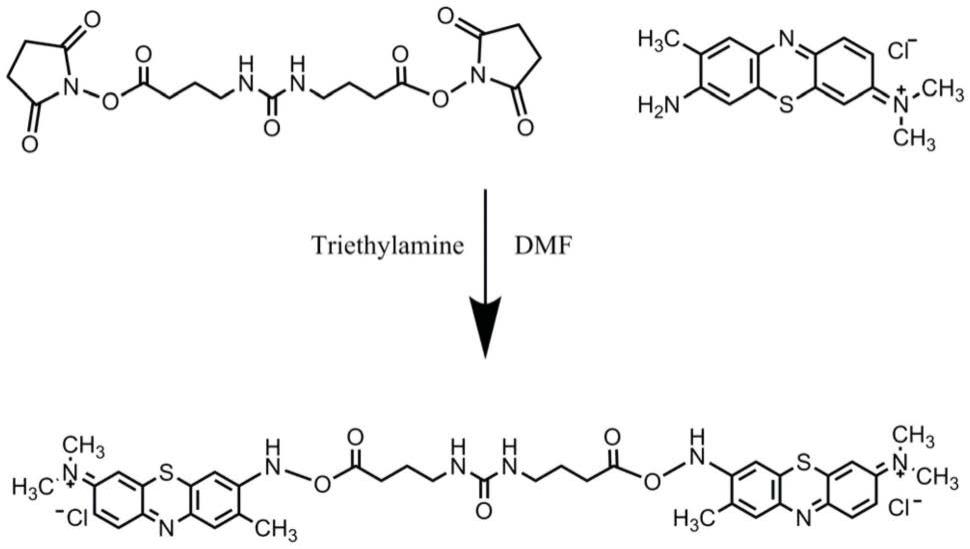
图1为本发明实施例1中荧光化合物合成的流程路径;
[0025]
图2为本发明实施例1荧光化合物核磁共振氢谱1h nmr;
[0026]
图3为本发明实施例1荧光化合物测定的尿素酶浓度与荧光量的线性关系。
具体实施方式
[0027]
以下详细描述本发明的技术方案。本发明实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,其均应涵盖在本发明的权利要求范围中。
[0028]
在以下实施例中,除非另有指明,所有温度为摄氏温度(℃)。除非另有指明,各种起始原料和试剂均通过商业化渠道即可获得,如西格玛-奥德里奇(sigma-aldrich)、赛默飞世尔科技(thermofisher scientific)。所获得的原料和试剂均不经进一步纯化而直接使用。
[0029]
玻璃器皿用烘箱干燥和/或加热干燥。反应用玻璃硅胶-60 f254平板(0.25mm)(tlc)上进行跟踪。分析性薄层色析并以适当的溶剂比例(v/v)加以展开。
[0030]1h nmr图谱是用bruker仪器(400mhz)测定而得,化学位移用ppm表示。使用四甲基硅烷内标准(0.00ppm)。1h nmr的表示方法:s=单峰,d=双重峰,t=三重峰,m=多重峰,br=变宽的,dd=双重峰的双重峰。若提供偶合常数时,其单位为hz。
[0031]
产物的分子量采用lc/ms质谱仪测定得到,离子化方式为esi或apci。
[0032]
本发明提供的制备方法应当被理解为出于充分公开的必要而进行的举例,而不是对本发明所要求的保护范围的限定。本领域技术人员根据教科书、实验手册或本发明所列举的实施例的指导就能够制得本发明提供的各种化合物。制取这些化合物也属于本领域普通技术人员的应当具备的一般技能,在现有技术的指导下也能完成。具体而言,本发明提供的部分化合物的制备方法如下图1所示。
[0033]
以4,4
′‑
(羰基二亚氨基)双-,1,1
′‑
双(2,5-二氧-1-吡咯烷基)酯、甲苯胺蓝为反应原料,以摩尔比1∶2的比例混合溶解在n,n-二甲基甲酰胺(n,n-dimethylformamide,dmf)溶剂中,并添加三乙胺(triethylamine)后在室温、避光条件下进行反应;反应结束后去除溶剂得到黑色油性固体,将其溶解在甲醇中,进一步用甲醇∶二氯甲烷20∶1进行层析纯化即可制备得到荧光化合物。
[0034]
1h nmr(400mhz,dmso)δ10.13(s,1h),9.90(s,1h),8.59(s,1h),8.31(s,1h),8.15(s,1h),7.93(s,1h),7.27(s,2h),7.14(s,1h),6.91(s,2h),6.65(s,2h),3.58(s,8h),3.17(s,2h),3.10(s,2h),3.04(s,2h),2.97(s,3h),2.89(m,1h),2.73(s,1h),2.58(s,6h),2.24(s,2h),2.10(s,2h),1.98(s,2h),1.56(s,4h),1.23(s,2h),0.95(s,2h)(图2)。es-ms(m/z):838.23(mh
+
)
[0035]
尿素酶的检测步骤包括以下:
[0036]
(1)用ph 7.4的磷酸盐缓冲液配置不同浓度的尿素酶溶液,使其在100μl检测体系中终浓度为0、1.25、2.5、5、10和20u/ml;在尿素酶溶液中加入终浓度为5mmol/l荧光化合物,在37℃温度条件下反应3分钟~5分钟,测定溶液中的荧光量,并根据尿素酶浓度及对应的荧光量制作标准曲线,参见图3,得到线性拟合方程y=1.029+0.078x。
[0037]
(2)将待测样本(如:唾液、胃液、尿液、土壤、胃黏膜活检组织样本等)加入至100μl检测体系中,并加入终浓度为5mmol/l荧光化合物,在37℃温度条件下反应3分钟~5分钟,
测定溶液中的荧光量,并根据标准曲线计算样本中的尿素酶酶活为。以某个唾液样本为例,测得相对荧光量为1.411,尿素酶酶活为1.68u/ml。
[0038]
整个过程中,仅需花费约10分钟即可完成,相比于现有技术,检测时间显著缩短。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1