一种用于糖代谢相关疾病基因治疗的核酸构建体的制作方法
1.本发明涉及基因治疗或生物医药技术领域,特别是涉及一种用于糖代谢相关疾病基因治疗的核酸构建体。
背景技术:
2.糖尿病是一种身体无法产生完全功能的胰岛素,或者无法正确利用及储存葡萄糖的疾病。葡萄糖存留于血液中引起血糖过高并引发一系列并发症为糖尿病的基础。2型糖尿病,或称成人型糖尿病、非胰岛素依赖型糖尿病,占糖尿病患者中的90%左右。良好的血糖控制对于逆转和减轻2型糖尿病并发症、降低致残率和死亡率、改善患者的生活质量至关重要。
3.基于胰岛素注射糖尿病治疗取得了一定进展,但是仍难以实现最佳血糖控制,在胰岛素注射治疗中伴随的低血糖和体重进一步增加,会加剧患者机体代谢紊乱以及糖尿病相关并发症,并导致相关的死亡风险。
4.基于胰高血糖素样肽1(glucagon
‑
like peptide
‑
1,glp
‑
1)的糖尿病治疗通过增加葡萄糖依赖性胰岛素分泌、减慢胃排空、降低餐后高血糖、减少食物摄入量等机制来安全有效的控制血糖,同时还能获得减肥和心血管保护等多方面的临床获益作用。基于glp
‑
1的糖尿病治疗有望代替胰岛素成为治疗糖尿病的一线药物。
5.目前主要的基于glp
‑
1的糖尿病治疗包括glp
‑
1受体激动剂和二肽基肽酶4(dipeptidyl peptidase
‑
4,dpp
‑
4)抑制剂,均以提高glp
‑
1有效浓度为目标。其中以liraglutide(利拉鲁泰),semaglutide(索马鲁泰)和dulaglutide(度拉鲁肽)为代表的新的长效胰高血糖素样肽
‑
1(glp
‑
1)受体激动剂在临床疗效及患者依从性等方面表现突出,已经作为一线用药进入欧美国家糖尿病指南。
6.但glp
‑
1及其类似物在体内很快被dpp
‑
4降解,半衰期较短。虽然glp
‑
1类似物显著延长了glp
‑
1在体内的作用时间,但仍需频繁(1
‑
7天)皮下给药。并且由于多肽药物的研制、生产、使用成本均远高于小分子糖尿病治疗药物,glp
‑
1类似物糖尿病治疗并不具有成本优势,长效以至于终身的glp
‑
1治疗对于部分中重度以及难控制血糖的糖尿病患者,具有现实及紧迫的临床需求。
7.病毒及非病毒载体递送的glp
‑
1类似物基因治疗技术路线,从理论上解决了glp
‑
1长期甚至终身表达的目标,可以一劳永逸提高glp
‑
1有效浓度,对于中重度及难控制糖尿病患者具有长期临床获益的巨大价值。然而多肽的基因表达载体的表达效率远低于大分子蛋白的基因表达载体,作为30个氨基酸左右的glp
‑
1及其类似物,过小的表达框架使其在任何病毒及非病毒载体上的有效表达均有不小的难度。同时较短血浆半衰期进一步增加了glp
‑
1及其类似物达到有效血液浓度的障碍。目前为止,尚未有任何病毒及非病毒载体递送的glp
‑
1类似物基因治疗技术路线获得有效的临床进展。
8.针对以上问题,基于病毒及非病毒载体递送的基因治疗技术路线的药物研发主要需要在以下两个方面取得突破:
9.如何以重组病毒或非病毒载体递送的基因载体,以基因组整合或非整合的方式在机体内长期稳定并高效的表达glp
‑
1及其类似物,使2型糖尿病及相关疾病患者一次治疗长期甚至终身获益,同时减少生产和使用成本。
技术实现要素:
10.鉴于以上所述现有技术的缺点,本发明的目的在于提供一种用于糖代谢相关疾病基因治疗的核酸构建体,用于解决现有技术中的问题。
11.为实现上述目的及其他相关目的,本发明提供一种核酸构建体,所述核酸构建体包括编码glp
‑
1或其类似物的多核苷酸,所述glp
‑
1或其类似物的总数量为两个以上,glp
‑
1与glp
‑
1之间、glp
‑
1与其类似物之间或glp
‑
1类似物与glp
‑
1与类似物之间通过编码连接肽的多核苷酸连接。
12.本发明还提供一种慢病毒,所述慢病毒由所述核酸构建体经病毒包装而成。
13.本发明还提供一种慢病毒载体系统,所述慢病毒载体系统包括所述的核酸构建体以及辅助质粒。
14.本发明还提供一种腺相关病毒载体系统,所述腺相关病毒载体系统包括所述的核酸构建体以及辅助质粒。
15.本发明还提供一种腺相关病毒,所述腺相关病毒由所述腺相关病毒载体系统经病毒包装而成。
16.本发明还提供一种细胞系,所述细胞系为经所述慢病毒或腺相关病毒感染的细胞系。
17.本发明还提供所述核酸构建体、慢病毒、慢病毒载体系统、腺相关病毒、腺相关病毒载体系统、细胞系在制备预防、治疗糖代谢相关疾病的产品中的用途。
18.如上所述,本发明的用于糖代谢相关疾病基因治疗的核酸构建体,具有以下有益效果:本发明创造了含串联共价二聚体或多聚体形式的glp
‑
1或其类似物的表达框架的核酸构建体,该核酸构建体在体内外均可用于高效表达具有活性的glp
‑
1及其类似物,这为极具潜力的2型糖尿病、机体代谢紊乱、糖尿病相关并发症以及肥胖症等糖代谢相关疾病的基因治疗药物开发了技术路线。本发明的应用范围包括各种形式基于glp
‑
1及其类似物的糖代谢相关疾病的基因治疗,例如所述构建体能用于病毒载体或非病毒载体递送的糖代谢相关疾病的基因治疗药物的临床研究及新药研发及生产。
附图说明
19.图1a显示为本发明的pkl
‑
kan
‑
lenti
‑
ef1α
‑
wpre质粒图谱。
20.图1b显示为本发明的paav
‑
mcs
‑
cmv
‑
egfp(反)质粒图谱。
21.图2显示为表达glp1受体激动剂的核酸构建体的表达框架的设计。
22.图3a显示为表达glp1受体激动剂的核酸构建体(慢病毒载体)的设计。
23.图3b显示为表达glp1受体激动剂的核酸构建体(腺相关病毒载体)的设计。
24.图4a显示为表达glp1受体激动剂的慢病毒转导细胞后对glp1受体激动剂的表达(westernblotting)还原凝胶电泳检测结果。
25.图4b显示为表达glp1受体激动剂的慢病毒转导细胞后对glp1受体激动剂的表达
(westernblotting)非还原凝胶电泳检测结果。
26.图5显示为表达glp1受体激动剂的慢病毒转导的细胞培养上清对带有glp1受体细胞的激活效果。a1
‑
a4(即第一行)分别为glp1(7
‑
37)8nm,40nm,200nm,1000nm;b1
‑
b4(即第二行)分别为kldi02不同转导体积:2μl、5μl、10μl、20μl;c1
‑
c4(即第三行)分别为kldi01不同转导体积:2μl、5μl、10μl、20μl。
27.图6显示为db/db小鼠接受表达glp1受体激动剂的腺相关病毒后的血糖浓度。
28.图7显示为c57bl/6小鼠接受表达glp1受体激动剂的腺相关病毒后的糖耐量。
具体实施方式
29.除非下文另外定义,本发明所提及的所有技术和科学用语具有本发明所属领域的技术人员通常理解的意义。
30.术语“核酸构建体”是指可以被引入靶细胞或组织中的人工构建的核酸区段,所述核酸构建体可以为慢病毒载体或腺相关病毒载体,慢病毒载体或腺相关病毒载体包括载体骨架即空载体与表达框架。
31.术语“表达框架”是指具有编码蛋白质潜能的序列。
32.本发明提供一种核酸构建体,所述核酸构建体包括编码glp
‑
1或其类似物的多核苷酸,所述glp
‑
1或其类似物的总数量为两个以上,glp
‑
1与glp
‑
1之间、glp
‑
1与其类似物之间或glp
‑
1类似物与glp
‑
1与类似物之间通过编码连接肽的多核苷酸连接。
33.在一种实施方式中,glp
‑
1类似物为glp
‑
1n端的7
‑
36或7
‑
37个氨基酸肽链。这一部分氨基酸是glp
‑
1生物活性部分,因此药物研发等均集中在这些氨基酸序列。glp
‑
1类似物还可以为在glp
‑
1n端的7
‑
36或7
‑
37个氨基酸中的个别氨基酸的替换、删除、增加,或者个别氨基酸与不同化合物连接。
34.所述glp
‑
1或其类似物的总数量例如可以是两个、三个、四个、五个或更多个。
35.所述glp
‑
1或其类似物的总数量的意思选自以下任一:
36.1)当构建体中含glp
‑
1而不含其类似物时,glp
‑
1的总数量为两个以上;
37.2)当构建体中含glp
‑
1类似物而不含glp
‑
1时,glp
‑
1类似物的总数量为两个以上;
38.3)当构建体中既含glp
‑
1又含glp
‑
1类似物时,glp
‑
1和glp
‑
1类似物的数量为两个以上。
39.所述的核酸构建体中glp
‑
1或其类似物之间的连接方式如下:信号肽——glp
‑
1或glp
‑
1类似物——连接肽——glp
‑
1或glp
‑
1类似物——连接肽——glp
‑
1或glp
‑
1类似物,其中glp
‑
1或glp
‑
1类似物——连接肽——glp
‑
1或glp
‑
1类似物单元的个数为一个或多个,例如可以是两个、三个、四个、五个或更多个。
40.所述连接肽由侧链小的氨基酸组成。例如:(gly)4,gsggsg,gsggsgg gsggsggg,ggggsggg,(ggggs)3。
41.所述核酸构建体可以有效的在体内表达胰高血糖素样肽1(glucagon
‑
like peptide
‑
1,glp
‑
1)或其类似物。所述核酸构建体表达的glp1或其类似物作为glp1受体的激动剂,所以所述核酸构建体亦可称为表达glp1受体激动剂的构建体。
42.所述核酸构建体为用于糖代谢相关疾病基因治疗的核酸构建体。
43.具体的,糖代谢相关疾病包括糖尿病或其并发症、肥胖症。
44.在一种实施方式中,所述糖尿病为2型糖尿病。
45.所述核酸构建体包括如seq id no:4或seq id no:6所示的表达框架。所述表达框架表达的glp1或其类似物作为glp1受体的激动剂。或者包括跟seq id no.4或seq id no.6比较至少具有75%,80%,85%,90%,95%,96%,97%,98%,或99%同源性的核苷酸序列。
46.所述核酸构建体中不包括能够表达除glp1或其类似物外的蛋白或多肽的多核苷酸。即,所述核酸构建体能够有效表达的蛋白或多肽仅有glp1或其类似物。
47.所述核酸构建体编码的多肽氨基酸序列如seq id no:3或seq id no:5所示。
48.所述核酸构建体被用于生产基于病毒的基因治疗载体,优选的所述基因治疗载体为慢病毒载体或腺相关病毒载体。
49.所述核酸构建体为病毒载体或非病毒载体。
50.在一些实施方式中,所述核酸构建体为慢病毒载体。所述慢病毒载体中载体骨架可以现有技术中的载体骨架。
51.在一种实施方式中,所述慢病毒载体的核苷酸序列如seq id no.12或seq id no.13所示。或者包括跟seq id no.12或seq id no.13比较至少具有75%,80%,85%,90%,95%,96%,97%,98%,或99%同源性的核苷酸序列。
52.在一些实施方式中,所述核酸构建体为腺相关病毒载体。所述腺相关病毒载体中载体骨架可以现有技术中的载体骨架。
53.在一种实施方式中,所述腺相关病毒载体的核苷酸序列如seq id no.17或seq id no.18所示。或者包括跟seq id no.17或seq id no.18比较至少具有75%,80%,85%,90%,95%,96%,97%,98%,或99%同源性的核苷酸序列。
54.本发明还提供一种慢病毒载体系统,所述慢病毒载体系统包括所述的核酸构建体以及辅助质粒。
55.更进一步的,所述辅助质粒编码gag和pol蛋白的一个或者多个核苷酸序列以及其它必需的病毒包装组件核苷酸序列,所述辅助质粒可以包括包装质粒和包膜质粒。
56.进一步的,所述慢病毒载体系统还包括宿主细胞。所述宿主细胞携带慢病毒载体。所述宿主细胞可以选自本领域各种可适用的宿主细胞,只要不对本发明的发明目的产生限制即可。具体的可适用的细胞可以为生产慢病毒的细胞,例如可以为293t细胞。
57.本发明还提供一种慢病毒,所述慢病毒由所述慢病毒载体系统经病毒包装而成。
58.本发明还提供一种腺相关病毒载体系统,所述腺相关病毒载体系统包括所述的核酸构建体以及辅助质粒。
59.更进一步的,所述辅助质粒编码gag和pol蛋白的一个或者多个核苷酸序列以及其它必需的病毒包装组件核苷酸序列,所述辅助质粒可以包括包装质粒和包膜质粒。
60.进一步的,所述腺相关病毒载体系统还包括宿主细胞。所述宿主细胞携带腺相关病毒载体。所述宿主细胞可以选自本领域各种可适用的宿主细胞,只要不对本发明的发明目的产生限制即可。具体的可适用的细胞可以为生产腺相关病毒的细胞,例如可以为293t细胞。
61.本发明还提供一种腺相关病毒,所述腺相关病毒由所述腺相关病毒载体系统经病毒包装而成。
62.本发明还提供一种细胞系,所述细胞系为经所述慢病毒或腺相关病毒感染的细胞
系。
63.该细胞系可以作为生物制剂用于制备预防或治疗神经退行性疾病的产品。
64.本发明还提供所述核酸构建体、慢病毒、慢病毒载体系统、腺相关病毒、腺相关病毒载体系统、细胞系在制备预防、治疗糖代谢相关疾病的产品中的用途。
65.具体的,糖代谢相关疾病包括糖尿病或其并发症、肥胖症。
66.在一种实施方式中,所述糖尿病为2型糖尿病。
67.以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
68.在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。
69.当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。
70.以下实施例包括:构建一系列能表达作为glp1受体激动剂的多肽及融合多肽的核酸构建体,并将其克隆到重组腺相关病毒或重组慢病毒载体中。在293t细胞中,包装相应的腺相关病毒和慢病毒载体,以一定生物学滴度病毒感染293t细胞,以及分化及未分化肌肉细胞系。用细胞上清中产生的多肽及融合多肽定量、定性检测,同时在报告基因细胞系的感染活性分析中检验其对glp
‑
1受体(glp
‑
1r)的结合和中和活性。再将上述包含多肽及融合多肽表达框架的腺相关病毒和慢病毒载体经纯化后,经静脉或肌肉注射的方式递送至野生型或糖尿病模型小鼠体内,在不同时间点检测受试小鼠的glp
‑
1多肽及融合多肽的血浆浓度,抗glp
‑
1多肽抗体,以及餐后血糖。具体的各实验步骤如下:
71.实施例1:表达glp1受体激动剂的核酸构建体表达框架的结构设计
72.如图2所示,glp1受体激动剂携带有信号肽序列,图2所示的整体序列在细胞中以一个完整的前体分子的形式被翻译出来,并被分泌出细胞。前体分子包括glp1、三个串联的柔性单元氨基酸组成的连接肽和辅助肽;其中辅助肽可以为glp1或glp1
‑
连接肽
‑
glp1,也可以为人源抗体igg1ch2和igg1ch3或其他结构。本发明中应用的glp1受体激动剂分子的结构为:
73.1.单体基因表达框架(glp
‑
1),由n端信号肽malltnllplcclallalpaqs(seq id no:30)以及单个glp
‑
1(7
‑
37)基因haegtftsdvssyle gqaakefiawlvkgrg(seq id no:31)组成。构建的glp1受体激动剂表达框架glp1蛋白序列见seq id no:1,dna序列见seq id no:2。
74.2.双glp
‑
1融合多肽基因表达框架(glp1
‑
glp1),由n端信号肽
malltnllplcclallalpaqs(seq id no:30),glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31),三个串联的柔性单元氨基酸组成的连接肽ggggsggggsggggs(seq id no:32),glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31)组成。构建的glp1受体激动剂表达框架kldi02的蛋白序列见seq id no:3,dna序列见seq id no:4。
75.3.叁glp
‑
1融合多肽基因表达框架(glp1
‑
glp1
‑
glp1),由n端信号肽malltnllplcclallalpaqs(seq id no:30),glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31),连接肽ggggsggggsggggs(seq id no:32),glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31),连接肽ggggsggggsggggs(seq id no:32),glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31)组成。构建的glp1受体激动剂基因表达框架kldi03的蛋白序列见seq id no:5,dna序列见seq id no:6。
76.4.glp
‑1‑
fc片段融合蛋白基因表达框架(glp
‑1‑
fc),由n端信号肽mxxxx,单个glp
‑
1(7
‑
37)基因haegtftsdvssylegqaakefiawlvkgrg(seq id no:31)以及人源抗体igg1ch2和igg1ch3组成。构建的glp1受体激动剂基因表达框架kldi01的蛋白序列见seq id no:7,dna序列见seq id no:8。此构建体将一个glp
‑
1类似物基因与抗体fc片段编码序列相连,利用类抗体分子二聚体的形成,优化glp
‑
1类似物基因的表达效率以及增加大分子药物的血浆半衰期。此构建体为现有技术,在申请中作为对照组。
77.实施例2:表达glp1受体激动剂的核酸构建体的构建
78.如图3a所示,将上述glp1受体激动剂基因表达框架以多片段重组连接的方式克隆到当前应用的最新一代慢病毒载体骨架pkl
‑
kan
‑
lenti
‑
ef1α
‑
wpre(图1a,核苷酸序列如seq id no:9)中。所述慢病毒载体骨架包括:5
′
ltr,其中用cmv启动子替换ltr的启动子区域;ψ包装信号;逆转录病毒输出元件rre;cppt;启动子cbh;编码hiv中和抗体片段的多肽的多核苷酸;转录后调节元件为wpre;ppt;δu3 3’ltr;以及poly a信号。实施例1设计的基因表达框架glp1、glp1
‑
fc、glp1
‑
glp1和glp1
‑
glp1
‑
glp1经通用生物系统(安徽)有限公司合成后,通过本领域熟知的以同源重组的方法克隆至慢病毒载体骨架pkl
‑
kan
‑
lenti
‑
ef1α
‑
wpre上的多克隆位点ecori/ecorv之间,克隆完成后以测序确认序列信息,质粒分别命名为pkl
‑
kan
‑
lenti
‑
ef1α
‑
glp1(dna序列见seq id no:10)、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi01(dna序列见seq id no:11)、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi02(dna序列见seq id no:12)和pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi03(dna序列见seq id no:13)。
79.如图3b所示,将来源于px261的cbh启动子(dna序列见seq id no:14)和存在于pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi01、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi02和pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi03的glp1受体激动剂基因表达框架kldi01、kldi02、kldi03以多片段重组连接的方式克隆到当前应用的最新一代腺相关病毒载体骨架paav
‑
mcs
‑
cmv
‑
egfp(反)(序列见seq id no:15)(见图1b)的多克隆位点mlui/sali之间。所述腺相关病毒载体骨架包括:aav2 itr,启动子cbh;编码glp1受体激动剂的多核苷酸;sv40 poly a信号,aav2 itr。质粒分别命名为paav
‑
cbh
‑
kldi01(dna序列见seq id no:16),paav
‑
cbh
‑
kldi02(dna序列见seq id no:17),paav
‑
cbh
‑
kldi03(dna序列见seq id no:18)。
80.实施例3:表达glp1受体激动剂的病毒包装及纯化
81.以慢病毒载体(pkl
‑
kan
‑
lenti
‑
ef1α
‑
glp1、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi01、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi02和pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi03)在293t细胞系中进行抗体基因治疗慢病毒载体的包装。将实施2中构建的抗体基因慢病毒载体(pkl
‑
kan
‑
lenti
‑
cbh
‑
glp1、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi01、pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi02和pkl
‑
kan
‑
lenti
‑
ef1α
‑
kldi03)、包膜质粒(pkl
‑
kan
‑
vsvg,其核苷酸序列如seq id no:19所示)和包装质粒(pkl
‑
kan
‑
rev,其核苷酸序列如seq id no:20所示;pkl
‑
kan
‑
gagpol,其核苷酸序列如seq id no:21所示)混合后同时共转染293t细胞(购自美国模式菌种收集中心(atcc),atcc保藏号为crl
‑
3216),在该293t细胞系中进行hiv中和抗体基因治疗慢病毒的包装。转染方法为pei阳离子聚合物介导的真核细胞瞬时转染,pei阳离子聚合物为购自polysciences的pei
‑
max转染试剂(购自polysciences,货号:24765
‑
1),转染操作参照生产商推荐标准化操作进行,转染规模为15cm细胞培养皿。转染完成48小时后,收获慢病毒载体(转染细胞培养上清),首先在台式吊桶式机上,室温4000rpm离心5分钟去除细胞碎片,再4度10000g离心4小时获得病毒颗粒沉淀,去除离心上清后,以1ml dmem完全培养基加入病毒颗粒沉淀中,以微量进样器重悬病毒颗粒,并将制备好的病毒重悬液分装冻存于
‑
80度备用。
82.以aav表达载体(paav
‑
cbh
‑
kldi01,paav
‑
cbh
‑
kldi02,paav
‑
cbh
‑
kldi03)在293t细胞系中进行抗体基因治疗aav载体的包装。将实施例2中构建的抗体基因aav载体(paav
‑
cbh
‑
kldi01,paav
‑
cbh
‑
kldi02,paav
‑
cbh
‑
kldi03)、包膜质粒(aav2/8,其核苷酸序列如seq id no:22所示)和包装质粒(phelper,其核苷酸序列如seq id no:23所示)混合后同时共转染293t细胞,在该293t细胞系中进行glp1受体激动剂基因治疗载体aav的包装。转染方法为pei阳离子聚合物介导的真核细胞瞬时转染,pei阳离子聚合物为购自polysciences的pei
‑
max转染试剂(购自polysciences,货号:24765
‑
1),转染操作参照生产商推荐标准化操作进行,转染规模为15cm细胞培养皿。转染后7h吸弃上清,更换为25ml产毒培养基。转染完成120小时后,收集上清和细胞,4200rpm离心10min,离心完成后分离上清跟细胞,细胞加裂解液跟核酶,裂解消化1h,10000g离心10min取裂解液上清。将裂解液上清及培养基上清经亲和层析纯化后分装冻存于
‑
80℃备用。
83.实施例4:glp1受体激动剂的细胞学表达
84.将包装好的慢病毒用于感染293t细胞。以慢病毒感染后细胞的培养上清载入sds
‑
page,以glp
‑
1抗体(6f117):sc
‑
71150作为1级抗体,以标记的羊抗鼠抗体作为2级抗体。western blotting结果(图4a和图4b)显示,不同的glp1受体激动剂慢病毒在体外转导细胞后均能有效地表达glp1受体激动剂,并将成熟的激动剂蛋白分泌到细胞培养上清中。
85.实施例5:表达glp1受体激动剂的慢病毒给药后上清表达的glp1受体激动剂的功能验证
86.glp1受体被glp1激活后,从细胞膜表面移位到细胞内。egfp标记蛋白对药物化合物或其他刺激的反应时的细胞易位。glp1r
‑
egfp稳转u2os细胞系可以辅助鉴定glp1受体激动剂的活性。如果glp1受体激动剂基因表达载体转导的细胞上清中,分泌表达的glp1受体激动剂具有完全的功能,将可以观察到glp1r
‑
egfp稳转u2os细胞中绿色荧光集中在细胞核周围。具体的功能验证实验步骤如下:
87.1.收集慢病毒感染的293t细胞,用pbs清洗细胞后4200rpm,5min,离心收集细胞,重悬以20μl快速抽提溶液(qe dnaextraction solution)并用pcr仪运行以下程序以裂解
细胞和抽提总dna。
88.表1细胞qe裂解pcr程序
89.温度时间65℃15min68℃15min95℃10min
90.通过本领域熟知的方法,以定量pcr计算出293t细胞感染慢病毒拷贝数(vector copy number,vcn)。
91.定量pcr使用的引物探针序列为:
92.lv forward primer 5
’‑
agtaagaccaccgcacagca
‑3’
(seq id no:24)
93.lv reverse primer 5
’‑
ccttggtgggtgctactcct
‑3’
(seq id no:25)
94.lv probe 5
’‑
cctccaggtctgaagatcagcggccgc
‑3’
(seq id no:26)
95.hk forward primer 5
’‑
gctgtcatctcttgtgggctgt
‑3’
(seq id no:27)
96.hk probe 5
’‑
cctgtcatgcccacacaaatctctcc
‑3’
(seq id no:28)
97.hk reverse primer 5
’‑
actcatgggagctgctggttc
‑3’
(seq id no:29)
98.其中lv probe中5’端带有6fam荧光基团,3’带有tamra荧光基团;
99.hk probe中5’端带有cy5荧光基团,3’带有dgb荧光基团。
100.定量pcr运行程序为:94℃5min;95℃10s,60℃30s,40cyclers。
101.vcn结果见表2。
102.表2慢病毒转导的细胞转导效率(单位:ng/ml)
103.转导体积2μl5μl10μl20μllv
‑
kldi0211.9626.5443.1190.51lv
‑
kldi0112.2112.6422.7844.63
104.2.在这个实验中,使用商业化购买的glp1(7
‑
37)(glpbio,货号:gc30058)为阳性对照。将glp1受体激动剂基因治疗载体转导的细胞培养上清与阳性对照,分别与glp1r
‑
egfp稳转的u2os细胞(北纳创联,货号:bncc352040)孵育一段时间。荧光显微镜通过观察egfp在细胞内的荧光来鉴别glp1受体激动剂的活性。
105.结果显示(图5)在体外细胞试验中,glp1受体激动剂慢病毒转导的细胞培养上清中glp1受体激动剂与glp1阳性对照(相对分子量为3355.67)有一样的活性,且生物活性高于8nm glp1阳性对照。培养上清中的glp1受体激动剂的活性相对于glp1等效值可以超过26.85ng/ml。
106.实施例6:表达glp1受体激动剂的腺相关病毒对糖尿病模型动物的高血糖药效学数据
107.由于慢病毒在小鼠肌肉注射的情况下表达框架不能整合到肌肉细胞,所以在小鼠体内几乎没有表达(数据未显示)。因此本技术采用腺相关病毒载体递送的glp1受体激动剂表达框,通过肌肉注射方法给药。将不同类型的能表达glp1受体激动剂的腺相关病毒通过肌肉注射给db/db小鼠给药后,每周剪尾用血糖仪(罗氏,卓越金)测血糖,比较不同给药组降血糖效果。
108.结果显示(图6)在体内试验中,paav
‑
cbh
‑
kldi02包装的腺相关病毒作为glp1受体
激动剂给药组小鼠血糖显著低于生理盐水组小鼠。
109.在给药后第4周、第6周、第8周取血,分离血清,用人glp1(7
‑
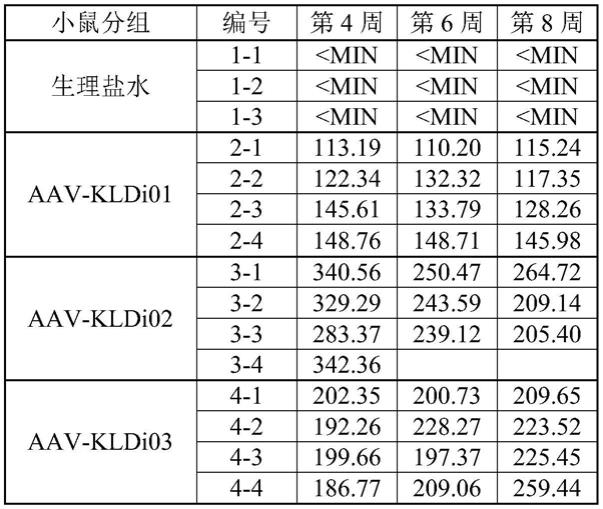
36)elisa试剂盒(abcam,ab184857)检测血清中glp1受体激动剂的含量。试验组小鼠(表3)血清中glp1受体激动剂的浓度显著达到正常人所需glp1水平。
110.表3 db/db小鼠接受表达glp1受体激动剂的腺相关病毒后的血清glp1受体激动剂浓度
[0111][0112]
实施例7:多肽及融合多肽对糖尿病模型动物的高血糖药效学数据
[0113]
将不同剂量的glp1受体激动剂腺相关病毒通过肌肉注射给c57bl/6小鼠给药。在给药5周后进行糖耐量检测,评估glp1受体激动剂腺相关病毒对正常餐食引起的血糖升高的影响。糖耐量检测:禁食12h,腹腔注射2.0g/kg体重的葡萄糖,在注射葡萄糖后0h,30min,60min,120min,剪尾取血测定血糖。
[0114]
结果显示(图7)在体内试验中,不同剂量的paav
‑
cbh
‑
kldi02包装的腺相关病毒作为glp1受体激动剂给药组小鼠的血糖显著低于生理盐水组小鼠,且成剂量正相关。
[0115]
综合以上实施例,本发明将两个以上的glp
‑
1或其类似物基因表达框架以柔性单元氨基酸组成的肽连接体(ggggs)3连接后组成串联共价二聚体或多聚体。实验结果显示,二聚体或多聚体形式的glp
‑
1或其类似物表达框架经重组病毒载体递送后获得了远高于单体glp
‑
1类似物表达框架的表达效率。同时实验结果显示,无论是在体外细胞学实验或者体内动物学实验中,二聚体或多聚体形式的glp
‑
1类似物均具有完全的glp
‑
1受体结合和激动能力。基于上述表达框架的glp
‑
1类似物分子经腺相关病毒递送至小鼠体内后显示出有效的血药浓度,同时也显示出积极的动物体内血糖调节效果。
[0116]
以上的实施例是为了说明本发明公开的实施方案,并不能理解为对本发明的限制。此外,本文所列出的各种修改以及发明中方法的变化,在不脱离本发明的范围和精神的前提下对本领域内的技术人员来说是显而易见的。虽然已结合本发明的多种具体优选实施例对本发明进行了具体的描述,但应当理解,本发明不应仅限于这些具体实施例。事实上,各种如上所述的对本领域内的技术人员来说显而易见的修改来获取发明都应包括在本发
明的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1