一种CHI3L1抗原、抗体及预测自体动静脉内瘘失功的试剂盒的制作方法
一种chi3l1抗原、抗体及预测自体动静脉内瘘失功的试剂盒
技术领域
1.本发明属于生物医学技术领域,更具体的说涉及一种chi3l1抗原、抗体及预测自体动静脉内瘘失功的试剂盒。
背景技术:
2.esrd(肾病)给整个社会、家庭及个人带来沉重的负担。数据显示我国尿毒症患者总数在近几年不断攀升,2011年我国新发及总透析患者数分别为每百万人口15.4人及237.3人。以上海为例,新发尿毒症患者从2007年的每百万人口89.4人,上升到2014年的每百万人口128.1人,总透析患者由每百万人口409.8人上升至898人。全国血液透析登记系统(cndrs)显示,截止到2018年全国血液透析患者约58万,腹膜透析患者约9.5万。由于肾移植供体来源及数量有限,目前血液透析是清除尿毒症毒素、纠正并发症、改变生活质量并延长尿毒症患者生命的关键治疗手段。
3.自体动静脉内瘘(avf)相比于其他血管通路(移植物内瘘、带cuff的皮下隧道导管)而言具有使用寿命长、感染率低且并发症少等优点,是血液透析患者的首选透析通路,被称为血液透析患者的“生命线”。然而,avf的失功严重制约着其临床应用,最新研究显示,avf1年的初级及次级通畅率分别为64%和79%,其中约21%avf建立后废弃没有使用。随着透析年龄的延长,avf的失功始终是困扰扩大血液透析患者及医务人员的难题。
4.目前在临床上还未有简便的预测自体动静脉内瘘早期失功的产品,而已有研究证明esrd患者当中,avf的失功后血清炎症标志物chi3l1水平升高。而且临床上还未有简便的预测自体动静脉内瘘早期失功的产品。因此,本发明一种chi3l1抗原、抗体及预测自体动静脉内瘘的失功的试剂盒。
技术实现要素:
5.本发明的目的在于提供一种chi3l1抗原表位肽,用该chi3l1抗原表位肽制备的chi3l1抗原和相应抗原制备的抗体,以及基于chi3l1抗原抗体的具有特异性的预测自体动静脉内瘘失功的试剂盒,能够快速简单的预测自体动静脉内瘘(avf)的失功。
6.本发明技术方案一种chi3l1抗原表位肽,包括chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ,
7.所述chi3l1抗原表位肽ⅰ的氨基酸链片段ⅰ为:
8.cys
‑
cys
‑
cys
‑
thr
‑
cys
‑
thr
‑
cys
‑
ala
‑
cys
‑
cys
‑
ala,
9.所述chi3l1抗原表位肽ⅱ的氨基酸链片段ⅱ为:
10.ala
‑
thr
‑
gln
‑
cys
‑
cys
‑
ala
‑
thr
‑
cys
‑
ala
‑
ala。
11.一种chi3l1抗原表位肽,将上述的氨基酸链片段ⅰ通过固相法合成所述chi3l1抗原表位肽ⅰ,将所述氨基酸链片段ⅱ通过固相法合成所述chi3l1抗原表位肽ⅱ。
12.一种chi3l1抗原,包括:通过上述的chi3l1抗原表位肽ⅰ与载体蛋白klh偶联制备chi3l1抗原ⅰ;通过使用上述的chi3l1抗原表位肽ⅱ与载体蛋白klh偶联制备chi3l1抗原
ⅱ
。
13.一种chi3l1抗体,包括:由上述的chi3l1抗原ⅰ制备的单克隆抗体ⅰ和由上述的chi3l1抗原ⅱ制备的单克隆抗体ⅱ。
14.一种预测自体动静脉内瘘失功的试剂盒,包括上述的单克隆抗体ⅰ和单克隆抗体ⅱ。
15.一种预测自体动静脉内瘘失功的试剂盒,包括单克隆抗体ⅰ或单克隆抗体ⅱ制备的chi3l1抗体微孔酶标板,所述chi3l1抗体微孔酶标板的制备方法为:
16.首先选用单克隆抗体ⅰ或单克隆抗体ⅱ任一种,用1xph=7.4的pbs缓冲液将其配置成0.5~1.5ng/ml的溶液a;
17.然后将溶液a滴至微孔酶标板之内,再将微孔酶标板放置于37℃培养箱内培养1.5~2h;
18.然后取出,用2%的bsa进行封闭,封闭完成后取出,并用1xph=7.4的pbs缓冲液洗涤,之后干燥0.5~1h,备用。
19.一种预测自体动静脉内瘘失功的试剂盒,还包括单克隆抗体ⅰ或单克隆抗体ⅱ制备的chi3l1检测抗体,所述chi3l1检测抗体的制备方法为:
20.首先选用单克隆抗体ⅰ或单克隆抗体ⅱ中的一种,且确保与chi3l1抗体微孔酶标板制备时选用的chi3l1抗体不同,然后将选用的抗体进行稀释,再取稀释后抗体与生物素偶联,混合旋转2h;
21.然后将偶联后溶液倒入透析袋中,在1xph=7.4的pbs缓冲液中4℃恒温下透析24h,期间换透析液4次,之后收取透析袋内溶液,即获得高浓度chi3l1检测抗体;
22.最后配置检测抗体保存液;然后将获得的高浓度检测抗体用检测抗体保存液稀释配制成0.2~1.0ng/ml的溶液待用。
23.优选的,上述生物素的体积为26ul~60ul,生物素的浓度为1umol/l~10mmol/l;
24.与生物素偶联的稀释抗体体积为1ml,稀释抗体浓度为150ug/ml~2mg/ml;
25.所述检测抗体保存液的配方为:2.2~5.4g的nah2po4,22.15~31.08g的na2hpo4·
12h2o,酪蛋白3~10g、0.15~0.35g的tween20、蒸馏水1l;
26.一种预测自体动静脉内瘘失功的试剂盒,还包括chi3l1校准品及质控品、亲和素标记hrp、底物液a和底物液b及终止液;
27.所述亲和素标记hrp用酶标保存液进行稀释;所述酶标保存液的配方为:1~1.36mol/l甘油、8.5~10mmol/l磷酸钠、26~30umol/l牛血清白蛋白、14~20umol/l细胞色素c;
28.所述底物液a的配方为:醋酸钠10.3~13.6g、柠檬酸1.2~1.6g、30%双氧水0.28ml~0.35ml和蒸馏水1l;
29.所述底物液b的配方为:乙二胺四乙酸二钠0.15~0.24g、柠檬酸0.14~0.18g、甘油36~52ml、tmb0.12~0.16g和蒸馏水1l;
30.所述终止液为硫酸,所述硫酸的浓度是1.6~2mol/l。
31.一种预测自体动静脉内瘘失功的试剂盒,用于预测自体动静脉内瘘早期失功的体外测试。
32.本发明技术方案与现有技术相比具有以下有益效果:
33.1、本发明技术方案中提供的基于原chi3l1抗原、抗体的预测自体动静脉内瘘的失功的试剂盒,为临床提供了一种可靠的用于预测自体动静脉内瘘早期失功的体外测试方法,且该试剂盒操作简便,不需要复杂的仪器进行协作,因此可进行广泛推广使用。
34.2、本发明技术方案中提供的chi3l1表位肽,在和载体蛋白连接后既具有免疫原性又具有免疫反应性,同时还能产生与chi3l1结合的特异性抗体。
附图说明
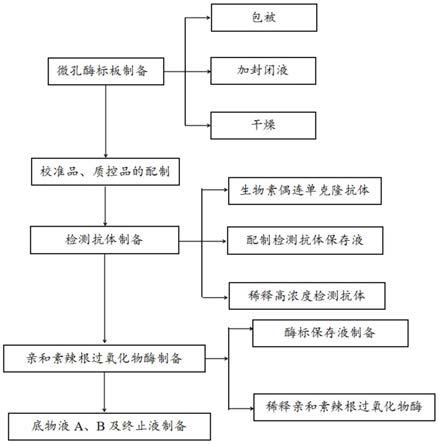
35.图1是本技术方案的预测自体动静脉内瘘失功的试剂盒的制备工艺流程图;
36.图2是本发明fmoc法合成固相肽的原理图;
37.图3是本发明单克隆抗体与生物素偶连的原理图;
38.图4是本发明试剂盒所作的线性图;
39.图5是本发明试剂盒与杭州普望公司试剂盒结果对比所作的相关性图。
具体实施方式
40.为便于本领域技术人员理解本发明技术方案,现结合说明书附图对本发明技术方案做进一步的说明。
41.一、本发明提出了一种chi3l1抗原表位肽
42.本发明中所述的chi3l1蛋白,即壳多糖酶3样蛋白1,是本领域已知的,其氨基酸序列是本领域已知的,可以在国家生物信息中心或ncbi等专业数据库中查到。
43.本发明的发明人经过大量的理论研究和实验摸索,最终从中筛选得到两种具有良好的抗原性的chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ。其分子量分别为1254.55和1104.24,其氨基酸链片段如下:
44.cys
‑
cys
‑
cys
‑
thr
‑
cys
‑
thr
‑
cys
‑
ala
‑
cys
‑
cys
‑
ala;
45.ala
‑
thr
‑
gln
‑
cys
‑
cys
‑
ala
‑
thr
‑
cys
‑
ala
‑
ala。
46.即,本发明技术方案一种chi3l1抗原表位肽,包括chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ,
47.所述chi3l1抗原表位肽ⅰ的氨基酸链片段ⅰ为:
48.cys
‑
cys
‑
cys
‑
thr
‑
cys
‑
thr
‑
cys
‑
ala
‑
cys
‑
cys
‑
ala。
49.所述chi3l1抗原表位肽ⅱ的氨基酸链片段ⅱ为:
50.ala
‑
thr
‑
gln
‑
cys
‑
cys
‑
ala
‑
thr
‑
cys
‑
ala
‑
ala。
51.本发明研究发现,本发明的抗原表位肽ⅰ和抗原表位肽ⅱ在和载体蛋白连接后既具有免疫原性又具有免疫反应性,同时还能产生与chi3l1结合的特异性抗体。
52.将上述氨基酸链片段各自合成抗原表位肽。即一种chi3l1抗原表位肽,包括利用氨基酸链片段ⅰ通过固相法合成所述chi3l1抗原表位肽ⅰ和利用氨基酸链片段ⅱ通过固相法合成所述chi3l1抗原表位肽ⅱ。
53.固相法即固相肽合成法,固相肽合成法的主要思想是:先将所要合成肽链的羧基末端氨基酸的羧基以共价键形式同一个不溶性的高分子化合物(树脂)相连接,然后以此结合在固相载体上的氨基酸作为氨基组份,经过脱去氨基保护基并同过量的活化羧基组份反应,接长肽链。重复上述操作,最后达到所需要合成的肽链的长度。
54.如图2所示,为本发明采用固相肽合成法抗原表位肽原理图(fmoc法合成固相肽的原理图)。主要步骤有:步骤(1)将fmoc保护的氨基酸进行氨基酸的活化(hobt/dcc法)
→
步骤(2)连接氨基酸到树脂上
→
步骤(3)脱去氨基酸的fmoc保护基
→
步骤(4)另一氨基酸的活化
→
步骤(5)偶联。
55.具体的过程为:
56.fmoc保护的氨基酸
[0057][0058]
步骤(1):氨基酸的活化(hobt/dcc法)
[0059][0060]
步骤(2):连接氨基酸到树脂上
[0061][0062]
步骤(3):脱去氨基酸的fmoc保护基
[0063][0064]
步骤(4):另一氨基酸的活化
[0065]
步骤(5):偶联
[0066][0067]
上述步骤流程中或如图2中所示,步骤(3)和步骤(5)需要多次重复,直至得到chi3l1抗原表位肽ⅰ的肽树脂142mg和chi3l1抗原表位肽ⅱ的肽树脂158mg。
[0068]
然后,分别裂解两肽树脂,过程为:用tfa(三氟乙酸)切割肽链,用edt(二巯基乙烷,3.0%指体积分数)、硫代苯甲醚(2.0%指体积分数)作清除剂,在室温下反应4.0h,去除切割试剂,再用乙醚萃取,分别得到chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ的粗品。
[0069]
最后,将chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ粗品进行纯化。
[0070]
用已有的技术将chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ进行纯化,并用已有技术对其进行鉴定。
[0071]
将所得到的chi3l1抗原表位肽ⅰ和chi3l1抗原表位肽ⅱ进行相应步骤的纯化后再进行鉴定,鉴定合成肽即为目的产物。
[0072]
二、本发明提出了一种chi3l1抗原
[0073]
本发明中所述的一种chi3l1抗原,包括:通过上述的chi3l1抗原表位肽ⅰ与载体蛋白klh(钥孔血蓝蛋白)偶联制备chi3l1抗原ⅰ;通过使用上述的chi3l1抗原表位肽ⅱ与载体蛋白klh(钥孔血蓝蛋白)偶联制备chi3l1抗原ⅱ。
[0074]
本发明的chi3l1抗原ⅰ和chi3l1抗原ⅱ既具有免疫原性又具有免疫反应性,同时还能产生与chi3l1结合的特异性抗体。
[0075]
三、本发明提出了种chi3l1抗体
[0076]
本发明中所述的一种chi3l1抗体,包括:由上述的chi3l1抗原ⅰ制备的单克隆抗体ⅰ和由上述的chi3l1抗原ⅱ制备的单克隆抗体ⅱ。
[0077]
四、本发明提出了一种chi3l1抗原试剂盒
[0078]
本发明中所述的chi3l1抗原试剂盒,即预测自体动静脉内瘘的失功的试剂盒,包括上述的单克隆抗体ⅰ和单克隆抗体ⅱ。
[0079]
基于上述chi3l1抗原试剂盒的技术方案,下面提出chi3l1抗原试剂盒的具体实施例。
[0080]
一种预测自体动静脉内瘘的失功的试剂盒,是基于chi3l1抗原表位肽制备的chi3l1抗原和相应抗原制备的抗体的试剂盒(简称chi3l1抗原试剂盒)。测试盒内有chi3l1抗体微孔酶标板、chi3l1校准品及质控品、chi3l1检测抗体、亲和素标记辣根过氧化物酶、底物液a和底物液b以及终止液。
[0081]
上述chi3l1抗原试剂盒的原理是:单克隆抗体ⅰ或单克隆抗体ⅱ制备的抗体被包被于微孔酶标板上形成固相抗体,然后向微孔板内依次加入适量的待检测样本及chi3l1检测抗体,形成固相抗体
‑
抗原
‑
检测抗体复合物,将酶标板进行洗涤后再加入亲和素标记hrp,最终形成固相抗体
‑
抗原
‑
检测抗体
‑
亲和素标记hrp复合物,再将酶标板进行彻底洗涤后依次加入底物a和b及终止液,之后用酶标仪在450nm波长下测定微孔板内的od值,以此获得样本中chi3l1抗原量。
[0082]
如图1所示,为上述chi3l1抗原试剂盒制备方法流程图,上述chi3l1抗原试剂盒内有chi3l1抗体微孔酶标板、chi3l1校准品及质控品、chi3l1检测抗体、亲和素标记辣根过氧化物酶、底物液a和底物液b以及终止液,分别制备chi3l1抗体微孔酶标板、chi3l1检测抗体、亲和素标记辣根过氧化物酶、底物液a和底物液b以及终止液,制备步骤后面详细描述。chi3l1校准品及质控品为直接购置的标准品。各个部分制备完成后,经过检测全部检测合格后再组合收纳放置在试剂盒内即可。
[0083]
(一)chi3l1抗体微孔酶标板
[0084]
chi3l1抗体微孔酶标板由单克隆抗体ⅰ或单克隆抗体ⅱ制备。所述chi3l1抗体微孔酶标板的制备方法为:
[0085]
首先选用单克隆抗体ⅰ或单克隆抗体ⅱ任一种,用1xph=7.4的pbs缓冲液(磷酸盐缓冲盐溶液)将其配置成0.5~1.5ng/ml的溶液a。
[0086]
然后将溶液a滴至微孔酶标板之内,再将微孔酶标板放置于37℃培养箱内培养1.5~2h。
[0087]
然后取出,用2%的bsa(牛血清白蛋白)进行封闭,封闭完成后取出,并用1xph=7.4的pbs缓冲液(磷酸盐缓冲盐溶液)洗涤,之后干燥0.5~1h,备用。
[0088]
(二)chi3l1检测抗体
[0089]
chi3l1检测抗体由单克隆抗体ⅰ或单克隆抗体ⅱ制备。值得注意的是制备chi3l1检测抗体与制备chi3l1抗体微孔酶标板的单克隆抗体不同。当包被(chi3l1抗体微孔酶标板)抗体来源于单克隆抗体ⅰ或单克隆抗体ⅱ中的一者时,制备chi3l1检测抗体的抗体来源于单克隆抗体ⅰ或单克隆抗体ⅱ中的另一者。
[0090]
chi3l1检测抗体的制备方法为:
[0091]
首先将选用的抗体(单克隆抗体ⅰ或单克隆抗体ⅱ)进行稀释,稀释至浓度为150ug/ml~2mg/ml,再取稀释后抗体1ml与26ul~60ul且浓度为1umol/l~10mmol/l的生物素偶联,混合旋转2h。
[0092]
然后将偶联后溶液倒入透析袋中,在1xph=7.4的pbs缓冲液中4℃恒温下透析24h,期间换透析液4次,之后收取透析袋内溶液,即获得高浓度chi3l1检测抗体。
[0093]
最后配置检测抗体保存液;所述检测抗体保存液的配方为:2.2~5.4g的nah2po4,22.15~31.08g的na2hpo4·
12h2o,酪蛋白3~10g、0.15~0.35g的tween20(聚山梨酯)、蒸馏水1l。再将获得的高浓度检测抗体用检测抗体保存液稀释配制成0.2~1.0ng/ml的溶液待用。
[0094]
(三)亲和素标记hrp
[0095]
试剂盒内亲和素标记hrp购自生工生物工程股份有限公司,其浓度为500u/ml。在使用时,用一定量的酶标保存液进行稀释,稀释比例为1:10000~1:30000。酶标保存液的配方为:1~1.36mol/l甘油、8.5~10mmol/l磷酸钠、26~30umol/l牛血清白蛋白、14~20umol/l细胞色素c。
[0096]
(四)chi3l1校准品及质控品
[0097]
chi3l1校准品及质控品为标准品,直接购置即可。
[0098]
(五)底物液a、底物液b及终止液
[0099]
所述底物液a的配方为:醋酸钠10.3~13.6g、柠檬酸1.2~1.6g、30%双氧水0.28ml~0.35ml和蒸馏水1l。
[0100]
所述底物液b的配方为:乙二胺四乙酸二钠0.15~0.24g、柠檬酸0.14~0.18g、甘油36~52ml、tmb0.12~0.16g和蒸馏水1l。
[0101]
所述终止液为硫酸,所述硫酸的浓度是1.6~2mol/l。
[0102]
本发明技术方案的chi3l1抗原试剂盒,用于预测自体动静脉内瘘早期失功的体外测试。其通过检测ersd患者血清中壳多糖酶3样蛋白1(chi3l1)的浓度来预测自体动静脉内瘘早期失功。当对患者血清进行检测时,只需将患者待测样品加入微孔内,后加入检测抗体,之后进行孵育后,再加入亲和素标记辣根过氧化物酶,进行二次孵育,最后加入底物液a和b及终止液后进行检测。该试剂盒操作简便、能为临床提供可靠的预测动静脉内瘘早期失功的方法的优点。
[0103]
为验证本发明技术方案中提出的chi3l1抗原试剂盒的质量,对试剂盒的各项性能进行检测,试剂盒主要的性能包括:试剂盒检测临界值的确定、相对敏感性、相对特异性、符合率、线性范围、准确度、重复性、稳定性、批间差,试剂盒相关性各个性能的检测方法如下。
[0104]
1、临界值的确定
[0105]
用建立好的elisa方法检测50份阴性血清,详细检测结果见表1.1
‑
1。
[0106]
表1.1
‑
1:50份阴性血清的elisa检测结果
[0107][0108]
根据统计学原理,确定阴阳性临界值即待测样品的检测值≥0.2943为阳性,待测样品的检测值≤0.2590为阴性,介于两者之间为可疑。
[0109]
2、相对敏感性、相对特异性及总符合率
[0110]
用建立的elisa检测方法检测50份不同抗体效价的血清样本,与杭州普望生物技术有限公司的chi3l1elisa试剂盒的检测结果相比(在试剂盒研发过程中,对已经研发出来的试剂盒需要与市场上已有试剂盒进行对比以便晓得研发试剂盒的有效性为试剂盒检测中重要一项),分析该方法的相对敏感性、相对特异性和总符合率,其计算公式如下(2.1)、(2.2)、(2.3)。
[0111]
相对敏感性(%)={阳性数/(阳性数+假阴性数)}
×
100%
………
(2.1)
[0112]
相对特异性(%)={阴性数/(阴性数+假阳性数)}
×
100%
………
(2.2)
[0113]
符合率(%)={(阳性数+阴性数)/检测总数}
×
100%
……………
(2.3)
[0114]
用建立的elisa方法检测50份不同抗体效价的血清样本,检测结果为阳性28份,阴性22份,杭州普望生物技术有限公司的chi3l1elisa试剂盒的检测结果的阳性为29份,阴性为21份,具体数据见表2.1
‑
1,相对敏感性、相对特异性及总符合率分别为:96.54%、91.67%、94%,符合试剂盒要求。
[0115]
表2.1
‑
1:50份血清的检测结果
[0116][0117][0118]
3、线性范围
[0119]
将chi3l1蛋白浓度为1.2ng/ml的高值样本按倍比稀释为5个浓度,将每一浓度样
本重复检测3次,计算其浓度的平均值,将结果平均值和稀释比例进行直线拟合,并计算线性相关系数r,结果应不低于0.9950,其检测结果如表3.1
‑
1所示,线性曲线图4所示,根据图表的信息可知该试剂盒线性符合要求。
[0120]
表3.1
‑
1:线性表格
[0121][0122]
理论值与测得值的相关性:r=0.9998
[0123]
4、准确度
[0124]
在空白的蒸馏水样本中分别加入不同浓度的chi3l1蛋白,根据该试剂盒的操作步骤对其添加回收率进行测定,测定结果如表4.1
‑
1所示,由表4.1
‑
1可知,chi3l1蛋白双抗体夹心法试剂盒回收率在86.11%~104.61%之间,变异系数在3.98%~7.21%之间,小于15%,说明该试剂盒准确度高。
[0125]
表4.1
‑
1:chi3l1蛋白双抗体夹心法试剂盒回收率测定结果
[0126][0127]
5、重复性
[0128]
5.1批内重复性
[0129]
用实验室试制的同一批次的chi3l1elisa检测试剂盒,分别于第1、2、3、5、7天分别检测已知背景血清30份,其中阴性血清10份,强阳性血清10份,弱阳性血清10份,每份血清做3个重复,计算标准差和变异系数,分析其批内重复性,测定结果如表5.1
‑
1、5.1
‑
2、5.1
‑
3所示,从表结果可知,30份血清的变异系数均小于15%,这表示同一批次的试剂盒批内重复性较好。
[0130]
表5.1
‑
1:批内重复性检测结果
[0131][0132]
表5.1
‑
2:批内重复性检测结果
[0133][0134]
表5.1
‑
3:批内重复性检测结果
[0135][0136]
5.2批间重复性
[0137]
用3个不同批次(批号分别为20200307、20200415、20200416)实验室试制的chi3l1elisa检测试剂盒,分别检测已知背景血清30份,其中阴性血清10份,强阳性血清10份,弱阳性血清10份,每份血清重复3次,结果见表5.2
‑
1、5.2
‑
2、5.2
‑
3,从表结果可知,30份血清的变异系数均小于15%,这表示3个批次试剂盒的批间重复性较好。
[0138]
表5.2
‑
1:批间重复性检测结果
[0139][0140]
表5.2
‑
2批间重复性检测结果
[0141][0142]
表5.2
‑
3批间重复性检测结果
[0143][0144]
6、稳定性试验
[0145]
将3个不同批次(批号分别为20200307、20200415、20200416)的chi3l1elisa检测试剂盒于2
‑
8℃保存,分别于0个月、1个月、2个月、3个月、4个月、5个月、6个月、8个月、10个月、12个月取出,用相同的50份血清进行elisa检测,与杭州普望elisa检测试剂盒进行敏感性、特异性和符合率的比较,结果见表6.1
‑
1。从结果可以看出,试剂盒的敏感性、特异性和符合率都比较稳定,说明试剂盒可以保存在8个月及以上。
[0146]
表6.1
‑
1试剂盒稳定性实验结果
[0147][0148]
7、相关性测试
[0149]
用本发明chi3l1校准品进行定标,随机测试100份人血清样本,测试结果与杭州普望生物技术有限公司的chi3l1elisa试剂盒测试的结果对比,对比结果如附图5所示。从附图5可知,其相关性r=0.9942,表明试剂盒相关性好。
[0150]
通过对试剂盒临界值、相对敏感性、相对特异性、符合率、线性范围、准确度、重复性、批间差、稳定性进行测试,可知产品的各项性能均符合要求,因此该试剂盒的质量合格。
[0151]
本发明技术方案在上面结合附图对发明进行了示例性描述,显然本发明具体实现并不受上述方式的限制,只要采用了本发明的方法构思和技术方案进行的各种非实质性改进,或未经改进将发明的构思和技术方案直接应用于其它场合的,均在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1