一种用于防治花生白绢病的贝莱斯芽孢杆菌、微生物菌剂、微生物肥料及其应用的制作方法
1.本技术涉及生防菌株的技术领域,更具体地说,它涉及一种用于防治花生白绢病的贝莱斯芽孢杆菌、微生物菌剂、微生物肥料及其应用。
背景技术:
2.花生作为我国四大油料作物之一,在农业生产和社会生产中占据重要的地位,但其产量受到病虫害的严重影响,其中白绢病对花生的危害更是呈现逐年加重的趋势。
3.目前,对于花生白绢病的防控措施主要有轮作、深耕、培育抗性品种以及使用化学药剂等,然而,上述防控方式均治标不治本,并且长时间使用化学药剂,还会导致田间土壤受到化学药剂的污染,造成农产品质量和产量均下降,甚至还会出现农产品的安全性问题。
4.生物防控是农业绿色发展的重要方向,利用生防菌株防控花生白绢病是一直以来农业绿色发展迫切需要解决的难题。
技术实现要素:
5.为了有效改善田间花生白绢病的发病情况,提高花生产量,本技术提供一种用于防治花生白绢病的贝莱斯芽孢杆菌、微生物菌剂、微生物肥料及其应用。
6.第一方面,本技术提供一种用于防治花生白绢病的贝莱斯芽孢杆菌,采用如下的技术方案:
7.一种用于防治花生白绢病的贝莱斯芽孢杆菌,所述贝莱斯芽孢杆菌命名为贝莱斯芽孢杆菌dpt
‑
03(bacillus velezensis dpt
‑
03),保藏于中国微生物菌种保藏管理委员会普通微生物中心(cgmcc),保藏编号为cgmcc no.20317。
8.本技术提供了一种高效抑制花生白绢病病原菌的的贝莱斯芽孢杆菌,通过探究该bacillus velezensis dpt
‑
03抑制花生白绢病病原菌的途径,并在田间多地进行实际应用效果试验,确定bacillus velezensis dpt
‑
03对花生白绢病病原菌具有较好的抑制效果,同时,bacillus velezensis dpt
‑
03在田间复杂环境下对bacillus velezensis dpt
‑
03的应用效果和防治效果具有较好的稳定性。因此,bacillus velezensis dpt
‑
03可用于制备抗性强、专一且稳定性高的花生白绢病生防制剂。
9.通过研究发现,bacillus velezensis dpt
‑
03能够明显抑制花生白绢病病原菌菌丝的生长,同时还能够抑制白绢病病原菌菌核的形成,从而减少花生白绢病病原菌的寄留和繁衍,故bacillus velezensis dpt
‑
03能够有效降低花生的病株率和死棵率,从而有效降低花生的发病率,对花生白绢病具有较好的防治效果。
10.本技术提供的bacillus velezensis dpt
‑
03是基于16s rdna序列构建系统发育树鉴定分析获得的,其16s rdna序列如seq id no 1所示。
11.第二方面,本技术提供一种利用上述用于防治花生白绢病的贝莱斯芽孢杆菌制备的菌悬液。
12.优选的,所述菌悬液的浓度为1.0
×
109‑
4.0
×
109cfu/ml。
13.在一个具体的实施方式中,所述菌悬液的浓度为1.0
×
109cfu/ml。
14.在一个具体的实施方式中,所述菌悬液的浓度为4.0
×
109cfu/ml。
15.第三方面,利用上述用于防治花生白绢病的贝莱斯芽孢杆菌和/或利用上述菌悬液制备的无菌发酵液。
16.第四方面,本技术提供一种微生物菌剂,采用如下的技术方案:
17.一种微生物菌剂,所述微生物菌剂包括上述贝莱斯芽孢杆菌、贝莱斯芽孢杆菌产生的挥发性气体、菌悬液和/或无菌发酵液。
18.优选的,所述微生物菌剂还包括用于携带或包埋菌体、挥发性气体、菌悬液和/或无菌发酵液的载体。
19.优选的,所述微生物菌剂为固体制剂或液体制剂。
20.优选的,所述固体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度大于或等于1x109cfu/ml。
21.优选的,所述固体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度为1x109‑
4x109cfu/ml。
22.在一个具体的实施方式中,所述固体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度为1x109cfu/ml。
23.优选的,所述液体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度大于或等于1x109cfu/ml。
24.优选的,所述液体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度为1x109‑
4x109cfu/ml。
25.在一个具体的实施方式中,所述液体制剂中bacillus velezensis dpt
‑
03菌悬液的浓度为1x109cfu/ml。
26.优选的,所述固体制剂的吸附载体为腐殖酸。
27.研究发现,将bacillus velezensis dpt
‑
03应用于制备微生物菌剂,该微生物菌剂能够高效、针对性强的预防和防治花生白绢病,减少花生的病株率和死棵率,同时还能够增加花生的产量。此外,利用抗性强、专一且稳定性高的bacillus velezensis dpt
‑
03制备的微生物菌剂代替化学农药,在一定程度上能够减少化学农药防治花生白绢病所带来的生态污染,同时弥补广谱生物制剂高效性和稳定性不足的缺点,为花生白绢病多发地区的花生健康种植和花生产量提供一定的保障。
28.第五方面,本技术提供一种微生物肥料,采用如下的技术方案:
29.一种微生物肥料,所述微生物肥料包括上述贝莱斯芽孢杆菌、上述贝莱斯芽孢杆菌产生的挥发性气体、上述菌悬液、上述无菌发酵液和/或上述微生物菌剂。
30.优选的,所述微生物肥料还包括复合肥。
31.优选的,所述微生物菌剂和复合肥的混合比例为1:(1
‑
2)。
32.在一个具体的实施方式中,所述微生物菌剂和复合肥的混合比例为4:5。
33.在一个具体的实施方式中,所述微生物菌剂和复合肥的混合比例为2:3。
34.第六方面,本技术提供上述贝莱斯芽孢杆菌、上述贝莱斯芽孢杆菌产生的挥发性气体、上述菌悬液、上述无菌发酵液、上述微生物菌剂或上述微生物肥料在制备用于改善
和/或预防花生白绢病的组合物中的应用。
35.综上所述,本技术具有以下有益效果:
36.1、本技术提供的bacillus velezensis dpt
‑
03对花生白绢病病原菌具有明显的抑制作用,其可用于制备抗性强、专一且稳定性高的花生白绢病生防制剂。
37.2、bacillus velezensis dpt
‑
03菌悬液、无菌发酵液、挥发性气体能够有效抑制花生白菌病病原菌的菌丝生长;接种5d时,上述三者对花生白菌病病原菌的菌丝生长的抑制率分别为71.39%、55.98%和20.68%;接种20d时,上述三者对花生白菌病病原菌的菌丝生长的抑制率分别为87.20%、53.27%和8.99%。因此,可知bacillus velezensis dpt
‑
03可以通过分泌强抑菌活性物质和产生抑菌性气体来抑制花生白绢病病原菌的生长。其中,bacillus velezensis dpt
‑
03主要通过分泌强抑菌活性物质来抑制花生白绢病病原菌的生长,且其抑制花生白绢病病原菌的持效期更长。
38.3、bacillus velezensis dpt
‑
03菌悬液和bacillus velezensis dpt
‑
03无菌发酵液均能高效抑制花生白绢病病原菌菌核形成;接种30d时,上述两者对花生白菌病病原菌菌核生长的抑制率分别为88.51%和76.34%。相关技术中,花生白菌病病原菌菌核在土壤中存活一年甚至几年后仍具有侵染活力,为花生白绢病的防治带来重大挑战,而本技术提供的bacillus velezensis dpt
‑
03可通过分泌代谢产物来抑制花生白菌病病原菌菌核的形成且其抑制效果显著,很大程度上减少了花生白菌病病原菌的繁衍和寄留,进一步降低了花生白菌病的发病率。
39.4、本技术提供的利用bacillus velezensis dpt
‑
03制备的微生物菌剂在多地田间应用中均能够有效抑制花生白绢病,减少花生发生率,降低花生死棵率,说明bacillus velezensis dpt
‑
03在土壤中的适应能力强,稳定性高。本技术提供的微生物制剂的使用有助于减少病害区花生的产量损失,进一步增加了花生的种植收益。
40.5、利用bacillus velezensis dpt
‑
03制备的微生物菌剂或微生物肥料代替化学肥料,能够有效减少化学农药的施用,进一步降低化学农药防治花生白绢病的生态污染,同时弥补广谱生物制剂专一性、高效性和稳定性不足的缺点,对花生白绢病多发地区的花生健康种植和花生产量提供一定的保障。
附图说明
41.图1为检测试验一中bacillus velezensis dpt
‑
03菌悬液在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
42.图2为检测试验一中bacillus velezensis dpt
‑
03无菌发酵液在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
43.图3为检测试验一中bacillus velezensis dpt
‑
03挥发性气体在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
44.图4为检测试验二中bacillus velezensis dpt
‑
03菌悬液在培养30d时对花生白绢病病原菌菌核生长的作用效果。
45.图5为检测试验二中bacillus velezensis dpt
‑
03无菌发酵液在培养30d时对花生白绢病病原菌菌核生长的作用效果。
46.图6为检测试验二中bacillus velezensis dpt
‑
03挥发性气体在培养30d时对花
生白绢病病原菌菌核生长的作用效果。
47.图7为检测试验三中bacillus velezensis dpt
‑
03防控花生白绢病的盆栽作用效果(图中,处理1
‑
处理4分别对应实施例3、实施例4、对比例1、对比例2)。
48.图8为检测试验五中微生物肥料对于花生白绢病的田间防治效果(图中,处理1
‑
处理3分别对应实施例8、对比例5、对比例6)。
49.图9为检测试验六中微生物肥料对于花生白绢病的田间防治效果(图中,处理1
‑
处理4分别对应实施例10、对比例7、对比例8、对比例9)。
具体实施方式
50.本技术提供了一种用于防治花生白绢病的贝莱斯芽孢杆菌,所述贝莱斯芽孢杆菌命名为贝莱斯芽孢杆菌dpt
‑
03(bacillus velezensis dpt
‑
03),保藏于中国微生物菌种保藏管理委员会普通微生物中心(cgmcc),保藏编号为cgmcc no.20317,保藏日期为2020年7月8日。其16s rdna序列如seq id no 1所示。
51.本技术还提供了利用上述用于防治花生白绢病的贝莱斯芽孢杆菌制备的菌悬液、无菌发酵液。
52.另外,本技术还提供了一种微生物菌剂,所述微生物菌剂包括上述贝莱斯芽孢杆菌、贝莱斯芽孢杆菌产生的挥发性气体、菌悬液和/或无菌发酵液。进一步地,所述微生物菌剂还包括用于携带或包埋菌体、挥发性气体、菌悬液和/或无菌发酵液的载体。进一步地,所述微生物菌剂为固体制剂或液体制剂。
53.此外,本技术还提供了一种微生物肥料,所述微生物肥料包括上述贝莱斯芽孢杆菌、贝莱斯芽孢杆菌产生的挥发性气体、菌悬液、无菌发酵液和/或微生物菌剂。进一步地,所述微生物肥料还包括复合肥。进一步地,所述微生物菌剂和复合肥的混合比例为1:(1
‑
2)。
54.本技术还提供了上述贝莱斯芽孢杆菌、贝莱斯芽孢杆菌产生的挥发性气体、菌悬液、无菌发酵液、微生物菌剂或微生物肥料在制备用于改善和/或预防花生白绢病的组合物中的应用。
55.以下实施例和对比例中所涉及的仪器、试剂、材料等,若无特别说明,均为相关技术中的常规仪器、试剂、材料等。下列实施例中所涉及的试验方法和检测方法,若无特别说明,均为相关技术汇中的常规试验方法和常规检测方法。
56.其中,本技术中涉及的以下内容具体为:
57.lb固体培养基的配方如下:以体积1l计,包括胰蛋白胨10g,酵母提取物5g,nacl 10g,琼脂15g。
58.lb液体培养基的配方如下:以体积1l计,包括胰蛋白胨10g,酵母提取物5g,nacl 10g。
59.pda液体培养基:以体积1l计,包括马铃薯200g,葡萄糖20g,自然ph。
60.pda固体培养基:以体积1l计,包括马铃薯200g,葡萄糖20g,琼脂15g,自然ph。
61.其中,本技术中的复合肥厂家为:北京世纪阿姆斯生物工程有限公司,型号为15
‑
15
‑
15;
62.市售微生物菌剂ⅰ的有效活菌数≥10亿/g,有效菌种:枯草芽孢杆菌+胶冻样芽孢
杆菌,规格40kg;
63.市售微生物菌剂ⅱ的有效活菌数≥10亿/g,有效菌种:枯草芽孢杆菌,规格40kg。
64.市售微生物菌剂ⅲ的有效活菌数≥10亿/g,有效菌种:枯草芽孢杆菌+地衣芽孢杆菌,规格40kg。
65.以下结合制备例1
‑
3、实施例1
‑
10、对比例1
‑
9、附图1
‑
9以及检测试验一
‑
六本技术作进一步详细说明。
66.制备例
67.制备例1
68.本制备例提供了bacillus velezensis dpt
‑
03的筛选方法。
69.一、采样地点
70.本制备例中的采样地点为北京世纪阿姆斯生物技术有限公司的花生试验田中的病害土壤。
71.二、菌株的分离、纯化
72.(1)于采样地点采集病害土壤块20g,带回实验室,作为土壤样品;
73.(2)称取10g步骤(1)获得的土壤样品,将称好的土壤样品添加至装有90ml无菌水的三角瓶中,然后将三角瓶置于150r/min、28℃的恒温摇床中培养30min,获得样品悬浮液;
74.(3)取1ml步骤(2)获得的样品悬浮液,按照10倍比例梯度稀释后,获得10
‑1、10
‑2、10
‑3、10
‑4、10
‑5和10
‑6倍的样品稀释液;
75.(4)分别取步骤(3)获得的10
‑4、10
‑5和10
‑6倍的样品稀释液100μl涂布于lb固体培养基平板上,并将涂布后的lb固体培养基平板置于28℃的恒温培养箱中培养48h;培养后lb固体培养基平板上有菌落生长;
76.(5)挑取步骤(4)的lb固体培养基平板上生长的单菌落,划线转移至新的lb固体培养基平板上,并将划线后的lb固体培养基平板置于28℃的恒温培养箱中培养48h;观察培养后的lb固体培养基平板中只有一种菌落形态,则表明分离纯化完成;将分离纯化完成后的lb固体培养基平板置于4℃的条件下保存,备用。
77.通过上述对土壤样品中菌株的分离、纯化,共获得8种菌株。
78.三、菌株的筛选
79.(1)分别将分离、纯化获得的8种菌株活化,接种至相应的lb液体培养基中,并将接种后的lb液体培养基置于150r/min、28℃的恒温摇床中培养24h;培养后lb液体培养基中菌株od
600
达到1.2以上,得到8种菌株的被测试菌液;
80.(2)利用对峙生长法筛选抗性菌株:
81.a.将花生白绢病病原菌置于pda固体培养基平板上活化,获得活化后的病原菌平板;
82.b.利用打孔器从活化后的病原菌平板上取样,获得病原菌菌块,并将病原菌菌块置于空白pda固体培养基平板的中央;然后在距离pda固体培养基平板中央20mm处平行放置2个6mm的灭菌滤纸片,并向其中一个滤纸片上加入10μl活化后的被测试菌液,作为检测样,向另一个滤纸片上加入10μl无菌pda液体培养基,作为对照样;将上述pda固体培养基平板置于28℃的恒温培养箱中培养72h;若培养后的pda固体培养基平板上出现抑菌带,则表明该菌株为白绢病病原菌抗性菌株。
83.分别利用上述步骤对步骤(1)获得的被测试菌液进行筛选,通过培养后pda固体培养基平板上是否产生抑菌带以及产生的抑菌带宽度,对8种菌株的抗菌能力进行初步判定。
84.经过筛选,最终获得一株抑菌带宽度超过15mm的菌株,命名为dpt
‑
03,菌株dpt
‑
03对花生白绢病病原菌表现出明显的抑制作用。将菌株dpt
‑
03利用lb液体培养基培养后,
‑
80℃甘油保藏。
85.制备例2
86.本制备例提供了bacillus velezensis dpt
‑
03的培养方法。
87.将bacillus velezensis dpt
‑
03接种于lb固体培养基平板,置于37℃的恒温培养箱中培养48h,菌落表面干燥褶皱,不透明,乳白色,边缘不规则或近圆形,有微突起。显微镜观察菌体形态特征为杆状,单细胞,革兰氏染色为阳性,有芽孢。
88.制备例3
89.本制备例提供了bacillus velezensis dpt
‑
03的鉴定方法。
90.将制备例1筛选获得的菌株dpt
‑
03接种于lb固体培养基中,培养过夜后,从平板上取一个新鲜的单菌落置于1.5ml离心管中,加入10ul的s2裂解液,将其震荡混匀,室温静置20min,随后稀释20倍,震荡混匀,12000r/min,离心2min,取上清液作为模板,进行pcr扩增。
91.扩增条件如下:
92.正向引物为27f:agagtttgatcctggctcag;
93.反向引物为1492r:tacggctaccttgttacgactt;
94.扩增酶为code#as11;
95.扩增程序为94℃5min;94℃30s;55℃30s;72℃90s;循环数35次,72℃7min,4℃保存。
96.扩增反应体系如下:2x easytaq supermix 15ul;27f(10μm)1.5ul;1492r(10μm)1.5ul;模板5ul;ddh2o 7ul;total 30ul。
97.将pcr扩增产物进行琼脂糖凝胶电泳,回收并纯化胶块。
98.琼脂糖凝胶电泳的配置体系如下:蒸馏水2.16ml;30%acr
‑
bis(29:1)2.64ml;1m tris ph=8.8 3.04ml;10%sds 0.08ml;10%过硫酸钠0.08ml;temed 0.0032ml;total 8ml。
99.将纯化后的产物进行sanger测序,获得正反向测序结果,利用dnaman软件对所得基因序列进行拼接,并在www.ezbiocloud.net数据库中进行16s rdna的比对,鉴定微生物的种类。
100.利用16s rdna序列比对,确定菌株dpt
‑
03系统发育相关的属,并基于16s rdna序列采用邻接法构建系统发育树。通过分析系统发育树,菌株dpt
‑
03和bacillus velezensis表现的亲缘关系最近,序列相似性为99.8%。基于菌株dpt
‑
03的16s rdna系统发育分析,确定筛选得到的菌株dpt
‑
03为贝莱斯芽孢杆菌dpt
‑
03(bacillus velezensis dpt
‑
03)。其16s rdna的序列如seq id no 1所示。
101.实施例
102.实施例1
103.本实施例提供了bacillus velezensis dpt
‑
03菌悬液的制备方法。
104.取4℃保存的lb固体培养基平板上的bacillus velezensis dpt
‑
03单菌落,接种
velezensis dpt
‑
03无菌发酵液,制备测试样,作为对照样。
122.将上述半lb固体培养基
‑
半pda固体培养基平板置于28℃的恒温培养箱中培养,分别在5d、20d时对抑菌情况进行统计。每个处理重复3次。
123.二、计算方法
124.用十字交叉法测量上述培养后的pda固体培养基平板中花生白绢病病原菌的菌落直径,并分别计算检测样菌落增长直径、对照样菌落增长直径以及抑菌率。
125.计算公式如下:
126.抑菌率(%)=(对照样菌落增长直径—检测样菌落增长直径)/对照样菌落增长直径
×
100%;
127.菌落增长直径(mm)=菌落直径
‑
7.5。
128.三、检测结果
129.检测结果如表1以及图1
‑
3所示。
130.图1为bacillus velezensis dpt
‑
03菌悬液在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
131.图2为bacillus velezensis dpt
‑
03无菌发酵液在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
132.图3为bacillus velezensis dpt
‑
03挥发性气体在培养5d、20d时对花生白绢病病原菌菌丝生长的作用效果。
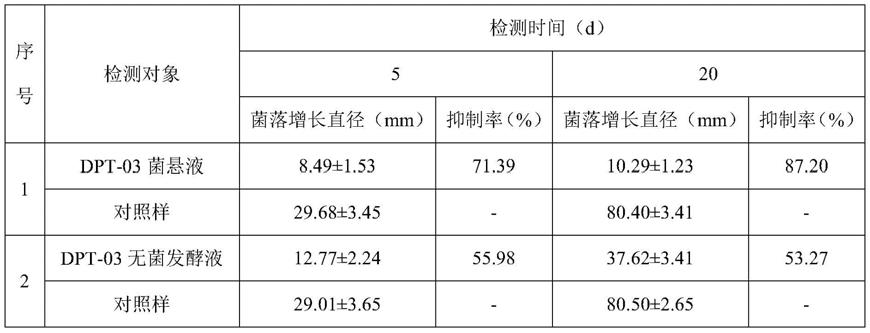
133.表1检测试验一的检测结果
[0134][0135][0136]
如表1所示的检测结果,结合图1,可知bacillus velezensis dpt
‑
03菌悬液对花生白绢病病原菌菌丝的生长具有显著的抑制效果。其中,培养至5d时,bacillus velezensis dpt
‑
03菌悬液对花生白绢病病原菌菌丝生长的抑制率为71.39%;培养至20d时,bacillus velezensis dpt
‑
03菌悬液对花生白绢病病原菌菌丝生长的抑制率达到了87.20%。由上述结果可知,随着培养时间的增加,bacillus velezensis dpt
‑
03菌悬液对花生白绢病病原菌菌丝生长抑制率表现出一定的上升趋势。
[0137]
结合图2,可知bacillus velezensis dpt
‑
03无菌发酵液对花生白绢病病原菌菌丝的生长具有显著的抑制效果。其中,培养至5d时,bacillus velezensis dpt
‑
03无菌发酵
液对花生白绢病病原菌菌丝生长的抑制率为55.98%;培养至20d时,bacillus velezensis dpt
‑
03无菌发酵液对花生白绢病病原菌菌丝生长的抑制率达到了53.27%。由上述结果可知,bacillus velezensis dpt
‑
03无菌发酵液含有抑制花生白绢病病原菌菌丝生长的活性物质,此活性物质能够抑制花生白绢病病原菌菌丝的扩张和生长。
[0138]
结合图3,可知bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌丝的生长具有一定的抑制效果。其中,培养至5d时,bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌丝生长的抑制率为20.68%;培养至20d时,bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌丝生长的抑制率达到了8.99%。由上述结果可知,随着培养时间的增加,bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌丝生长抑制率具有一定的下降趋势。从整体检测结果来看,bacillus velezensis dpt
‑
03菌悬液和bacillus velezensis dpt
‑
03无菌发酵液对花生白绢病病原菌菌丝生长的抑制作用均优于bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌丝生长的抑制作用。
[0139]
检测试验二
[0140]
以实施例1制备的bacillus velezensis dpt
‑
03菌悬液、实施例2制备的bacillus velezensis dpt
‑
03无菌发酵液以及bacillus velezensis dpt
‑
03挥发性气体为检测对象,检测其对花生白绢病病原菌菌核生长的影响。
[0141]
一、检测方法
[0142]
(1)菌悬液的检测:按照“检测试验一”中“菌悬液的检测”方法制备测试样,分别作为检测样和对照样。将上述制备的检测样和对照样对应的pda固体培养基平板置于28℃的恒温培养箱中培养30d,对菌核生长情况进行统计。
[0143]
(2)无菌发酵液的检测:按照“检测试验一”中“无菌发酵液的检测”方法制备测试样,分别作为检测样和对照样。将上述制备的检测样和对照样对应的pda固体培养基平板置于28℃的恒温培养箱中培养30d,对菌核生长情况进行统计。
[0144]
(3)挥发性气体的检测:按照“检测试验一”中“挥发性气体的检测”方法制备测试样,分别作为检测样和对照样。将上述制备的检测样和对照样对应的半lb固体培养基
‑
半pda固体培养基平板置于28℃的恒温培养箱中培养30d,对菌核生长情况进行统计。
[0145]
二、计算方法
[0146]
分别计数检测样菌核数量、对照样菌核数量以及菌核抑菌率。
[0147]
菌核抑菌率的计算公式如下:
[0148]
菌核抑制率(%)=(对照样菌核数量—检测样菌核数量)/对照样菌核数量
×
100%三、检测结果
[0149]
检测结果如表2以及图4
‑
6所示。
[0150]
图4为bacillus velezensis dpt
‑
03菌悬液在培养30d时对花生白绢病病原菌菌核生长的作用效果。
[0151]
图5为bacillus velezensis dpt
‑
03无菌发酵液在培养30d时对花生白绢病病原菌菌核生长的作用效果。
[0152]
图6为bacillus velezensis dpt
‑
03挥发性气体在培养30d时对花生白绢病病原菌菌核生长的作用效果。
[0153]
表2检测试验二的检测结果
[0154][0155]
如表2所示的检测结果,结合图4,可知连续培养30天时,利用bacillus velezensis dpt
‑
03菌悬液制备的检测样中,花生白绢病病原菌菌核生长的数量平均为4.33个,而对照样中花生白绢病病原菌菌核生长的数量平均达到37.67个,bacillus velezensis dpt
‑
03菌悬液对花生白绢病病原菌菌核生长的抑制率达到88.51%。由上述结果可知,bacillus velezensis dpt
‑
03菌悬液能较大程度上减少花生白绢病病原菌菌核的形成,进一步降低了花生白绢病病原菌的寄留和繁衍能力,对防控花生白绢病病原菌具有一定的优势。
[0156]
结合图5,可知连续培养30天时,利用bacillus velezensis dpt
‑
03无菌发酵液制备的检测样中,花生白绢病病原菌菌核生长的数量平均为10.33个,而对照样中花生白绢病病原菌菌核生长的数量平均达到43.67个,bacillus velezensis dpt
‑
03无菌发酵液对花生白绢病病原菌菌核生长的抑制率达到76.34%。由上述结果可知,bacillus velezensis dpt
‑
03无菌发酵液能较大程度上减少花生白绢病病原菌菌核的形成。bacillus velezensis dpt
‑
03会分泌具有抑菌作用的活性物质,一方面该活性物质能够抑制花生白绢病病原菌菌丝的生长,另一方面该活性物质也能抑制花生白绢病病原菌菌核的形成。
[0157]
结合图6,可知连续培养30天时,利用bacillus velezensis dpt
‑
03挥发性气体制备的检测样中,花生白绢病病原菌菌核生长的数量平均为36.33个,而对照样中花生白绢病病原菌菌核生长的数量平均达到40.67个,bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌核生长的抑制率为10.67%。由上述结果可知,bacillus velezensis dpt
‑
03挥发性气体会产生具有一定抑菌作用的活性气体来抑制花生白绢病病原菌菌核的形成。从整体检测结果来看,bacillus velezensis dpt
‑
03菌悬液和bacillus velezensis dpt
‑
03无菌发酵液对花生白绢病病原菌菌核生长的抑制作用均优于bacillus velezensis dpt
‑
03挥发性气体对花生白绢病病原菌菌核生长的抑制作用。
[0158]
实施例3
[0159]
本实施例提供了一种包括bacillus velezensis dpt
‑
03菌悬液的盆栽。利用的bacillus velezensis dpt
‑
03菌悬液为实施例1制备的bacillus velezensis dpt
‑
03菌悬液。
[0160]
上述盆栽的制备方法如下:
[0161]
(1)制备花生盆栽:将2kg土壤与1g复合肥料15
‑
15
‑
15混合均匀,并置于花盆中,将3粒饱满健康的花生粒埋入土壤中,待15d后进行间苗,每盆保留1棵花生苗;
[0162]
(2)病原菌的接种:20d后将花生白绢病病原菌接种到花生盆栽的土壤中,接种量为20ml,浓度为1.0
×
108cfu/ml;
[0163]
(3)菌悬液的接种:花生白绢病病原菌接种2d后将浓度为1.0
×
109cfu/ml的bacillus velezensis dpt
‑
03菌悬液接种到花生盆栽的土壤中,接种量为每个盆栽20ml,制得包括bacillus velezensis dpt
‑
03菌悬液的盆栽。
[0164]
实施例4
[0165]
本实施例提供了一种包括bacillus velezensis dpt
‑
03无菌发酵液的盆栽。利用的bacillus velezensis dpt
‑
03无菌发酵液为实施例2制备的bacillus velezensis dpt
‑
03无菌发酵液。
[0166]
上述盆栽的制备方法与实施例3中的制备方法的不同之处在于:
[0167]
步骤(3)为:无菌发酵液的接种:花生白绢病病原菌接种2d后将浓度为1.0
×
109cfu/ml的bacillus velezensis dpt
‑
03无菌发酵液接种到花生盆栽的土壤中,接种量为每个盆栽20ml,制得包括bacillus velezensis dpt
‑
03无菌发酵液的盆栽。
[0168]
对比例1
[0169]
本对比例提供了一种包括处理药剂的盆栽。其制备方法与实施例3的不同之处在于:
[0170]
步骤(3)为:噻呋酰胺农药的接种:花生白绢病病原菌接种2d后将噻呋酰胺农药接种到花生盆栽的土壤中,接种量为每个盆栽20ml,制得包括处理药剂的盆栽。其中,噻呋酰胺农药为240g/l噻呋酰胺悬浮剂,且将噻呋酰胺农药稀释500倍使用。
[0171]
对比例2
[0172]
本对比例提供了一种盆栽。其制备方法与实施例3的不同之处在于:
[0173]
步骤(3)为:无菌水的接种:花生白绢病病原菌接种2d后将无菌水接种到花生盆栽的土壤中,接种量为每个盆栽20ml,制得包括无菌水的盆栽。
[0174]
检测试验三
[0175]
以实施例3、实施例4、对比例1、对比例2制备的盆栽为检测对象,上述每种盆栽分别设置15个平行,检测各盆栽的发病情况。
[0176]
一、检测方法
[0177]
分别在花生盆栽接种花生白绢病病原菌20d、40d、60d时,对花生盆栽的发病情况进行检测,统计花生盆栽的发病率、病情指数和防治效果。
[0178]
二、计算方法
[0179]
分别计算花生盆栽的发病率、病情指数和防治效果。
[0180]
(1)发病率的计算公式如下:
[0181]
发病率(%)=发病株数/总株数
×
100%;
[0182]
(2)病情指数的计算公式如下:
[0183]
病情指数=∑(各级发病株树
×
各病级数)/(调查总株树
×
最高病级数)
×
100%;
[0184]
花生白绢病的发病程度采用0~4级的分级标准:
[0185]
0级,无症状;
[0186]
1级,仅茎基部产生病斑;
[0187]
2级,染病部位占整株的三分之一以下;
[0188]
3级,染病部位占整株的三分之二以下;
[0189]
4级,植株接近或已经死亡。
[0190]
(3)防治效果的计算公式如下:
[0191]
防治效果(%)=(对照病情指数
‑
处理病情指数)/对照病情指数
×
100%
[0192]
三、检测结果
[0193]
检测结果如表3以及图7所示。
[0194]
图7为bacillus velezensis dpt
‑
03防控花生白绢病的盆栽作用效果。其中,处理1
‑
处理4分别对应实施例3、实施例4、对比例1、对比例2。
[0195]
表3检测试验三的检测结果
[0196][0197]
如表3所示的检测结果,结合图7,通过对比例2的检测结果,可知花生盆栽中单独接种花生白绢病病原菌时,花生植株的发病时间较早,在接种花生白绢病病原菌20d时花生植株的发病率即达到了20.00%,发病植株也达到了20.00。而通过实施例3、实施例4以及对比例1的检测结果,可知同样在接种花生白绢病病原菌20d,接种bacillus velezensis dpt
‑
03菌悬液、bacillus velezensis dpt
‑
03无菌发酵液以及处理药剂的花生盆栽中,花生植株均未出现发病情况,上述三者对于花生白绢病的防治效果均达到了100%。由上述结果可知,无论是本技术提供的bacillus velezensis dpt
‑
03菌悬液,还是本技术提供的bacillus velezensis dpt
‑
03无菌发酵液,均能够在短期内保证花生植株不出现发病情况。故在花生植株培育的过程中,本技术提供的bacillus velezensis dpt
‑
03能够有效预防短期内花生植株出现花生白绢病,同时还能够推迟花生植株的发病时间和发病指数。
[0198]
通过对比花生盆栽接种花生白绢病病原菌40d时实施例3、实施例4、对比例1、对比例2的结果可知,此时,接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果达到了59.01%,接种bacillus velezensis dpt
‑
03无菌发酵液的花生盆栽对于花生白绢病的防治效果达到了49.98%;接种处理药剂的花生盆栽对于花生白绢病的防治效果达到了59.01%。由上述结果可知,当花生盆栽接种花生白绢病病原菌40d时,接种bacillus velezensis dpt
‑
03菌悬液、bacillus velezensis dpt
‑
03无菌发酵液以及处理药剂的花生盆栽对于花生白绢病的防治效果较接种花生白绢病病原菌20d的防治效果均有
所下降,且此时接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果与接种处理药剂的花生盆栽对于花生白绢病的防治效果基本相同,而接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果则优于接种bacillus velezensis dpt
‑
03无菌发酵液的花生盆栽对于花生白绢病的防治效果。故在花生植株培育的过程中,本技术提供的bacillus velezensis dpt
‑
03菌悬液能够有效提高中期内对于花生白绢病的防治效果。
[0199]
通过对比花生盆栽接种花生白绢病病原菌60d时实施例3、实施例4、对比例1、对比例2的结果可知,此时,接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果达到了62.50%,接种bacillus velezensis dpt
‑
03无菌发酵液的花生盆栽对于花生白绢病的防治效果达到了30.36%;接种处理药剂的花生盆栽对于花生白绢病的防治效果达到了57.14%。由上述结果可知,当花生盆栽接种花生白绢病病原菌60d时,接种bacillus velezensis dpt
‑
03无菌发酵液、处理药剂的花生盆栽对于花生白绢病的防治效果较接种花生白绢病病原菌40d的防治效果均有所下降,尤其是接种bacillus velezensis dpt
‑
03无菌发酵液的花生盆栽对于花生白绢病的防治效果下降趋势更为明显;而接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果较接种花生白绢病病原菌40d的防治效果有一定的上升趋势,且此时接种bacillus velezensis dpt
‑
03菌悬液的花生盆栽对于花生白绢病的防治效果不仅优于接种bacillus velezensis dpt
‑
03无菌发酵液的花生盆栽对于花生白绢病的防治效果,而且也优于接种处理药剂的花生盆栽对于花生白绢病的防治效果。因此,说明在花生植株培育的过程中,bacillus velezensis dpt
‑
03菌悬液中的菌体能够在盆栽土壤中稳定繁殖,并不断产生具有抑制花生白绢病病原菌的活性物质,从而具有持续防控花生白绢病病原菌的作用,并能够有效降低花生白绢病的发病率及病情指数。
[0200]
实施例5
[0201]
本实施例提供了bacillus velezensis dpt
‑
03菌悬液用于试验田的案例。利用的bacillus velezensis dpt
‑
03菌悬液为实施例1制备的bacillus velezensis dpt
‑
03菌悬液。
[0202]
试验田地址:河南正阳县张楼村。
[0203]
试验田基本情况:该试验田为多年花生连作田,地块平整,花生白绢病严重。
[0204]
试验田肥力:试验田0~20cm土壤肥力状况为:有机质11.60g/kg、碱解氮154.39mg/kg、速效磷(p2o5)56.62mg/kg、速效钾(k2o)168.0mg/kg。
[0205]
bacillus velezensis dpt
‑
03菌悬液用于试验田的方法如下:
[0206]
(1)利用农用喷雾器一次性将bacillus velezensis dpt
‑
03菌悬液以10l/亩的浓度喷入土壤,bacillus velezensis dpt
‑
03菌悬液的浓度为1
×
109cfu/ml,然后对试验田进行翻地;
[0207]
(2)翻地后在试验田内播种花生。
[0208]
对比例3
[0209]
本对比例提供了处理药剂用于试验田的案例。
[0210]
本对比例与实施例5的不同之处在于利用处理药剂代替实施例5中的bacillus velezensis dpt
‑
03菌悬液。处理药剂为噻呋酰胺农药。其中,噻呋酰胺农药为240g/l噻呋
酰胺悬浮剂,亩用量为100ml,稀释100倍使用。
[0211]
对比例4
[0212]
本对比例提供了无菌水用于试验田的案例。
[0213]
本对比例与实施例5的不同之处在于利用无菌水代替实施例5中的bacillus velezensis dpt
‑
03菌悬液。
[0214]
检测试验四
[0215]
以实施例5、对比例3、对比例4提供的案例为检测对象。检测各案例中花生白绢病病原菌的田间防治效果。
[0216]
一、检测方法
[0217]
在试验田随机取组排列,每个案例选取3个小组,每个小组面积为180m2,统计各案例的发病率、病情指数和防治效果。
[0218]
二、计算方法
[0219]
发病率、病情指数和防治效果的计算公式与“检测试验三”中相应的公式相同。
[0220]
三、检测结果
[0221]
检测结果如表4所示。
[0222]
表4检测试验四的检测结果
[0223]
检测对象调查株数(株)发病株数(株)发病率(%)病情指数防治效果(%)实施例530033b11.00b17.89b63.61对比例330037b12.33b18.58b62.21对比例430080a26.67a49.16a
‑
[0224]
如表4所示的检测结果,通过对比例4的检测结果,接种无菌水的试验田中花生植株的发病率为26.67%,而通过实施例5、对比例3的检测结果,可知接种bacillus velezensis dpt
‑
03菌悬液、处理药剂的试验田中,花生植株的发病率分别为11.00%、12.33%,防治效果分别为63.61%、62.21%。由上述结果可知,bacillus velezensis dpt
‑
03菌悬液能够减少试验田中花生白绢病的发病率和病情指数,提高试验田中花生白绢病的防治效果。同时,不仅利用bacillus velezensis dpt
‑
03菌悬液对于试验田中花生白绢病的当季防治效果高于利用处理药剂对于试验田中花生白绢病的防治效果,而且对于生物防治的持续性和安全性而言,利用bacillus velezensis dpt
‑
03菌悬液进行试验田中花生白绢病的防治具有更大的应用潜力和安全性。
[0225]
实施例6
[0226]
本实施例提供了一种包括bacillus velezensis dpt
‑
03的固体微生物菌剂。
[0227]
该固体微生物菌剂的制备方法如下:
[0228]
(1)将bacillus velezensis dpt
‑
03菌悬液浓缩:通过预先配置的离心机对bacillus velezensis dpt
‑
03菌悬液进行高速离心处理,收集菌泥,其中,所述离心机的转速为4000rpm,所述离心处理的时间为5min,菌泥有效活菌数≥100
×
109cfu/g;
[0229]
(2)bacillus velezensis dpt
‑
03菌粉的制备:将步骤(1)收集到的菌泥与预先配置的腐殖酸粉,按1:10的质量比混合吸附,吸附后于30℃干燥8h,粉碎,过100目筛,制成bacillus velezensis dpt
‑
03菌粉,有效活菌数≥10
×
109cfu/g;
[0230]
(3)利用步骤(2)获得的bacillus velezensis dpt
‑
03菌粉对腐殖酸母粒进行外
包膜,制得的固体微生物菌剂。其中,固体微生物菌剂中有效bacillus velezensis dpt
‑
03活菌数为1
×
109cfu/g。
[0231]
实施例7
[0232]
本实施例提供了一种微生物肥料。
[0233]
该微生物肥料包括以下重量份的组分:实施例6提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂40kg,以及市售的复合肥50kg。该微生物肥料的制备方法如下:按照上述加入量将包括bacillus velezensis dpt
‑
03的固体微生物菌剂和市售的复合肥混匀,备用。
[0234]
实施例8
[0235]
本实施例提供了将实施例7制备的的微生物肥料用于试验田的案例。
[0236]
试验田地址:山东菏泽市安德村。
[0237]
试验田基本情况:该试验田为多年花生连作田,花生死颗情况严重,白绢病严重。
[0238]
试验田肥力:试验田0~20cm土壤肥力状况为:有机质13.49g/kg、碱解氮106.08mg/kg、速效磷(p2o5)63.41mg/kg、速效钾(k2o)239.0mg/kg。
[0239]
利用随机播种施肥一体机将上述制备的微生物肥料施肥于试验田。
[0240]
对比例5
[0241]
本对比例提供了一种微生物肥料用于试验田的案例。
[0242]
该案件与实施例8的不同之处在于所利用的微生物肥料不同。
[0243]
该微生物肥料与实施例7的不同之处在于利用市售微生物菌剂ⅰ代替包括bacillus velezensis dpt
‑
03的固体微生物菌剂。
[0244]
对比例6
[0245]
本对比例提供了一种复合肥用于试验田的案例。
[0246]
该案例与实施例8的不同之处在于利用的复合肥50kg代替实施例8中的微生物肥料。
[0247]
检测试验五
[0248]
以实施例8、对比例5、对比例6提供的案例为检测对象。检测各案例中花生白绢病病原菌的田间防治效果。
[0249]
一、检测方法
[0250]
在试验田随机取组排列,每个案例选取3个小组,每个小组面积为90m2。在花生收获前20d统计发病率、病情指数和防治效果。后期管理相同,成熟期进行计产。
[0251]
二、计算方法
[0252]
发病率、病情指数和防治效果的计算公式与“检测试验三”中相应的公式相同。
[0253]
三、检测结果
[0254]
检测结果如表5和图8所示。
[0255]
图8为微生物肥料对于花生白绢病的田间防治效果(图中,处理1
‑
处理3分别对应实施例8、对比例5、对比例6)。
[0256]
表5检测试验五的检测结果
[0257][0258]
如表5所示的检测结果,结合图8,通过对比例6的检测结果,仅施用复合肥的试验田中花生植株的死棵率为26.67%、发病率为32.33%,而通过实施例8、对比例5的检测结果,可知施用实施例7提供的微生物肥料、市售微生物肥料的试验田中,花生植株的死棵率分别为9.33%、17.67%,发病率分别为10.33%、23.67%,防治效果分别为55.62%、42.37%。由上述结果可知,本技术提供的微生物肥料能够有效降低花生植株的死棵率和发病率,且本技术提供的微生物肥料的死棵率和发病率均低于对比例5利用的微生物肥料的死棵率和发病率。说明本技术提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂对花生白绢病的防治效果要优于市售微生物菌剂ⅰ对花生白绢病的防治效果。
[0259]
另外,实施例8施用实施例7提供的微生物肥料的试验田中花生亩产量达到306.22kg/亩,明显高于对比例5施用市售微生物肥料的试验田中花生亩产量287.16kg/亩、以及对比例6仅施用复合肥的试验田中花生亩产量263.27kg/亩。说明利用本技术提供的微生物肥料在降低花生植株的死棵率和发病率的同时,还能够有效提高试验田中的花生亩产量。
[0260]
实施例9
[0261]
本实施例提供了一种微生物肥料。
[0262]
该微生物肥料包括以下重量份的组分:实施例6提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂40kg,以及市售的复合肥60kg。该微生物肥料的制备方法如下:按照上述加入量将包括bacillus velezensis dpt
‑
03的固体微生物菌剂和市售的复合肥混匀,备用。
[0263]
实施例10
[0264]
本实施例提供了将实施例9制备的的微生物肥料用于试验田的案例。
[0265]
试验田地址:河南确山县张楼村。
[0266]
试验田基本情况:该试验田为多年花生连作田,花生白绢病严重。
[0267]
试验田肥力:试验田0~20cm土壤肥力状况为:有机质17.18g/kg、碱解氮138.18mg/kg、速效磷(p2o5)75.26mg/kg、速效钾(k2o)218.0mg/kg。
[0268]
利用随机播种施肥一体机将上述制备的微生物肥料施肥于试验田。
[0269]
对比例7
[0270]
本对比例提供了一种微生物肥料用于试验田的案例。
[0271]
该案件与实施例10的不同之处在于所利用的微生物肥料不同。
[0272]
该微生物肥料与实施例9的不同之处在于利用市售微生物菌剂ⅱ代替包括bacillus velezensis dpt
‑
03的固体微生物菌剂。
[0273]
对比例8
[0274]
本对比例提供了一种微生物肥料用于试验田的案例。
[0275]
该案件与实施例10的不同之处在于所利用的微生物肥料不同。
[0276]
该微生物肥料与实施例9的不同之处在于利用市售微生物菌剂ⅲ代替包括bacillus velezensis dpt
‑
03的固体微生物菌剂。
[0277]
对比例9
[0278]
本对比例提供了一种复合肥用于试验田的案例。
[0279]
该案例与实施例10的不同之处在于利用的复合肥60kg代替实施例10中的微生物肥料。
[0280]
检测试验六
[0281]
以实施例10、对比例7、对比例8、对比例9提供的案例为检测对象。检测各案例中花生白绢病病原菌的田间防治效果。
[0282]
一、检测方法
[0283]
在试验田随机取组排列,每个案例选取3个小组,每个小组面积为60m2。在花生收获前20d统计发病率、病情指数和防治效果。后期管理相同,成熟期进行计产。
[0284]
二、计算方法
[0285]
发病率、病情指数和防治效果的计算公式与“检测试验三”中相应的公式相同。
[0286]
三、检测结果
[0287]
检测结果如表6和图9所示。
[0288]
图9为微生物肥料对于花生白绢病的田间防治效果(图中,处理1
‑
处理4分别对应实施例10、对比例7、对比例8、对比例9)。
[0289]
表6检测试验六的检测结果
[0290][0291]
如表6所示的检测结果,结合图9,通过对比例9的检测结果,仅施用复合肥的试验田中花生植株的死棵率为16.00%、发病率为23.00%,而通过实施例10、对比例7、对比例8的检测结果,可知施用实施例9提供的微生物肥料、市售微生物菌剂ⅱ、市售微生物菌剂ⅲ的试验田中,花生植株的死棵率分别为6.66%、11.00%、12.33%,发病率分别为9.00%、14.00%、14.33%,防治效果分别为60.64%、47.09%、44.37%。由上述结果可知,本技术提供的微生物肥料能够有效降低花生植株的死棵率和发病率,且本技术提供的微生物肥料的死棵率和发病率均低于对比例6、对比例7利用的微生物肥料的死棵率和发病率。说明本技术提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂对花生白绢病的防治效果要优于市售微生物菌剂ⅱ市售微生物菌剂ⅲ对花生白绢病的防治效果。
[0292]
另外,实施例10施用实施例9提供的微生物肥料的试验田中花生亩产量达到349.32kg/亩,明显高于对比例7施用市售微生物肥料的试验田中花生亩产量323.24kg/亩、对比例8施用市售微生物肥料的试验田中花生亩产量316.86kg/亩、以及对比例6仅施用复合肥的试验田中花生亩产量301.25kg/亩。且从图9中所示的花生籽粒可以看出,实施例10施用实施例9提供的微生物肥料的试验田中花生籽粒的饱满度明显高于对比例7、对比例8、对比例9对应的试验田中花生籽粒的饱满度,进一步说明利用本技术提供的微生物肥料在降低花生植株的死棵率和发病率的同时,还能够有效提高试验田中的花生亩产量。
[0293]
本技术提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂具有明显的降低花生白绢病发病率和发病程度的功效,同时还能够有效降低花生植株的死棵率。另外,本技术提供的包括bacillus velezensis dpt
‑
03的固体微生物菌剂还能够增强花生植株的抗病、抗逆能力,同时改良田间土壤的品质,并增加花生植株的产量。因此,本技术提供的微生物菌剂高效、专一、稳定,对于典型发病地区花生白绢病的防治更有一定的应用优势,且更有利于花生的健康种植和产量收益。
[0294]
本具体实施例仅仅是对本技术的解释,其并不是对本技术的限制,本领域技术人员在阅读完本说明书后可以根据需要对本实施例做出没有创造性贡献的修改,但只要在本技术的权利要求范围内都受到专利法的保护。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1