基于醌氧化还原酶的茶叶提取物EGCG前药及其制备方法和应用与流程
基于醌氧化还原酶的茶叶提取物egcg前药及其制备方法和应用
技术领域
1.本发明涉及分子生物学技术领域,具体涉及基于醌氧化还原酶的茶叶提取物egcg前药及其制备方法和应用。
背景技术:
2.茶,是我国的传统饮品。究其根源可以追溯到神话时期的“神农尝百草,日遇七十二毒,得荼(茶)而解之。”,由此可见,中国的饮茶文化历史悠久,源远流长。近年来,在对茶叶的广泛研究中发现,茶叶中具有广谱疾病预防作用的有效成分主要是茶叶中的多酚类物质,儿茶素作为肿瘤多药耐药性的逆转剂,在癌细胞的化疗敏感性及减轻对心脏的毒性方面有很好的疗效。因此,对于茶叶的活性物质的深入研究在抗癌药物的开发中具有深远的意义。
3.儿茶素(catechin),又称茶单宁、儿茶酸。儿茶素是茶叶中黄烷醇类物质的总称,占茶多酚含量的60%-80%。最早儿茶素是由中药材儿茶中提取出来的,在绿茶中含量较为丰富。儿茶素是茶叶中主要活性物质,具有抗氧化、抗肿瘤、预防心血管疾病等作用。目前已从茶叶中分离纯化鉴定出多种儿茶素单体。例如,茶黄素双没食子酸酯可通过诱导no合成酶(inos)的合成降低,抑制内源性致癌物质的形成进而抑制肿瘤形成和发展。茶色素对t淋巴细胞的转化、自然杀伤细胞的活性有显著地增强作用,还可有效抑制由黄曲霉素、苯并芘等致癌物导致的细胞突变、基因与染色体的突变及由放射线诱导的细胞癌变。
4.茶多酚被证实其在抗癌、抗氧化、抗突变、抗辐射、抗自由基及在防治动脉粥样硬化等方面具有良好的效果。研究发现,导致人体多病变体系发生的主要原因是由于机体产生过量的自由基,这些自由基在生物机体内的过量积累对机体生物活性分子进行攻击导致的。儿茶素作为一类高效的自由基清除剂,在许多研究中已证实其在清除包括超氧阴离子自由基、羟基自由基及单线态氧等自由基方面有很好的清除效果。同时,茶多酚作为一种重要的天然抗氧化剂,可以有效地防止食品因氧化而导致的酸败变质,如茶多酚在食用油中的添加可以阻止或延缓油脂的酸化,同时,在防止食品由于氧化而导致的营养物质损失上也有很好的效果。
5.癌症是严重威胁人类健康的恶性疾病,发病率逐年上升,肿瘤转移前的早期发现对提高患者生存率非常重要,基于肿瘤早发现早治疗的原则,寻找恶性肿瘤有效的检测方法迫在眉睫。小分子荧光探针是当今检测肿瘤的主要手段之一,醌氧化还原酶1(nqo1)是一种癌症特异性胞浆黄素酶,在许多癌细胞中的含量过度升高,特别是在非小细胞肺癌中,其结构性过表达量是相关正常组织的100倍以上。nqo1可以直接催化多种底物的两电子还原反应,包括通过fadher(h-)介导的从辅因子nad(p)h到醌类底物的转移。
6.荧光成像(fli)以其无创检测、高灵敏度、可原位加工和高时间分辨率的固有优势,在生物医学领域的基础研究和实际应用中引起了极大的兴趣。
7.目前,免疫荧光和基于配体的荧光系统是常用的癌症检测工具。在免疫荧光的癌
症检测中,与荧光染料偶联的抗体对高表达的受体具有高度的特异性,实现了对癌细胞的高特异性响应。
技术实现要素:
8.本发明的目的是为了解决现有技术中的问题,而提出的一种毒副作用相对较低、水溶性好的醌氧化还原酶茶叶提取物egcg前药的制备方法及其应用。
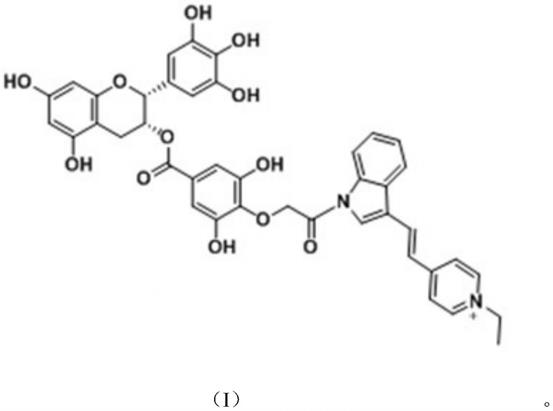
9.为了实现上述目的,本发明采用了如下技术方案:本发明的一种醌氧化还原酶茶叶提取物egcg前药,如式(i)所示:
[0010][0011]
本发明的一种醌氧化还原酶茶叶提取物egcg前药的制备方法,包括如下步骤:
[0012]
化合物1
[0013]
(2-(4-((((2r,3r)-5,7-dihydroxy-2-(3,4,5-trihydroxyphenyl)chroman-3-yl)oxy)carbonyl)-2,6-dihydroxyphenoxy)acetic acid)的合成:将egcg溶解于dmf中,冰浴条件下加入溴乙酸和ki,随后保持温度反应1h;然后升高温度至80℃后反应过夜,tlc检测反应结束;反应结束后,减压浓缩得到相应粗产物,用硅胶柱层析进行色谱纯化,制得化合物1;
[0014]
(2)化合物2(1-ethyl-4-methylpyridin-1-ium)的合成:称取对甲基吡啶溶于适量乙腈中,随后加入碘乙烷,82℃搅拌反应12小时;然后真空下除去溶剂,加入适量乙醚超声震荡,析出固体,抽滤制得化合物2的白色固体;
[0015]
(3)化合物3((e)-4-(2-(1h-indol-3-yl)vinyl)-1-ethylpyridin-1-ium)的合成:称取化合物3溶于适量甲醇中,随后加入3-吲哚甲醛,65℃下搅拌反应5分钟,随后加入
哌啶;然后65℃搅拌反应12小时,反应完成后冷却至室温,加入乙酸乙酯搅拌,析出固体,抽滤制得褐色固体;
[0016]
(4)化合物4(4-((e)-2-(1-(2-(4-((((2r,3r)-5,7-dihydroxy-2-(3,4,5-trihydroxyphenyl)chroman-3-yl)oxy)carbonyl)-2,6-dihydroxyphenoxy)acetyl)-1h-indol-3-yl)vinyl)-1-ethylpyridin-1-ium)的合成:称取化合物1溶于10ml二氯甲烷,随后加入1.5倍当量的dmap,edc.hcl,冰水浴活化1.5小时,然后加入化合物,常温搅拌反应6小时,反应完成后冷却至室温,真空除去溶剂,使用二氯甲烷和甲醇柱层析,制得褐色固体醌氧化还原酶茶叶提取物egcg前药。
[0017]
进一步地,在步骤(1)中,所述的egcg与dmf的摩尔体积比为10mmol:25ml,所述的溴乙酸与ki的摩尔比为15:1。
[0018]
进一步地,在步骤(2)中,所述的对甲基吡啶与碘乙烷的摩尔比为1:1。
[0019]
进一步地,在步骤(3)中,所述的化合物3与3-吲哚甲醛的摩尔比为1:1;所述的哌啶与乙酸乙酯的体积比为1ul:2ml。
[0020]
进一步地,在步骤(4)中,中,所述的化合物1、dmap、edc.hcl和化合物3为质量比为103:25:38:50,所述的二氯甲烷和甲醇的体积比为20:1。
[0021]
进一步地,在步骤(1)中,所述的egcg为10mmol,dmf为25ml;所述的溴乙酸为201mg,15mmol,ki为1mmol;在步骤(2)中,所述的对甲基吡啶为500mg,碘乙烷为850mg;在步骤(3)中,所述的化合物3为290mg;所述的3-吲哚甲醛为245mg,所述的哌啶为200μl,所述的乙酸乙酯为400ml;所述的化合物2的白色固体为540mg;在步骤(4)中,所述的化合物1为412mg,所述的dmap为100mg,edc.hcl为152mg,化合物3为200mg。
[0022]
本发明所述的醌氧化还原酶茶叶提取物egcg前药在制备检测肿瘤内环境中过表达的醌氧化还原酶nqo1的药物中的应用。
[0023]
进一步地,所述的egcg前药具有对醌氧化还原酶响应的作用。
[0024]
本发明所述的醌氧化还原酶茶叶提取物egcg前药在制备抗肿瘤活性的药物中的应用。
[0025]
有益效果:本发明采用由茶叶中提取的egcg进行位点修饰,得到对nqo1特异性响应的egcg前药。该前药表现出显著的原位检测性质以及抗肿瘤活性,同时,由于该egcg是由茶叶中提取而来,其毒副作用相对较低,并且水溶性更好,更加有利于人体组织的吸收及代谢。
[0026]
与现有技术相比,本发明具备以下优点:
[0027]
(1)本发明的原料来源丰富,由茶叶中提取而来。本发明具有诊疗一体化的作用。
[0028]
(2)本发明的毒副作用较低,水溶性更好,生物相容性更好。
附图说明
[0029]
图1为本发明的ph干扰性测试的示意图;
[0030]
图2为本发明的紫外吸收光谱示意图;
[0031]
图3为本发明的共聚焦荧光成像的示意图。
具体实施方式
[0032]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。
[0033]
实施例1
[0034]
本发明的一种醌氧化还原酶茶叶提取物egcg前药,如式(i)所示:
[0035][0036]
本发明的一种醌氧化还原酶茶叶提取物egcg前药的制备方法,包括如下步骤:
[0037]
areagentsand conditions:(a)
[0038]
2-bromoacetic acid,ki,rt,24h;(b)iodoethane,acetonitrile,82℃;(c)indole-3-carboxaldehyde,ch3oh,65℃;(d)compound 1,dmap,edc.hcl,rt.
[0039]
(1)化合物1(2-(4-((((2r,3r)-5,7-dihydroxy-2-(3,4,5-trihydroxyphenyl)chroman-3-yl)oxy)carbonyl)-2,6-dihydroxyphenoxy)acetic acid)的合成:将egcg溶解于dmf中,冰浴条件下加入溴乙酸和ki,随后保持温度反应1h;然后升高温度至80℃后反应过夜,tlc检测反应结束;反应结束后,减压浓缩得到相应粗产物,用硅胶柱层析进行色谱纯化,制得化合物1,产率为36.2%。由于中间酚羟基的位点较为活泼,选择性较大,故只在中间酚羟基上反应;所述的egcg与dmf的摩尔体积比为10mmol:25ml;所述的溴乙酸与ki的摩尔比为15:1。
[0040]
(2)化合物2(1-ethyl-4-methylpyridin-1-ium)的合成:称取对甲基吡啶溶于适量乙腈中,随后加入碘乙烷,82℃搅拌反应12小时;然后真空下除去溶剂,加入适量乙醚超声震荡,析出固体,抽滤制得化合物2的白色固体;所述的对甲基吡啶与碘乙烷的摩尔比为
1:1。
[0041]
(3)化合物3((e)-4-(2-(1h-indol-3-yl)vinyl)-1-ethylpyridin-1-ium)的合成:称取化合物3溶于适量甲醇中,随后加入3-吲哚甲醛,65℃下搅拌反应5分钟,随后加入哌啶;然后65℃搅拌反应12小时,反应完成后冷却至室温,加入乙酸乙酯搅拌,析出固体,抽滤制得褐色固体;所述的化合物3与3-吲哚甲醛的摩尔比为1:1;所述的哌啶与乙酸乙酯的体积比为1ul:2ml;
[0042]
(4)化合物4(4-((e)-2-(1-(2-(4-((((2r,3r)-5,7-dihydroxy-2-(3,4,5-trihydroxyphenyl)chroman-3-yl)oxy)carbonyl)-2,6-dihydroxyphenoxy)acetyl)-1h-indol-3-yl)vinyl)-1-ethylpyridin-1-ium)的合成:称取化合物1溶于10ml二氯甲烷,随后加入1.5倍当量的dmap,edc.hcl,冰水浴活化1.5小时,然后加入化合物,常温搅拌反应6小时,反应完成后冷却至室温,真空除去溶剂,使用二氯甲烷和甲醇柱层析,制得褐色固体醌氧化还原酶茶叶提取物egcg前药。所述的化合物1、dmap、edc.hcl和化合物3为质量比为103:25:38:50,所述的二氯甲烷和甲醇的体积比为20:1。
[0043]
实施例4
[0044]
本发明的一种醌氧化还原酶茶叶提取物egcg前药的制备方法,包括如下步骤:
[0045]
在步骤(1)中,化合物1的合成:egcg(10mmol)溶解于dmf(25ml)中,冰浴条件下加入溴乙酸(201mg,15mmol),ki(1mmol),随后保持温度反应1h。然后升高温度至80℃后反应过夜,tlc检测反应结束。反应结束后,减压浓缩得到相应粗产物,用硅胶柱层析进行色谱纯化,即得化合物1,产率为36.2%。(由于中间酚羟基的位点较为活泼,选择性较大,故只在中间酚羟基上反应)
[0046]
在步骤(2)中,化合物2的合成:
[0047]
称取对甲基吡啶(500mg,5.4mmol)溶于适量乙腈中,随后加入碘乙烷(850mg,5.4mmol),82℃搅拌反应12小时。然后真空下除去溶剂,加入适量乙醚超声震荡,析出固体,抽滤得白色固体(540mg,89%)。
[0048]
在步骤(3)中,化合物3的合成:
[0049]
称取化合物3(290mg,2mmol)溶于适量甲醇中,随后加入3-吲哚甲醛(245mg,2mmol),65℃下搅拌反应5分钟,随后加入哌啶(200μl)。然后65℃搅拌反应12小时,反应完成后冷却至室温,加入乙酸乙酯(400ml)搅拌,析出固体,抽滤得褐色固体(600mg,80%)。
[0050]
在步骤(4)中,化合物4的合成:
[0051]
称取化合物1(412mg,0.8mmol)溶于适量二氯甲烷,随后加入1.5倍当量的dmap(100mg),edc.hcl(152mg),冰水浴活化1.5小时。然后加入化合物3(200mg,0.8mmol),常温搅拌反应6小时。反应完成后冷却至室温,真空除去溶剂,二氯甲烷:甲醇=20:1柱层析,得褐色固体(165mg,43%)。
[0052]1h nmr(600mhz,dmso-d6)δ8.97(s,2h),8.57(s,4h),8.29(s,6h),8.24(s,3h),8.21(s,2h),7.65(s,1h),7.43(s,2h),4.53(s,2h),3.83(s,2h),2.15(s,3h),1.93(s,3h),1.78(s,2h),1.53(s,3h);
13
c nmr(151mhz,dmso-d6)δ168,165,158,152.54,146.26,143.38,137.43,137.01,135.15,136,131.89,128.39,125.35,123.76,122.67,122.23,119.85,117.71,111.65,110.36,115.60,54.56,48.20,36.85,21.66,15.58;
[0053]
试验例1
[0054]
技术方案:nqo1小分子荧光探针的合成与表征:
[0055]
areagents and conditions:(a)2-bromoacetic acid,ki,rt,24h;(b)iodoethane,acetonitrile,82℃;(c)indole-3-carboxaldehyde,ch3oh,65℃;(d)compound 1,dmap,edc.hcl,rt.
[0056]
生物活性初步评价
[0057]
ph干扰性测试:如图1所示,该egcg前药(1mm)以及荧光团在ph=2-10的范围内,荧光强度并未发生显著的变化,表明该egcg前药不受ph变化的干扰,依旧能够保留其在溶液中的稳定性,从而证明该前药具有良好的稳定性及生物相容性。
[0058]
紫外吸收光谱:如图2所示,在加入nqo1后,该egcg前药的紫外吸收出现显著的增强以及红移,说明nqo1与egcg显著发生反应,表明该egcg前药具有明显的响应性,说明该探针具有对nqo1特异性响应的能力。共聚焦荧光成像:egcg前药(50um)在a549细胞中孵育24h的共聚焦荧光成像。
[0059]
如图3所示,首先可以发现荧光,表明该egcg前药显著的靶向到了癌细胞,靶向性优异,其次表明该egcg前药如设计的那样,在肿瘤部位发生反应,释放出aie荧光团。达到了对nqo1特异性响应的目的。从而达到诊断及治疗一体化的作用。该egcg前药生物活性的初步评价均表明该前药具有对醌氧化还原酶响应的作用,可以应用于nqo1过表达的癌细胞的原位检测及治疗。
[0060]
以上详细描述了本发明的优选实施方式及生物活性评价,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种等同变换,这些等同变换均属于本发明的保护范围。另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合。为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1