一种细菌抗病毒分子甄别用试剂盒制备方法与流程
1.本发明涉及细菌抗病毒分子甄别技术领域,具体为一种细菌抗病毒分子甄别用试剂盒制备方法。
背景技术:
2.病毒是由一个核酸分子与蛋白质构成的非细胞形态,靠寄生生活的介于生命体及非生命体之间的有机物种。病毒可以感染几乎所有具有细胞结构的生命体。依非韦仑是一种hiv
‑
1病毒逆转录酶的非竞争性抑制剂,它是一种非核苷类药物,主要与其他抗病毒药物联用,适用于hiv
‑
1病毒感染的人群,它被认为是一种最具兼容性的一线抗结核药物。
3.细菌的抗病毒分子甄别过程中目前的方式都是经过多次的取样单一进行培养并且进行实验对比,这样的操作对比方式比较繁琐,效率较低,并且实验对比性不够直观。
技术实现要素:
4.本发明的目的在于提供一种细菌抗病毒分子甄别用试剂盒制备方法,解决了背景技术中所提出细菌的抗病毒分子甄别过程中目前的方式都是经过多次的取样单一进行培养并且进行实验对比,这样的操作对比方式比较繁琐,效率较低,并且实验对比性不够直观的问题。
5.为实现上述目的,本发明提供如下技术方案:一种细菌抗病毒分子甄别用试剂盒制备方法,包括以下步骤:
6.s1:准备两组相同的病毒感染细胞,并且向病毒感染细胞中加入荧光蛋白基因进行充分培养混合;
7.s2:采集两组细菌,为细菌a和细菌b,进行培养备用;
8.s3:将步骤1中带有荧光蛋白基因的病毒感染细胞移放到试剂盒中,并且进行培养保护待用;
9.s4:将细菌a或细菌b其中的一组进行分离细胞、裂解细胞和分离细胞壁,另一组直接移放在步骤3中的其中一个试剂盒中,进行培养观察;
10.s5:将进行分离细胞壁后的细菌分子移放在步骤3中的另外一个试剂盒中,进行培养吞噬观察;
11.s6:进行对比步骤4和步骤5中的细菌a和细菌b中荧光分布数量。
12.作为本发明的一种优选实施方式,所述步骤4中,分离细胞的步骤为将细胞移至离心瓶内,在950
‑
1050转/分的速度下离心分离。
13.作为本发明的一种优选实施方式,所述步骤4中裂解细胞的步骤为将离心后的细菌细胞移至收集瓶内,并且加入重量加入细胞裂解液,裂解细胞得细菌细胞溶解物。
14.作为本发明的一种优选实施方式,所述细胞裂解液的配制为向纯化水中加入0.1mol/ml的tris
‑
hcl溶液,调ph值为中性。
15.作为本发明的一种优选实施方式,所述步骤4中分离细胞壁的方式为:
16.向细胞裂解后的细菌细胞溶解物中加入氯仿,并加入适量聚乙二醇8000,进行离心,分离细胞壁厚的提取物。
17.作为本发明的一种优选实施方式,所述聚乙二醇8000在所述混合溶液中的浓度为3.5mg/ml。
18.作为本发明的一种优选实施方式,所述步骤4和步骤5中的病原体的将病毒与液体待检测材料在试管中直接孵育40min左右。
19.与现有技术相比,本发明的有益效果如下:
20.本发明设置经过离心分离细胞壁的细菌以及没有经过处理的细菌进行试剂盒处理,如果没有经过离心分离细胞壁后的细菌中检测出的荧光数量较少,经历过分离细胞壁后的细菌分子在试剂盒中被检测出荧光数量较多时,说明细菌的细胞壁具有良好的抗病毒作用,并且整个检测筛选机构仅仅需要采用两组试剂盒就可以在同一个试剂盒检测机构中一次性检测出来,效率较高。
具体实施方式
21.为使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施方式,进一步阐述本发明。
22.实施例一:
23.本发明提供一种技术方案:一种细菌抗病毒分子甄别用试剂盒制备方法,包括以下步骤:
24.s1:准备两组相同的病毒感染细胞,并且向病毒感染细胞中加入荧光蛋白基因进行充分培养混合;
25.s2:采集两组细菌,为细菌a和细菌b,进行培养备用;
26.s3:将步骤1中带有荧光蛋白基因的病毒感染细胞移放到试剂盒中,并且进行培养保护待用;
27.s4:将细菌a或细菌b其中的一组进行分离细胞、裂解细胞和分离细胞壁,另一组直接移放在步骤3中的其中一个试剂盒中,进行培养观察;
28.s5:将进行分离细胞壁后的细菌分子移放在步骤3中的另外一个试剂盒中,进行培养吞噬观察;
29.s6:进行对比步骤4和步骤5中的细菌a和细菌b中荧光分布数量。
30.本实施例中,所述步骤4中,分离细胞的步骤为将细胞移至离心瓶内,在950
‑
1050转/分的速度下离心分离。
31.在具体实施方式中,所述步骤4中裂解细胞的步骤为将离心后的细菌细胞移至收集瓶内,并且加入重量加入细胞裂解液,裂解细胞得细菌细胞溶解物。
32.进一步的,所述细胞裂解液的配制为向纯化水中加入0.1mol/ml的tris
‑
hcl溶液,调ph值为中性。
33.更进一步的,所述步骤4中分离细胞壁的方式为:
34.向细胞裂解后的细菌细胞溶解物中加入氯仿,并加入适量聚乙二醇8000,进行离心,分离细胞壁厚的提取物。
35.更进一步的,所述聚乙二醇8000在所述混合溶液中的浓度为3.5mg/ml,所述步骤4
和步骤5中的病原体的将病毒与液体待检测材料在试管中直接孵育40min左右,保证充分的融合效果。
36.实施例二:
37.本发明提供一种与实施例一不同的技术方案:一种细菌抗病毒分子甄别用试剂盒制备方法,包括以下步骤:
38.s1:准备两组相同的病毒感染细胞,并且向病毒感染细胞中加入荧光蛋白基因进行充分培养混合;
39.s2:采集两组细菌,为细菌a和细菌b,进行培养备用;
40.s3:将步骤1中带有荧光蛋白基因的病毒感染细胞移放到试剂盒中,并且进行培养保护待用;
41.s4:将细菌a或细菌b直接移放在步骤3中的其中一个试剂盒中,进行培养观察;
42.s5:进行对比步骤3和步骤4中的细菌a和细菌b中荧光分布数量。
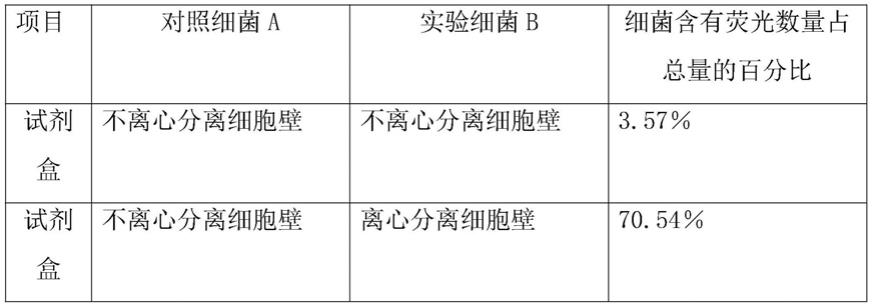
43.经历过分离细胞壁后的细菌分子在试剂盒中被检测出荧光数量实验数据表如下:
[0044][0045]
由上表可以知道如果没有经过离心分离细胞壁后的细菌中检测出的荧光数量较少,经历过分离细胞壁后的细菌分子在试剂盒中被检测出荧光数量较多时,说明细菌的细胞壁具有良好的抗病毒作用,并且整个检测筛选机构仅仅需要采用两组试剂盒就可以在同一个试剂盒检测机构中一次性检测出来,效率较高。
[0046]
需要说明的是,本发明为一种细菌抗病毒分子甄别用试剂盒制备方法,各个件均为通用标准件或本领域技术人员知晓的部件,其结构和原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知。
[0047]
工作原理:步骤1:准备两组相同的病毒感染细胞,并且向病毒感染细胞中加入荧光蛋白基因进行充分培养混合;采集两组细菌,为细菌a和细菌b,进行培养备用;步骤2:将上述步骤中带有荧光蛋白基因的病毒感染细胞移放到试剂盒中,并且进行培养保护待用;将细菌a或细菌b其中的一组进行分离细胞、裂解细胞和分离细胞壁,另一组直接移放在步骤3中的其中一个试剂盒中,进行培养观察;将进行分离细胞壁后的细菌分子移放在步骤3中的另外一个试剂盒中,进行培养吞噬观察;进行对比步骤4和步骤5中的细菌a和细菌b中荧光分布数量,如果没有经过离心分离细胞壁后的细菌中检测出的荧光数量较少,经历过分离细胞壁后的细菌分子在试剂盒中被检测出荧光数量较多时,说明细菌的细胞壁具有良好的抗病毒作用,并且整个检测筛选机构仅仅需要采用两组试剂盒就可以在同一个试剂盒检测机构中一次性检测出来,效率较高。
[0048]
以上显示和描述了本发明的基本原理和主要特征和本发明的优点,对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
[0049]
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1