靶向PD-1的双特异性抗体、及其制备和应用的制作方法
靶向pd-1的双特异性抗体、及其制备和应用
技术领域
1.本发明涉及生物技术领域。更具体地说,本发明涉及靶向pd-1的双特异性抗体及其制备方法和用途。
背景技术:
2.pd-1(程序性死亡受体1,programmed cell death protein 1,pd-1)及其配体pd-l1是肿瘤免疫的重要靶点。pd-1、pd-l1是一对免疫抑制分子,是免疫系统防止自身免疫过激的重要组成部分,其通路的激活具有抑制肿瘤免疫应答、诱导肿瘤特异性t细胞凋亡的作用,与肿瘤发展关系密切。利用单克隆抗体阻断pd-1、pd-l1通路治疗肿瘤,目前在临床上显示出良好的疗效和安全性,已有多种抗体类药物获批上市,适应症包括黑色素瘤、非小细胞肺癌、晚期肾细胞癌等多种恶性肿瘤,同时很多正在进行的临床试验尝试开发更多新的适应症。
3.pd-1除了在激活的t细胞、nkt细胞、b细胞和活化的单核细胞表面表达外,在耗竭的t细胞表面也会高表达。而其配体pd-l1除了在b细胞、t细胞、树突状细胞等免疫细胞表达外,还在外周微血管内皮细胞、心脏和肺脏等器官表达。而pd-l2只在巨噬细胞和树突状细胞表面表达。值得注意的是,pd-l1的表达已经在人类肿瘤中被广泛发现,包括人肺癌、黑色素瘤、卵巢癌和结肠癌等。在体外和体内试验中,阻断pd-l1/pd-1通路可以显著增加t细胞的增殖,细胞因子分泌和t细胞对肿瘤细胞的杀伤作用。在动物体内,阻断pd-l1/pd-1通路显著阻断肿瘤生长。使用pd-1抗体阻断pd-1/pd-l1信号通路,显著增强肿瘤特异t细胞的扩增和肿瘤浸润。以上结果证明了pd-1/pd-l1阻断抗体在肿瘤治疗中的重要应用价值。
4.目前上市在售的抗体药物多为单克隆抗体。然而,患者接受单克隆抗体治疗可能产生耐药性或无应答,并且单一靶点的免疫疗法并不足以摧毁癌细胞。因此,需要通过组合不同的药物,或是使用多特异性抗体的多重靶向策略来实现。
5.目前,双功能抗体是抗体药物的研发方向之一,但面临诸如临床前评价模型、表达量低、稳定性差、工艺复杂、质控差异性大等问题,因此一直以来双功能抗体的研发困难重重。
6.因此,本领域迫切开发一种特异性佳、疗效好且易于制备的抗肿瘤双特异性抗体。
技术实现要素:
7.本发明的目的就是提供一种靶向pd-1的双特异性抗体。
8.本发明还有一目的是提供所述双特异性抗体的制备方法以及其用途。
9.在第一方面,本发明提供一种双特异性抗体,所述双特异性抗体包括第一抗体和第二抗体,所述第一抗体是靶向pd-1的单域抗体的vhh链、靶向pd-1的抗体的重链可变区、靶向pd-1的单域抗体、人源化的靶向pd-1的单域抗体的vhh链、或靶向pd-1的抗体;和
10.所述第二抗体是靶向其它靶点的抗体;
11.其中所述的靶向pd-1的单域抗体的vhh链或靶向pd-1的抗体的重链可变区包括
seq id no:53所示的cdr1、seq id no:54所示的cdr2和seq id no:55所示的cdr3;
12.所述靶向pd-1的单域抗体具有所述的vhh链;
13.所述人源化的靶向pd-1的单域抗体的vhh链是以所述的vhh链为基础对框架区fr1、fr2、fr3和fr4进行人源化;和
14.所述靶向pd-1的抗体包括一个或多个所述的靶向pd-1的单域抗体的vhh链或所述的人源化的靶向pd-1的单域抗体的vhh链。
15.在优选的实施方式中,所述pd-1为人pd-1。
16.在优选的实施方式中,上述氨基酸序列中任意一种氨基酸序列还包括任选地经过添加、缺失、修饰和/或取代至少一个(如1-3个,较佳地1-2个,更佳地1个)氨基酸并能保留与pd-1高亲和力结合、阻断pd-l1与pd-1结合的衍生序列。
17.在优选的实施方式中,所述vhh链还包括框架区fr1、fr2、fr3和fr4,所述的fr1、fr2、fr3和fr4如seq id no:51所示的氨基酸序列的1-25位、36-49位、67-98位和110-120位所示。
18.在优选的实施方式中,所述靶向pd-1的单域抗体的vhh链的氨基酸序列如seq id no:51所示。
19.在优选的实施方式中,所述靶向pd-1的抗体的重链可变区的氨基酸序列如seq id no:51所示。
20.在优选的实施方式中,所述人源化的靶向pd-1的单域抗体的vhh链的框架区fr1、fr2、fr3和fr4分别如seq id no:51、或seq id no:57、或seq id no:58、或seq id no:59、或seq id no:60、或seq id no:61所示氨基酸序列的1-25位、36-49位、67-98位和110-120位所示。
21.在优选的实施方式中,所述人源化的靶向pd-1的单域抗体的vhh链氨基酸序列分别如seq id no:51、或seq id no:57、或seq id no:58、或seq id no:59、或seq id no:60、或seq id no:61所示。
22.在优选的实施方式中,所述的靶向pd-1的抗体包括单体、二价抗体、和/或多价抗体。
23.在优选的实施方式中,所述其它靶点是除pd-1以外的免疫检查点相关靶点或非免疫检查点相关靶点。
24.在优选的实施方式中,所述的免疫检查点相关靶点是ctla-4、lag-3、pd-l1、tigit、btla、tim-3、vista、cd47/sirp-alpha、cd73、ox40、icos、4-1bb或cd28等;非免疫检查点相关靶点是egfr、her2、claudin18.2、vegf、vegfr、tgf-beta、psck-9、il-1b、il-8等。
25.在优选的实施方式中,所述靶向其它靶点的抗体包括靶向il-8、vegf、ctla-4、tgf-β和psck-9的抗体。
26.在优选的实施方式中,所述的双特异性抗体包括1-3个抗pd-1单域抗体;较佳地,包括1或2个抗pd-1单域抗体。
27.在优选的实施方式中,所述的pd-1单域抗体可以阻断pd-1和pd-l1的相互作用。
28.在优选的实施方式中,所述的第二抗体是双链抗体。
29.在优选的实施方式中,所述的双特异性抗体还包含fc段。
30.在优选的实施方式中,所述双特异性抗体的fc段选自下组:人igg结构域、ch1+cl1
结构域,或其组合。
31.在优选的实施方式中,所述人igg结构域是经改造的突变型igg结构域,优选地为lala突变型的igg结构域。
32.在优选的实施方式中,所述第一抗体连接于所述第二抗体重链ch1和铰链区之间;或者所述第一抗体连接于所述第二抗体重链n端;或者所述第一抗体连接于所述第二抗体重链c端;或者所述第一抗体直接与所述第二抗体重链铰链区连接。
33.在优选的实施方式中,所述第一抗体连接于所述第二抗体重链n端。
34.在优选的实施方式中,先将所述第一抗体串联,例如2-4个或2-3个第一抗体串联后,再与所述第二抗体连接。
35.在优选的实施方式中,所述靶向il-8的抗体的重链氨基酸序列如seq id no:1所示,或与seq id no:1所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
36.在优选的实施方式中,所述靶向il-8的抗体的轻链氨基酸序列如seq id no:2所示,或与seq id no:2所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
37.在优选的实施方式中,所述靶向vegf的抗体的重链氨基酸序列如seq id no:3或5所示,或与seq id no:3或5所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
38.在优选的实施方式中,所述靶向vegf的轻链氨基酸序列如seq id no:4或6所示,或与seq id no:4或6所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
39.在优选的实施方式中,所述靶向ctla-4的抗体的重链氨基酸序列如seq id no:7所示,或与seq id no:7所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
40.在优选的实施方式中,所述靶向ctla-4的抗体的轻链氨基酸序列如seq id no:8所示,或与seq id no:8所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
41.在优选的实施方式中,所述靶向tgf-β的抗体的重链氨基酸序列如seq id no:9所示,或与seq id no:9所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
42.在优选的实施方式中,所述靶向tgf-β的抗体的轻链氨基酸序列如seq id no:10所示,或与seq id no:10所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
43.在优选的实施方式中,所述靶向psck-9的抗体的重链氨基酸序列如seq id no:11或13所示,或与seq id no:11或13所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
44.在优选的实施方式中,所述靶向psck-9的抗体的轻链氨基酸序列如seq id no:12或14所示,或与seq id no:12或14所示序列具有≥85%(优选地90%,更优选地95%)的序列同一性。
45.在优选的实施方式中,所述第一抗体通过连接肽与所述第二抗体连接。
46.在优选的实施方式中,所述连接肽是(ggggs)1、(ggggs)2或(ggggs)3。
47.在优选的实施方式中,所述种双特异性抗体是以下抗体:
48.抗体a,重链氨基酸序列如seq id no:15所示,轻链氨基酸序列如seq id no:16所示;
49.抗体b,重链氨基酸序列如seq id no:17所示,轻链氨基酸序列如seq id no:18所示;
50.抗体c,重链氨基酸序列如seq id no:19所示,轻链氨基酸序列如seq id no:20所示;
51.抗体d,重链氨基酸序列如seq id no:21所示,轻链氨基酸序列如seq id no:22所示;
52.抗体e,重链氨基酸序列如seq id no:23所示,轻链氨基酸序列如seq id no:24所示;
53.抗体f,重链氨基酸序列如seq id no:25所示,轻链氨基酸序列如seq id no:26所示;
54.抗体g,重链氨基酸序列如seq id no:27所示,轻链氨基酸序列如seq id no:28所示;
55.抗体h,重链氨基酸序列如seq id no:29所示,轻链氨基酸序列如seq id no:31所示;
56.抗体i,重链氨基酸序列如seq id no:30所示,轻链氨基酸序列如seq id no:31所示;
57.抗体j,重链氨基酸序列如seq id no:32所示,轻链氨基酸序列如seq id no:34所示;
58.抗体k,重链氨基酸序列如seq id no:33所示,轻链氨基酸序列如seq id no:34所示;
59.抗体l,重链氨基酸序列如seq id no:35所示,轻链氨基酸序列如seq id no:36所示;
60.抗体m,重链氨基酸序列如seq id no:37所示,轻链氨基酸序列如seq id no:38所示;
61.抗体n,重链氨基酸序列如seq id no:39所示,轻链氨基酸序列如seq id no:40所示;
62.抗体o,重链氨基酸序列如seq id no:41所示,轻链氨基酸序列如seq id no:42所示;
63.抗体p,重链氨基酸序列如seq id no:43所示,轻链氨基酸序列如seq id no:44所示;
64.抗体q,重链氨基酸序列如seq id no:45所示,轻链氨基酸序列如seq id no:46所示;
65.抗体r,重链氨基酸序列如seq id no:47所示,轻链氨基酸序列如seq id no:48所示;和
66.抗体s,重链氨基酸序列如seq id no:49所示,轻链氨基酸序列如seq id no:50所示。
67.在第二方面,本发明提供一种分离的多核苷酸,所述多核苷酸编码第一方面所述的双特异性抗体。
68.在第三方面,本发明提供一种表达载体,所述表达载体含有第二方面所述的多核苷酸。
69.在优选的实施方式中,所述的表达载体选自下组:dna、rna、病毒载体、质粒、转座
子、其他基因转移系统、或其组合;优选地,所述表达载体包括病毒载体,如慢病毒、腺病毒、aav病毒、逆转录病毒、或其组合。
70.在第四方面,本发明提供一种宿主细胞,所述宿主细胞含有第三方面所述的表达载体,或其基因组中整合有第二方面所述的多核苷酸;
71.或者,所述的宿主细胞表达第一方面所述的双特异性抗体。
72.在优选的实施方式中,所述的宿主细胞包括原核细胞或真核细胞。
73.在优选的实施方式中,所述的宿主细胞选自下组:大肠杆菌、酵母细胞、哺乳动物细胞。
74.在第五方面,本发明提供一种产生第一方面所述的双特异性抗体的方法,包括步骤:
75.(a)在合适的条件下,培养第四方面所述的宿主细胞,从而获得含所述双特异性抗体的培养物;和
76.(b)对步骤(a)中得到的培养物进行纯化和/或分离,获得所述的双特异性抗体。
77.在优选的实施方式中,所述纯化可以通过a蛋白亲和柱纯化分离获得目标抗体。
78.在第六方面,本发明提供一种免疫偶联物,所述免疫偶联物含有:
79.(a)第一方面所述的双特异性抗体;和
80.(b)偶联部分。
81.在优选的实施方式中,所述偶联部分为可检测标记物、药物、毒素、细胞因子、放射性核素、或酶、金纳米颗粒/纳米棒、纳米磁粒、病毒外壳蛋白或vlp、或其组合。
82.在优选的实施方式中,所述的放射性核素包括:
83.(i)诊断用同位素,所述的诊断用同位素选自下组:tc-99m、ga-68、f-18、i-123、i-125、i-131、in-111、ga-67、cu-64、zr-89、c-11、lu-177、re-188、或其组合;和/或
84.(ii)治疗用同位素,所述的治疗用同位素选自下组:lu-177、y-90、ac-225、as-211、bi-212、bi-213、cs-137、cr-51、co-60、dy-165、er-169、fm-255、au-198、ho-166、i-125、i-131、ir-192、fe-59、pb-212、mo-99、pd-103、p-32、k-42、re-186、re-188、sm-153、ra223、ru-106、na24、sr89、tb-149、th-227、xe-133、yb-169、yb-177、或其组合。
85.在另一优选的实施方式中,所述偶联部分为药物或毒素。
86.在另一优选的实施方式中,所述的药物为细胞毒性药物。
87.在另一优选的实施方式中,所述的细胞毒性药物选自:抗微管蛋白药物、dna小沟结合试剂、dna复制抑制剂、烷化试剂、抗生素、叶酸拮抗物、抗代谢药物、化疗增敏剂、拓扑异构酶抑制剂、长春花生物碱、或其组合。例如,dna小沟结合试剂、dna烷基化试剂、和微管蛋白抑制剂、典型的细胞毒性药物包括、例如奥瑞他汀(auristatins)、喜树碱(camptothecins)、多卡霉素/倍癌霉素(duocarmycins)、依托泊甙(etoposides)、美登木素(maytansines)和美登素类化合物(maytansinoids)(例如dm1和dm4)、紫杉烷(taxanes)、苯二氮卓类(benzodiazepines)或者含有苯二氮卓的药物(benzodiazepine containing drugs)(例如吡咯并[1,4]苯二氮卓类(pbds)、吲哚啉苯并二氮卓类(indolinobenzodiazepines)和噁唑烷并苯并二氮卓类(oxazolidinobenzodiazepines))、长春花生物碱(vinca alkaloids)、或其组合。
[0088]
在优选的实施方式中,所述的毒素选自:耳他汀类(例如,耳他汀e、耳他汀f、mmae
和mmaf)、金霉素、类美坦西醇、篦麻毒素、篦麻毒素a-链、考布他汀、多卡米星、多拉司他汀、阿霉素、柔红霉素、紫杉醇、顺铂、cc1065、溴化乙锭、丝裂霉素、依托泊甙、替诺泊甙(tenoposide)、长春新碱、长春碱、秋水仙素、二羟基炭疽菌素二酮、放线菌素、白喉毒素、假单胞菌外毒素(pe)a、pe40、相思豆毒素、相思豆毒素a链、蒴莲根毒素a链、α-八叠球菌、白树毒素、迈托毒素(mitogellin)、局限曲菌素(retstrictocin)、酚霉素、依诺霉素、麻疯树毒蛋白(curicin)、巴豆毒素、卡奇霉素、肥皂草(sapaonaria officinalis)抑制剂、糖皮质激素、或其组合。
[0089]
在优选的实施方式中,所述偶联部分为可检测标记物。
[0090]
在优选的实施方式中,所述偶联物选自:荧光或发光标记物、放射性标记物、mri(磁共振成像)或ct(电子计算机x射线断层扫描技术)造影剂、或能够产生可检测产物的酶、放射性核素、生物毒素、细胞因子(如il-2)、抗体、抗体fc片段、抗体scfv片段、金纳米颗粒/纳米棒、病毒颗粒、脂质体、纳米磁粒、前药激活酶(如dt-心肌黄酶(dtd)或联苯基水解酶-样蛋白质(bphl))、化疗剂(如顺铂)。
[0091]
在优选的实施方式中,所述免疫偶联物含有:多价(如二价)的本发明双特异性抗体。
[0092]
在优选的实施方式中,所述多价是指在所述免疫偶联物的氨基酸序列中包含多个重复的本发明的双特异性抗体。
[0093]
在第七方面,本发明提供第一方面所述的双特异性抗体,或第六方面所述的免疫偶联物的用途,用于制备药剂、试剂、检测板或试剂盒;
[0094]
其中,所述试剂、检测板或试剂盒用于:检测样品中pd-1和/或其它其它靶点;其中,所述药剂用于治疗或预防表达pd-1(即pd-1阳性)的肿瘤或是表达其它靶点的肿瘤。
[0095]
在优选的实施方式中,所述的免疫偶联物的偶联部分为诊断用同位素。
[0096]
在优选的实施方式中,所述的试剂为选自下组的一种或多种试剂:同位素示踪剂、造影剂、流式检测试剂、细胞免疫荧光检测试剂、纳米磁粒和显像剂。
[0097]
在优选的实施方式中,所述检测样品中pd-1和/或其它靶点的试剂为(体内)检测pd-1和/或其它靶点的造影剂。
[0098]
在另一优选的实施方式中,所述的检测为体内检测或体外检测。
[0099]
在另一优选的实施方式中,所述的检测包括流式检测、细胞免疫荧光检测。
[0100]
在另一优选的实施方式中,所述的药剂用于阻断pd-1和pd-l1的相互作用,同时阻断其它靶点与其受体或配体之间的相互作用。
[0101]
在另一优选的实施方式中,所述的肿瘤包括但不限于:急性髓细胞白血病、慢性粒细胞性白血病、多发性骨髓病、淋巴细胞白血病、淋巴瘤、结直肠癌、乳腺癌、胆囊癌、胃癌、肝癌、肾癌、头颈部肿瘤、脑部肿瘤、胶质母细胞瘤、肺癌、小肠癌、骨癌、前列腺癌、卵巢癌、宫颈癌、肾上腺肿瘤、膀胱肿瘤、肉瘤等。
[0102]
在第八方面,本发明提供一种药物组合物,所述药物组合物含有:
[0103]
(i)第一方面所述的双特异性抗体,或第六方面所述的免疫偶联物;和
[0104]
(ii)药学上可接受的载体。
[0105]
在优选的实施方式中,所述的药物组合物中还含有治疗肿瘤的其他药物,如细胞毒性药物。
[0106]
在优选的实施方式中,所述的治疗肿瘤的其他药物包括紫杉醇、多柔比星、环磷酰胺、阿西替尼、乐伐替尼、派姆单抗。
[0107]
在优选的实施方式中,所述的药物组合物或其它药物用于阻断pd-1和pd-l1的相互作用,同时阻断其它靶点与其受体或配体之间的相互作用。
[0108]
在另一优选的实施方式中,所述的药物组合物用于治疗表达pd-1蛋白(即pd-1阳性)和/或表达所述其它靶点的肿瘤。
[0109]
在优选的实施方式中,所述的药物组合物为注射剂型。
[0110]
在优选的实施方式中,所述的药物组合物用于制备防治肿瘤的药物。
[0111]
在第九方面,本发明提供第一方面所述的双特异性抗体的用途,所述用途是选自下组的一种或多种用途:
[0112]
(i)检测人pd-1分子和/或所述其它靶点;
[0113]
(ii)流式检测;
[0114]
(iii)细胞免疫荧光检测;
[0115]
(iv)治疗肿瘤;
[0116]
(v)肿瘤诊断;
[0117]
(vi)阻断pd-1和pd-l1的相互作用;和
[0118]
(vii)阻断其它靶点与其受体或配体之间的相互作用。
[0119]
在优选的实施方式中,所述的肿瘤为表达pd-1蛋白(即pd-1阳性)和/或表达其它靶点的肿瘤。
[0120]
在优选的实施方式中,所述用途为非诊断的和非治疗的。
[0121]
在第十方面,本发明提供一种重组蛋白,所述的重组蛋白具有:
[0122]
(i)第一方面所述的双特异性抗体;和
[0123]
(ii)任选的协助表达和/或纯化的标签序列。
[0124]
在优选的实施方式中,所述的标签序列包括6his标签、ha标签和fc标签。
[0125]
在优选的实施方式中,所述的重组蛋白特异性结合pd-1和/或所述的其它靶点。
[0126]
在第十一方面,本发明提供一种检测样品中pd-1和/或其它靶点的方法,所述方法包括步骤:
[0127]
(1)将样品与如第一方面所述的双特异性抗体接触;和
[0128]
(2)检测是否形成抗原-抗体复合物,其中形成复合物就表示样品中存在pd-1和/或其它靶点。
[0129]
在第十二方面,本发明提供一种pd-1和/或其它靶点的检测试剂,所述的检测试剂包含如第六方面所述的免疫偶联物和检测学上可接受的载体。
[0130]
在优选的实施方式中,所述的免疫偶联物的偶联部分为诊断用同位素。
[0131]
在优选的实施方式中,所述的检测学上可接受的载体为无毒的、惰性的水性载体介质。
[0132]
在优选的实施方式中,所述的检测试剂为选自下组的一种或多种试剂:同位素示踪剂、造影剂、流式检测试剂、细胞免疫荧光检测试剂、纳米磁粒和显像剂。
[0133]
在优选的实施方式中,所述的检测试剂用于体内检测。
[0134]
在优选的实施方式中,所述的检测试剂的剂型为液态或粉状(如水剂,针剂,冻干
粉,片剂,含服剂,吸雾剂)。
[0135]
在第十三方面,本发明提供一种检测pd-1和/或其它靶点的试剂盒,所述试剂盒含有如第六方面所述的免疫偶联物或如第十二方面所述的检测试剂,以及使用所述试剂盒或检测试剂检测pd-1和/或其它靶点的使用说明书。
[0136]
在优选的实施方式中,所述的说明书记载,所述的试剂盒用于非侵入性地检测待测对象的pd-1和/或其它靶点的表达。
[0137]
在优选的实施方式中,所述的试剂盒用于检测表达pd-1蛋白(即pd-1阳性)和/或表达其它靶点的肿瘤的检测。
[0138]
在本发明的第十四方面,提供了一种治疗疾病的方法,所述方法包括:给需要的对象施用如本发明第一方面所述的双特异性抗体、如本发明第六方面所述的免疫偶联物,或如本发明第八方面所述的药物组合物。
[0139]
在另一优选的实施方式中,所述的对象包括哺乳动物,优选人。
[0140]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
[0141]
图1显示本发明的抗-pd-1/vegf双特异性抗体pd-1端的结合elisa活性;
[0142]
图2显示了通过报告基因法检测的本发明的抗-pd-1/vegf双特异性抗体pd-1端的生物学活性;
[0143]
图3显示了本发明的抗-pd-1/vegf双特异性抗体vegf端的结合elisa活性;
[0144]
图4显示了本发明的抗-pd-1/il-8双特异性抗体pd-1端的结合elisa活性;
[0145]
图5显示了通过报告基因法检测的本发明的抗-pd-1/il-8双特异性抗体pd-1端的生物学活性;
[0146]
图6显示了本发明的抗-pd-1/il-8双特异性抗体il-8端的结合elisa活性;
[0147]
图7显示了本发明的抗-pd-1/ctla-4双特异性抗体pd-1端的结合elisa活性;
[0148]
图8显示了通过报告基因法检测的本发明的抗-pd-1/ctla-4双特异性抗体pd-1端的生物学活性;
[0149]
图9显示了本发明的抗-pd-1/ctla-4双特异性抗体ctla-4端的结合elisa活性;
[0150]
图10显示了本发明的抗-pd-1/tgf-β双特异性抗体pd-1端的结合elisa活性;
[0151]
图11显示了通过报告基因法检测的本发明的抗-pd-1/tgf-β双特异性抗体pd-1端的生物学活性;
[0152]
图12显示了本发明的抗-pd-1/tgf-β双特异性抗体tgf-β端的结合elisa活性;
[0153]
图13显示了本发明的抗-pd-1/psck9双特异性抗体pd-1端的结合elisa活性;
[0154]
图14显示了通过报告基因法检测的本发明的抗-pd-1/psck9双特异性抗体pd-1端的生物学活性;
[0155]
图15显示双特异性抗体结构示意图(方框内为双特异性抗体组成元件);其中a显示vhh连接于抗体重链ch1和铰链区之间;b显示vhh连接于抗体重链n端;c显示vhh连接于抗体重链c端;d显示vhh串联后直接与抗体重链铰链区连接;
[0156]
图16显示了pd-1vhh单抗组、阳性对照opdivo analogue组和抗-pd-1/vegf双抗组的相对肿瘤抑制率tgi%;和
[0157]
图17显示了pd-1vhh单抗组、阳性对照opdivo analogue组、抗-pd-1/tgf-β双抗组和抗-pd-1/pcsk9双抗组的相对肿瘤抑制率tgi%。
具体实施方式
[0158]
发明人经过广泛而深入的研究,出乎意料地发现利用本发明人制备的靶向pd-1的单域抗体能够简便地制备双特异性抗体。该双特异性抗体靶向pd-1与其它靶点的亲和力与相应的单特异性抗体的亲和力基本相当,并且具备生产工艺简便,体内活性优于相应的单特异性抗体等等优点,从而为开发全新的靶向pd-1和其它靶点的双特异性抗体抗体奠定了新的物质基础。在此基础上完成了本发明。
[0159]
术语定义
[0160]
本文所用的术语具有与本领域技术人员常规理解的相同或相似的含义。为清晰起见,对其中的一些术语定义如下。但本领域技术人员应该理解,对以下术语的定义并不是要在任何程度上限制本发明的保护范围。
[0161]
单域抗体(single domain抗body,sdab)
[0162]
在本文中,“单域抗体”与本领域技术人员理解的相同。其是指一类特殊的,只包含一条抗体重链的抗体。和传统双链抗体类似,它可以选择性地与特定抗原结合。单域抗体最早在骆驼科动物中被发现,之后在护士鲨等软骨鱼纲动物中也被发现。单域抗体单个重链抗体可变区(vhh)是能完整结合抗原的单个功能域,只有12-15kda。vhh结构简单,在与抗原结合时具有高特异性、高亲和力、免疫原性低、渗透性好以及在进行肿瘤治疗时具有接触到不能被常规抗体接触的较为隐蔽靶点的能力等优点。此外,因为单域抗体只有一条链,所以不会产生双链抗体融合时的错配问题。
[0163]
pd-1及其它靶点由于免疫检查点抑制剂pd-1和pd-l1抗体在临床上取得了极大的成功,针对pd-1或者pd-l1和其它免疫检查点的双特异性抗体目前是国际研究热点。pd-1或者pd-l1之外另一个靶点的选择,主要集中于两个方向:免疫检查点相关靶点和非免疫检查点相关靶点。目前在研的结合pd-1的免疫检查点相关靶点主要包括:ctla-4、lag-3、pd-l1、tigit、btla、tim-3、vista、cd47、cd73、ox40、icos、4-1bb、cd28等。而非免疫检查点相关靶点主要有:egfr、her2、claudin18.2、vegf、tgf-beta、psck9、il-1b、il-8等。同时靶向两个免疫检查点的理论依据是,在一些临床研究中,靶向这些检查点的单抗的联合治疗相比于单抗,取得了更好的临床效果。比如联合使用pd-1抗体和ctla-4抗体,在肺癌中取得了良好疗效。但值得注意的是,两种单克隆抗体的联合治疗也显著增加了免疫相关不良事件。为了提高靶向pd-1和ctla-4双特异性抗体的安全性,优化双特异性抗体的设计是关键。同样,选择非免疫检查点相关靶点的理论依据也是在一些临床研究中,联合使用pd-1或pd-l1抗体和非免疫检查点相关靶点,相比于单抗,取得了更好的临床效果。比如,在肝癌中,联合使用pd-l1抗体和vegf抗体,取得了的效果。因此,靶向pd-1和非免疫检查点抗体的双特异性抗体也有很大的临床治疗潜力。
[0164]
在具体的实施方式中,可能与pd-1组合的靶点有:ctla-4、il-8、vegf、tgf-beta、psck-9、cd47/sirp-alpha、egfr、pd-l1、her2、lag-3、tim-3,tigit、cd137、claudin18.2、
ox40、icos。
[0165]
例如,血管内皮生长因子又称血管通透因子或血管调理素是首先从肿瘤细胞分离出来的能与肝素结合的二聚体糖蛋白分子。其能特异性地作用于血管内皮细胞,是血管内皮细胞特异的有丝分裂素。具有增加微静脉、小静脉通透性、促进血管内皮细胞分裂、增殖以及诱导血管形成等作用。vegf参与许多血管生成依赖性疾病的发病及其进展,包括癌症、某些炎性疾病以及糖尿病视网膜病变等。因此,在抗肿瘤药物研究中,vegf是一个重要的靶点。
[0166]
本发明的双特异性抗体
[0167]
1960年,来自纽约罗斯威尔公园纪念研究所的nisonoff及其合作者首次提出了双特异性抗体(bispecific抗bodies;bsab)的概念。在之后的几十年间,随着抗体生物学和抗体工程领域的快速进展,构建双特异性抗体的技术不断成熟。目前已经有100多种双特异性抗体构建模式(formats),其中约四分之一已发展成技术平台,由生物技术公司和制药公司负责项目开发和商业化。
[0168]
双特异性抗体是自然界不存在的,经过基因工程改造而成的基因工程抗体。双特异性抗体能够同时靶向两个不同的抗体结合表位,这两个表位可以来自于不同抗原或者同一个抗原。双特异性抗体能同时阻断两个表位,也能成为细胞之间的桥梁,激发具有导向性的免疫反应,应用广泛。目前的许多研究都已表明双特异性抗体在治疗肿瘤、自身免疫性疾病、代谢性疾病和hiv等病原体感染等疾病中显示出巨大的治疗潜力,现已成为抗体工程领域的研究热点。目前大多数双特异性抗体项目都是针对癌症的,许多双特异性抗体正项目已经进入临床试验阶段。
[0169]
与单克隆抗体相比,双特异性抗体的主要优势在于可介导空间效应和双靶向的协同效用,产生两种抗体联合使用达不到的效果。但同时,双特异性抗体的技术门槛和研发成本都较高,在双抗研发中过程,都需要综合考虑靶点生物学、抗体工程和后续筛选策略等问题。在双抗构建过程中经常会遇到表达量低、质量稳定性差以及模型建立难的问题。
[0170]
基于本发明的教导以及本领域的公知常识,本领域技术人员会理解,本文中的“本发明的双特异性抗体”、“本发明的靶向pd-1的双特异性抗体”或“靶向pd-1的双特异性抗体”具有相同的含义,均是指包括第一抗体和第二抗体的双特异性抗体,所述第一抗体是靶向pd-1的单域抗体的vhh链、靶向pd-1的抗体的重链可变区、靶向pd-1的单域抗体、人源化的靶向pd-1的单域抗体的vhh链、或靶向pd-1的抗体;所述第二抗体是靶向上述其它靶点的抗体。
[0171]
在本发明的双特异性抗体的基础上,本发明还提供了一种编码所述双特异性抗体的分离的多核苷酸,包含所述多核苷酸的表达载体、以及含有所述表达载体或其基因组中整合有所述多核苷酸或表达所述双特异性抗体的宿主细胞。
[0172]
本领域技术人员知晓可以用于实施本发明的表达载体的类型,包括但不限于:dna、rna、病毒载体、质粒、转座子、其他基因转移系统、或其组合;优选地,所述表达载体包括病毒载体,如慢病毒、腺病毒、aav病毒、逆转录病毒、或其组合。本领域技术人员也知晓用于实施本发明的宿主细胞的类型,包括但不限于:原核细胞或真核细胞;优选大肠杆菌、酵母细胞或哺乳动物细胞。
[0173]
本领域技术人员知晓如何利用上述宿主细胞制备本发明的双特异性抗体的方法,
例如可以在合适的条件下,培养所述宿主细胞,从而获得含所述双特异性抗体的培养物。在获得所述培养物之后,可以对得到的培养物进行纯化和/或分离,从而获得所述的双特异性抗体。在优选的实施方式中,所述纯化是a蛋白亲和柱纯化分离获得目标抗体。
[0174]
本发明不仅包括完整的抗体,还包括所述抗体的片段、衍生物和类似物。如本文所用,术语“片段”、“衍生物”和“类似物”是指基本上保持本发明抗体相同的生物学功能或活性的多肽。本发明的多肽片段、衍生物或类似物可以是(i)有一个或多个保守或非保守性氨基酸残基(优选保守性氨基酸残基)被取代的多肽,而这样的取代的氨基酸残基可以是也可以不是由遗传密码编码的,或(ii)在一个或多个氨基酸残基中具有取代基团的多肽,或(iii)成熟多肽与另一个化合物(比如延长多肽半衰期的化合物,例如聚乙二醇)融合所形成的多肽,或(iv)附加的氨基酸序列融合到此多肽序列而形成的多肽(如前导序列或分泌序列或用来纯化此多肽的序列或蛋白原序列,或与6his标签形成的融合蛋白)。根据本文的教导,这些片段、衍生物和类似物属于本领域技术人员公知的范围。
[0175]
本发明抗体指具有pd-1蛋白结合活性以及其它靶点结合活性的、包括上述cdr区的多肽。该术语还包括具有与本发明抗体相同功能的、包含上述cdr区的多肽的变异形式。这些变异形式包括(但并不限于):一个或多个(通常为1-50个,较佳地1-30个,更佳地1-20个,最佳地1-10个)氨基酸的缺失、插入和/或取代,以及在c末端和/或n末端添加一个或数个(通常为20个以内,较佳地为10个以内,更佳地为5个以内)氨基酸。例如,在本领域中,用性能相近或相似的氨基酸进行取代时,通常不会改变蛋白质的功能。又比如,在c末端和/或n末端添加一个或数个氨基酸通常也不会改变蛋白质的功能。该术语还包括本发明抗体的活性片段和活性衍生物。该多肽的变异形式包括:同源序列、保守性变异体、等位变异体、天然突变体、诱导突变体、在高或低的严紧度条件下能与本发明抗体的编码dna杂交的dna所编码的蛋白、以及利用抗本发明抗体的抗血清获得的多肽或蛋白。
[0176]
除了几乎全长的多肽外,本发明还包括了本发明单域抗体的片段。通常,该片段具有本发明抗体的至少约50个连续氨基酸,较佳地至少约50个连续氨基酸,更佳地至少约80个连续氨基酸,最佳地至少约100个连续氨基酸。
[0177]
在本发明中,“本发明抗体的保守性变异体”指与本发明抗体的氨基酸序列相比,有至多10个,较佳地至多8个,更佳地至多5个,最佳地至多3个氨基酸被性质相似或相近的氨基酸所替换而形成多肽。这些保守性变异多肽最好根据表1进行氨基酸替换而产生。
[0178]
表1
[0179]
最初的残基代表性的取代优选的取代ala(a)val;leu;ilevalarg(r)lys;gln;asnlysasn(n)gln;his;lys;argglnasp(d)gluglucys(c)sersergln(q)asnasnglu(e)aspaspgly(g)pro;alaalahis(h)asn;gln;lys;argarg
ile(i)leu;val;met;ala;pheleuleu(l)ile;val;met;ala;pheilelys(k)arg;gln;asnargmet(m)leu;phe;ileleuphe(f)leu;val;ile;ala;tyrleupro(p)alaalaser(s)thrthrthr(t)sersertrp(w)tyr;phetyrtyr(y)trp;phe;thr;serpheval(v)ile;leu;met;phe;alaleu
[0180]
本发明还提供了编码上述抗体或其片段或其融合蛋白的多核苷酸分子。本发明的多核苷酸可以是dna形式或rna形式。dna形式包括cdna、基因组dna或人工合成的dna。dna可以是单链的或是双链的。dna可以是编码链或非编码链。编码本发明的成熟多肽的多核苷酸包括:只编码成熟多肽的编码序列;成熟多肽的编码序列和各种附加编码序列;成熟多肽的编码序列(和任选的附加编码序列)以及非编码序列。
[0181]
术语“编码多肽的多核苷酸”可以是包括编码此多肽的多核苷酸,也可以是还包括附加编码和/或非编码序列的多核苷酸。本发明还涉及与上述的序列杂交且两个序列之间具有至少50%,较佳地至少70%,更佳地至少80%相同性的多核苷酸。本发明特别涉及在严格条件下与本发明所述多核苷酸可杂交的多核苷酸。在本发明中,“严格条件”是指:(1)在较低离子强度和较高温度下的杂交和洗脱,如0.2
×
ssc,0.1%sds,60℃;或(2)杂交时加有变性剂,如50%(v/v)甲酰胺,0.1%小牛血清/0.1%ficoll,42℃等;或(3)仅在两条序列之间的相同性至少在90%以上,更好是95%以上时才发生杂交。并且,可杂交的多核苷酸编码的多肽与成熟多肽有相同的生物学功能和活性。
[0182]
本发明的抗体的核苷酸全长序列或其片段通常可以用pcr扩增法、重组法或人工合成的方法获得。一种可行的方法是用人工合成的方法来合成有关序列,尤其是片段长度较短时。通常,通过先合成多个小片段,然后再进行连接可获得序列很长的片段。此外,还可将重链的编码序列和表达标签(如6his)融合在一起,形成融合蛋白。一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。本发明所涉及的生物分子(核酸、蛋白等)包括以分离的形式存在的生物分子。
[0183]
目前,已经可以完全通过化学合成来得到编码本发明蛋白(或其片段,或其衍生物)的dna序列。然后可将该dna序列引入本领域中已知的各种现有的dna分子(或如载体)和细胞中。此外,还可通过化学合成将突变引入本发明蛋白序列中。
[0184]
本发明还涉及包含上述的适当dna序列以及适当启动子或者控制序列的载体。这些载体可以用于转化适当的宿主细胞,以使其能够表达蛋白质。宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。代表性例子有:大肠杆菌,链霉菌属;鼠伤寒沙门氏菌的细菌细胞;真菌细胞如酵母;果蝇s2或sf9的昆虫细胞;cho、cos7、293细胞的动物细胞等。
[0185]
用重组dna转化宿主细胞可用本领域技术人员熟知的常规技术进行。当宿主为原核生物如大肠杆菌时,能吸收dna的感受态细胞可在指数生长期后收获,用cacl2法处理,所用的步骤在本领域众所周知。另一种方法是使用mgcl2。如果需要,转化也可用电穿孔的方法进行。当宿主是真核生物,可选用如下的dna转染方法:磷酸钙共沉淀法,常规机械方法如显微注射、电穿孔,脂质体包装等。
[0186]
获得的转化子可以用常规方法培养,表达本发明的基因所编码的多肽。根据所用的宿主细胞,培养中所用的培养基可选自各种常规培养基。在适于宿主细胞生长的条件下进行培养。当宿主细胞生长到适当的细胞密度后,用合适的方法(如温度转换或化学诱导)诱导选择的启动子,将细胞再培养一段时间。
[0187]
在上面的方法中的重组多肽可在细胞内、或在细胞膜上表达、或分泌到细胞外。如果需要,可利用其物理的、化学的和其它特性通过各种分离方法分离和纯化重组的蛋白。这些方法是本领域技术人员所熟知的。这些方法的例子包括但并不限于:常规的复性处理、用蛋白沉淀剂处理(盐析方法)、离心、渗透破菌、超处理、超离心、分子筛层析(凝胶过滤)、吸附层析、离子交换层析、高效液相层析(hplc)和其它各种液相层析技术及这些方法的结合。
[0188]
本发明的抗体可以单独使用,也可与可检测标记物(为诊断目的)、治疗剂、pk(蛋白激酶)修饰部分或任何以上这些物质的组合结合或偶联。用于诊断目的可检测标记物包括但不限于:荧光或发光标记物、放射性标记物、mri(磁共振成像)或ct(电子计算机x射线断层扫描技术)造影剂、或能够产生可检测产物的酶。
[0189]
因此,本发明还提供了一种免疫偶联物,其含有本发明的双特异性抗体;和偶联部分。可与本发明抗体结合或偶联的治疗剂包括但不限于:1.放射性核素;2.生物毒素;3.细胞因子,如il-2等;4.金纳米颗粒/纳米棒;5.病毒颗粒;6.脂质体;7.纳米磁粒;8.药激活酶(例如,dt-心肌黄酶(dtd)或联苯基水解酶-样蛋白质(bphl));9.治疗剂(例如,顺铂)或任何形式的纳米颗粒等。在优选的实施方式中,所述免疫偶联物是抗体-药物偶联物(antibody-drug-conjugate,adc)。
[0190]
药物组合物
[0191]
本发明还提供了一种药物组合物,它含有上述的双特异性抗体或其活性片段或其融合蛋白,以及药学上可接受的载体。通常,可将这些物质配制于无毒的、惰性的和药学上可接受的水性载体介质中,其中ph通常约为5-8,较佳地ph约为6-8,尽管ph值可随被配制物质的性质以及待治疗的病症而有所变化。配制好的药物组合物可以通过常规途径进行给药,其中包括(但并不限于):瘤内、腹膜内、静脉内、或局部给药。
[0192]
本发明的药物组合物可直接用于结合pd-1蛋白,从而阻断pd-1和pd-l1的相互作用,本发明的药物组合物可直接用于结合其它靶点,从而阻断所述其它靶点与其受体或配体的结合。因此,本发明的药物组合物可用于治疗肿瘤。在优选的实施方式中,所述肿瘤选自下组:急性髓细胞白血病、慢性粒细胞性白血病、多发性骨髓病、淋巴细胞白血病、淋巴瘤、结直肠癌、乳腺癌、胆囊癌、胃癌、肝癌、肾癌、头颈部肿瘤、脑部肿瘤、胶质母细胞瘤、肺癌、小肠癌、骨癌、前列腺癌、卵巢癌、宫颈癌、肾上腺肿瘤、膀胱肿瘤、肉瘤等。此外,本发明的药物组合物还可与其他治疗剂联用。
[0193]
本发明的药物组合物含有安全有效量(如0.001-99wt%、较佳地0.01-90wt%、更佳地0.1-80wt%)的本发明上述的单域抗体(或其偶联物)以及药学上可接受的载体或赋形
剂。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、及其组合。药物制剂应与给药方式相匹配。本发明的药物组合物可以被制成针剂形式,例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。药物组合物如针剂、溶液宜在无菌条件下制造。
[0194]
活性成分的给药量是治疗有效量,例如每天约10微克/千克体重-约50毫克/千克体重。使用药物组合物时,是将安全有效量的免疫偶联物施用于哺乳动物,其中该安全有效量通常至少约10微克/千克体重,而且在大多数情况下不超过约50毫克/千克体重,较佳地该剂量是约10微克/千克体重-约10毫克/千克体重。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。
[0195]
检测方法
[0196]
本发明还涉及检测pd-1蛋白和/或其它靶蛋白的方法。该方法步骤大致如下:将待测样品与本发明的双特异性抗体接触;随后检测是否形成抗原-抗体复合物,如果形成复合物就表示样品中存在pd-1蛋白和/或其它靶蛋白。
[0197]
检测试剂或试剂盒
[0198]
本发明还提供了一种含有本发明的双特异性抗体、重组蛋白或免疫偶联物等的检测试剂或试剂盒。在具体的实施方式中,所述的试剂盒还包括容器、使用说明书、缓冲剂等。
[0199]
应用
[0200]
如上所述,本发明的双特异性抗体有广泛生物应用价值和临床应用价值,其应用涉及到与pd-1和/或其它靶点相关的疾病的诊断和治疗、基础医学研究、生物学研究等多个领域。
[0201]
在优选的实施方式中,本发明的双特异性抗体用于针对pd-1和/或其它靶点的临床诊断和靶向治疗,如肿瘤治疗。
[0202]
本发明的优点:
[0203]
1.本发明的双特异性抗体靶向pd-1与其它靶点的亲和力与相应的单特异性抗体的亲和力基本相当;
[0204]
2.生产本发明的双特异性抗体不存在抗体链错配问题,后续纯化工艺简单,从而能够实现大规模生产;
[0205]
3.本发明的双特异性抗体均有较高的表达量,利于工业化生产。
[0206]
4.本发明的双特异性抗体相对分子量较小,利于抗体的肿瘤组织浸润,发挥更好的生物学活性。
[0207]
5.本发明的双特异性抗体的体内活性优于相应的单特异性抗体;
[0208]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(new york:cold spring harbor laboratory press,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
[0209]
实施例
[0210]
实施例1.基于pd-1vhh的双特异性抗体的表达和纯化
[0211]
1.序列设计
[0212]
双特异性抗体中pd-1母本抗体的序列来源于中国发明专利申请(申请号:2021100481961,靶向pd-1的单域抗体及其衍生物和用途,其内容通过引用全文纳入本文)的pd-1vhh抗体序列。选取克隆huvhh3-3构建双特异性抗体(氨基酸序列:seq id no.51,dna序列:seq id no.52)。vhh只有一条链,方便与传统双链抗体组合形成双特异性抗体。分别选取靶向il-8、vegf、ctla-4、tgf-β和psck-9的抗体序列,五种抗体均为包含一条重链和一条轻链的双链抗体。
[0213]
il-8抗体序列来源于克隆10f8,重链氨基酸序列来自于us20040208873a1_seq8,轻链氨基酸序列来自于us_2004_0208873_a1_seq 12(重链氨基酸序列:seq id no.1;轻链氨基酸序列:seq id no.2)。
[0214]
vegf抗体序列来源于ranibizumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.3;轻链氨基酸序列:seq id no.4);或bevacizumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.5;轻链氨基酸序列:seq id no.6)。
[0215]
ctla-4抗体序列来源于ipilimumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.7;轻链氨基酸序列:seq id no.8)。
[0216]
tgf-b抗体序列来源于fresolimumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.9;轻链氨基酸序列:seq id no.10)。
[0217]
psck9抗体序列来源于alirocumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.11;轻链氨基酸序列:seq id no.12);或evolocumab(https://go.drugbank.com)(重链氨基酸序列:seq id no.13;轻链氨基酸序列:seq id no.14)。以上抗体相关的氨基酸序列总结于下文:
[0218]
母本抗体pd-1vhh抗体克隆huvhh3-3:evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvss(seq id no:51);
[0219]
huvhh3-3的dna序列:gaggtccagttggtagaaagtggtggtgggttggtgcaacccggtggctcattgaggctgtcttgtgctgcgagtggcaggacatcctctatgtatgcgatgggatggttccgacaagctccaggaaacgagcgcgagttcgtagccggaattggttgggaaaacaatacgccctattatgcacggtctgtcgaggggaggttcactatctcacgcgacaacgtcaagaacacagtgtttcttcagatgaaccgactccgggcggaggatacggccgtatattattgcgcagcgcaaatcggtatatccggcactcttggtgactattggggccagggtacacaagtgacagtctcttca(seq id no:52);
[0220]
huvhh3-3的cdr1:grtssmyamg(seq id no:53);cdr2gigwenntpyyarsveg(seq id no:54);cdr3 qigisgtlgdy(seq id no:55);
[0221]
il-8抗体序列来源于us20040208873a1中的10f8单抗
[0222]
重链氨基酸序列:seq id no.1
[0223]
qvqlvesgggvvqpgrslrlsctasgftfshygmywvrqapgkglewvaviwydgsyeynedsvkgrftisrdnskntlylqmnslraedtavyycardrvglfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0224]
轻链氨基酸序列:seq id no.2
[0225]
eivltqspgtlslspgeratlscrasqsisssylawyqqkpgqaprlliygpssratgipdrfsgsgsgtdftltisrlepedfavyycqqyagsltfgpgtkvdikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0226]
vegf抗体序列来源于ranibizumab
[0227]
重链氨基酸序列:seq id no.3
[0228]
evqlvesggglvqpggslrlscaasgytftnygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakyphyygsshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0229]
轻链氨基酸序列:seq id no.4
[0230]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgtdftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0231]
vegf抗体序列来源于avastin
[0232]
重链氨基酸序列:seq id no.5
[0233]
evqlvesggglvqpggslrlscaasgydfthygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakypyyygtshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0234]
轻链氨基酸序列:seq id no.6
[0235]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgtdftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0236]
ctla-4抗体序列来源于ipilimumab
[0237]
重链氨基酸序列:seq id no.7
[0238]
qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
[0239]
轻链氨基酸序列:seq id no.8
[0240]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreak
vqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0241]
tgf-β抗体序列来源于fresolimumab
[0242]
重链氨基酸序列:seq id no.9
[0243]
qvqlvqsgaevkkpgssvkvsckasgytfssnviswvrqapgqglewmggvipivdianyaqrfkgrvtitadeststtymelsslrsedtavyycastlglvldamdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcpscpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0244]
轻链氨基酸序列:seq id no.10;
[0245]
etvltqspgtlslspgeratlscrasqslgssylawyqqkpgqaprlliygassrapgipdrfsgsgsgtdftltisrlepedfavyycqqyadspitfgqgtrleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0246]
psck9抗体序列来源于alirocumab
[0247]
重链氨基酸序列:seq id no.11
[0248]
evqlvesggglvqpggslrlscaasgftfnnyamnwvrqapgkgldwvstisgsggttnyadsvkgrfiisrdsskhtlylqmnslraedtavyycakdsnwgnfdlwgrgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0249]
轻链氨基酸序列:seq id no.12
[0250]
divmtqspdslavslgeratinckssqsvlyrsnnrnflgwyqqkpgqppnlliywastresgvpdrfsgsgsgtdftltisslqaedvavyycqqyyttpytfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0251]
psck9抗体序列来源于evolocumab
[0252]
重链氨基酸序列:seq id no.13
[0253]
evqlvqsgaevkkpgasvkvsckasgytltsygiswvrqapgqglewmgwvsfyngntnyaqklqgrgtmttdpststaymelrslrsddtavyycargygmdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0254]
轻链氨基酸序列:seq id no.14
[0255]
esaltqpasvsgspgqsitisctgtssdvggynsvswyqqhpgkapklmiyevsnrpsgvsnrfsgsksgntasltisglqaedeadyycnsytstsmvfgggtkltvlrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0256]
然后,利用dna重组技术,将pd-1vhh抗体连接到双链抗体的重链或者轻链的n端或者c端。pd-1vhh抗体通过连接肽与双链抗体连接,连接的长度可以根据试验需求进行调整,
三种连接肽分别为:(ggggs)*1,(ggggs)*2,或者(ggggs)*3。通过上述方法,利用pd-1vhh作为母本抗体设计了五类,共17种靶向五种不同靶点的双特异性抗体,除pd-1之外的另一个靶点分别是:il-8、vegf、ctla-4、tgf-β和psck-9。我们将这17种双特异性抗体分别命名为:
[0257]
抗pd-1/il-8-1(图15结构a;重链氨基酸序列:seq id no.15;轻链氨基酸序列:seq id no.16);
[0258]
抗pd-1/il-8-2(图15结构b;重链氨基酸序列:seq id no.17;轻链氨基酸序列:seq id no.18);
[0259]
抗pd-1/vegf-1(图15结构c;重链氨基酸序列:seq id no.19;轻链氨基酸序列:seq id no.20);
[0260]
抗pd-1/vegf-2(图15结构b;重链氨基酸序列:seq id no.21;轻链氨基酸序列:seq id no.22);
[0261]
抗pd-1/vegf-3(图15结构b;重链氨基酸序列:seq id no.23;轻链氨基酸序列:seq id no.24);
[0262]
抗pd-1/vegf-4(图15结构b;重链氨基酸序列:seq id no.25;轻链氨基酸序列:seq id no.26);
[0263]
抗pd-1/ctla-4-1(图15结构b;重链氨基酸序列:seq id no.27;轻链氨基酸序列:seq id no.28);
[0264]
抗pd-1/ctla-4-2(图15结构b;重链1氨基酸序列:seq id no.29;重链2氨基酸序列:seq id no.30;轻链氨基酸序列:seq id no.31);
[0265]
抗pd-1/ctla-4-3(图15结构d;重链1氨基酸序列:seq id no.32;重链2氨基酸序列:seq id no.33;轻链氨基酸序列:seq id no.34);
[0266]
抗pd-1/ctla-4-4(图15结构b;重链氨基酸序列:seq id no.35;轻链氨基酸序列:seq id no.36);
[0267]
抗pd-1/ctla-4-5(图15结构b;重链氨基酸序列:seq id no.37;轻链氨基酸序列:seq id no.38);
[0268]
抗pd-1/ctla-4-6(图15结构b;重链氨基酸序列:seq id no.39;轻链氨基酸序列:seq id no.40);
[0269]
抗pd-1/tgf-β-1(图15结构c;重链氨基酸序列:seq id no.41;轻链氨基酸序列:seq id no.42);
[0270]
抗pd-1/tgf-β-2(图15结构b;重链氨基酸序列:seq id no.43;轻链氨基酸序列:seq id no.44);
[0271]
抗pd-1/tgf-β-3(图15结构b;重链氨基酸序列:seq id no.45;轻链氨基酸序列:seq id no.46);
[0272]
抗pd-1/psck9-1(图15结构b;重链氨基酸序列:seq id no.47;轻链氨基酸序列:seq id no.48);
[0273]
抗pd-1/psck9-2(图15结构b;重链氨基酸序列:seq id no.49;轻链氨基酸序列:seq id no.50)。
[0274]
以上所有双特异性抗体的氨基酸的序列总结于下文:
[0275]
antipd-1/il-8-1
[0276]
重链氨基酸序列:seq id no.15
[0277]
qvqlvesgggvvqpgrslrlsctasgftfshygmywvrqapgkglewvaviwydgsyeynedsvkgrftisrdnskntlylqmnslraedtavyycardrvglfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrvggggsggggsggggsevqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggseskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0278]
轻链氨基酸序列:seq id no.16
[0279]
eivltqspgtlslspgeratlscrasqsisssylawyqqkpgqaprlliygpssratgipdrfsgsgsgtdftltisrlepedfavyycqqyagsltfgpgtkvdikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0280]
antipd-1/il-8-2;
[0281]
重链氨基酸序列:seq id no.17
[0282]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsqvqlvesgggvvqpgrslrlsctasgftfshygmywvrqapgkglewvaviwydgsyeynedsvkgrftisrdnskntlylqmnslraedtavyycardrvglfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0283]
轻链氨基酸序列:seq id no.18
[0284]
eivltqspgtlslspgeratlscrasqsisssylawyqqkpgqaprlliygpssratgipdrfsgsgsgtdftltisrlepedfavyycqqyagsltfgpgtkvdikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0285]
antipd-1/vegf-1
[0286]
重链氨基酸序列:seq id no.19
[0287]
evqlvesggglvqpggslrlscaasgydfthygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakypyyygtshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgaggggsggggsggggsevqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvss
[0288]
轻链氨基酸序列:seq id no.20
[0289]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgt
dftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0290]
antipd-1/vegf-2
[0291]
重链氨基酸序列:seq id no.21
[0292]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsevqlvesggglvqpggslrlscaasgydfthygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakypyyygtshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0293]
轻链氨基酸序列:seq id no.22
[0294]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgtdftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0295]
antipd-1/vegf-3
[0296]
重链氨基酸序列:seq id no.23
[0297]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsevqlvesggglvqpggslrlscaasgytftnygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakyphyygsshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0298]
轻链氨基酸序列:seq id no.24
[0299]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgtdftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0300]
antipd-1/vegf-4
[0301]
重链氨基酸序列:seq id no.25
[0302]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsevqlvesggglvqpggslrlscaasgytftnygmnwvrqapgkglewvgwintytgeptyaadfkrrftfsldtskstaylqmnslraedtavyycakyphyygsshwyfdvwgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvl
dsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0303]
轻链氨基酸序列:seq id no.26;
[0304]
diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapkvliyftsslhsgvpsrfsgsgsgtdftltisslqpedfatyycqqystvpwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0305]
antipd-1/ctla-4-1
[0306]
重链氨基酸序列:seq id no.27
[0307]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsqvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
[0308]
轻链氨基酸序列:seq id no.28
[0309]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0310]
antipd-1/ctla-4-2
[0311]
重链1氨基酸序列:seq id no.29
[0312]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcrdeltknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
[0313]
重链2氨基酸序列:seq id no.30;
[0314]
qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsrdeltknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnrftqkslslspgk
[0315]
轻链氨基酸序列:seq id no.31
[0316]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0317]
antipd-1/ctla-4-3
[0318]
重链1氨基酸序列:seq id no.32
[0319]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsevqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcrdeltknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
[0320]
重链2氨基酸序列:seq id no.33
[0321]
qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsrdeltknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnrftqkslslspgk
[0322]
轻链氨基酸序列:seq id no.34
[0323]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0324]
antipd-1/ctla-4-4
[0325]
重链氨基酸序列:seq id no.35
[0326]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
[0327]
轻链氨基酸序列:seq id no.36
[0328]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0329]
antipd-1/ctla-4-5
[0330]
重链氨基酸序列:seq id no.37
[0331]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsqvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpss
iektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0332]
轻链氨基酸序列:seq id no.38
[0333]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0334]
antipd-1/ctla-4-6
[0335]
重链氨基酸序列:seq id no.39
[0336]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsqvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0337]
轻链氨基酸序列:seq id no.40
[0338]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0339]
antipd-1/tgf-β-1
[0340]
重链氨基酸序列:seq id no.41
[0341]
qvqlvqsgaevkkpgssvkvsckasgytfssnviswvrqapgqglewmggvipivdianyaqrfkgrvtitadeststtymelsslrsedtavyycastlglvldamdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgaggggsggggsggggsevqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvss
[0342]
轻链氨基酸序列:seq id no.42
[0343]
etvltqspgtlslspgeratlscrasqslgssylawyqqkpgqaprlliygassrapgipdrfsgsgsgtdftltisrlepedfavyycqqyadspitfgqgtrleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0344]
antipd-1/tgf-β-2
[0345]
重链氨基酸序列:seq id no.43
[0346]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytfssnviswvrqapgqglewmggvipivdianyaqrfkgrvtitadeststtymelsslrs
edtavyycastlglvldamdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0347]
轻链氨基酸序列:seq id no.44
[0348]
etvltqspgtlslspgeratlscrasqslgssylawyqqkpgqaprlliygassrapgipdrfsgsgsgtdftltisrlepedfavyycqqyadspitfgqgtrleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0349]
antipd-1/tgf-β-3
[0350]
重链氨基酸序列:seq id no.45
[0351]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsqvqlvqsgaevkkpgssvkvsckasgytfssnviswvrqapgqglewmggvipivdianyaqrfkgrvtitadeststtymelsslrsedtavyycastlglvldamdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0352]
轻链氨基酸序列:seq id no.46
[0353]
etvltqspgtlslspgeratlscrasqslgssylawyqqkpgqaprlliygassrapgipdrfsgsgsgtdftltisrlepedfavyycqqyadspitfgqgtrleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0354]
antipd-1/psck9-1
[0355]
重链氨基酸序列:seq id no.47
[0356]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsevqlvesggglvqpggslrlscaasgftfnnyamnwvrqapgkgldwvstisgsggttnyadsvkgrfiisrdsskhtlylqmnslraedtavyycakdsnwgnfdlwgrgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0357]
轻链氨基酸序列:seq id no.48
[0358]
divmtqspdslavslgeratinckssqsvlyrsnnrnflgwyqqkpgqppnlliywastresgvpdrfsgsgsgtdftltisslqaedvavyycqqyyttpytfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
[0359]
antipd-1/psck9-2
[0360]
重链氨基酸序列:seq id no.49
[0361]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlraedtavyycaaqigisgtlgdywgqgtqvtvssggggsggggsggggsevqlvqsgaevkkpgasvkvsckasgytltsygiswvrqapgqglewmgwvsfyngntnyaqklqgrgtmttdpststaymelrslrsddtavyycargygmdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
[0362]
轻链氨基酸序列:seq id no.50
[0363]
esaltqpasvsgspgqsitisctgtssdvggynsvswyqqhpgkapklmiyevsnrpsgvsnrfsgsksgntasltisglqaedeadyycnsytstsmvfgggtkltvlrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec。
[0364]
2.表达纯化
[0365]
参考上述双特异性抗体的核酸序列表,使用dna合成和分子克隆构建双特异性抗体表达载体。载体构建成功后,使用293系统表达上述双特异性抗体。基本步骤:将双特异性抗体基因克隆至表达载体pcdna4(invitrogen,cat v86220)中。使用瞬时转染hek293悬浮细胞的方法对双特异性抗体进行表达。表达完成后,收取上清液,使用protein a亲和层析柱纯化,最终获得纯化的双特异性抗体。
[0366]
在双特异性抗体纯化完成后,使用紫外分光光度法检测不同抗体的蛋白浓度和总蛋白量,然后根据表达体积来计算每个双抗的表达量。基本步骤如下:由于蛋白质分子中含有酪氨酸、色氨酸和苯丙氨酸等苯环结构,在紫外280nm波长附近有最大吸收峰。根据朗伯-比尔定律,蛋白溶液在某一固定紫外波长的吸光度值(a)与蛋白质的消光系数(ε)、浓度(c)以及光透过路径(l)存在一定关系:a=εlc。因此,蛋白溶液的浓度可以通过固定波长的吸光度值、比色皿的光径和该蛋白物质的消光系数计算获得。使用nanodrop 1000在波长280nm处读取样品溶液吸光值a280,通过公式c(mg/ml)=a280/ε(ε为1.482ml/mg
·
cm-1
)计算样品的蛋白浓度。
[0367]
同时使用凝胶电泳sds-page评价不同抗体的纯度。基本步骤如下:采用invitrogen公司xcell surelock novex mini cell电泳槽及nupage 4-12%bis-tris gel梯度胶对样品进行电泳分离。将样品稀释至约1mg/ml,加入适量还原剂、loading buffer和纯水,混合后,于70℃加热约10分钟,上样量为2~10μg,电泳电压约200v,电泳时间约35分钟,染色时间约2小时,脱色时间约3小时。脱色完成后利用proteinsimple公司alpha view-alpha imager sa软件凝胶成像系统拍照并分析计算主带的纯度。
[0368]
此外,使用分子排阻高效液相色谱法(sec-hplc法)评价不同抗体的纯度。基本步骤如下:将样品稀释至约1.0mg/ml,采用tskgel g3000swxl色谱柱,设置柱温为25℃,用100mm磷酸缓冲液、100mm硫酸钠、ph 7.0
±
0.2作为流动相,进样体积为20~50μl,在1.0ml/min的流速下,等度洗脱20min,280nm波长下进行检测,采用峰面积归一化法得到单体的含量。
[0369]
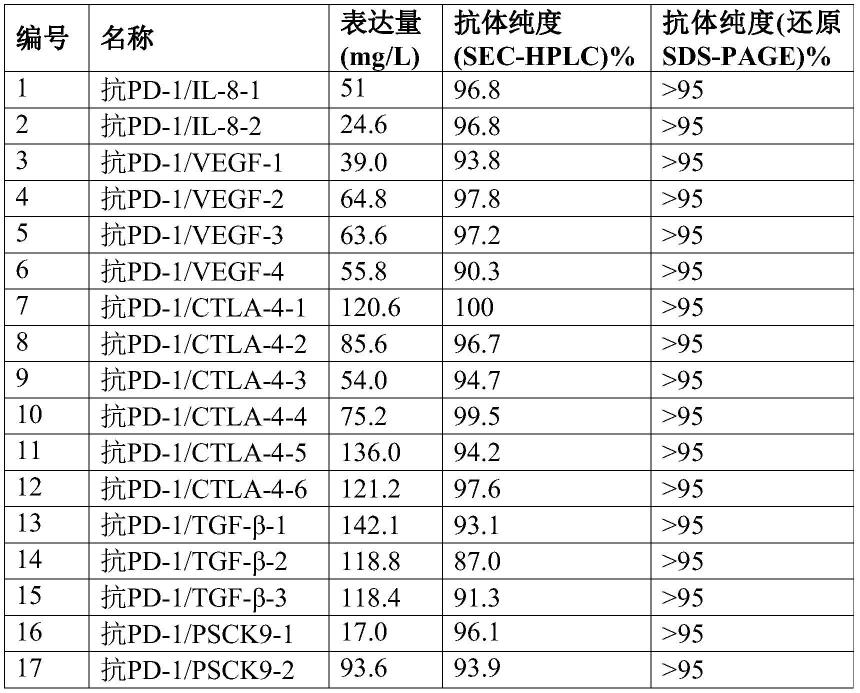
不同双特异性抗体的表达量和纯度信息见表1。除抗pd-1/il-8-2和抗pd-1/psck9-1外,其它双抗的表达量在39.0~142.1mg/l的范围,证明本发明的双抗结构具有较
高的表达量。除抗pd-1/tgf-β-2的sec-hplc单体纯度为87.0%之外,其它双抗的sec-hplc的单体纯度均在90%以上。同时,所有双抗的还原sds-page的纯度均在95%以上。这些结果证明本发明的双抗结构通过一步亲和层析纯化便具有较高的纯度,杂质水平较低。
[0370]
表5:双特异性抗体的表达量和纯度检测结果
[0371][0372]
由以上结果可知,双特异性抗体的表达量和纯度都较好,可以用来进行进一步筛选和评价。
[0373]
实施例2.双特异性抗体的体外生物学活性检测
[0374]
使用结合elisa方法检测评价双特异性抗体与pd-1抗原及另一端抗原的结合能力。以抗-pd-1/vegf双特异性抗体为例,分别检测双特异性抗体与pd-1抗原和vegf抗原的亲和力。基本步骤如下:首先将人pd-1蛋白(购自北京百普赛斯,货号pd1-h5221)或vegf蛋白(购自北京百普赛斯,货号ve5-h5248)使用pbs(购自hyclone公司)稀释至1μg/ml,按照100μl/孔加入96孔酶标板进行抗原包被,置于37℃恒温培养箱中孵育60min。孵育结束后洗板三次并按照200μl/孔加入含有2%bsa的pbs进行封闭,置于37℃恒温培养箱内孵育60min。同时,将样品抗-pd-1/vegf双抗及对照抗体pd-1vhh用稀释液(含有2%bsa的pbs)稀释至100ng/ml,并在样品稀释板上以3倍梯度依次稀释至0.05ng/ml。然后,按照100μl/孔将样品加入到96孔酶标板中并置于37℃恒温培养箱内孵育60min。孵育结束后洗板并将二抗山羊抗-人igg(fc特异性)-hrp抗体(购自sigma公司,货号a-0170)用2%bsa稀释6000倍,按照100μl/孔加入酶标板并置于37℃恒温培养箱内孵育30min。孵育结束后洗板三次并按照100μl/孔加入显色液,显色液为100μg/ml的tmb(3,3',5,5'-四甲基联苯胺),置于37℃恒温培养箱内避光孵育15min。最后,按照100μl/孔加入终止液(2m/l盐酸溶液)并使用酶标仪
(thermo fisher scientific,varioskan lux)检测450nm/620nm测吸收值,使用graphpad prism分析数据。
[0375]
使用报告基因法检测评价双特异性抗体pd-1端的生物学活性。培养cho/pd-l1细胞(购自promega公司)后消化并用含有10%fbs的f-12营养混合物完全培养基重悬细胞,根据细胞计数结果使用完全培养基调整细胞密度至5
×
105个细胞/ml。随后将细胞悬液转移至加样槽中并使用多道移液器以100μl/孔加入到96孔板中,放置于37℃的5%co2培养箱中培养16~22h。同时,培养jurkat/pd-1细胞(购自promega公司)细胞并根据细胞计数结果使用分析培养基(rpmi 1640medium+2%fbs)调整细胞密度至2
×
106个细胞/ml。将加入cho/pd-l1细胞的细胞培养板从培养箱中取出并使用多道移液器每孔取出100μl培养液,随后按照40μl/孔加入梯度稀释(起始浓度为1650nm)的待测样品。然后,将上述jurkat/pd-1细胞悬液转移至加样槽中并按照40μl/孔加入到细胞培养板中,置于37℃的5%co2培养箱培养4~6h。培养结束后取出细胞培养板,置于室温放置5~10min,然后每孔加入40μl one-glo试剂(购自promega公司,货号e6130),置于混匀器上混匀5~10min,然后使用多功能酶标仪读取化学发光信号值,使用graphpad prism分析数据。
[0376]
结果如图1-3和表2所示,对照抗体pd-1vhh结合pd-1蛋白的ec
50
为20.2ng/ml,而抗pd-1/vegf双抗与pd-1蛋白的ec
50
为38.6~43.7ng/ml(除抗pd-1/vegf-1外)。pd-1端的细胞生物学活性方面,对照抗体pd-1vhh的ec
50
为0.2~0.5μg/ml,而抗pd-1/vegf双抗的ec
50
为0.9~1.9μg/ml。综合来看,除抗pd-1/vegf-1之外,本发明其它双抗与pd-1抗原的亲和力及pd-1端的生物学活性与对照抗体pd-1vhh基本相当。此外,vegf端的抗原结合活性方面,抗pd-1/vegf双抗与对照抗体ranibizumab或bevacizumab基本相当。这些数据说明本发明抗pd-1/vegf双抗结构基本不影响pd-1端和vegf端的生物学活性。
[0377]
表6:抗-pd-1/vegf双特异性抗体的生物学活性
[0378][0379][0380]
抗pd-1/il-8双特异性抗体使用类似的试验步骤进行elisa结合活性或pd-1报告基因法的生物学活性评价。针对抗pd-1/il-8双特异性抗体,结果如图4-6和表7所示,对照抗体pd-1vhh结合pd-1蛋白的ec
50
为16.4ng/ml,而抗pd-1/il-8双抗与pd-1蛋白的ec
50
为35.5~35.9ng/ml。pd-1端的细胞生物学活性方面,对照抗体pd-1vhh的ec
50
为0.4μg/ml,而抗pd-1/il-8-2双抗的ec
50
为1.3μg/ml。综合来看,本发明抗pd-1/il-8与pd-1抗原的亲和力及pd-1端的生物学活性与对照抗体pd-1vhh基本相当。此外,il-8端的抗原结合活性方面,抗pd-1/il-8双抗与对照抗体基本相当。这些数据说明本发明抗pd-1/il-8双抗结构基本不影响pd-1端和il-8端的生物学活性。
[0381]
表7.抗-pd-1/il-8双特异性抗体的生物学活性
[0382][0383]
抗pd-1/ctla-4双特异性抗体使用类似的试验步骤进行elisa结合活性或pd-1报告基因法的生物学活性评价。针对抗pd-1/ctla-4双特异性抗体,结果如图7-9和表8所示,对照抗体pd-1vhh结合pd-1蛋白的ec
50
为7.3~16.4ng/ml,而抗pd-1/ctla-4双抗与pd-1蛋白的ec
50
为10.2~43.1ng/ml。pd-1端的细胞生物学活性方面,对照抗体pd-1vhh的ec
50
为0.2μg/ml,而抗pd-1/ctla-4双抗的ec
50
为0.5~2.1μg/ml。综合来看,本发明抗pd-1/ctla-4与pd-1抗原的亲和力及pd-1端的生物学活性与对照抗体pd-1vhh基本相当。此外,ctla-4端的抗原结合活性方面,抗pd-1/ctla-4双抗与对照抗体ipilimumab基本相当。这些数据说明本发明抗pd-1/ctla-4双抗结构基本不影响pd-1端和ctla-4端的生物学活性。
[0384]
表8.抗-pd-1/ctla-4双特异性抗体的生物学活性
[0385][0386][0387]
抗pd-1/tgf-β双特异性抗体使用类似的试验步骤进行elisa结合活性或pd-1报告基因法的生物学活性评价。针对抗pd-1/tgf-β双特异性抗体,结果如图10-12和表9所示,对照抗体pd-1vhh结合pd-1蛋白的ec
50
为7.3~12.2ng/ml,而抗pd-1/tgf-β-2和抗pd-1/tgf-β-3双抗与pd-1蛋白的ec
50
为13.7~21.3ng/ml,但抗pd-1/tgf-β-1的pd-1结合活性降低较明显(ec
50
为170.1ng/ml)。pd-1端的细胞生物学活性方面,对照抗体pd-1vhh的ec
50
为0.2μg/ml,而抗pd-1/tgf-β双抗的ec
50
为0.7~1.7μg/ml,但抗pd-1/tgf-β-1的活性降低较明显(ec
50
为1.7μg/ml)。综合来看,除抗pd-1/tgf-β-1双抗外,本发明抗pd-1/tgf-β与pd-1抗原的亲和力及pd-1端的生物学活性与对照抗体pd-1vhh基本相当。此外,tgf-β端的抗原结合活性方面,抗pd-1/tgf-β双抗与对照抗体fresolimumab基本相当。这些数据说明本发明抗pd-1/tgf-β双抗结构基本不影响pd-1端和tgf-β端的生物学活性。
[0388]
表9.抗-pd-1/tgf-β双特异性抗体的生物学活性
[0389][0390]
抗pd-1/pcsk9双特异性抗体使用类似的试验步骤进行elisa结合活性或pd-1报告基因法的生物学活性评价。针对双抗与抗原pcsk9的结合活性,本次实验使用fortebio公司的octet red 96e型分子相互作用分析仪进行检测。使用protein a探针(fortebio)先分别捕获候选抗体分子(浓度为5μg/ml)。再将探针分别浸入30nm或120nm的人pcsk9抗原溶液中,使候选抗体分子与抗原结合时间为180s。然后将探针浸入缓冲液中,解离时间为1400s,测量结合与解离信号。使用软件octet data analysis software拟合结合解离曲线来确定亲和力kd值。
[0391]
结果如图13-14和表10所示,对照抗体pd-1vhh结合pd-1蛋白的ec
50
为5.3ng/ml,而抗pd-1/pcsk9-1和抗pd-1/pcsk9-2双抗与pd-1蛋白的ec
50
为分别为14.9ng/ml和64.1ng/ml。pd-1端的细胞生物学活性方面,对照抗体pd-1vhh的ec
50
为0.5μg/ml,而抗pd-1/pcsk9-1和抗pd-1/pcsk9-2双抗的ec
50
分别为0.9μg/ml和4.0μg/ml。综合来看,抗pd-1/pcsk9-2的pd-1结合活性降低较明显,本发明抗pd-1/pcsk9-1的抗原的亲和力及pd-1端的生物学活性与对照抗体pd-1vhh基本相当。此外,pcsk9端的抗原结合活性方面,对抗pd-1/tgf-β双抗与对照抗体基本相当。这些数据说明本发明抗pd-1/pcsk9-2双抗结构基本不影响pd-1端和pcsk9端的生物学活性。
[0392]
表10.抗-pd-1/psck9双特异性抗体的生物学活性
[0393][0394]
实施例3.双特异性抗体的体内活性检测
[0395]
使用pd-1人源化小鼠模型对双特异性抗体的动物体内活性进行评价。基本步骤如下:取6-8周龄雌性hpd-1c57/b6小鼠(pd-1基因人源化小鼠,购自百奥塞图),将1
×
106个mc38细胞接种小鼠的右侧皮下,待肿瘤生长到约100mm3时将小鼠按肿瘤体积随机分组(每组5只),包括溶媒对照组(vehicle,pbs)、pd-1vhh单抗组、阳性对照opdivo analogue组以及本发发明的双特异性抗体给药组(抗-pd-1/vegf、抗-pd-1/tgf-β和抗-pd-1/pcsk9双特异性抗体),具体药物信息和剂量详见图注。所有组的给药途径均为腹腔注射,每周给药2次,连续给药5~6次,每周测量肿瘤体积2次并记录肿瘤体积。实验结束时将小鼠安乐死。根据肿瘤体积计算相对肿瘤抑制率tgi%=(1-(ti-t0)/(vi-v0))
×
100%。(ti:治疗组或阳性对照组在给药第i天的肿瘤体积均值;t0:治疗组或阳性对照组在给药第0天的肿瘤体积均值;vi:阴性对照组在给药第i天的肿瘤体积均值;v0:阴性对照组在给药第0天的肿瘤体
积均值)。
[0396]
如图16所示,在首次给药后第25天,与阴性对照组相比,pd-1vhh单抗组、阳性对照opdivo analogue组和抗-pd-1/vegf双抗组的相对肿瘤抑制率tgi%分别为87.3%、92.3%和83.1%。表明本发明抗-pd-1/vegf双抗能够在体内抑制hpd-1人源化小鼠mc38皮下移植瘤的生长,且抑瘤作用与pd-1vhh单抗或阳性对照opdivo analogue类似。如图17所示,在首次给药后第18天,与阴性对照组相比,pd-1vhh单抗组、阳性对照opdivo analogue组、抗-pd-1/tgf-β双抗组和抗-pd-1/pcsk9双抗组的相对肿瘤抑制率tgi%分别为86.6%、77.2%、95.0%和91.2%。表明本发明抗-pd-1/tgf-β双抗和抗-pd-1/pcsk9双抗能够在体内抑制hpd-1人源化小鼠mc38皮下移植瘤的生长,且抑瘤作用类似或优于pd-1vhh单抗或阳性对照opdivo analogue。
[0397]
由以上结果可知,本发明的双特异性抗体的体内活性优于单克隆抗体,为后续产品开发奠定基础。
[0398]
实施例4.基于其它pd-1vhh的双特异性抗体的表达和纯化
[0399]
本发明人还利用来源于中国发明专利申请(申请号:2021100481961,靶向pd-1的单域抗体及其衍生物和用途,其内容通过引用全文纳入本文)的其它pd-1vhh抗体序列作为双特异性抗体中pd-1母本抗体的序列。选取了克隆ll-vhh01、huvhh3-1、huvhh3-2、huvhh3-4、huvhh3-5和huvhh3-6构建双特异性抗体。
[0400]
其中,ll-vhh01的氨基酸序列:
[0401]
qlqlvesggglvqaggslrlscaasgrtssmyamgwfrqspgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlkpedaavyfcaaqigisgtlgdywgqgtqvtvss(seq id no:56);
[0402]
huvhh3-1的氨基酸序列:
[0403]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgkgrefvagigwenntpyyarsvegrftisrdnvkntvylqmnslraedtavyycaaqigisgtlgdywgqgtqvtvss(seq id no:57)
[0404]
huvhh3-2的氨基酸序列为:
[0405]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvylqmnslraedtavyycaaqigisgtlgdywgqgtqvtvss(seq id no:58)
[0406]
huvhh3-4的氨基酸序列为:
[0407]
evqlvesggglvqpggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlkpedtavyycaaqigisgtlgdywgqgtqvtvss(seq id no:59)
[0408]
huvhh3-5的氨基酸序列为:
[0409]
elqlvesggglvqaggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlkpedtavyycaaqigisgtlgdywgqgtqvtvss(seq id no:60)
[0410]
huvhh3-6的氨基酸序列为:
[0411]
elqlvesggglvqaggslrlscaasgrtssmyamgwfrqapgnerefvagigwenntpyyarsvegrftisrdnvkntvflqmnrlkpedaavyfcaaqigisgtlgdywgqgtqvtvss(seq id no:61)。
[0412]
结果发现,这些双特异性抗体均能够具备与上述双特异性抗体相同或相似的体外或体内活性。
[0413]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可
以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1