一种检测回复突变的探针库、检测方法以及试剂盒与流程
1.本发明涉及基因检测领域,具体而言,本发明涉及一种检测brca1、brca2、palb2、 rad51c、rad51d基因回复突变的探针及检测方法。该方法可以精准地富集brca1、brca2、 palb2、rad51c、rad51d基因外显子突变序列,所得dna样本库可进一步结合下一代测序技术(ngs),精准地判断病人的brca1、brca2、palb2、rad51c、rad51d基因回复突变情况,并为相关肿瘤的诊断,预后,及临床治疗方案的设计提供指导及理论基础。
背景技术:
2.同源重组修复(homologous recombination repair,hrr)通路是一种dna双链损伤的重要修复方式,其中brca1和brca2基因编码蛋白是该通路的关键蛋白,此外参与该通路的基因还包括palb2、rad51c、rad51d等。如果brca1/2基因或其它hrr基因出现突变导致蛋白失去功能,就会引起hrr功能异常,即出现dna同源重组缺陷(homologous recombinationdeficiency,hrd),此类癌细胞对铂类药物和多聚腺苷二磷酸核糖聚合酶抑制剂(polyadenosine diphosphate
–
ribose polymerase inhibitor,parpi)parp抑制剂的敏感性相关。parp抑制剂基于“合成致死”效应来杀死存在错配修复基因缺陷的癌细胞。目前已有多款parp抑制剂先后获批上市,在卵巢癌,乳腺癌,胰腺癌等治疗中取得巨大成功,在抗肿瘤领域占有重要地位。然而,parp抑制剂治疗过程中随之而来的耐药问题也受到了研究者的关注。研究发现,parp抑制剂耐药机制是多因素的,其中一个重要的耐药机制为:同源重组信号通路的恢复中报道较多的是brca1/2基因回复突变(reverse mutation)。
3.brca1/2基因回复突变是一种体细胞突变,它可以恢复现有生殖系和/或体细胞功能缺失的brca1/2基因突变的开放阅读框(orf),重建brca蛋白功能,使细胞恢复同源重组修复的功能,从而导致细胞对parp抑制剂和dna损伤因子的敏感性降低。回复突变的类型包括小的插入与缺失(indels)、单核苷酸变异(snv)、基因内大片段缺失(large genomicrearrangement,lgr),且不仅与原发突变是顺式关系(cis),还呈现多克隆异质性,同一个标本的回复突变可能多达十几或几十种。目前检测大片段重排最常用的方法为多重连接探针扩增技术(multiplex ligation
‑
dependent probe amplification,mlpa),但该方法通量低、周期长,无法及时出结果来指导临床治疗方案的制定。
4.除了brca1/2基因发生回复突变外,其他hrr基因也可能出现回复突变,影响治疗疗效。有研究显示,携带生殖系brca1、brca2突变患者检测到回复突变的比例分别为11%(1/9)、 24%(8/33)。除brca1/2外,在palb2、rad51c、rad51d基因中,也检出过回复突变,同样可以恢复原有生殖系和/或体细胞功能缺失的基因突变的开放阅读框(orf),重建蛋白功能,使细胞恢复同源重组修复的功能。
技术实现要素:
5.针对上述技术问题,本发明人通过大量实验,开发了用于检测brca1、brca2、palb2、 rad51c、rad51d基因回复突变的方法,该方法利用探针液相捕获、二代测序技术,不
仅可以实现几千倍地富集的brca1、brca2、palb2、rad51c、rad51d基因外显子及其附近内含子的dna片段,而且实现了较高的检测特异性和敏感性。
6.本发明同时在采用上述的探针库进行相关临床样本检测中,找到了新的应用于铂类化疗药物耐药评估的标志物,
7.一种检测回复突变的探针库,所述的回复突变包括brca1、brca2、palb2、rad51c、 rad51d基因回复突变,所述的探针库中包含有核苷酸序列如seq id no.1~192所示的探针,或者与其具有相同功能的探针。
8.所述的具有相同功能的探针是指具有80%、90%或者95%以上相同的碱基。
9.一种检测回复突变的方法,包括如下步骤:
10.步骤1,提取样本的dna并进行片段化;
11.步骤2,将片段化的dna与探针库中的探针进行杂交,富集后并分离;
12.步骤3,将分离的dna片段进行扩增后进行测序。
13.所述的步骤1中,片段化是指将dna破碎150~200bp。
14.所述的步骤2中,通过探针上的生物素和磁珠上的链霉亲和素的相互作用进行富集。
15.一种用于检测回复突变的试剂盒,其含有上述的探针库。
16.本发明第三个目的,提供了:
17.用于检测palb2基因回复突变的试剂在用于制备检测乳腺癌患者对铂类药物耐药的试剂中的应用。
18.本发明第四个目的,提供了:
19.用于检测brca2基因回复突变的试剂在用于制备检测结肠癌患者对铂类药物耐药的试剂中的应用。
20.本发明第五个目的,提供了:
21.用于检测rad51d基因回复突变的试剂在用于制备检测乳腺癌患者对铂类药物耐药的试剂中的应用。
22.所述的铂类药物选自顺铂、锡铂、顺氯氨铂、奈达铂、依铂、卡波铂、碳铂、洛铂、奥沙利铂、诺贝铂或者赛特铂。
23.有益效果
24.本发明提供了一种具有较高检测灵敏度的用于检测brca1、brca2、palb2、rad51c、 rad51d基因回复突变的检测探针库以及检测方法。
25.本发明同时也找到了新的用于对铂类药物耐药的回复突变靶点,可以更好地用于临床治疗效果评估。
附图说明
[0026][0027]
图1为本发明的探针覆盖范围示意图。
[0028]
图2是上机测序结果示意图。
[0029]
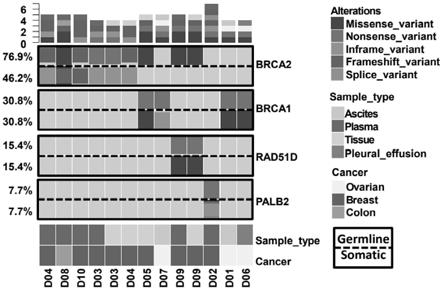
图3是患者耐药后的分析结果。
具体实施方式
[0030]
下面通过具体实施方式对本发明作进一步详细说明。但本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
[0031]
在本文中所使用的术语”dna”为脱氧核糖核酸(英文:deoxyribonucleicacid,缩写为 dna)是一种由脱氧核糖核苷酸组成的双链分子。可组成遗传指令,引导生物发育与生命机能运行,其碱基排列顺序构成了遗传信息,所以在遗传病的诊断中具有重要的作用。
[0032]
在本文中所使用的术语“高通量测序技术”指的是第二代高通量测序技术及之后发展的更高通量的测序方法。第二代高通量测序平台包括但不限于illumina
‑
solexa(miseq、hiseq
‑
2000、 hiseq
‑
2500、hiseq x ten等)、abi
‑
solid和roche
‑
454测序平台等。随着测序技术的不断发展,本领域技术人员能够理解的是还可以采用
[0033]
其他方法的测序方法和装置进行本检测。根据本发明的具体示例,可以将根据本发明实施例的核酸标签用于illumina
‑
solexa、abi
‑
solid和roche
‑
454测序平台等的至少一种进行测序。高通量测序技术,例如miseq测序技术具有以下优势:(1)高灵敏度:高通量测序,例如miseq的测序通量大,目前一个实验流程下来可以产生最多15g碱基数据,高的数据通量可以再测序序列数确定的情况下,使得每条序列获得高的测序深度,所以可以检测到含量更低的突变,同时因其测序深度高,其测序结果也更为可靠。(2)高通量,低成本:利用根据本发明实施例的标签序列,通过一次测序可以检测上万份样本,从而大大降低了成本。
[0034]
本发明中的“突变”、“核酸变异”、“基因变异”可通用,本发明中的“snp”(snv)、“cnv”、“插入缺失”(indel)和“结构变异”(sv)同通常定义,但本发明中对各种变异的大小不作特别限定,这样这几种变异之间有的有交叉,比如当插入/缺失的为大片段甚至整条染色体时,也属于发生拷贝数变异(cnv)或是染色体非整倍性,也属于sv。这些类型变异的大小交叉并不妨碍本领域人员通过上述描述执行实现本发明的方法和/或装置并且达到所描述的结果。
[0035]
dna样本的提取和片段化
[0036]
采用商品化的dna提取试剂盒对组织样本、血浆样本、腹水样本或者胸水样本进行dna 的提取,通过nanodrop和qubit进行定量质控,对于组织和胸腹水dna样本,由于dna片段较长,需要采用超声破碎。
[0037]
dna样本的纯化及末端修复
[0038]
将上述步骤得到的dna样本加无酶水补齐至100ul,再加入150ul的axygen beads磁珠,重悬后磁力分离除上清,并加入200ul的80%乙醇洗涤于磁力架上孵育后去乙醇,干燥至所有乙醇挥发干净;加入28ul无酶水混合均匀,将dna从磁珠上洗脱下来,取1ug进入末端修复,加无水酶补至25ul。加入末端修复试剂于适当条件下进行末端修复。
[0039]
接头连接及产物纯化
[0040]
使用浓度为15um的通用接头,并根据进入末端修复的dna总量进行接头稀释工作。向接头连接反应液中加入如下试剂:
[0041][0042]
将上述反应液短暂离心后,至于pcr仪上于20℃孵育15分钟后,在上述反应液加入 9.5ulaxygen beads重悬,磁力分离后除上清,再加入200ul的80%乙醇清洗,于室温下孵育后去乙醇,晾干,加20ul无酶水洗脱磁珠。
[0043]
文库扩增
[0044]
上述的纯化产物采用如下所示的反应体系进行pcr扩增,使产物达到测序要求。
[0045][0046]
扩增条件为:98℃预变性45秒,98℃变性15秒,65℃退火30秒,72℃延伸30秒,循环12次;72℃延伸1分钟。
[0047]
探针的设计、dna片段的捕获和富集
[0048]
针对5个hrr基因(brca1、brca2、palb2、rad51c、rad51d)外显子准备dna 探针库。本领域技术人员知晓:捕获的特异性受各种因素影响,如捕获探针的设计不佳,捕获条件不理想,基因组dna中重复序列的封闭不充分及基因组dna与捕获探针的比例不合适等因素都会影响捕获的特异性、敏感性、测序覆盖率等诸多结果。为了实现目标基因的高度富集和低脱靶率,本领域技术人员需要对探针的类型、长度、序列、杂交条件等进行大量实验摸索,需要通过创造性的探索工作才能够获得最佳的参数组合,如果探针特异性太高,在dna捕获时就会产生有利于参考序列(与探针完全互补的序列)的选择,这在后期数据统计上就会产生明显的偏差,同时太短的探针结合目标dna片段的结合力度不足以将目标 dna捕获下来;而探针太长,探针合成的效率降低,并且合成成本大大增加。探针设计策略见图1和图2。其中,侧翼序列长度为内含子序列,内含子序列的重复性较高。探针重叠区域为每个探针之间的重叠碱基数目。重叠区域越大,目标区域覆盖率越高;重叠区域越小,甚至探针间隔分布,测序成本则越低。探针长度越长,测序时对于单核苷酸多态性(snp) 的容忍度越高。最终合成得到的探针序列如seq id no.1
‑
192所示,且5’端有生物素(biotin)。
[0049]
将dna样本库与杂交缓冲液(10mmtris
‑
hcl,2%牛血清白蛋白,ph8.0)混合(混合后, dna样本库浓度至多不超过50ng/ul),反应条件为95℃5分钟,之后保持在65℃。反应在 pcr扩增仪中进行。然后以dna样本库:探针库为1:100的摩尔比,将探针库加入上述混合物,反应条件为65℃5分钟。将杂交反应置于pcr扩增仪中,65℃孵育24小时。
[0050]
将50ul的dynabeads磁珠与200ul结合缓冲液(含10mm tris
‑
hcl、2%bsa)进行混合,并通过磁选机分离出磁珠,重复3次;再将杂交反应产物与链霉亲和素磁珠混合,在磁选机中分离后,向磁珠中加入500ul的洗涤缓冲液(含有0.1%tween
‑
20、0.1%sds),并于60℃下孵育15min,重复3次;将磁珠与50ul的洗脱缓冲液(含有10mm的naoh)混合,20℃下孵育15min,通过磁选机分离出磁珠,上清液中获得检测文库。
[0051]
上述的文库采用如下所示的反应体系进行pcr扩增,使产物达到测序要求。
[0052][0053]
扩增条件为:98℃预变性45秒,98℃变性20秒,65℃退火30秒,72℃延伸25秒,循环5次;72℃延伸3分钟。
[0054]
测序与分析
[0055]
使用illumina hiseq2000下一代测序系统进行测序,并进行数据分析,获得基因突变信息。
[0056]
探针设计的优化
[0057]
根据上述的探针设计思路,在设定于2x覆盖倍数的条件下考察了探针长度对于测序结果的影响,分别测试了100bp/120bp/140bp长度的探针,每次实验重复三次,结果如下:
[0058][0059]
通过以上的测试可以看出,长度为140bp的探针具有最高的中靶率,而100bp探针最低, 120bp的探针与140bp的接近,从经济的角度上来看,优选采用120bp。
[0060]
另外,在设定于120bp长度探针的情况下考察了覆盖倍数对于测序结果的影响,分别测试了1x、1.5x、2x和2.5x,结果如下:
[0061][0062]
并且我们分析了每个探针目标区域dna序列的测序深度,结果如下:
[0063][0064][0065]
注:>0.2x平均覆盖占比的意思是大于目标区域dna序列平均覆盖倍数20%的区域在总区域中的占比,同理0.5x和1x平均覆盖占比的意思是大于目标区域平均覆盖倍数50%/100%的区域在总区域中的占比。
[0066]
根据测序结果可以得到,随着探针覆盖倍数的增加,目标区域的平均覆盖倍数逐渐增加,并且均一性更好。但是外显子的探针捕获效率与内含子的探针捕获效率不一样,外
显子在2x 探针覆盖的情况下可以得到较好的目标区域覆盖,而内含子在2.5x探针覆盖的情况下才能得到与2x探针外显子类型的目标区域覆盖。综合中靶率、经济性,最后选择2x的探针作为外显子区域的覆盖倍数,选择2.5x探针作为内含子预期的覆盖倍数。
[0067]
采用下一代测序技术检测brca1、brca2、palb2、rad51c、rad51d的基因结构突变对临床诊疗的指导价值。
[0068]
对13例存在回复突变的患者样本和7例阴性样本进行dna提取,并通过本发明优选的探针和方法进行测序,结果中见下表,阳性样本和阴性样本的测序结果与mlpa/sanger测序法所得结果相同,证明了本方法的可靠性,结果见表1。
[0069]
1、本发明的探针组合可用于经铂类药物治疗进展患者的耐药机制检测。
[0070]
从世和基因生物技术股份有限公司数据库中随机筛选出10例患者铂类药物治疗进展的患者,这10例患者样本携带brca1、brca2、palb2、rad51d等基因的种系突变,并且耐药后样本中检测到相关基因的继发体细胞回复突变。其中6例患者为乳腺癌,3例卵巢癌,1例结肠癌。本发明的探针组合不仅能检测相关基因的种系突变,还能检测基因继发体细胞回复突变。检测的突变类型具有多样性,包括错义突变、移码突变、非移码突变、大片段缺失突变、无义突变等。7例患者检测到基因种系无义突变,其中4例患者在耐药样本中检测到基因对应氨基酸上的错义突变,其他3例患者是检测基因对应氨基酸前的非移码突变,可能恢复开放阅读框架,导致药物耐药。对于临床耐药机制探究,指导患者临床转归具有重要意义。患者耐药回复突变见表2。
[0071]
2、本发明的探针组合检测的样本类型具有多样性。
[0072]
10例铂类/parp抑制剂治疗进展的患者合计检测了16个样本,其中13个样本中检测到了回复突变,包括4个组织样本(4/5)、6个血浆样本(6/8)、2个腹水样本(2/2)、1个胸水样本(1/1)。100%的胸水和腹水样本中检测hrr种系突变和体细胞回复突变。此外有一例患者组织样本中未检测到回复突变,但是其胸水样本中检测到相关回复突变,说明组织可能由于时间或空间异质性问题,导致耐药突变漏检,而血浆或胸腹水等体液样本可以克服肿瘤异质性,揭示患者耐药机制。患者耐药后如图3所示。
[0073]
表1本发明探针ngs测序结果与mlpa/sanger测序结果比对表
[0074][0075]
续表1
[0076][0077]
表2本发明探针检测基因继发耐药的回复突变结果
[0078]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1