嗜酸乳杆菌LA-03在制备抗幽门螺杆菌药物中的应用的制作方法
嗜酸乳杆菌la-03在制备抗幽门螺杆菌药物中的应用
技术领域
1.本发明涉及微生物技术领域,更具体的说是涉及嗜酸乳杆菌la-03在制备抗幽门螺杆菌药物中的应用。
背景技术:
2.幽门螺杆菌是一种导致一系列胃病的主要病原体,可引起胃十二指肠炎症、消化性溃疡和胃癌。幽门螺杆菌感染可诱导促炎细胞因子和趋化因子的产生,如白介素-1β(il-1β)、白介素-6(il-6)、白介素-8(il-8)、肿瘤坏死因子-α(tnf-α),导致以浆细胞、淋巴细胞、中性粒细胞和单核细胞浸润胃黏膜为特征的胃炎症。胃上皮细胞分泌的il-8是一种有效的中性粒细胞激活和趋化剂,在幽门螺杆菌引起的粘膜炎症中起主要作用。据报道,幽门螺杆菌感染患者的胃液和活检样本中il-8水平升高。此外,幽门螺杆菌感染患者胃黏膜中il-8mrna的水平与胃炎的严重程度和胃癌的风险显著相关。
3.使用质子泵抑制剂或雷尼替丁柠檬酸铋联合两种抗生素的三联疗法是幽门螺杆菌感染最常推荐的治疗方法。抗生素治疗对幽门螺杆菌感染并不总是有效的,因为抗生素耐药性是一个日益严重的世界问题。此外,不建议对所有无症状的幽门螺杆菌感染者使用抗生素治疗。因此,有必要开发替代方法。
4.益生菌已被证明具有有益的效果,并被推荐作为治疗幽门螺杆菌的辅助药物。大量研究表明益生菌具有抑制胃上皮细胞分泌促炎细胞因子的作用,并被认为是预防胃癌的一种方法。唾液乳杆菌ucc118通过降低幽门螺杆菌cag分泌系统的功能来抑制幽门螺杆菌诱导胃上皮细胞ags分泌il-8。此外,加氏乳酸杆菌oll2716能抑制幽门螺杆菌诱导胃上皮细胞mkn45分泌il-8,并降低幽门螺杆菌感染患者胃粘膜中il-8的水平。商业益生菌约氏乳杆菌la1的发酵上清液减少了幽门螺杆菌在体外模型和动物模型中的存活率。
5.然而,当前国际益生菌专利申请集中于美、日、俄传统研发强国,而我国缺乏拥有自主知识产权的功能性菌株。国内生产企业所用益生菌菌种长期依赖进口,而且国外菌株未必适合我国居民胃肠道生理状况。另外,益生菌的功能缺乏有力的科学研究证据,严重影响了益生菌及其制品的推广。基于此,针对菌种资源的功能深入挖掘,筛选出拥有自主知识产权、具有特定功能性质、适合中国人群生理特性的新型益生菌菌株,对提高我国益生菌生产企业的核心竞争力,促进我国益生菌制品发展尤为重要。
6.因此,提供嗜酸乳杆菌la-03在制备抗幽门螺杆菌药物中的应用是本领域技术人员亟需解决的问题。
技术实现要素:
7.有鉴于此,本发明提供了嗜酸乳杆菌la-03在制备抗幽门螺杆菌药物中的应用。
8.为了实现上述目的,本发明采用如下技术方案:
9.嗜酸乳杆菌(lactobacillus acidophilus)la-03在制备抗幽门螺杆菌药物中的应用,所述嗜酸乳杆菌la-03的保藏编号为cgmcc no.22239,已保藏于中国微生物菌种保藏
管理委员会普通微生物中心,简称cgmcc,地址北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,保藏日期为2021年04月25日,分类命名为嗜酸乳杆菌lactobacillus acidophilus。
10.进一步,所述的嗜酸乳杆菌la-03在制备治疗幽门螺杆菌引起的炎症药物中的应用。
11.进一步,所述嗜酸乳杆菌la-03为菌悬液或发酵上清液。
12.进一步,所述菌悬液或发酵上清液显著抑制幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8。
13.本发明所述嗜酸乳杆菌la-03,能显著抑制幽门螺杆菌生长,以及显著抑制幽门螺杆菌对胃上皮细胞ags的粘附,表现出良好的抗幽门螺旋杆菌的益生功效;同时该菌株显著抑制幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8,表现出良好的改善幽门螺杆菌引起炎症反应的作用。
14.本发明所述显著抑制幽门螺杆菌生长,和显著抑制幽门螺杆菌对胃上皮细胞ags的粘附,以及显著抑制幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8的菌株la-03,包括菌株la-03的发酵上清液(胞外分泌物)、菌悬液(菌体)。
15.经由上述的技术方案可知,与现有技术相比,本发明公开提供了嗜酸乳杆菌la-03在制备抗幽门螺杆菌药物中的应用,嗜酸乳杆菌la-03是从广东省广州市农家自然发酵泡菜液中分离筛选得到的,具有显著抑制幽门螺杆菌生长,和显著抑制幽门螺杆菌对胃上皮细胞ags的粘附,以及显著抑制幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8的潜能,此为利用嗜酸乳杆菌la-03开发抗幽门螺旋杆菌的益生菌制剂提供理论参考和指导依据。
附图说明
16.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
17.图1附图为本发明嗜酸乳杆菌la-03形成的菌落形态图;
18.图2附图为本发明嗜酸乳杆菌la-03革兰氏染色后的显微形态观察;
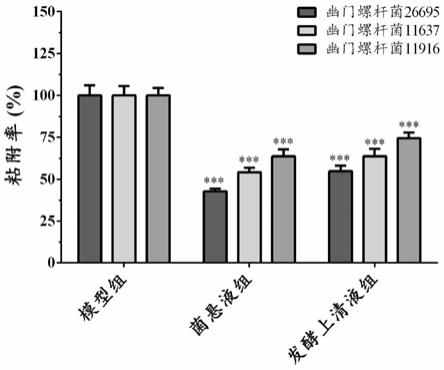
19.图3附图为本发明嗜酸乳杆菌la-03的发酵上清液、菌悬液对幽门螺杆菌粘附胃上皮细胞ags的影响;
20.图4附图为本发明嗜酸乳杆菌la-03的发酵上清液、菌悬液对幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8的影响。
具体实施方式
21.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
22.实施例1嗜酸乳杆菌la-03分离、鉴定及保藏
23.(1)分离:将辣白菜发酵液经梯度稀释后,分别接种于bhi固体培养基、tpy固体培养基、mrs固体培养基和bds固体培养基中,37℃厌氧培养48h,挑取平板上的单菌落划线分离得到纯菌落。将平板上的纯菌落接种于mrs液体培养基中,37℃厌氧培养12~16h,加入20%甘油,置于-80℃冰箱中保存。
24.(2)菌株形态学鉴定:对筛选出的菌株革兰氏染色后于显微镜下观察,革兰氏阳性菌呈紫色,革兰氏阴性菌呈红色。
25.(3)菌株的分子生物学鉴定:对所获得的菌株提取基因组dna,通过pcr技术利用16s rdna通用引物27f和1492r扩增16s rdna全长片段,之后进行测序,鉴定菌株的种属。
26.其中,通用引物27f和1492r的引物序列如下:
27.27f:5
’‑
agagtttgatcctggctcag-3’;seq id no.1;
28.1492r:5
’‑
ggttaccttgttacgactt-3’;seq id no.2。
29.实验结果:从广东省广州市农家自然发酵泡菜液中筛选出的菌株,经形态观察、16s rdna鉴定,其中菌株la-03被鉴定为嗜酸乳杆菌,其16s rdna序列如seq id no.3所示。
30.agacggctccttcccgaggttaggccaccggctttgggcattgcagactcccatggtgtgacgggcggtgtgtacaaggcccgggaacgtattcaccgcggcgtgctgatccgcgattactagcgattccagcttcgtgcagtcgagttgcagactgcagtccgaactgagaacagctttaagagattcgcttgccttcgcaggcttgctcctcgttgtactgtccattgtagcacgtgtgtagcccaggtcataaggggcatgatgacttgacgtcatccccaccttcctccggtttgtcaccggcagtctcattagagtgcccaacttaatgctggcaactaatgacaagggttgcgctcgttgcgggacttaacccaacatctcacgacacgagctgacgacagccatgcaccacctgtcttagtgtccccgaagggaactccgtatctctacggattgcactagatgtcaagacctggtaaggttcttcgcgttgcttcgaattaaaccacatgctccaccgcttgtgcgggcccccgtcaattcctttgagtttcaaccttgcggtcgtactccccaggcggagtgcttaatgcgttagctgcagcactgagaggcggaaacctcccaacacttagcactcatcgtttacggcatggactaccagggtatctaatcctgttcgctacccatgctttcgagcctcagcgtcagttgcagaccagagagccgccttcgccactggtgttcttccatatatctacgcattccaccgctacacatggagttccactctcctcttctgcactcaagaaaaacagtttccgatgcagttcctcggttaagccgagggctttcacatcagacttattcttccgcctgcgctcgctttacgcccaataaatccggacaacgcttgccacctacgtattaccgcggctgctggcacgtagttagccgtgactttctggttgattaccgtcaaataaaggccagttactacctctatccttcttcaccaacaacagagctttacgatccgaaaaccttcttcactcacgcggcgttgctccatcagactttcgtccattgtggaagattccctactgctgcctcccgtaggagtttgggccgtgtctcagtcccaatgtggccgatcagtctctcaactcggctatgcatcattgccttggtaggccgttaccctaccaactagctaatgcaccgcggggccatcccatagcgacagcttacgccgccttttataagctgatcatgcgatctgctttcttatccggtattagcacctgtttccaagtggtatcccagactatggggcaggttccccacgtgttactcacccatccgccgctcgcgttcccaacgtcatcaccgaagtgaatctgttggttcagctcgctcgactgcatgtatag;seq id no.3。
31.菌株la-03单菌落接种到mrs固体培养基上,37℃厌氧生长良好,菌落白色、呈球形、表面光滑、不透明、边缘整齐(图1),革兰氏染色呈阳性(图2)。菌株la-03已保藏于中国微生物菌种保藏管理委员会普通微生物中心,简称cgmcc,地址北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,保藏日期为2021年04月25日,分类命名为嗜酸乳杆菌lactobacillus acidophilus,保藏编号为cgmcc no.22239。
32.实施例2嗜酸乳杆菌la-03发酵上清液(胞外分泌物)、菌悬液(菌体)的制备
33.将嗜酸乳杆菌la-03活化培养后接种于mrs液体培养基中,37℃培养15h后,调整发酵菌浓度为1.5
×
107cfu/ml,4℃,6000r/min离心10min,得到培养上清液和菌体沉淀,上清液经0.22μm滤膜过滤后得发酵上清液(胞外分泌物);菌体沉淀经pbs两次洗涤后,将菌体用pbs重新悬浮,调整细胞浓度为1.5
×
107cfu/ml得到菌悬液(菌体)。
34.实施例3嗜酸乳杆菌la-03对幽门螺杆菌生长的抑制作用
35.将100μl浓度均为1
×
108cfu/ml的幽门螺杆菌26695(atcc 700392)、幽门螺杆菌11637(atcc 43504)、幽门螺杆菌11916(atcc 43526)分别均匀涂布在哥伦比亚琼脂平板上(平板直径90mm),不含抗生素。然后在每个哥伦比亚琼脂平板上放入3个牛津杯,并向3个牛津杯中分别加入120μl嗜酸乳杆菌la-03菌悬液、120μl发酵上清液、120μl pbs,将平板在微需氧条件下于37℃孵育72h,然后测量抑菌圈的直径。pbs作为空白对照组。实验重复3次。
36.采用spss 19.0软件统计处理数据,实验数据均用x
±
sem数据表示,用单因素方差分析。与空白对照组相比:***p《0.005。
37.嗜酸乳杆菌la-03对幽门螺杆菌生长的抑制作用结果见表1。
38.表1嗜酸乳杆菌la-03对幽门螺杆菌生长的影响
[0039][0040]
由表1可知,与空白对照组相比,嗜酸乳杆菌la-03的菌悬液均显著抑制幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916的生长(p《0.005),抑菌圈直经分别为10.04
±
0.63mm、10.19
±
0.26mm和9.52
±
0.42mm。另外,嗜酸乳杆菌la-03的发酵上清液对幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916的生长均具有抑制作用,抑菌圈直经分别为12.20
±
0.65mm、11.43
±
0.54mm和10.82
±
0.28mm,与空白对照组相比较均差异性显著(p《0.005)。上述结果表明,嗜酸乳杆菌la-03菌悬液和发酵上清液对幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916均有较好的抑制作用。
[0041]
实施例4嗜酸乳杆菌la-03对幽门螺杆菌粘附胃上皮细胞ags的影响
[0042]
将对数生长期的胃上皮细胞ags,经胰酶消化、吹打制备成细胞数为5
×
105个/ml的细胞悬液,接种于24孔细胞培养板中,每孔0.5ml,置37℃、5%co2培养箱中孵育24h,吸弃上清液,然后每孔加入0.5ml rpmi 1640培养液,进行分组试验。空白对照组和模型组均加入50μl无菌pbs,菌悬液组加入50μl嗜酸乳杆菌la-03的菌悬液,发酵上清液组加50μl嗜酸乳杆菌la-03的发酵上清液,孵育2h后,空白对照组加入50μl无菌pbs,模型组、菌悬液组、发酵上清液组均加入50μl 1.5
×
107cfu/ml幽门螺杆菌菌悬液(幽门螺杆菌26695、幽门螺杆菌11637或幽门螺杆菌11916),再孵育2h后,用无菌pbs将每孔洗涤3次以去除未粘附的幽门螺杆菌。最后,每孔加入500μl脲酶试剂(7mm磷酸盐缓冲液,ph 6.8、110mm尿素、10mg/l酚红),37℃下孵育1h后,使用酶标仪在560nm波长处测定od值。每组分别设6个复孔。幽门螺杆
菌对胃上皮细胞ags的粘附率计算如下:
[0043][0044]
采用spss 19.0软件统计处理数据,实验数据均用x
±
sem数据表示,用单因素方差分析。与模型组比较:*p《0.05,**p《0.01,***p《0.005。
[0045]
结果见图3;由图3可知,与模型组(幽门螺杆菌26695:100.00
±
6.15%、幽门螺杆菌11637:100.00
±
5.64%、幽门螺杆菌11916:100.00
±
4.56%)相比,嗜酸乳杆菌la-03的菌悬液均显著抑制幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916对胃上皮细胞ags的粘附(p《0.005),粘附率分别为42.78
±
1.55%、54.17
±
2.69%、63.65
±
4.10%。另外,嗜酸乳杆菌la-03的发酵上清液对幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916粘附胃上皮细胞ags均具有抑制作用,粘附率分别为54.73
±
3.35%、63.69
±
4.50%、74.42
±
3.38%,与模型组(幽门螺杆菌26695:100.00
±
6.15%、幽门螺杆菌11637:100.00
±
5.64%、幽门螺杆菌11916:100.00
±
4.56%)相比较均差异性显著(p《0.005)。上述结果表明,嗜酸乳杆菌la-03菌悬液和发酵上清液均抑制幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916对胃上皮细胞ags的粘附。
[0046]
实施例5嗜酸乳杆菌la-03对幽门螺杆菌诱导胃上皮细胞ags分泌炎症因子il-8的影响
[0047]
将对数生长期的胃上皮细胞ags,经胰酶消化、吹打制备成细胞数为4
×
104个/ml的细胞悬液,接种于24孔细胞培养板中,每孔1ml,置37℃、5%co2培养箱中孵育24h,吸弃上清液,然后每孔加入0.5ml rpmi 1640培养液,进行分组试验。空白对照组和模型组均加入50μl无菌pbs,菌悬液组加入50μl嗜酸乳杆菌la-03的菌悬液,发酵上清液组加50μl嗜酸乳杆菌la-03的发酵上清液,孵育30min后,空白对照组加入50μl无菌pbs,模型组、菌悬液组、发酵上清液组均加入50μl 1.5
×
107cfu/ml幽门螺杆菌菌悬液(幽门螺杆菌26695、幽门螺杆菌11637或幽门螺杆菌11916),置37℃、5%co2培养箱中孵育24h,收集细胞上清,用elisa试剂盒(南京草本源生物科技有限公司)检测il-8的分泌。每组分别设6个复孔。
[0048]
采用spss 19.0软件统计处理数据,实验数据均用x
±
sem数据表示,用单因素方差分析。与空白对照组相比:
###
p《0.005;与模型组相比:**p《0.01,***p《0.005。
[0049]
结果见图4;由图4可知,与空白对照组(245.18
±
5.46pg/ml)相比,模型组的炎症因子il-8分泌量(幽门螺杆菌26695:872.38
±
29.57pg/ml、幽门螺杆菌11637:858.74
±
21.03pg/ml、幽门螺杆菌11916:875.09
±
28.58pg/ml)显著增加(p《0.005),说明本次幽门螺杆菌刺激有效。
[0050]
与模型组(幽门螺杆菌26695:872.38
±
29.57pg/ml、幽门螺杆菌11637:858.74
±
21.03pg/ml、幽门螺杆菌11916:875.09
±
28.58pg/ml)相比,嗜酸乳杆菌la-03的菌悬液均显著抑制幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916诱导胃上皮细胞ags分泌炎症因子il-8(p《0.01),炎症因子il-8分泌量分别为610.27
±
20.69pg/ml、652.19
±
28.25pg/ml、677.31
±
23.75pg/ml。另外,嗜酸乳杆菌la-03的发酵上清液对幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916诱导粘附胃上皮细胞ags分泌炎症因子il-8均具有抑制作用,炎症因子il-8分泌量分别为469.05
±
21.68pg/ml、514.62
±
14.82pg/ml、
601.17
±
27.12pg/ml,与模型组(幽门螺杆菌26695:872.38
±
29.57pg/ml、幽门螺杆菌11637:858.74
±
21.03pg/ml、幽门螺杆菌11916:875.09
±
28.58pg/ml)相比较均差异性显著(p《0.005)。上述结果表明,嗜酸乳杆菌la-03菌悬液和发酵上清液均抑制幽门螺杆菌26695、幽门螺杆菌11637、幽门螺杆菌11916诱导胃上皮细胞ags分泌炎症因子il-8,表现出良好的改善幽门螺杆菌引起炎症反应的作用。
[0051]
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1