一种表面结合靶向配体的细菌及其应用
1.本发明属于生物医药领域,涉及一种表面结合靶向配体的细菌及其应用,具体地,是 一种表面结合靶向配体的细菌、其制备方法、包含该细菌的药物组合物、药物递送体系及 其应用。
背景技术:
2.近年来,恶性肿瘤的发病率逐年上升,各种治疗方法层出不穷。特别地,随着近年来 免疫学和生物技术领域的进步,细菌作为免疫调节剂和药物递送载体在肿瘤生物治疗中越 来越受到关注。细菌感染能够促进肿瘤的免疫原性,进一步诱导有效的抗肿瘤免疫反应。 此外,肿瘤组织中细菌的定植能够触发先天免疫细胞的激活和促炎因子的释放,从而导致 肿瘤血管系统的破坏以及相关的血栓形成。以细菌作为药物载体的应用,最大的优势在于 其有利于在肿瘤部位的定植,这归因于肿瘤内的厌氧条件、富营养化和免疫抑制微环境。 但是,不利地,细菌介导的肿瘤治疗总是受到肿瘤生长抑制效率低和不良剂量依赖性副作 用的困扰。
3.虽然已经通过化学或基因技术手段,来修饰或改造细菌以应对这些挑战。例如,为了 降低全身毒性,通过将包括李斯特菌、大肠杆菌和梭状芽孢杆菌在内的几种细菌菌株去除 关键毒力因子基,进而使其减毒;或者,在细菌表面装饰各种类型的底物,如合成纳米颗 粒和治疗药物,以此用于增强抗肿瘤活性。但是,现有技术中通过化学和基因技术手段进 行的修改,仍然不能提高细菌在给药后的肿瘤特异性及其在肿瘤部位的定位能力。因此, 如何提高细菌的肿瘤靶向性从而提高细菌疗法的安全性和抗肿瘤功效,仍是本领域至今未 能解决或取得显著改善的技术难题。
4.此外,现有研究表明,核酸适配体,也被称之为“化学抗体”,由于其能够特异地识别 细胞表面靶标(如核酸和蛋白质)、全细胞甚至组织,已被广泛用作靶向配体。与抗体类似, 核酸适配体表现出许多有利的特征,例如,高亲和力、优异的特异性和低免疫原性。此外, 核酸适配体可以通过成熟的固态合成技术在体外合成,并可以用各种官能团进行化学修饰。 凭借这些独特的性质,现有技术中,已有研究者在临床试验中评估部分治疗性核酸适配体 在癌症治疗中的潜力。然而,基于核酸适配体的药物递送主要集中在开发核酸适配体-药物 偶联物和核酸适配体功能化的纳米颗粒,至今还不存在通过使用核酸适配体通过特定的配 体-受体相互作用将活细胞主动地输送到肿瘤部位的方法或产品。
5.基于此,本技术的发明人及其团队期望通过核酸适配体的辅助,调控细菌的行为,增 强细菌肿瘤定位的能力,并由此提高生物疗法的治疗效果。
技术实现要素:
6.针对现有技术中细菌和靶向核酸适配体在肿瘤治疗领域中的空白和上述不足,本发明 申请的发明人及其团队提出一种表面结合靶向配体的细菌及其应用,具体地,是一种表面 结合靶向配体的细菌、其制备方法、包含该细菌的药物组合物、药物递送体系及其在
制备 肿瘤治疗药物中的应用。
7.第一方面,本发明申请提供了一种表面结合靶向配体的细菌,该细菌是通过单步酰胺 化过程将核酸适配体结合到细菌表面。
8.进一步地,该细菌是选自革兰氏阴性细菌中的任意一种或多种。任选地,是大肠杆菌; 任选地,是沙门氏菌,优选地,是减毒沙门氏菌。
9.进一步地,该靶向配体是一种核酸适配体,优选地,是氨基化的核酸适配体。
10.第二方面,本发明申请提供了一种制备上述表面结合靶向配体的细菌的方法,包括: 通过单步酰胺化过程将靶向配体结合到细菌表面,其中,该靶向配体是一种核酸适配体。
11.进一步地,该核酸适配体是氨基化的核酸适配体。
12.进一步地,该细菌是选自革兰氏阴性细菌中的任意一种或多种。任选地,是大肠杆菌; 任选地,是沙门氏菌,优选地,是减毒沙门氏菌。
13.进一步地,该单步酰胺化过程,具体地,在室温下,磁力搅拌600rpm,将 0.10-0.02μmol/ml功能化适配体、edc和nhs加入细菌悬液中,搅拌,获得表面结合适 的细菌。
14.进一步地,氨基化核酸适配体可以是如seq1或seq2所示的寡核酸链。
15.进一步地,该细菌表面的核酸适配体的接枝密度为0.7
×
10
5-5.7
×
105个核酸适配体/ 细胞。
16.第三方面,本发明申请提供了一种药物组合物,其包括上述任一种表面结合靶向配体 的细菌及其药学上可接受的载体。
17.进一步地,在该药物组合物中,该表面结合靶向配体的细菌含量为1-99.9重量%。优 选地,10-90重量%,更优选地,50-80重量%。其中,核酸适配体的接枝密度为0.7
×
10
5-5.7
ꢀ×
105个核酸适配体/细胞。
18.第四方面,本发明申请提供了一种用于肿瘤治疗的药物递送体系,该体系至少包括上 述任一种表面结合靶向配体的细菌,该细菌是通过单步酰胺化过程将靶向配体结合到细菌 表面,其中,该靶向配体是一种核酸适配体。
19.进一步地,该细菌是选自革兰氏阴性细菌中的任意一种或多种。任选地,是大肠杆菌; 任选地,是沙门氏菌,优选地,是减毒沙门氏菌。
20.进一步地,该核酸适配体是氨基化的核酸适配体。
21.进一步地,氨基化核酸适配体可以是如seq1或seq2所示的寡核酸链。
22.进一步地,该细菌表面的核酸适配体的接枝密度为0.7
×
10
5-5.7
×
105个核酸适配体/ 细胞。
23.进一步地,该药物递送体系以该表面结合靶向配体的细菌为载体,负载其它活性药物 组分。例如,纳米抗体、小分子药物,更具体地,免疫抑制剂。
24.第五方面,本发明申请还提供了上述任一种表面结合靶向配体的细菌在制备用于治疗 肿瘤的药物方面的用途。
25.进一步地,根据选择的核酸适配体不同,用于治疗不同类型的肿瘤。该肿瘤可以是常 见的实体瘤,包括肺癌、胃癌、结肠癌、子宫癌、直肠癌、咽喉癌、乳腺癌等,优选地, 胃癌、乳腺癌。
26.通过酰胺缩合,氨基化的核酸适配体与细菌细胞壁上的n-乙酰胞壁酸的羧基结
合,其 结合的稳定性很好。利用核酸适配体被结合在细菌的表面,不仅提高了核酸适配体在体内 环境的稳定性,还提高其对靶标部位的特异性和定植能力,例如肿瘤部位及细胞,高度激 活肿瘤内部的免疫反应。采用这种被修饰细菌作为药物载体,还可以最大优势地在其定制 在靶标位置后释放药物,提高药物在肿瘤组织中的积累和渗透,从而使其治疗效果最大化。
27.有益效果
28.本发明公开了上述表面结合靶向配体的细菌、其制备方法、及包含该细菌的药物组合 物、以该细菌的药物递送体系及其用途。
29.基于实验研究,该核酸适配体结合到细菌表面的过程是和细胞相容的酰胺化过程,可 以显著促进细菌给药后在全身肿瘤部位的定位。该适配体的表面密度可以通过不同的投料 比例轻松调整。而且,与单独使用适配体相比较,通过化学键结合在细菌细胞壁表面能够 提高适配体在体内环境的稳定性。与未修饰的细菌相比,分别在12和60h在肿瘤组织中产 生近2倍和4倍的集聚。在4t1和h22荷瘤小鼠模型中,结合核酸适配体的减毒沙门氏菌 显示出了显著增强的抗肿瘤疗效和肿瘤内部高度激活的免疫反应。本发明申请的实施例和 实验例证明了,核酸适配体结合的细菌在靶向肿瘤及其在肿瘤内定植方面具体突出的进步 性,这显示了其在肿瘤生物治疗方面的巨大潜力和重要的临床应用价值。
附图说明
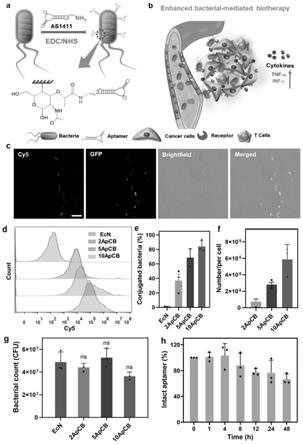
30.图1示出了apcb的设计、制备及表征。其中:
31.(a)酰胺缩合法制备apcb;
32.(b)核酸适配体辅助肿瘤定位的细菌,用于加强生物治疗;
33.(c)适配体结合的细菌的典型lscm图像,红色和绿色通道分别表示与cy5和ecn结合 的适配体产生gfp,比例尺:10μm;
34.(d)流式细胞术分析ecn和与cy5标记且as1411结合的ecn;
35.(e)不同进料比例下被结合细菌ecn的百分比,其中误差棒表示标准差(n=3),数据以 平均值
±
sd表示;
36.(f)通过计算反应后适配体溶液荧光强度的差异,量化每个细菌上适配体的平均结合数 量,其中误差棒表示标准差(n=3),数据以平均值
±
sd表示;
37.(g)lb琼脂平板计数ecn、2apcb、5apcb、10apcb的细菌活力,其中,在计数前, 培养皿在37℃下孵育24h(n=3),数据以平均值
±
sd表示,采用非配对双尾student’s检 验(two-tailed)评估其差异显著性,ns表示无显著差异;
38.(h)在37℃下,被结合的as1411在90%磷酸盐缓冲血清溶液中的降解动力学,其中误 差棒表示标准差(n=3)。
39.图2通过跟踪cy5标记as1411的荧光强度示出了流式细胞术分析ecn和apcb。
40.图3示出了apcb与4t1细胞结合。其中:
41.(a)在37℃下分别与pbs、ecn
gfp
、ctl
gfp
、2apcb
gfp
、5apcb
gfp
和10apcb
gfp
孵 育2h后4t1细胞的代表性lscm图像,其中,在观察前用pbs冲洗细胞,绿色通道表示 ecn产生gfp,比例尺:10μm;
42.(b)共孵育4t1细胞的流式细胞分析。
43.图4中,(a)用pe标记的抗核仁蛋白抗体孵育293t、h22和4t1细胞后,流式细胞术 分析细胞表面核仁蛋白;(b)37℃共孵育2h后与apcb
gfp
结合的4t1细胞百分比。误差棒 表示标准差(n=3)。数据以平均值
±
sd表示。采用非配对双尾student’s检验(two-tailed) 评估其差异显著性,给出p值:10apcb vs ecn,0.000004;5apcb vs ecn,0.0001;2apcbvs ecn,0.0007;pbs vs ecn,0.0004。ns表示无显著差异。***p《0.001,****p《0.0001。
44.图5示出了apcb与癌细胞的特异性结合。其中:
45.(a)分别与ecn和5apcb在37℃下孵育2h后4t1细胞的代表性sem图像,细菌被红 色虚线圈起来,比例尺:5μm;
46.(b)293t细胞分别与ecn
gfp
和5apcb
gfp
在37℃共孵育2h后的流式细胞分析;
47.(c)分别在37℃共孵育2h后与ecngfp和5apcbgfp结合的293t细胞的百分比,其 中误差棒表示标准差(n=3),数据以平均值
±
sd表示,采用非配对双尾student’s检验 (two-tailed)评估其差异显著性,ns表示无显著差异;
48.(d)293t细胞分别与ecngfp和5apcbgfp在37℃孵育2h后的典型lscm图像,其 中,观察前用pbs冲洗细胞,绿色通道表示ecn产生gfp,比例尺:10μm。
49.(e)静脉注射1
×
107cfu细菌后12h,肿瘤组织切片的共聚焦图像,其中绿色和蓝色表 示cyanine3标记的抗大肠杆菌和dapi染色的细胞核,比例尺:20μm。
50.图6示出了评估的体内炎症反应。其中,血液常规分析包括(a)白细胞计数和(b)血小板 计数。具体地,用市售酶联免疫吸附试验(elisa)试剂盒测定血清中细胞因子水平,包括(c) il-6和(d)il-10。尾静脉注射样品,60h后眼眶内取血。误差棒表示标准差(n=4)。数据以 平均值
±
sd表示。采用非配对双尾student’s检验(two-tailed)评估其差异显著性,ns表示 无显著差异。
51.图7示出了apcb在荷瘤小鼠体内的生物分布。其中:
52.(a)分别在尾静脉注射pbs或1
×
107cfu ecn
lux
、ctl
lux
和5apcb
lux
后12、36、60h 对4t1荷瘤小鼠进行ivis成像;
53.(b)注射后12、36和60h肿瘤部位发光信号的平均强度,其中,发光强度(原子单位(a.u.)) 是由caliper ivis lumina ii系统进行量化,绘制出包含整个实体肿瘤的感兴趣区域(n=4), 数据以平均值
±
sd表示。采用非配对双尾student’s检验(two-tailed)评估其差异显著性, 给出p值:在60h时,5apcb vs pbs,0.081;5apcb vs ecn,0.0131;5apcb vs ctl,0.0132; 在36h时,5apcb vs pbs,0.0370,5apcb vs ecn 0.0339,5apcb vs ctl,0.0287;ns,无 显著性差异。
54.(c)分别用pbs或1
×
107cfu的ecn、ctl和5apcb尾静脉注射60h后,小鼠主要器 官和肿瘤组织内细菌的生物分布。用平板计数法测定细菌数量,数据以平均值
±
sd表示(n= 4)。采用非配对双尾student’s检验(two-tailed)评估其差异显著性,给出p值:5apcb vs pbs, 0.0012;5apcb vs ecn,0.0138;5apcb vs ctl,0.0108;ns:无显著差异。
55.(d)注射后12h,ecn定植于肿瘤内的数量,其中误差棒表示标准差(n=3),数据以平均 值
±
sd表示。采用非配对双尾student’s检验(two-tailed)评估其差异显著性,给出p值: 5apcb vs pbs,0.0027;5apcb vs ecn,0.0251;5apcb vs ctl,0.0390;ns表示无显著 差异。*p《0.05,**p《0.01。
56.图8示出了核酸适配体结合vnp的特性。其中:
57.(a)适配体结合vnp的典型lscm图像。其中,红色和绿色通道分别表示与cy5和vnp 结合的适配子产生gfp。比例尺:10μm。
58.(b)流式细胞术分析与cy5标记as1411结合的vnp和vnp。
59.(c)不同进料比例下结合vnp的百分比。误差棒表示标准差(n=3)。数据以平均值
±ꢀ
sd表示。
60.(d)通过计算反应后适配体溶液荧光强度的差异,量化每个细菌上适配体的平均结合数 量。误差棒表示标准差(n=3)。数据以平均值
±
sd表示。
61.图9示出了apcb的体内治疗效果。其中:
62.(a)不同治疗后肿瘤相对生长情况(n=5)。数据以平均值
±
sd表示。采用非配对双尾 student’s检验(two-tailed)评估其差异显著性,给出p值:5apcb vs pbs,0.000005;5apcbvs vnp,0.00002。
63.(b)治疗结束时小鼠肿瘤组织的代表性照片。比例尺:1cm。
64.(c)观察每个处理期间治疗小鼠体重变化(n=5),其中数据以平均值
±
sd表示。
65.(d)治疗后肿瘤内部ki67(cd3+细胞门控)的百分比(n=4),其中数据以平均值
±
sd表 示;采用非配对双尾student’s检验(two-tailed)评估其差异显著性,给出p值:5apcb vs pbs, 0.0003;5apcb vs vnp,0.0411。
66.(e)用流式细胞术分析治疗后肿瘤内cd4+t细胞(cd3+细胞门控)的数量(n=4)其中数 据以平均值
±
sd表示;采用非配对双尾student’s检验(two-tailed)评估其差异显著性,给 出p值:5apcb vs pbs,0.0002;5apcb vs vnp,0.0088。
67.(f)治疗后肿瘤内部ifn-γ(对cd3+细胞门控)的百分比(n=4),其中数据以平均值
±
sd 表示;采用非配对双尾student’s检验(two-tailed)评估其差异显著性,给出p值:5apcb vspbs,0.00009;5apcb vs vnp,0.0192。
68.(g)、(h)肿瘤组织用tnf-α(绿色)和tunel(绿色)染色。蓝色为dapi染色细胞核。比 例尺:50μm。
69.(i)不同治疗后肿瘤切片的典型h&e染色图像。坏死区域用白色虚线圈起来。比例尺: 200μm。其中,*p《0.05,**p《0.01,***p《0.001,****p《0.0001。
70.图10示出了apcb与4t1细胞的结合。其中:
71.(a)分别用pbs、vnp
gfp
、ctl
gfp
、2apcb
gfp
、5apcb
gfp
、10apcb
gfp
在37℃孵育2h 后4t1细胞的代表性lscm图像。观察前用pbs冲洗细胞。绿色通道表示vnp产生gfp。 比例尺:15μm。
72.(b)共孵育4t1细胞的流式细胞分析。
73.图11示出了具有tls11a适配体的apcb在h22肿瘤模型中的应用。其中:
74.(a)通过酰胺缩合反应,将vnp与tls11a结合制备apcb。
75.(b)h22细胞与pbs、vnp、t-5apcb在37℃共孵育1h后流式细胞术分析。
76.(c)治疗后第12天小鼠的数码照片。肿瘤用红色圆圈标记。h22荷瘤小鼠(接种1
×
106癌细胞)被随机分为三组,静脉注射pbs和5
×
105cfu vnp或t-5apcb,当肿瘤大小达到 约100mm3(定义为第0天)。
77.(d)不同治疗后肿瘤的相对生长(n=5),其中,数据以平均值
±
sd表示;采用非配对双 尾student’s检验(two-tailed)评估其差异显著性,给出p值:t-5apcb vs pbs,0.000002; t-5apcb vs vnp,0.0052。
78.(e)h22荷瘤小鼠经不同处理后的生存曲线(n=7),其中数据以平均值
±
sd表示。采用 非配对双尾student’s检验(two-tailed)评估其差异显著性,给出p值:t-5apcb vs pbs,p《 0.0001;t-5apcb vs vnp,0.0017。
79.(f)治疗期间体重的变化,其中,**p《0.01,****p《0.0001。
80.其中,*表示p《0.05,**表示p《0.01,***表示p《0.001,****表示p《0.0001,ns 表示没有显著性差异(n=5)。
81.图12示出了37℃共孵育2h后4t1细胞与apcbgfp结合的百分比。采用流式细胞术 对细胞进行定量分析。误差棒表示标准差(n=3)。数据以平均值
±
sd表示。采用非配对双尾 student’s检验(two-tailed)评估其差异显著性,给出p值:10apcb vs vnp,0.0158;5apcbvs vnp,0.0006;2apcb vs vnp,0.0096;pbs vs vnp,0.0016。*p《0.05,**p《0.01, ***p《0.001,ns表示物显著性差异。
82.图13中,(a)ki67的百分比,(b)cd4+t细胞的数量,(c)不同治疗后肿瘤内ifn-γ的 百分比。所有细胞都是cd3+细胞的门控细胞。
83.图14示出了不同治疗后(a)tnf-α和(b)tunel染色的肿瘤组织图像。比例尺:50μm。
84.图15示出了h22细胞与t-5apcb
gfp
共孵育后的几何平均荧光强度,pbs和vnp均作 为对照组。误差棒表示标准差(n=3)。数据以平均值
±
sd表示。采用非配对双尾student
’ꢀ
s检验(two-tailed)评估其差异显著性,给出p值:t-5apcb vs pbs,0.0004;t-5apcb vs vnp, 0.0279。*p《0.05,***p《0.001。
85.图16示出了用于细胞分类的门控策略。具体地,是从图9.d-f和图13示出的体内培养 的肿瘤细胞中筛选cd3+、cd4+、ifn-γ、ki67细胞的门选策略。
具体实施方式
86.下面结合具体实施方式对本发明的技术方案做进一步说明,但是并不以此限制本发明。 在不背离本发明的技术构思及技术方案的前提下,对本发明所属领域的普通技术人员来说, 能够实现的任何修改、调整或修饰、或者等同替换方法都将落入本发明的要求保护的范围 内。
87.下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的 材料、试剂等,如无特殊说明,均可从商业途径得到。
88.在本发明申请的实施方案中,通过单步酰胺化过程将核酸适配体结合到细菌表面,由 此获得一种表面结合靶向配体的细菌。
89.进一步地,该细菌是选自革兰氏阴性细菌中的任意一种或多种,优选地,大肠杆菌或 沙门氏菌,更优选地,是减毒沙门氏菌。
90.进一步地,该靶向配体是一种核酸适配体,优选地,是氨基化的核酸适配体。
91.在实验例中,该氨基化核酸适配体是如seq1或seq2所示的寡核酸链。
92.seq1:5
’‑
ggt ggt ggt ggt tgt ggt ggt ggt ggt ttt ttt ttt tt-nh2-3’93.seq2:5
’‑
aca gca tcc cca tgt gaa caa tcg cat tgt gat tgt tac ggt ttc cgc ctc atg gac gtg ctg ttt-nh2-3’94.第二方面,本发明申请提供了一种制备上述表面结合靶向配体的细菌的方法,包括: 通过单步酰胺化过程将靶向配体结合到细菌表面,其中,该靶向配体是一种核酸适配
体。
95.进一步地,该核酸适配体是氨基化的核酸适配体。
96.进一步地,该细菌是选自革兰氏阴性细菌中的任意一种或多种。在一个实施例中,选 择沙门氏菌作为被改造的原菌株,优选地,是减毒沙门氏菌。
97.在另一个实施例中,选择益生菌作为被改造的原菌株,优选地,选择大肠杆菌,例如, nissle 1917(ecn)。
98.进一步地,该单步酰胺化过程。具体地,在室温下,将0.1ml氨基功能化适配体(0.05 μmol/ml)、0.55mg edc和0.65mg nhs加入细菌悬液中,搅拌3h后,获得表面结合核 酸适配体的细菌。
99.进一步地,氨基化核酸适配体可以是如seq1或seq2所示的寡核酸链。
100.进一步地,该细菌表面的核酸适配体的接枝密度为0.7
×
10
5-5.7
×
105个核酸适配体/ 细胞。
101.第三方面,本发明申请提供了一种药物组合物,其包括上述任一种表面结合靶向配体 的细菌及其药学上可接受的载体。
102.进一步地,在该药物组合物中,该表面结合靶向配体的细菌含量为1-99.9重量%。优 选地,10-90重量%,更优选地,50-80重量%。其中,核酸适配体的接枝密度为0.7
×
10
5-5.7
ꢀ×
105个核酸适配体/细胞。
103.第四方面,本发明申请提供了一种用于肿瘤治疗的药物递送体系,该体系至少包括上 述任一种表面结合靶向配体的细菌,该细菌是通过单步酰胺化过程将靶向配体结合到细菌 表面,其中,该靶向配体是一种核酸适配体。
104.进一步地,该药物递送体系还可以是以该表面结合靶向配体的细菌为载体负载其它药 物组分的递送体系。
105.第五方面,本发明申请还提供了上述任一种表面结合靶向配体的细菌在制备用于治疗 肿瘤的药物方面的用途。
106.进一步地,根据选择的核酸适配体不同,用于治疗不同类型的肿瘤。该肿瘤可以是常 见的实体瘤,包括肺癌、胃癌、结肠癌、子宫癌、直肠癌、咽喉癌、乳腺癌等,优选地, 胃癌、乳腺癌。具体地,根据肿瘤的类型,选择不同的靶向配体,更具体地,从现有文库 中选择特定肿瘤类型的核酸适配体。
107.在各实施例中,通过酰胺缩合,将氨基化的核酸适配体与细菌细胞壁上的n-乙酰胞壁 酸的羧基结合,获得表面结合核酸适配体的细菌,并通过实验例证明其具体的特征及参数。
108.实施例1:制备表面被核酸适配体结合的细菌
109.通过酰胺缩合反应,氨基化的核酸适配体结合在细菌表面。具体地,将1
×
108个细胞 的细菌分散在1ml pbs溶液中,在室温下,将0.1ml氨基化的核酸适配体(0.05μmol/ml)、 0.55mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和0.65mg n-羟基琥珀酰亚胺 (nhs)同时加入细菌悬液中。
110.在酰胺缩合过程中,edc能够活化羧基,形成不稳定的o-酰基异脲。由于反应混合 物中加入nhs可以稳定活化的羧基,由此提高酰胺缩合的转化率。
111.搅拌3h后,通过离心分离修饰的细菌,10000rpm,1min,并用pbs洗涤3次。
112.实验例1.1:
113.通过酰胺缩合反应,将氨基化适配体as1411连接在大肠杆菌nissle 1917(ecn)表面。 具体地,将1
×
108ecn细胞分散在1ml pbs溶液中,在室温下,将0.1ml氨基功能化 适配体(0.05μmol/ml)、0.55mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和0.65 mg n-羟基琥珀酰亚胺(nhs)同时加入细菌悬液中。搅拌3h后,通过离心(10000rpm, 1min)分离修饰的细菌,并用pbs洗涤3次。
114.实验例1.2:
115.通过酰胺缩合反应,将氨基化适配体as1411连接在减毒鼠伤寒沙门氏菌vnp20009 (vnp)表面。具体地,将1
×
108vnp细胞分散在1ml pbs溶液中,在室温下,将0.1ml 氨基功能化适配体(0.05μmol/ml)、0.55mg edc和0.65mg nhs加入细菌悬液中。搅拌 3h后,通过离心(10000rpm,1min)分离被修饰的细菌,并用pbs洗涤3次。
116.实验例1.3:
117.通过酰胺缩合反应,将氨基化适配体tls11a连接在减毒鼠伤寒沙门氏菌vnp20009 (vnp)表面。具体地,将1
×
108vnp细胞分散在1ml pbs溶液中,在室温下,将0.1ml 氨基功能化适配体(0.05μmol/ml)、0.55mg edc和0.65mg nhs加入细菌悬液中。搅 拌3h后,通过离心(10000rpm,1min)分离被修饰的细菌,并用pbs洗涤3次。
118.材料与方法
119.1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟琥珀酰亚胺(nhs)购自 adamas-beta(中国上海)。rpmi 1640培养基、抗生素/抗真菌液、及磷酸盐缓冲生理盐水(1
×ꢀ
pbs)均由sigma-aldrich(美国)提供。
120.下述核酸适配体和寡核苷酸链均由tsingke合成生物科技有限公司(中国,上海)合成并 提供。
121.as1411(5'ggt ggt ggt ggt tgt ggt ggt ggt ggt ttt ttt ttt tt-nh2-3’)
122.tls11a(5'aca gca tcc cca tgt gaa caa tcg cat tgt gat tgt tac ggt ttc cgc ctc atg gac gtg ctg ttt-nh
2-3’)
123.ctl(5
’‑
cct cct cct cct tct cct cct cct cct ttt ttt ttt tt-nh
2-3’)
124.ecn和salmonella typhimurium均购自中国普通微生物菌种保藏管理中心gmcc。
125.4t1乳腺癌细胞株和293t细胞株均从美国模式生物培养集存库(atcc)获得, crl-2539;crl-3216)。h22肝癌细胞株购自bena培养集存库(bncc)(catalog: bncc338327)。两种细胞系均在dulbecco改良eagle培养基(sigma,美国)中培养,培养基 中添加10%(v/v)灭活胎牛血清(fbs)(sigma,美国)和1%(v/v)抗生素/抗真菌液(sigma,美 国),37℃,5%co2培养箱中培养。定期对细胞培养环境进行支原体评估,以确保没有支 原体污染。
126.质粒pbbr1mcs2-tac-gfp、pmd18-luxcdabe等所有试剂均购自国内供应商。
127.balb/c雌性小鼠(6~8周,18~20g)由杰思捷实验动物有限公司(中国上海)提供。所有 小鼠饲养于12/12h的暗/光循环和spf(环境温度(25℃)和湿度(55%)条件下。动物研究方案 由上海交通大学医学院动物护理和使用委员会审核批准。当肿瘤大小超过2000mm3时,小 鼠被安乐死。肿瘤大小/负荷未超过最大值。
128.i.实验及检测
129.在fluoromax-4荧光光谱仪上测量光致发光(pl)光谱。采用共聚焦激光扫描显微
镜 (clsm,leica,sp8)对细胞荧光图像进行表征。流式细胞术(beckman cytoflex)定量检测细胞 荧光。小鼠的体内成像由美体内成像系统(caliper lifesciences,usa)完成。在扫描电子显微 镜(sem)(sirion 200,usa)上进行形态学观察。
130.实验1:细菌的生长
131.将携带pbbr1mcs2-tac-gfp或pmd18-luxcdabe的ecn在37℃下、添加50μg/ml 卡那霉素的10ml lb液体培养基中培养过夜。
132.鼠伤寒沙门氏菌在37℃下胰蛋白胨大豆肉汤(tsb)培养基中培养,过夜培养之后,1:50 (v/v)稀释至新鲜lb液体培养基,37℃下,继续培养2-3h。收集细菌,6000
×
g离心10min, 置于冰冷的pbs中重悬,获得细菌悬液。将获得的细菌悬液稀释后,置于37℃lb琼脂平 板上培养过夜,计数菌落形成单位(cfu),测定细菌并计数。
133.实验2:制备apcb
134.通过酰胺缩合反应,氨基化的核酸适配体结合在细菌表面。具体地,将1
×
108个细胞 的细菌分散在1ml pbs溶液中,在室温下,将0.1ml氨基化的核酸适配体(0.05μmol/ml)、 0.55mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和0.65mg n-羟基琥珀酰亚胺 (nhs)同时加入细菌悬液中。具体地,选择的细菌和核酸适配体参见上文实验例1.1-1.3。
135.在酰胺缩合过程中,edc能够活化羧基,形成不稳定的o-酰基异脲。由于反应混合 物中加入nhs可以稳定活化的羧基,由此提高酰胺缩合的转化率。
136.搅拌3h后,通过离心分离修饰的细菌,10000rpm,1min,并用pbs洗涤3次。
137.实验3:计算每个细菌表面结合适配体的平均数量。
138.首先,制备一定浓度的几种cy5标记的as1411溶液。然后,利用激发波长为647nm、 发射波长为670nm的光致发光光谱,绘制cy5标记的as1411浓度的荧光强度,建立标准 曲线。在确定标准曲线的回归方程后,可计算出反应后游离的cy5标记as1411的浓度。 按照下述公式计算每个细菌细胞表面结合适配体的数量。
139.n
avg
=((c0v-cav)
×
na)/na140.其中,navg表示平均数值/细菌细胞,c0表示反应前游离的cy5-labelled as1411的浓度, ca表示反应后游离的cy5-labelled as1411的浓度,v是反应发生的体积,na是阿伏伽德罗 常数6.02
×
10
23
,na是细菌细胞的总数。
141.实验4:检测被结合细菌在血清中的稳定性
142.为了研究表面结合适配体的细菌的血清稳定性,将表面结合cy5-labelled as1411的1
ꢀ×
109cfu apcb在37℃下悬浮于含10%胎牛血清的5ml pbs中,并预先确定时间点0、1、 4、8、12、24和48h。在每个时间点结束时,从每个样品取出100μl,离心。用pbs冲洗 后,将最终样品重悬在100μl pbs中,置于石英试管中。在室温下,在647nm激发光和 670nm发射光下,测量各样品的荧光发射强度。利用标准曲线得到的回归方程,计算被结 合适配体的浓度。
143.实验5:细胞吸收
144.以每个共聚焦皿中2
×
105个细胞的密度,将细胞接种在1ml含有10%胎牛血清和抗生 素的rpmi-1640培养基中。4t1细胞在37℃5%co2中培养24h。然后,用新鲜1640培养 基替换原培养液,用等体积的ecn或apcb在37℃处理2h,pbs洗涤3次后,用lscm 观察细胞。
145.为了定量分析细胞摄取行为,将细胞消化并收集进行流式细胞术分析。
cd4 (biolegend,catalog:100412)、pe-cy7-labeled anti-ifn-γ(biolegend,catalog:505826)和 fitc-labeled anti-ki67(ebioscience,catalog:11-5698-82)。抗体的稀释倍数为1:200。使用 cytoflex进行数据分析,并使用cytexpert(beckman coulter,usa)和flowjo(treestar,usa) 软件进行分析。
159.统计分析和再现性
160.所有数据以至少三次独立试验的平均值
±
标准差(sd)表示。采用prism 8.0(graphpad, usa)进行统计分析。两组间比较,采用非配对双尾student’s检验(two-tailed)。图1.c、3.a、 5.a、5.d-e、7.b-d和图8.a、10.a、13.a-b,n=3个独立实验。在所有事件中,如果p《0.05 (*p《0.05,**p《0.01,***p《0.001,and****p《0.0001),则认为具有统计学差异。
161.ii.实验和检测结果
162.1.制备的apcb与表征
163.通过酰胺缩合过程,氨基化的as1411与n-乙酰胞壁酸的羧基相连(图2)。因为n-乙 酰胞壁酸广泛存在于革兰氏阴性菌的细胞壁中,与谷氨酸或天冬氨酸残基的其他羧基相比 较,具有更高的反应活性。
164.在1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和n-羟基琥珀酰亚胺(nhs)的帮助 下,将ecn与as1411在磷酸盐缓冲盐水(pbs)中室温共孵育3h制备apcb,所得细菌简单 离心纯化。为了进行激光扫描共聚焦显微镜(lscm)和流式细胞术的测量,使用在序列5' 末端标记有荧光色素cyanine5(cy5)的as1411制备apcb。如图1.c所示,lscm图像显 示,在实验条件下,表达绿色荧光蛋白(gfp)的ecn被as1411(红色)有效修饰。流式细胞 术进一步证实,as1411成功地修饰在细菌细胞表面。apcb的平均荧光强度约为ecn的10 倍(图2)。
165.取一定数量的1
×
108cfu的ecn,分别与0、2、5和10nmol的cy5标记as1411(具 体地,ecn cy5
,2apcb
cy5
,5apcb
cy5
和10apcb
cy5
)孵育。然后,用流式细胞仪对产生的细菌 进行分析。结果是,荧光信号增强,且as1411的浓度提高,清楚地表明明显的连续曲线的 转向更高的强度(图1.d和e)。计算每细胞上接枝的寡核苷酸适配体的数量,采用荧光分光 光度计检测与不同浓度的cy5-labelled as1411结合的ecn。如图1.f所示,计算as1411在 2apcbcy5、5apcbcy5和10apcbcy5每个细胞表面的结合量分别为0.7
×
105、2.8
×
105、 和5.7
×
105个适配体。
166.为了研究制备过程和适配体是否对细菌活力有无毒副作用,我们采用平板计数法评估 apcb的生长。将ecn、2apcb、5apcb、10apcb连续稀释后涂布于luria bertani(lb) 琼脂平板上。37℃孵育24h后,通过记录菌落数量来测定apcb的活力。由图1.g可见, 与ecn相比,2apcb、5apcb、10apcb的菌落数cfu无显著差异,这说明结合适配体后 细菌活力未受影响。
167.此外,基于适配体的治疗药物的血清耐受性对体内应用至关重要。基于现有理论和实 验数据。可以推测,在细菌表面结合适配体可以大大增加as1411被核酸酶的酶水解的空间 位阻。
168.为了证明这一推断,我们通过跟踪cy5标记as1411的荧光强度来监测被结合在ecn 上的适配体的稳定性。将apcbcy5与10%胎牛血清在37℃pbs中孵育至预定时间点后, 用流式细胞仪分析apcbcy5。根据本技术发明人团队之前曾报道,超过60%的游离as1411 在48h
的孵育后迅速降解(j.am.chem.soc.2020,142,2,937
–
944)。但是,值得注意的是, 在相同的实验条件下,当as1411结合到ecn表面,其稳定性得到了很大的提高,在相同 时间点被结合的适配体70%以上仍保持完整(图1.h)。
169.2.apcb与癌细胞的结合增加
170.ctl是一种与as1411碱基数量相同但没有二级结构的杂乱寡核苷酸,在此作为对照。 为了研究as1411在表面结合as1411的ecn侵袭癌细胞中的作用,我们使用过表达核仁素 的4t1细胞评估了分别在pbs、ecn
gfp
、ctl
gfp
、2apcb
gfp
、5apcb
gfp
和10apcb
gfp
的 细胞结合效率(图4.a)。lscm成像显示,as1411结合在细胞表面可以增强ecn与4t1细 胞的结合(图3.a)。根据共聚焦成像结果和流式细胞分析图像,as1411接枝密度是从0.5
×
105ꢀ‑
2.8
×
105/细胞,随接枝密度增加,结合效率增加。接枝密度进一步增加到5.5
×
105,随后 结合效率开始下降(图3.b)。
171.在同样的培养条件下,ecn分别与pbs、ecn
gfp
、ctl
gfp
、2apcb
gfp
、5apcb
gfp
和 10apcb
gfp
孵育2h后,4t1细胞与ecn结合的比例分别约为0.2%、5.5%、4.5%、15%、 50%、30%(图4.b)。这些结果表明,适配体修饰可以通过特异性的配体-受体识别促进细菌 与靶向癌细胞的相互作用,而且这取决于嫁接密度。
172.为了直观地观察apcb与癌细胞的结合情况,分别用扫描电子错拷贝(sem)观察与ecn 共孵育后的4t1细胞和5apcb细胞(图5.a)。具有代表性的sem图像显示,与ecn相比较, 在4t1细胞表面附着更多的细菌5apcb,这与流式细胞分析结果一致。
173.流式细胞分析显示,293t细胞分别地与ecn
gfp and 5apcb
gfp
结合后的荧光强度无显 著差异(图5.b和c)。同时,lscm图像显示,5apcbgfp与293t细胞结合效率与ecngfp 相似。在293t细胞表面存在有限的细菌附着(图5.d)。
174.此外,为了进一步评估apcb与体内癌细胞的结合效率,我们建立了4t1肿瘤模型, 将获得的荷瘤小鼠分别静脉给药pbs和1
×
107cfu的ecn或5apcb。在注射后12h,取 肿瘤组织,并用fitc-labelled anti-escherichia coli和4',6-二氨基-2-苯基吲哚(dapi)染色(图 5.e)。
175.采用4t1荷瘤小鼠模型并通过肿瘤成像,确定apcb的肿瘤靶向定植能力。根据体外 实验结果,采用结合效率最高的5apcb评价肿瘤的集聚。为了实现可视化跟踪,将 luxcdabe工程化的5apcblux通过尾静脉静脉注射到荷瘤小鼠体内,而pbs、ctl
lux
和 表面不含适配体的ecn
lux
作为对照组。在注射后指定的时间点,用体内成像系统(ivis)观察 给药小鼠。
176.如图7.a所示,从给药后12-60h,ivis获得的肿瘤平均发光信号随着时间间隔的增加 而不断增加。重要的是,在每个时间点,注射5apcblux的小鼠肿瘤部位的发光信号的平 均强度显著高于分别注射pbs、ctl
lux
和ecn
lux
的小鼠(图7.b)。特别地,在注射后60h, 相对信号强度是ctl
lux
和ecn
lux
组的8倍。
177.为了量化肿瘤定植能力,在动物研究的终点检测细菌的生物分布。将小鼠安乐死后, 收集心、肾、肝、肺、脾及肿瘤组织,均质后,涂布在lb琼脂平板上进行细菌计数。经计 算,注射5apcb的小鼠切片肿瘤组织中的细菌数量是ecn和ctl组的4倍(图7.c)。
178.与主要器官相比,细菌在肿瘤组织中的分布是非同寻常的,大约99.9%的细菌定植于肿 瘤内部。ecn在肿瘤组织内的大量聚集与它们偏爱缺氧、富营养化和肿瘤的免疫抑制微环 境有关。为了证明这一假设,我们用平板计数法对注射后较短时间内ecn在4t1肿瘤
内的 定位进行了量化。如图7.d所示,5apcb给药后12h,定位于肿瘤组织内的细菌数量达到 1.75
×
107cfu/g组织,是未结合或ctl修饰的ecn的2倍。也就是说,表面接合确实提 供了一个更大的机会,使之通过适配体修饰的细菌和肿瘤细胞之间的配体-受体相互作用来 定位肿瘤位点。
179.另外,通过血常规和细胞因子检测评价5apcb的潜在副作用。注射一定剂量5apcb 的小鼠的白细胞(wbc)和血小板(plt)的值与注射pbs 60h后的pbs组的白细胞介素-6 (il-6)和白细胞介素(il-10)的值相似,这表明有令人满意的相容性(图6)。
180.3.评估apcb的抗癌疗效
181.与ecn相比,由于as1411的修饰,在vnp与4t1细胞结合的过程中,可导致可比较 的增量vnp(图7、9和12)。使用4t1小鼠皮下肿瘤模型,获得的荷瘤小鼠被随机分为三 组(n=5),然后分别接收不同的治疗方法,包括pbs、vnp和5apcb。曾有报道称,单次 静脉注射vnp剂量1
×
10
4-1
×
106cfu/只小鼠是可耐受的(详见oncol res.2001;12(11-12): 501-8)。因此,vnp组和5apcb组中每个小鼠都在第0天静脉注射5
×
105cfu细菌。简明 地评估肿瘤体积肿瘤抑制作用的研究表明,与pbs组相比较,vnp和5apcb可以抑制肿 瘤的生长(图9.a和b)。如图9所示,治疗后小鼠体重记录每隔一天的变化揭示,在实验剂 量下下细菌存在有限的副作用。
182.为了揭示细菌介导的免疫反应,在治疗结束时分析肿瘤组织中t细胞的激活。以细胞 核上非组蛋白ki67为标记物,检测肿瘤中cd3+t细胞的浸润。如图9.d、图13.a和图16 所示,与pbs组和vnp组相比,经5apcb处理小鼠的cd3+t细胞增殖明显增加。此外, 5apcb处理显著提高了cd3+cd4+t细胞的百分比(图9.e,图13.b和图16),这表明,被 适配体修饰的细菌可以更有效地促进免疫效应细胞的肿瘤浸润。
183.进一步地,本技术发明人还检测了主要调节细胞免疫应答的肿瘤细胞因子(例如干扰 素-γ(ifn-γ)和肿瘤坏死因子-α(tnf-α)的百分比。结果表明,经5apcb处理的小鼠体内该 百分比显著增加(图9.f和g,图13.c和14.a)。肿瘤组织中tnf-α和ifn-γ水平升高表明 5apcb治疗激活了抗肿瘤免疫应答。末端脱氧核苷酸转移酶dutp标记(tunel)染色显示, 5apcb诱导的肿瘤细胞凋亡水平最高(图9.h和图14.b)。此外,苏木精和伊红(h&e)染色 显示,适配体结合的处理后,肿瘤组织明显坏死(图9.i)。
184.综上所述,肿瘤生长的抑制可以归因于适配体介导的细菌在肿瘤定值能力增强以及细 菌相关的抗肿瘤免疫反应的激活。
185.4.apcb的多功能性
186.同样地,以tls11a为基础的apcb(t-apcb)是通过与vnp共孵育得到(图11.a)。 t-apcb的制备细节在此简要描述。具体地,将1
×
108cfu的vnp与5nmol tls11a孵育, 制备t-5apcb。
187.流式细胞分析显示,与t-5apcb
gfp
共孵育的h22细胞荧光强度高于与vnpgfp共孵 育的h22细胞,这表明,tls11a结合的细菌与癌细胞结合的亲和力增强(图11.b和图15)。
188.接下来,我们评估了由此产生的t-5apcb在h22荷瘤小鼠中的抗肿瘤疗效。第0天单 次静脉注射pbs、5
×
105cfu的vnp或t-5apcb(肿瘤大小约100mm3),记录治疗小鼠 肿瘤大小和体重。
189.如图11.c和d所示,与pbs组和vnp组相比,t-5apcb组对肿瘤生长有明显的抑制 作
用,这是由于适配体在其表面的结合增加了细菌在瘤内的定位能力。不同组的存活率进 一步验证了,t-5apcb对h22荷瘤小鼠的治疗显著延长了生存期,近70%的治疗小鼠在36 天内成功存活(图11.e)。而在相同条件下pbs组或vnp组的小鼠均不能存活。此外,在处 理过程中体重的变化显示,在注射细菌的组中小鼠体重略有下降,但很快地恢复到与pbs 组相同的水平(图11.f)。体重的轻微波动表明,5apcb在实验剂量时副作用是有限的。
190.综上,在本发明申请中,该核酸适配体结合到细菌表面的过程是和细胞相容的酰胺化 过程,该过程可以显著促进细菌在全身给药后在肿瘤部位的定位。适配体的表面密度可以 通过不同的投料比例轻松调整,耦合能够提高锚定适配体的稳定性。平均每个细胞结合2.8
ꢀ×
105个适配体的最佳,被耦合适配体的细菌提高了其对体外肿瘤细胞的特异性,其中当, 平均每个细胞结合2.8
×
105个适配体时,特异性最佳。与未修饰的细菌相比,分别在12和 60h在肿瘤组织中产生近2倍和4倍的集聚量。在4t1和h22荷瘤小鼠模型中,结合适配 体的减毒沙门氏菌显示出显著增强的抗肿瘤疗效,以及肿瘤内部高度激活的免疫反应。这 项工作证明了被修饰后细菌的行为是如何通过表面偶联来调节的,并支持了核酸适配体偶 联细菌在靶向肿瘤内定位和增强肿瘤生物治疗方面的潜力。
191.以上仅是本发明的具体实施例以及用于证实本发明申请发明构思的实验例,但并不以 此限制本发明。本领域的普通技术人员能从本发明公开的内容直接导出或联想到的所有变 形,均应认为包含在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1