lncRNALINC00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用的制作方法
lncrna linc00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用
技术领域
1.本发明涉及生物医药领域,特别涉及lncrna linc00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用。
背景技术:
2.在过去的几十年中,在亚洲,美国和欧洲,肾细胞癌(rcc)的发病率呈逐年上升趋势,每年达到约3%,并且每年在全世界范围内造成约90,000例死亡。在最初诊断时,30%的患者病变已经有转移,超过30%的患者最终发展为转移性肾细胞癌(mrcc)。对于已经转移的肾细胞癌,可用的疗法通常无法有效减少肿瘤的生长或达到缓解的目的,这些治疗的缓解率在15%~25%,因此mrcc患者的总体生存期不到1年。因此早期发现转移性肾细胞癌可能会提高患者预后。但与胃肠道肿瘤不同,目前尚无用于肾细胞癌早期诊断和监测的生物标志物。为了设计出具有更高疗效的治疗策略,至关重要的是要破译参与肾细胞癌发生和发展的分子机制。
3.高通量测序技术又称深度测序技术,近十余年来逐渐兴起,在基础研究和临床研究领域得到广泛应用。该技术测序通量大,而且灵敏度高,能检测到表达量很低的基因的表达,且能识别新的转录产物。
4.非编码rna(ncrna)是没有蛋白质编码特性的rna,但自发现以来,ncrna在生命活动及病理过程中起着关键作用。近年研究表明,lncrna与mirnas、mrnas及蛋白质形成庞大而复杂的调控网络,参与诸多细胞生命进程及人类疾病的发生发展。目前报道有大量lncrna参与肿瘤的发生发展过程,其生物学特性使其可以作为肿瘤诊断和预后的生物标志物及精准治疗的靶点。虽然在以往的研究里,肾癌组织中的lncrna已被广泛研讨,但lncrna对于肾癌分子诊断的意义尚不清楚。因此急需寻找新的lncrnas,并探讨其对肾癌的生物学效应,以获得用于诊断和胃癌基因治疗的潜在治疗靶点。
技术实现要素:
5.有鉴于此,本发明针对现有技术存在的不足,通过基因芯片筛查与肾细胞癌相关的lncrna生物标志物,选择差异表达明显的lncrna00113,在不同分期肾癌组织中检测其表达差异,通过检测该lncrna的表达水平,判断受试者是否的肾癌分期与预后,为临床上判断肾癌是否发生转移提供支持。
6.为了实现上述发明目的,本发明提供以下技术方案:
7.第一方面,本发明提供了lncrna linc00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用;所述lncrna linc00113的核苷酸序列如seq id no.1所示。
8.在本发明的一些具体实施方案中,所述lncrna linc00113表达显著下调。
9.在本发明的一些具体实施方案中,所述lncrna linc00113表达显著下调时,肾癌发生可能性大或肾癌远期预后差,生存率低。
10.第二方面,本发明还提供了肾癌检测引物,包括核苷酸序列如seq id no.2所示的上游引物和核苷酸序列如seq id no.3所示的下游引物。
11.第三方面,本发明还提供了肾癌检测试剂,包括所述的肾癌检测引物以及可接受的助剂。
12.在本发明的一些具体实施方案中,还包括扩增gapdh内参基因的引物,所述引物包括核苷酸序列如seq id no.4所示的上游引物和核苷酸序列如seq id no.5所示的下游引物。
13.第四方面,本发明还提供了肾癌检测试剂盒,其特征在于,包括如权利要求5或6所述的肾癌检测试剂。
14.在本发明的一些具体实施方案中,还包括qrt
‑
pcr和/或逆转录反应常用的酶和试剂,优选反转录酶,缓冲液,dntps,depc水和taq酶。
15.本发明实验结果表明:linc00113在肾癌患者中表达下调,通过检测linc00113的表达,判断受试者是否有患肾癌的风险,通过比较linc00113的表达量,可以评估提示肾癌患者的远期预后和生存率,因此linc00113可作为肾癌临床诊断评估的重要指标。
附图说明
16.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
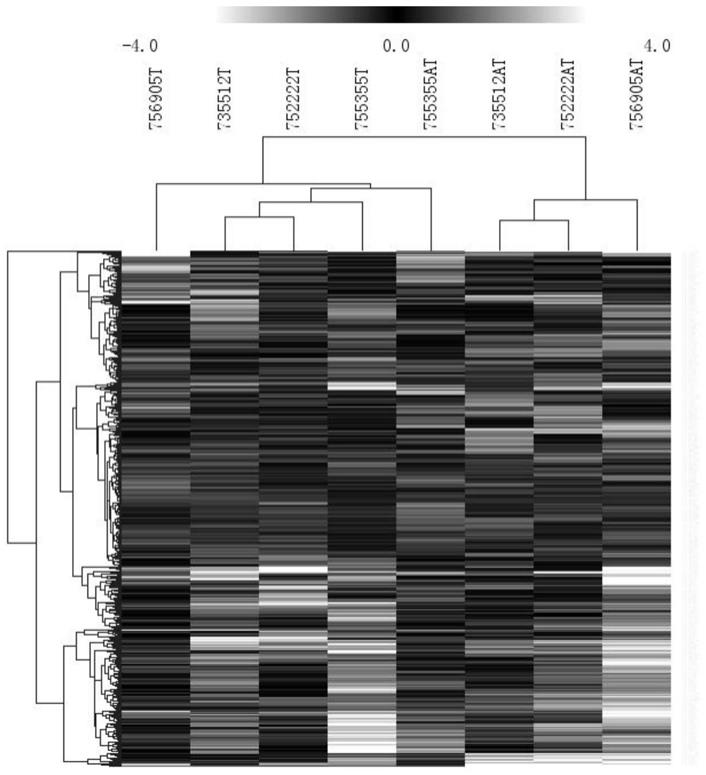
17.图1示通过高通量测序,热图分析在正常组和肾癌组中差异表达的lncrna;
18.图2示linc00113在染色体中的位置信息;
19.图3示qrt
‑
qpcr验证在肾癌组织颌正常组中中linc00113的表达差异;
20.图4示高表达linc00113和低表达linc00113的肾癌患者的总体生存分析曲线;
21.图5示高表达linc00113和低表达linc00113的肾癌患者的无病生存分析曲线。
具体实施方式
22.本发明公开了lncrna linc00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
23.本发明提供了一种非编码rna标志物,所述标志物为linc00113,核苷酸序列如seq id no.1所示。与正常组织相比,当linc00113表达水平显著下调时,提示患者肾癌风险。更低表达的linc00113,提示患者肾癌远期预后差,生存率低。
24.作为本发明的优选方案,所述标志物用于肾癌诊断的标志物。
25.本发明还提供一种用于验证如上述标志物的试剂,所述试剂包括特异性扩增linc00113的的引物,核苷酸序列如seq id no.2所示。
26.本发明还提供一种用于检测上述标志物的试剂盒,包括反转录pcr和实时定量pcr,扩增gapdh内参基因的引物,核苷酸序列如seq id no.3所示,qrt
‑
pcr和逆转录反应常
用的酶和试剂,如反转录酶,缓冲液,dntps,depc水和taq酶。
27.本发明所述的linc00113在肾癌患者中表达下调,通过检测linc00113的表达,判断受试者是否有患肾癌的风险,通过比较linc00113的表达量,可以评估提示肾癌患者的远期预后和生存率,因此linc00113可作为肾癌临床诊断评估的重要指标。
28.本发明提供的lncrna linc00113作为标志物在制备肾癌检测试剂或检测试剂盒中的应用中,所用原料及试剂均可由市场购得。
29.下面结合实施例,进一步阐述本发明:
30.实施例1 linc00113的芯片筛选
31.1、选用临床上配对肾癌组织4例和正常组织4例
32.2、采用芯片agilent human lncrna(4*180k,042818),完成8个样本检测和分析(图1)。
33.3、候选lncrna筛选。选择下调最明显linc00113研究其在肾癌中的作用。
34.实施例2 linc00113在肾癌组中表达情况
35.1、linc00113在染色体中的位置如图2所示,序列信息见seq id no.1。
36.2、设计linc00113qrt
‑
pcr引物,上下游引物为seq id no.2。
37.3、收集我院收治的90例正常组织和90例癌组织置于液氮中保存,避免rna降解。所收取的样本均经病理学检查确诊。
38.4、提取组织总rna
39.①
研磨组织所用的研钵,研杵等用品用锡箔纸包好,200℃烤4h,冷却后待用;
40.②
研磨前用液氮将研钵研杵预冷,从液氮中取出所收集的组织,立刻放入研钵中,加液氮反复研磨直至成为粉末状,加入1ml rnaiso plus将所有粉末覆盖,待rnaiso plus融化后,转移至1.5ml ep管中;
41.③
trizol法裂解后加入200μl氯仿,振荡混匀,室温静置2min,12000g,4℃离心15min;
42.④
将上层透明清液转移至新的1.5ml ep管中,加入等体积异丙醇,颠倒混匀,室温静置10min,12000g,4℃离心10min,弃上清;
43.⑤
向
④
的ep管中加入1ml 75%乙醇,颠倒洗涤rna沉淀,12000g,4℃离心5min,弃上清;
44.⑥
瞬时离心
⑤
中ep管,弃上清,室温晾干至沉淀透明,加入depc水30μl;
45.⑦
组织总rna电泳鉴定其质量,a260/a280=1.8
‑
2.0且28s:18s=1.8
‑
2.0时,rna质好,可用于后续研究。整个过程中所用的试剂和耗材均为rnase
‑
free的。
46.5、反转录
47.参照takara公司的037a试剂盒说明书进行操作。反转录体系为20μl具体步骤如下:
48.①
microtube管中配制上述
①
中的rna1μg,用depc水不齐至13μl,mix7μl,总体积20μl。
49.②
混匀后瞬时离心;
50.③
将
②
中microtube管置于pcr仪中,依次进行三个温度反应:37℃,15min;85℃保温15s;4℃保持冷却,得到的cdna溶液可直接用于pcr扩增及qrt
‑
pcr等。
51.6、qrt
‑
pcr
52.采用sybr
‑
green染料法(real
‑
time qpcr master mix,takara,dalian)进行实时荧光定量pcr,以检测正常和肾癌组织中linc00113的表达水平。具体操作如下:
53.①
取上述步骤中得到cdna,反应体系为:sybr 10μl,forward primer(10μm)0.5μl,reverse primer(10μm),0.5μl,cdna 2μl,加水至总体积为20μl。反应条件为:95℃,预变性30s;95℃,5s;60℃,20s;72℃,10s;40个反应循环。
54.②
实时荧光定量pcr使用仪器型号为罗氏rt
‑
pcrlc480ⅱ;
55.采用计算表达差异:
56.qpcr具体计算方法:通过实时荧光定量qpcr罗氏rt
‑
pcr lc480ⅱ获得该lncrna和内参gapdh的ct值并计算平均值,用lncrna的ct值减去gapdh的ct值,得
△
ct值,用癌组织的
△
ct值减去癌旁组织的
△
ct值得到
△△
ct值,计算2
‑△△
ct的值。
57.7、统计方法:采用spss17.0统计软件进行统计,所有数据以均数
±
标准差的形式表示,组间比较采用lsd
‑
t和dunnettt
‑
检验方法检验,p<0.05为有统计意义,差异显著。
58.效果分析
59.结果如图3所示所示,在90例肾癌与癌旁正常组织中,linc00113的表达在肾癌组织中显著降低(p=0.0004),这表明linc00113是诊断肾癌潜在的靶点。
60.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1