一种医用聚乳酸可降解导管及其制备方法与流程
1.本发明涉及医用导管技术领域,具体为一种医用聚乳酸可降解导管及其制备方法。
背景技术:
2.医用导管是用于医疗的管状制品,需要与人体中的组织、血液、体液等进行接触,根据应用环境,医用导管需满足各式各样的实际性能,一些导管常通过挤出机挤出,形成管状,冷却后再切割,制得医用导管,能够在生物体内或者生物体内外连通,可使用在排液、血液传输、辅助导入其他医疗器具及通过感应元件检测生物体内状况等过程中,能够制作医用导管的材料种类、及制备方法多种多样。有些医用导管需要植入人体中,为避免二次手术,植入的医用导管利用人体自然代谢,经过体液水解,并最终降解为水和二氧化碳。聚乳酸为以乳酸为主要原料的聚合物,具有生物降解能力,但其韧性较差,易发生弯曲变形。因此,我们提出一种医用聚乳酸可降解导管及其制备方法。
技术实现要素:
3.本发明的目的在于提供一种医用聚乳酸可降解导管及其制备方法,以解决上述背景技术中提出的问题。
4.为了解决上述技术问题,本发明提供如下技术方案:一种医用聚乳酸可降解导管的制备方法,包括以下步骤:
5.(1)改性聚膦腈的制备:
6.1.1取1,8-辛二酸、异山梨醇、癸二酸1,4-丁二醇,依次反应,得到酯化物a;与糖醇反应,得到酯化物b;
7.取甘氨酸、酯化物b混合,通入氯化氢,反应,得到氨基酸酯盐酸盐a;取甘氨酸、无水庚醇混合,通入氯化氢,反应,得到氨基酸酯盐酸盐b;
8.1.2取六氯三聚膦腈,加热,开环聚合,得到聚二氯膦腈;
9.将聚二氯膦腈,依次与氨基酸酯盐酸盐a、氨基酸酯盐酸盐b反应;再加入多巴胺、氨水反应,得到改性聚膦腈;
10.(2)改性聚乳酸的制备:
11.取丙交酯,在改性聚膦腈存在下聚合,得到改性聚乳酸;
12.(3)医用导管的制备:
13.取三氯甲烷,加入改性聚乳酸、聚乳酸,蒸发溶剂,真空干燥,通过挤出机挤出,形成管状,冷却,切割,制得医用导管。
14.进一步的,所述(1)包括以下工艺:
15.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至140~145℃,搅拌,反应2~4h;加入癸二酸,反应2~4h;加入1,4-丁二醇,继续反应2~4h,得到酯化物a;以异山梨醇、1,4-丁二醇为二醇原料,1,8-辛二酸、癸二酸为二酸原料,
通过加入时机、投料比的设置,得到刚柔嵌段、端部分别含有羟基、羧基的线性酯化物a,能够保持所制医用导管的降解能力,同时提高所制改性聚膦腈的机械性能、热稳定性,改善所制改性聚乳酸与聚乳酸间的相容性,促进链段结晶成核,进一步提高其韧性、弹性和热稳定性;
16.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应2~5h,得到酯化物b;糖醇为肌醇、异麦芽酮糖醇、甘露糖醇、异己糖醇中的一种或多种,多为刚性、亲水基团,能够改善物料的亲水性能、降解能力,与细胞间的亲和性;糖醇中羟基与酯化物a中的羧基反应,得到糖基改性的酯化物b,含有羟基;将糖基引入医用导管体系中,能够维持物料的生物降解能力,显著改善所制医用导管的生物相容性、物料的加工性能,链段的结晶能力提高,改性聚乳酸的力学性能、热稳定性能得到进一步改善;
17.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入1~2h,加热回流反应20~30min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b中的羟基与甘氨酸中的羧基反应,得到甘氨酸酯a;
18.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1~2h,加热回流反应20~30min,减压蒸馏,得到氨基酸酯盐酸盐b;庚醇中的羟基与甘氨酸中的羧基反应,得到甘氨酸酯b;
19.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8~12h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
20.1.2取六氯三聚膦腈纯化;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10~20h,得到聚二氯膦腈;
21.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18~36h;加入氨基酸酯溶液b,反应18~36h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18~24h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈。通过聚二氯膦腈上具有高活性的氯基,将甘氨酸酯a、甘氨酸酯b引入体系中,含糖基的生物基酯化物、氨基酸长链酯的存在,提高了改性聚膦腈的韧性、热稳定、降解性能,能够改善所制聚乳酸的机械性能;在制备聚膦腈的反应末期,引入多巴胺及其聚合物来取代聚二氯膦腈中未反应的氯基,避免发生聚膦腈的自身交联;聚膦腈主链的降解产物中含有磷酸根、胺类化合物,具有ph缓冲作用,与其支链上的氨基酸酯基团协同,缓解物料降解时产生的酸性,有效预防无菌性炎症的发生,具备一定的抗炎,并能够促矿化、骨细胞分化,表现出优异的生物相容性;
22.进一步的,所述(2)包括以下工艺:
23.取三氯甲烷,加入改性聚膦腈、丙交酯,加热至50~60℃,搅拌至完全溶解,在氮气氛围中,加入异辛酸亚锡,升温至130~140℃,回流反应24~36h;洗涤,干燥,得到改性聚乳酸。
24.在上述技术方案中,在改性聚膦腈存在条件下,丙交酯水解自聚,得到聚乳酸,并利用改性聚膦腈中的多巴胺,与改性聚膦腈交联,得到改性聚乳酸,至此,形成聚膦腈-聚乳酸网络结构,能够保持聚乳酸的降解性能,对医用聚乳酸导管进行增韧,改善导管与组织间的亲和性,防止所制医用导管的滑移;
25.进一步的,所述(3)包括以下工艺:
26.取三氯甲烷,加入改性聚乳酸、聚乳酸,充分溶解,蒸发溶剂,60~70℃真空干燥12
~24h,通过挤出机挤出,形成管状,冷却,切割,制得医用导管。
27.进一步的,所述1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5。
28.进一步的,所述糖醇为肌醇、异麦芽酮糖醇、甘露糖醇、异己糖醇中的一种或多种。
29.进一步的,所述氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为(1~3):(1~2):(3~10)。
30.进一步的,所述1.2中的纯化工艺为0.1mmhg,60℃减压升华。
31.进一步的,所述异辛酸亚锡的质量分数为1%;所述改性聚乳酸、聚乳酸的质量比为(15~30):100。
32.与现有技术相比,本发明的有益效果如下:
33.本发明的医用聚乳酸可降解导管及其制备方法,通过在聚膦腈中引入含糖基的生物基线性酯化物、氨基酸长链酯、多巴胺及其聚合物,对聚乳酸进行改性,建立改性聚乳酸的交联网络结构,在维持可降解性能的同时,改善其韧性、热稳定及其生物亲和性,导入医用导管体系中,能够有效提高所制医用导管的韧性、与组织间的亲和能力。
具体实施方式
34.下面将对本发明实施例中的技术方案进行清楚完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
35.实施例1
36.(1)改性聚膦腈的制备:
37.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h;加入1,4-丁二醇,继续反应2h,得到酯化物a;1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
38.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应2h,得到酯化物b;糖醇为甘露糖醇、异己糖醇;
39.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、甘氨酸的摩尔比为1:1;
40.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
41.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
42.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
43.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18h;加入氨基酸酯溶液b,反应18h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为1:1:3;
44.(2)改性聚乳酸的制备:
45.取三氯甲烷,加入改性聚膦腈、丙交酯,加热至50℃,搅拌至完全溶解,在氮气氛围中,加入异辛酸亚锡,异辛酸亚锡的质量分数为1%;升温至130℃,回流反应24h;洗涤,干燥,得到改性聚乳酸;
46.(3)医用导管的制备:
47.取三氯甲烷,加入改性聚乳酸、聚乳酸,改性聚乳酸、聚乳酸的质量比为15:100,充分溶解,蒸发溶剂,60℃真空干燥12h,通过挤出机挤出,形成管状,冷却,切割,制得医用导管。
48.实施例2
49.(1)改性聚膦腈的制备:
50.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至142℃,搅拌,反应3h;加入癸二酸,反应3h;加入1,4-丁二醇,继续反应3h,得到酯化物a;1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
51.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应3h,得到酯化物b;糖醇为肌醇、甘露糖醇;
52.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入1.5h,加热回流反应25min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、甘氨酸的摩尔比为1:1;
53.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1.5h,加热回流反应25min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
54.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流10h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
55.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合15h,得到聚二氯膦腈;
56.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应24h;加入氨基酸酯溶液b,反应24h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应21h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为2:1.5:6;
57.(2)改性聚乳酸的制备:
58.取三氯甲烷,加入改性聚膦腈、丙交酯,加热至55℃,搅拌至完全溶解,在氮气氛围中,加入异辛酸亚锡,异辛酸亚锡的质量分数为1%;升温至135℃,回流反应30h;洗涤,干燥,得到改性聚乳酸;
59.(3)医用导管的制备:
60.取三氯甲烷,加入改性聚乳酸、聚乳酸,改性聚乳酸、聚乳酸的质量比为22:100,充分溶解,蒸发溶剂,65℃真空干燥18h,通过挤出机挤出,形成管状,冷却,切割,制得医用导管。
61.实施例3
62.(1)改性聚膦腈的制备:
63.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至145℃,搅拌,反应4h;加入癸二酸,反应4h;加入1,4-丁二醇,继续反应4h,得到酯化
物a;1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
64.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应5h,得到酯化物b;糖醇为异麦芽酮糖醇、甘露糖醇;
65.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入2h,加热回流反应30min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、甘氨酸的摩尔比为1:1;
66.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入2h,加热回流反应30min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
67.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流12h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
68.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合20h,得到聚二氯膦腈;
69.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应36h;加入氨基酸酯溶液b,反应36h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应24h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为3:2:10;
70.(2)改性聚乳酸的制备:
71.取三氯甲烷,加入改性聚膦腈、丙交酯,加热至60℃,搅拌至完全溶解,在氮气氛围中,加入异辛酸亚锡,异辛酸亚锡的质量分数为1%;升温至140℃,回流反应36h;洗涤,干燥,得到改性聚乳酸;
72.(3)医用导管的制备:
73.取三氯甲烷,加入改性聚乳酸、聚乳酸,改性聚乳酸、聚乳酸的质量比为30:100,充分溶解,蒸发溶剂,70℃真空干燥24h,通过挤出机挤出,形成管状,冷却,切割,制得医用导管。
74.对比例1
75.(1)改性聚膦腈的制备:
76.1.1取三氯甲烷,加入1,4-丁二醇、1,4-丁二酸、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h;加入1,4-丁二醇,继续反应2h,得到酯化物a;1,4-丁二酸、1,4-丁二醇、癸二酸的摩尔比为1:2.5:2;
77.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应2h,得到酯化物b;糖醇为甘露糖醇、异己糖醇;
78.取酯化物b、丙氨酸混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、丙氨酸的摩尔比为1:1;
79.取丙氨酸、无水庚醇混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、丙氨酸的摩尔比为1:1;
80.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
81.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
82.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18h;加入氨基酸酯溶
液b,反应18h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为1:1:3;
83.其他步骤与实施例1相同,制得医用导管。
84.对比例2
85.(1)改性聚膦腈的制备:
86.1.1取三氯甲烷,加入1,4-丁二醇、1,4-丁二酸、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h;加入1,4-丁二醇,继续反应2h,得到酯化物a;1,4-丁二酸、1,4-丁二醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
87.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应2h,得到酯化物b;糖醇为甘露糖醇、异己糖醇;
88.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、甘氨酸的摩尔比为1:1;
89.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液a;
90.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
91.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:多巴胺的摩尔比为1:1:3;
92.其他步骤与实施例1相同,制得医用导管。
93.对比例3
94.(1)改性聚膦腈的制备:
95.1.1取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
96.取氨基酸酯盐酸盐b,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液b;
97.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
98.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液b,反应18h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐b:多巴胺的摩尔比为1:1:3;
99.其他步骤与实施例1相同,制得医用导管。
100.对比例4
101.(1)改性聚膦腈的制备:
102.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h;加入1,4-丁二醇,继续反应2h,得到酯化物a;1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
103.取糖醇、酯化物a混合,加热熔融,加入二氯化锗,反应2h,得到酯化物b;糖醇为甘
露糖醇、异己糖醇;
104.取酯化物b、甘氨酸混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物b、甘氨酸的摩尔比为1:1;
105.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
106.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
107.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
108.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18h;加入氨基酸酯溶液b,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b的摩尔比为1:1;
109.其他步骤与实施例1相同,制得医用导管。
110.对比例5
111.(1)改性聚膦腈的制备:
112.1.1取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h,得到酯化物a;1,4-丁二酸、1,4-丁二醇、癸二酸的摩尔比为1:2:2;
113.取酯化物a、甘氨酸混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐a;酯化物a、甘氨酸的摩尔比为1:1;
114.取甘氨酸、无水庚醇混合,通入氯化氢气体,持续通入1h,加热回流反应20min,减压蒸馏,得到氨基酸酯盐酸盐b;无水庚醇、甘氨酸的摩尔比为1:1;
115.取氨基酸酯盐酸盐a,加入四氢呋喃、三乙醇胺的混合溶液中,回流8h,过滤,得到溶液a;取氨基酸酯盐酸盐b,重复上述操作,得到溶液b;
116.1.2取六氯三聚膦腈纯化,纯化工艺为0.1mmhg,60℃减压升华;在氮气氛围中,0.1mmhg真空条件下,升温至250℃,开环聚合10h,得到聚二氯膦腈;
117.将聚二氯膦腈溶于四氢呋喃,缓慢加入氨基酸酯溶液a,反应18h;加入氨基酸酯溶液b,反应18h;加入多巴胺盐酸盐,加入氨水的醇水溶液,反应18h;加入蒸馏水沉淀,过滤,水洗,干燥;提纯,真空干燥,得到改性聚膦腈;氨基酸酯盐酸盐a:氨基酸酯盐酸盐b:多巴胺的摩尔比为1:1:3;
118.其他步骤与实施例1相同,制得医用导管。
119.对比例6
120.取三氯甲烷,加入1,8-辛二酸、异山梨醇、钛酸正四丁酯混合,在氮气氛围中,升温至140℃,搅拌,反应2h;加入癸二酸,反应2h;加入1,4-丁二醇,继续反应2h,重复多次,得到生物基聚酯;1,8-辛二酸、异山梨醇、癸二酸、1,4-丁二醇的摩尔比为1:2:2:0.5;
121.与聚乳酸按照15:100的质量比共混,制得医用导管。
122.对比例7
123.取聚乳酸,制得医用导管。
124.实验
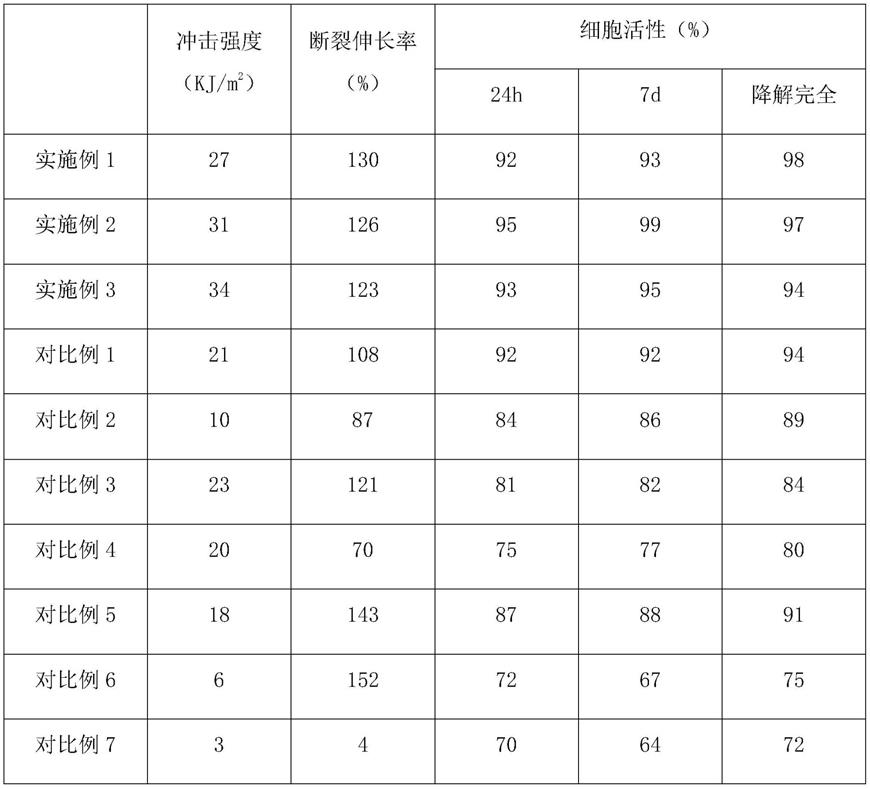
125.取实施例1-3、对比例1-7中得到的医用导管,制得试样,分别对其性能进行检测并记录检测结果:
126.细胞活性测试:取试样灭菌处理,浸没于培养基(99wt%高糖dmem+1wt%双抗)中,浸提24h、7d、试样完全降解,离心取上清液,加入血清,使得血清浓度为10wt%,稀释10倍,培养24h,采用mtt比色法,测定活细胞数量,判断细胞活性;
[0127][0128]
根据上表中的数据,可以清楚得到以下结论:
[0129]
实施例1-3中得到的医用导管与对比例1-7得到的光医用导管形成对比,检测结果可知,
[0130]
与对比例7相比,实施例1-3中得到的医用导管,具有更高的冲击强度、断裂伸长率数据、细胞活性数据,这充分说明了本技术实现了对所制医用导管韧性、生物亲和能力的提高;
[0131]
与实施例1相比,对比例1中酯化物a的组分不同、并将甘氨酸替换为丙氨酸,对比例2中未引入氨基酸酯盐酸盐b,对比例3中未引入氨基酸酯盐酸盐a,对比例4中未引入多巴胺盐酸盐,对比例5中未引入糖醇,对比例6中为生物基聚酯与聚乳酸的直接共混,对比例7为纯聚乳酸,其冲击强度、断裂伸长率数据各有变化,细胞活性数据明显低于实施例,可知本技术所制医用导管的组分及其制备工艺能够促进其韧性、生物亲和能力的提高。
[0132]
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实
体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程方法物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程方法物品或者设备所固有的要素。
[0133]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改等同替换改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1