一株东洋芽孢杆菌及其应用
1.本发明属于植物内生细菌的提取与开发技术领域,具体涉及一株东洋芽孢杆菌及其应用。
背景技术:
2.益生菌是一类对宿主有益的活性微生物。益生菌能竞争性地占据粘膜上皮细胞的受体,并抑制病原体与上皮壁的粘附。此外,益生菌会产生细菌素、过氧化氢和有机酸等抗菌物质,这些物质可以减少病原菌的数量和组成。
3.植物组织内含有一类有益的共生微生物(主要是细菌和真菌),称为内生菌。在植物-内生菌的关系中,植物为内生菌提供营养和保护,而内生菌增强了植物的防御能力和抗逆性。研究表明,内生菌会产生许多具有活性的次级代谢产物,其功能与各自植物宿主的生化成分相同。
4.紫茎泽兰(ageratina adenophora)是菊科一种入侵性极强的杂草,在世界范围内造成了巨大的经济损失。紫茎泽兰能引起动物中毒,并且对周围植物有较强的化感作用,对畜牧业以及农业具有较大的危害性。
5.目前,对紫茎泽兰的研究已逐渐从毒性预防转向生物利用。然而,紫茎泽兰中具有益生菌潜力的内生菌尚未完全报道。因此,本研究首次利用小鼠模型对紫茎泽兰中潜在的益生内生菌进行分离和鉴定,并评价其对动物健康、生长性能、抗氧化活性、肠道完整性和肠道微生物区系的生物学效应,为进一步研究和开发紫茎泽兰益生菌奠定基础。
技术实现要素:
6.针对现有技术存在的问题,本发明提供一株东洋芽孢杆菌及其应用,该东洋芽孢杆菌是从紫茎泽兰内生菌中分离获得,具有调节肠道微生物群、改善生长性能、抗氧化能力等作用,有望进一步开发成人类及动物益生菌。本发明的技术方案为:
7.第一方面,本发明提供一株东洋芽孢杆菌,保藏编号为cctcc no:m20211138,已于2021年9月6日在中国典型培养物保藏中心提交保藏,分类命名为东洋芽孢杆菌sau-19(bacillus toyonensissau-19)。
8.进一步地,所述东洋芽孢杆菌具有革兰氏阳性、过氧化氢酶阳性、耐胆盐、耐盐、耐ph和发酵糖特性。
9.益生菌特性试验表明该菌株能显著改善小鼠的生长性能、抗氧化能力、小肠的结构和完整性,并在不引起任何健康并发症的情况下调节肠道微生物群。基于此技术效果,第二方面,本发明提出保藏编号为cctcc no:m 20211138的东洋芽孢杆菌在防治肠道菌群失衡中的应用或者在制备防治肠道菌群失衡的益生菌制剂中的应用。
10.第三方面,本发明提供一种益生菌制剂,包括保藏编号为cctcc no:m20211138的东洋芽孢杆菌。
11.第四方面,本发明提供上述益生菌制剂在制备动物饲料中的应用。
12.第五方面,本发明提供一种提高动物生长性能和免疫力的饲养方法,包括:采用包含上述益生菌制剂的饲料饲喂动物。
13.综上,本发明从入侵性毒草紫茎泽兰中分离出天然植物内生细菌,选出了一株具有益生菌功效的内生细菌sau-19,经形态学和分子生物学鉴定确定其为东洋芽孢杆菌。动物实验表明京东芽孢杆菌sau-19在给药35天后能显著改善小鼠的生长性能、抗氧化能力、小肠的结构和完整性,并在不引起任何健康并发症的情况下调节肠道微生物群。因此,东洋芽孢杆菌sau-19有望作为未来人类和动物的益生菌。
附图说明
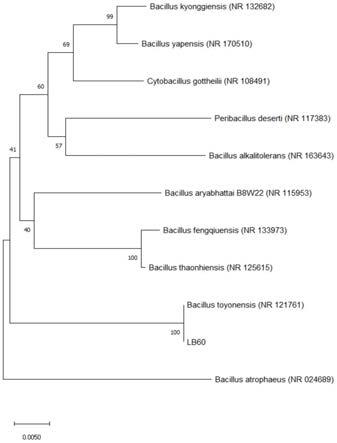
14.图1为本发明实施例2中菌株sau-19的系统发育进化树。
15.图2为本发明实施例3中用东洋芽孢杆菌sau-19灌胃35d后小鼠小肠切片的组织病理学观察,其中,图a为治疗组组织病理学染色照片,图b为小鼠小肠回肠段组织学炎症损伤评分;炎症细胞浸润用白色箭头表示,出血用灰色箭头表示,结构损伤用黑色箭头表示。
16.图3为本发明实施例3中东洋芽孢杆菌sau-19对小鼠小肠绒毛高度和隐窝深度的影响,其中,图a为小鼠回肠绒毛高度,图b为小鼠回肠隐窝深度。
17.图4为本发明实施例3中东洋芽孢杆菌sau-19对小鼠抗氧化指数、dao和siga活性的影响,其中,图a为血清中mda酶的水平,图b为血清中sod酶的水平,图c为血清中dao的浓度,图d为小肠内容物中siga的水平。
18.图5为本发明实施例3中东洋芽孢杆菌sau-19对小鼠小肠组织紧密连接蛋白的影响,其中,图a为肠切片的免疫组织化学染色照片(黄色区域代表occludin),图b为各组小鼠小肠occludin水平的免疫组化分析,图c为occludin在小肠组织中的mrna表达,图d为zo-1在小肠组织中的mrna表达。
19.图6为本发明实施例3中东洋芽孢杆菌sau-19对小鼠小肠组织中促炎和抗炎相关细胞因子的相对mrna表达的影响,其中,图a-c为促炎细胞因子的mrna表达,图d-e为抗炎细胞因子的mrna表达。
20.图7为本发明实施例3中东洋芽孢杆菌sau-19对小鼠小肠内容物中细菌计数的影响,其中,图a为大肠杆菌菌落计数,图b为沙门氏菌菌落计数,图c为金黄色葡萄球菌菌落计数,图d为乳酸杆菌菌落计数。
21.图8为本发明实施例3中东洋芽孢杆菌sau-19对小鼠盲肠内容物中细菌计数的影响,其中,图a为大肠杆菌菌落计数,图b为沙门氏菌菌落计数,图c为金黄色葡萄球菌菌落计数,图d为乳酸杆菌菌落计数。
具体实施方式
22.本发明菌种sau-19,分类命名:东洋芽孢杆菌sau-19(bacillus toyonensissau-19),于2021年9月6日在中国典型培养物保藏中心(cctcc)提交保藏,地址为湖北省武汉市武昌区八一路299号,保藏号为:cctcc no:m 20211138。
23.本发明实施例采用的紫茎泽兰采集自四川省凉山彝族自治州德昌县苍州街道办王所村。
24.本发明实施例采用的小白鼠和基础日粮(表1)由成都达硕实验动物有限公司购
买,日粮组成如表1所示。
25.表1.基础日粮的组成。
[0026][0027]
本发明实施例采用的大肠杆菌cmcc 44103、鼠伤寒沙门氏菌st19和鼠李糖乳杆菌ggatcc 53103来自中国四川农业大学兽医学院。
[0028]
在本发明的描述中,需要说明的是,实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0029]
下面结合附图和具体实施方式对本发明作进一步详细的说明,以帮助本领域的技术人员对本发明的发明构思、技术方案有更完整、准确和深入的理解,本发明的保护范围包括但不限于以下实施例,在不偏离本技术的精神和范围的前提下任何对本发明的技术方案的细节和形式所做出的修改均落入本发明的保护范围内。
[0030]
实施例1
[0031]
本实施例提供一株东洋芽孢杆菌sau-19株的分离过程,具体如下:
[0032]
(1)植物样本表面消毒:取无菌水冲洗新鲜的紫茎泽兰根、茎、叶、花组织后,用无菌滤纸吸干水分,先用3%naclo浸泡3min,然后用0.1%hgcl2浸泡3min,接着用75%乙醇3min,无菌水冲洗5次后,用无菌滤纸吸干水分。取最后一次清洗组织的无菌水0.2ml,涂布于pda培养基上,28℃培养,检验样品表面消毒是否彻底。
[0033]
(2)将表面消毒后的植物样本,用无菌刀片切割成1cm
×
1cm大小的片段,接种到lb琼脂培养基上。在30℃培养箱内培养20h,待其切口边缘长出菌落后,将组织块周围生长的细菌菌斑用接种环挑取到lb琼脂培养基上,采用四区划线法反复纯化直至获得纯净菌株,分离出共计8株内生细菌。将纯化的内生细菌用30%的甘油保存在-80℃冰箱中,以供后续研究。
[0034]
为筛选出具有潜在益生功能的内生细菌,对以上8株内生细菌进行形态学和分子生物学测试,选择具有革兰氏阳性、过氧化氢酶阴性反应、杆状、白色或乳白色类似乳酸菌(lab)表型特征的菌落。共筛选出一株具有以上特征的菌株sau-19,如表1所示。
[0035]
表1紫茎泽兰内生细菌sau-19形态及生化部分特征
[0036][0037][0038]
实施例2
[0039]
本实施例对实施例1获得的一株菌株sau-19进行生理生化和分子生物学鉴定,具体过程如下:
[0040]
(1)糖类发酵试验
[0041]
在浓度为2%的葡萄糖、蔗糖和d-山梨醇中加入0.004%的酚红,在lb发酵液中进行葡萄糖、蔗糖和d-山梨醇的发酵。所有试管在121℃下灭菌15min。试管接种单一菌落。细菌的阳性反应通过培养基的颜色变化(从红色到黄色)来表示。
[0042]
表2紫茎泽兰内生细菌sau-19糖酵解
[0043][0044]
(2)ph耐受性试验
[0045]
用1m hcl和1m naoh制备不同ph值的lb肉汤。将sau-19菌液接种到不同ph(2.5、4.5和6.5)的lb培养基中,37℃下培养24小时。观察到培养基浑浊则具有ph耐受性。结果如表2所示:内生菌sau-19在不同ph值的培养基中都有生长。
[0046]
(3)耐胆盐试验
[0047]
将sau-19菌液接种到含有不同浓度(0、0.2和0.4%)胆汁盐(脱氧胆酸钠(dca))的lb培养基中,37℃下培养24小时。观察到培养基浑浊则具有胆盐耐受性。不含胆盐的培养基作为阳性对照,不含菌液的培养基作为阴性对照。结果如表3所示:内生菌sau-19在不同胆盐浓度下的培养基中都有生长。
[0048]
(4)耐盐性试验
[0049]
将sau-19菌液接种到含不同浓度(0、2、4、6.5%)nacl的lb培养基中,37℃下培养24小时。观察到培养基浑浊则具有耐盐性。不含nacl的培养基作为阳性对照,不含菌液的培养基作为阴性对照。结果如表3所示:内生菌sau-19在不同nacl浓度下的培养基中都有生长。
tgatcmtggctcag和1492r:gtattaccgcggctgctgag)通过pcr(applied biosystems-9700)扩增16s rdna,将扩增产物送去有康生物(成都)有限公司进行测序。将测定的16s rdna序列与genbank中已知核酸序列进行blsat分析,从中获得与菌株同源的序列,利用mega7.0软件构建系统发育树。根据16s rdna测序结果,sau-19与东洋芽孢杆菌(bacillus toyonensis)菌株bct-7112具有高度的序列同源性(99.86%),判定其为东洋芽孢杆菌(bacillus toyonensis),登录号:mw287198,命名为bacillus toyonensissau-19。基于16s rrna基因序列的菌株系统发育分析如图1所示。
[0067]
实施例3
[0068]
本实施例提供强化实施例1获得的菌株sau-19的动物(体内)实验,具体如下:
[0069]
(1)实验动物
[0070]
本研究选用健康雄性spfkm小鼠48只(5周龄,体重25-30g)。12只小鼠用于安全性实验,36只小鼠用于喂养实验。为进行安全性实验,将小鼠平均分成3组,对照组给予普通饲料和生理盐水1ml,其余两组分别给予普通饲料和1
×
106cfu/ml的菌悬液1ml(益生菌最低摄入量范围)。在受控温度(22-24℃)和湿度(40-60%)的条件下,生理盐水及菌悬液均加入饮用水中进行采食。每天记录死亡率、疾病(如腹泻和呕吐)和采食量,直到第20天。结果表明,每天服用sau-19菌液不会减少采食量,也不会导致任何疾病和死亡,因此在试验中使用这种细菌内生菌是安全的。
[0071]
(2)商业益生菌
[0072]
鼠李糖乳杆菌(lactobacillus rhamnosus)gg atcc 53103是一种在世界各地使用的商业产品。它最初是由中国成都四川农业大学兽医学院倪雪芹教授的实验室从一名健康成人的粪便中分离出来的。该菌株在1
×
10
6-1
×
10
11
cfu/ml或cfu/g的安全剂量范围内可促进家禽和大型动物的生长和健康。此外,该菌株的有益作用已在临床和人类干预研究中得到广泛研究,因此,本试验选择鼠李糖乳杆菌作为我们研究的阳性对照。
[0073]
(3)实验设计
[0074]
将36只雄鼠(5周龄;bw 25-30g)随机分为3组,每组12只小鼠。a组(阴性对照)饲喂正常饲料(20g)+1ml每日0.9%生理盐水(ns),b组(阳性对照)饲喂正常饲料(20g)+1ml每日1
×
106cfu ml-1
鼠李糖乳杆菌gg(lgg)菌悬液,c组饲喂正常饲料(20g)+1ml的1
×
106cfuml-1
bacillus toyonensis sau-19菌悬液。实验室温度(22-24℃)、湿度(40-60%),光照12h,实验共计35天。每天监测动物是否有任何异常、疾病(如腹泻或呕吐)和死亡。在整个实验过程中,在上午8:00时,分别向各组补充饲料及样品。在整个实验期间每天监测和记录采食量,保证饮水安全及环境卫生。
[0075]
3-1)菌悬液制备
[0076]
在35天的试验期后,检测各组小鼠体重及饲料转化率。用co2窒息法对小鼠进行安乐死(n=8只/组);所有小鼠在安乐死前禁食12小时。解剖时,将腹主动脉的血液收集到涂有抗凝剂的试管中;在超净台内取出小肠及盲肠内容物进行后续测定。
[0077]
3-2)组织病理学分析
[0078]
称重分离的肠后,无菌切割肠道片段,将样品(尸检时收集的每个肠的1/2)固定在4%多聚甲醛中,然后在分级(70-100%)乙醇中脱水。在二甲苯中澄清后,将每个样品包埋在石蜡中并制备5μm厚的切片。为了分析,将样品用苏木精和伊红染料染色,然后使用光学
显微镜进行观察。同时测量肠断绒毛高度和隐窝深度。
[0079]
3-3)小鼠血清dao水平的测定
[0080]
使用elisa试剂盒(jingmei biological technology,江苏,中国)测定血清中二胺氧化酶(dao)的浓度,以评估肠道粘膜屏障损伤的程度。每个试剂盒的灵敏度水平为0.1pg/ml。
[0081]
3-4)小鼠血清抗氧化能力的测定
[0082]
使用试剂盒(南京建成生物工程研究所,南京,江苏,中国)测量血清中的超氧化物歧化酶(sod)和丙二醛(mda)。
[0083]
3-5)小鼠小肠内容物中siga水平的测定
[0084]
将采集的小肠内容物储存于-80℃冰箱中。使用elisa试剂盒(sagon biotech,中国上海)测定小肠内容物中的siga水平。试剂盒的灵敏度水平为0.1μg/ml。
[0085]
(4)总rna提取和定量实时rt-pcr(qrt-pcr)
[0086]
小肠组织样品(30mg/只小鼠)用液氮快速冷冻后,研磨成粉末。使用动物总rna分离试剂盒(sagon biotech,上海)提取总rna。测定其浓度和纯度后,并使用primescrip rt试剂盒(takara,tokyo japan)进行反转录。然后用sybr premix extaq(takara)和cfx96热循环仪(biorad,hercules,ca)进行qrt-pcr。pcr的条件如下所示:95℃5分钟,然后40个循环的95℃,变性15秒,60℃,退火60秒和70℃,延伸25秒。每个qrt-pcr反应体积为10μl,含有5μltb green tm premix(takara),1μl正向和反向引物,1μlcdna和2μl不含dnase/rnase的去离子水(tiangen,beijing,中国)。用于分析目的基因的引物由ncbi的genbank设计,如表5所示。将每个样品中的相对基因表达标准化为内部对照(β-肌动蛋白);数据分析是使用2-δδct法。重复三次。
[0087]
表5用于实时pcr分析的引物
[0088]
[0089][0090]
(5)小鼠小肠和盲肠微生物含量的定量测定
[0091]
将采集的小肠和盲肠内容物(1g)以1:10的比例在无菌盐水溶液中稀释。将稀释的内容物涡旋2分钟以获得均匀的悬浮液,然后将0.1ml涂布在不同的培养基上用于总细菌计数。用大肠杆菌显色培养基计数大肠杆菌、亚硫酸铋琼脂培养基计数沙门氏菌、甘露醇盐琼脂培养基计数金黄色葡萄球菌,而mrs培养基计数乳酸杆菌。在37℃厌氧条件下培养24小时。
[0092]
(6)统计分析
[0093]
使用spss 20统计分析软件对所有数据进行统计分析。shapiro-wilk检验用于检验数据的正态性。所有实验结果均以平均值
±
标准差表示,统计显著性采用单因素方差分析(anova)和tukey检验。在p《0.05时,数值差异显著。
[0094]
6-1)东洋芽孢杆菌sau-19对小鼠生长性能、器官指数和脾脏免疫指数的影响
[0095]
根据我们的观察,所有治疗组看起来都健康、活跃。治疗组未出现死亡或胃肠道不适症状,如呕吐和腹泻(数据未显示)。此外,与阴性对照组(表6)相比,在35天的实验期后,sau-19组通过增加体重和提高饲料转化率(p《0.05)改善了小鼠的生长性能,与lgg组相比无显著差异。与对照组相比,sau-19组小鼠肝脏重量与肝指数无显著差异(表6,p》0.05),但脾重量和脾指数显著增加(表6,p《0.05)。
[0096]
表6喂食从紫茎泽兰中分离的toyonensis bacillus sau-19的小鼠的增重(g)、饲料转化率(frc)和器官指数。
[0097][0098]
该表以平均值
±
标准偏差(sd)表示。不同上标a-b的色谱柱在统计学上存在差异(p《0.05)。对照组给予小鼠生理盐水。lgg给予106株鼠李糖乳杆菌,sau-19组给予106株bacillus toyonensis sau-19。
[0099]
6-2)组织病理学结果
[0100]
如图2的a图所示,与对照组相比,治疗组的小肠结构完整,没有明显的病理变化。粘膜下层、肌层和肠腺排列正常,固有层和上皮层形态完整。此外,与对照组相比,治疗组的粘膜和肌肉层清晰。对照组出现明显的病理改变,表现为肠道结构损伤、出血、粘膜下水肿、上皮层轻度局部炎性浸润。此外,回肠切片的组织学检查显示,与对照组相比,治疗组的炎症损伤累积分数较低(图2的b图,p《0.05),且lgg治疗组和b.toyo sau-19治疗组差距不大。对照组出现出血、水肿、坏死、炎症等病理改变,而治疗组未见。
[0101]
6-3)东洋芽孢杆菌sau-19对小鼠小肠绒毛高度和隐窝深度的影响
[0102]
治疗组小肠回肠段的绒毛高度和隐窝深度显著高于对照组(如图3所示,p《0.05),且lgg治疗组和b.toyo sau-19治疗组差距不大。
[0103]
6-4)东洋芽孢杆菌sau-19对小鼠抗氧化指标、dao活性和siga水平的影响
[0104]
本研究结果表明,与对照组相比,所有治疗组的血清mda水平均降低(图4的a图,p《0.05)。相反,治疗组的sod水平显著高于对照组(图4的b图,p《0.05)。然而,两个治疗组在这两种情况下均无显著差异(p》0.05)。
[0105]
对于血清中dao活性,结果显示,治疗组中的dao活性低于对照组(图4的c图,p《0.05)。然而,lgg和sau-19之间无显著差异(p>0.05)。
[0106]
对于小肠内容物中的siga水平,结果显示,治疗组中的siga水平高于对照组(图4的d图,p《0.05)。然而,lgg和sau-19之间无显著差异(p>0.05)。
[0107]
6-5)东洋芽孢杆菌sau-19对小鼠小肠组织紧密连接蛋白的影响
[0108]
免疫组织化学分析显示,与对照组相比,治疗组中的occludin水平增加(图5的a图和b图,p《0.05)。此外,我们观察到,lgg组中occludin的水平显着高于b组。toyo sau-19(p<0.05)。此外,紧密连接蛋白的相对mrna表达结果显示,与对照组相比,治疗组中紧密连接蛋白(occludin和z0-1)的水平显着更高(图5的c图和d图,p《0.05)。此外,lgg和sau-19组之间没有显著差异。
[0109]
6-6)东洋芽孢杆菌sau-19对小鼠小肠组织促炎症和抗炎相关细胞因子相对mrna表达的影响
[0110]
炎症相关细胞因子的相对mrna表达结果显示,与对照组相比,治疗组小肠组织中促炎细胞因子(il-1β、tfn-α、il-2)水平降低,抗炎细胞因子(il-4和il-10)水平升高(图6的a-e图,p《0.05)。
[0111]
6-7)东洋芽孢杆菌sau-19对小鼠小肠及盲肠细菌计数的影响
[0112]
小肠和盲肠内容物的微生物计数结果如图7和图8所示。与对照组相比,lgg组和sau-19组小肠及盲肠中大肠杆菌、沙门氏菌及金黄色葡萄球菌的数量显著降低(p《0.05)。此外,与对照组相比,sau-19组小肠及盲肠中乳酸杆菌的数量显著增加(p《0.05),并且sau-19组与lgg组效果相当。
[0113]
显然,可以将本发明的东洋芽孢杆菌开发成益生菌制剂应用到动物饲料和饲养过程中,进而起到提高动物生长性能和免疫力的作用。
[0114]
综上,本发明从入侵性毒草紫茎泽兰中分离出天然植物内生细菌,选出了一株具有益生菌功效的内生细菌sau-19,经形态学和分子生物学鉴定确定其为东洋芽孢杆菌。动物实验表明京东芽孢杆菌sau-19在给药35天后能显著改善小鼠的生长性能、抗氧化能力、小肠的结构和完整性,并在不引起任何健康并发症的情况下调节肠道微生物群。因此,东洋芽孢杆菌sau-19有望作为未来人类和动物的益生菌。
[0115]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1