一种癌细胞分析基因电路组件及其制备方法与流程
1.本发明涉及基因工程技术领域,具体而言,涉及一种癌细胞分析基因电路组件及其制备方法。
背景技术:
2.随着医疗手段的不断演进和基因技术的突飞猛进的发展,医学工作者发现,经基因改造的细胞可以对其他细胞,如癌细胞的特定状态作出高特异性的检测,如基于hela细胞中特有的microrna表达模式所建立的能够区分人宫颈癌细胞hela与人正常健康细胞hek293的人工合成基因电路。这些人工合成基因电路可以在甄别癌细胞以及靶向杀灭癌细胞方面发挥优异的性能。
3.但是,现有的基因电路所使用的驱动元件往往仅通过较为单一固定的microrna及自然启动子的表达模式来组成,而这套表达模式仅能区分癌细胞与正常健康细胞,不能区分在癌细胞总群体中因癌细胞之间的异质性而出现的各类癌细胞亚群,而癌细胞之间的异质性恰恰就是癌细胞耐药复发的最关键因素,对于同时存在的多种状态的癌细胞进行准确识别并判断所占比例将有助于研究癌细胞之间的异质性。因此,亟待提供一种癌细胞分析基因电路组件及制备方法,从而能够更好的识别癌细胞的状态,并判断各个状态的癌细胞的比例。
技术实现要素:
4.本发明的目的是提供一种癌细胞分析基因电路组件及制备方法,以至少部分地解决上述的技术问题。
5.根据本发明的一个方面,本发明提供一种癌细胞分析基因电路组件,包括至少两种癌细胞分析基因电路,每种所述癌细胞分析基因电路分别针对不同的癌细胞状态且并联连接;
6.每种所述癌细胞分析基因电路至少包括依次连接且与所针对的癌细胞状态对应的正向合成启动子、条形码区域和负向合成启动子,所述正向合成启动子包含所述癌细胞状态下的癌细胞具备的正向增强子,所述负向合成启动子包含所述癌细胞状态下的癌细胞具备的负向增强子。
7.优选地,所述正向合成启动子的蛋白结合区域单一。
8.优选地,所述负向合成启动子的蛋白结合区域单一。
9.优选地,在所述负向合成启动子的下游端还包括荧光蛋白序列。
10.优选地,所述荧光蛋白序列为eyfp荧光蛋白序列。
11.优选地,所述荧光蛋白序列的下游端还依次连接有正向合成启动子、条形码区域和负向合成启动子。
12.优选地,每种所述癌细胞分析基因电路包括依次连接的3'utr段、荧光蛋白序列、lac启动子、正向合成启动子、条形码区域、cmv启动子、mscarlet序列、wpre、负向合成启动
子、lac终止子和3'utr段,且每种所述癌细胞分析电路中的所述正向合成启动子所包含的正向增强子和负向合成启动子所包含的负向增强子均来自于对应的所述癌细胞状态下的癌细胞。
13.优选地,所述条形码区域的序列如seq id no.1所示。
14.优选地,所述癌细胞状态为mhcc97h系癌细胞的高侵袭型细胞状态、细胞骨架重组活跃型细胞状态、高干性型细胞状态、高分化型细胞状态、快分裂周期型细胞状态、慢分裂周期型细胞状态、免疫逃逸型细胞状态、抗凋亡型细胞状态中的至少两种。
15.本发明实施例还提供一种癌细胞分析基因电路的制备方法,包括如下步骤:
16.步骤1:分别获取至少两种癌细胞状态下的癌细胞的正向增强子和负向增强子;
17.步骤2:基于每种所述癌细胞状态对应的所述正向增强子和所述负向增强子获得正向合成启动子和负向合成启动子;
18.步骤3:获取条形码区域,将所述正向合成启动子、所述条形码区域和所述负向合成启动子依次相连,即获得癌细胞分析基因电路。本发明通过对获取能够表征肿瘤细胞不同表型的正向增强子和负向增强子,从而构成正向合成启动子和负向合成启动子,并结合能够辅助判断的条形码区域,使得本发明可以精准标定癌细胞状态,并可以通过高通量细胞实验等手段分析出各种状态的癌细胞的所占比例信息,有助于帮助分析癌细胞之间的异质性。
附图说明
19.通过阅读参照以下附图所作的对非限制性实施例的详细描述,本发明的其它特征、目的和优点将会变得更明显:
20.图1是根据本发明的获取癌细胞分析基因电路的方法的示意图;
21.图2是根据本发明的癌细胞分析基因电路的示意图。
具体实施方式
22.下面结合附图和实施例对本发明作进一步的详细说明。可以理解的是,此处所描述的具体实施例仅用于解释相关发明,而非对该发明的限定。为了便于描述,附图中仅示出了与发明相关的部分。
23.需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
24.本技术实施例提供一种癌细胞分析基因电路组件及制备癌细胞分析基因电路的方法,需要说明的是,该基因电路组件中的癌细胞分析基因电路可以应用于多种状态的癌细胞的识别,如smmc-7721或mhcc997h癌细胞系在耐药条件下所产生免疫逃逸、骨架重组、侵袭迁移等多种状态,也可以与靶向药物相结合,制备得到能够精准杀灭某种亚型的癌细胞的靶向药物等,其具体用途本技术并不作限制。对应的,本技术实施例中所述的癌细胞分析基因电路,即由启动子或包含启动子的元件所构成的,具备识别功能的一段基因片段,因其负责识别特定的目标基因片段并启动后续的识别显示或治疗过程,因此称其为基因电路。
25.本技术实施例中的癌细胞系,主要是指基因表达类似的一组癌细胞的总称,例如
smmc-7721或mhcc997h系,本技术实施例中的癌细胞可为肝癌、胶质母细胞瘤、胆道癌、肺癌、胰腺癌、黑素瘤、骨癌、乳腺癌、结直肠癌、胃癌、前列腺癌、白血病、子宫癌、卵巢癌、淋巴瘤或脑癌,更优选为肝癌、胶质母细胞瘤或胆道癌,最优选为肝癌。
26.本技术中的癌细胞状态,主要是指在药物作用或连续培养的情况下,癌细胞所表现出的肿瘤癌干性维持分化、免疫逃逸、骨架重组、侵袭迁移、细胞分裂周期快慢等多种状态,其基因表达与所属的癌细胞系有一定区别,尤其是不同癌细胞状态下的癌细胞的基因序列中的增强子会有较大区别。这样的不同癌细胞状态的癌细胞往往是在癌症治疗过程中反复复发的元凶,其具备耐药性,同时还有可能具备高转移性等其它恶性性状,也是本发明所针对的主要目标。
27.在本技术实施例中,对本发明所提供的癌细胞分析基因电路组件进行测试和实践所使用的病毒载体可为来源于逆转录病毒,例如,人免疫缺陷病毒(human immunodeficiency virus,hiv)、小鼠白血病病毒(murine leukemia virus,mlv)、禽肉瘤/白血病病毒(avian sarcoma/leucosis virus,aslv)、脾脏坏死病毒(spleennecrosis virus,snv)、劳氏肉瘤病毒(rous sarcoma virus,rsv)、小鼠乳腺肿瘤病毒(mouse mammary tumor virus,mmtv)等)、腺病毒(adenovirus)、腺相关病毒(adeno-associated virus,aav)、或单纯疱疹病毒(herpes simplex virus,hsv)等,但不限于此。基于逆转录病毒构建启动子测试慢病毒的技术为本领域技术人员所熟知,此处不再赘述。
28.本技术实施例中,除了如启动子、操纵子、起始密码子、终止密码子、聚腺苷酸化信号和增强子的表达调控元件以外,本发明的载体还包括用于膜靶向或分泌的信号序列或前导序列,并可以根据目的以各种方式进行制备。载体的启动子可为组成型或诱导型。此外,表达载体包含用于选择含有载体的宿主细胞的选择标记,并且当表达载体为可复制的表达载体时,可包括复制子。载体可自我复制或整合到宿主dna中。
29.在本技术实施例中,所使用的术语“相连”和“连接”是指,执行常规功能的核酸表达调控序列与编码目的基因的核酸序列的功能性连接(functional linkage)。例如,当在逆转录病毒的基因序列中插入启动子时,逆转录病毒的基因序列的表达可处于启动子的影响或调控之下。当启动子的基因序列与逆转录病毒的基因序列之间的连接特性不诱导移码突变,且在表达调控序列不抑制核酶的表达时,则可以认为完成了本技术实施例中的“相连”或“连接”。可使用本领域公知的基因重组技术来实现该“相连”或“连接”过程,并且可以采用本领域公知的酶来进行位点特异性dna的切割和连接。
30.本技术实施例中的荧光蛋白,可以选自萤光素酶(luciferase)、绿色荧光蛋白(gfp)、修饰型绿色荧光蛋白(modified green fluorescent protein,mgfp)、增强型绿色荧光蛋白(enhanced green fluorescentprotein,egfp)、红色荧光蛋白(rfp)、修饰型红色荧光蛋白(modified red fluorescent protein,mrfp)、增强型红色荧光蛋白(erfp)、蓝色荧光蛋白(bfp)、增强型蓝色荧光蛋白(ebfp)、黄色荧光蛋白(yfp)、增型黄色荧光蛋白(eyfp)、青色荧光蛋白(cfp)或增强型青色荧光蛋白(ecfp)等,但不限于此。通过将荧光蛋白插入于目的基因中,可以观察到癌细胞特异性核酶的表达水平。对于本领域技术人员来说,可以理解的是,可用这种方法来判断是否存在特定种类的癌细胞状态下的癌细胞。
31.本技术实施例中的增强子的获取方式,可以是通过已经探明各种癌细胞状态的癌细胞株的文献记载,也可以是通过联合耐药培养等手段培养出不同癌细胞状态的癌细胞,
并从其中分析得到不同癌细胞状态的癌细胞所包含的增强子等,本发明对于增强子的获得方式并不作过多限制,能够获得足以满足制作启动子要求的正向增强子和负向增强子即可。
32.本技术实施例中的条形码区域(barcode region),主要是可以是适于独特识别基因类型相关特征的任何长度和序列。条形码区域可用于表示癌细胞任何类型的独特特征,包括修饰类型(例如dna甲基化、组蛋白甲基化、组蛋白变体等)、复制数量(例如,技术复制(technical replicates))或浓度。条形码区域也可以表示不存在任何修饰。在一些实施方案中,条形码区域具有约6至约50个碱基对,例如约7至约30个碱基对,例如约8至约20个碱基对,例如约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个碱基对或其中的任何范围的长度。
33.上述的条形码区域的序列的一种实现方式的序列如seq id no.1所示,具体如下:
34.gggcgagcgcgcgcaaatggcggcgactagtgatatccgtctctcggcgctgtgctcgttccacacaccgg。
35.本发明提供一种癌细胞分析基因电路组件,包括不少于两种癌细胞分析基因电路,每种癌细胞分析基因电路分别针对一种癌细胞状态。例如,对于mhcc97h系癌细胞,目前已经探明的癌细胞状态就包括高侵袭型细胞、细胞骨架重组活跃型细胞、高干性型细胞、高分化型细胞、快分裂周期型细胞、慢分裂周期型细胞、免疫逃逸型细胞、抗凋亡型细胞8种不同的癌细胞状态,当然,本技术实施例中的癌细胞分析基因电路可以是针对某一系癌细胞所有可能出现的细胞状态,也可以是仅针对其中部分的癌细胞状态。
36.在本技术实施例中,癌细胞分析基因电路至少包括依次连接且与所针对的癌细胞状态对应的正向合成启动子、条形码区域和负向合成启动子,正向合成启动子包含癌细胞状态下的癌细胞具备的正向增强子,负向合成启动子包含癌细胞状态下的癌细胞具备的负向增强子。这里的正向增强子和负向增强子,又称为强增强子和弱增强子或正增强子和负增强子,前者是对基因转录起正向增强作用,后者对基因转录起负调节作用,两者联用,即可完成一个完整的控制转录的过程。由于这里的正向增强子和负向增强子均来自于某个癌细胞状态下的癌细胞,因此可以准确识别该癌细胞状态下的癌细胞,从而达到针对性的识别的技术效果。
37.在本技术实施例中,基于正向增强子及负向增强子构建正向合成启动子和负向合成启动子的具体实现方式可以是基于增强子与启动子的核心序列较为接近的本领域的公知常识,利用如将增强子序列与cpg岛序列重叠并进行蛋白修饰等本领域技术人员常用的技术手段,即可制备包含对应增强子的正向合成启动子及负向合成启动子。本技术对如何合成正向合成启动子及负向合成启动子的具体方式并不做具体限制,其手段为本领域技术人员所熟知。
38.本技术中的癌细胞分析基因电路组件,主要是指包含至少两个不同的癌细胞分析基因电路的集合,这样集合了针对多种不同的癌细胞状态的癌细胞分析基因电路的组件可以在一次测试中区分不同状态下的癌细胞。
39.本发明通过对获取能够表征肿瘤细胞不同表型的正向增强子和负向增强子,从而构成正向合成启动子和负向合成启动子,并结合能够辅助判断的条形码区域,使得本发明
可以精准标定癌细胞状态,并可以通过高通量细胞实验等手段分析出各种状态的癌细胞的所占比例信息,有助于帮助分析癌细胞之间的异质性。
40.优选地,正向合成启动子可以设置为蛋白结合区域单一,同时负向合成启动子也可以设置为蛋白结合区域单一。这里的蛋白结合区域单一,是指的是该段启动子,包括上述的正向合成启动子和负向合成启动子,的序列是简单重复,比如atgca,结构就是atgca***atgca***重复多次,这样和这个启动子结合的转录因子蛋白只有1种,不会有其它蛋白和这段启动子结合,本发明实施例中将其称之为“蛋白结合区域单一”,这样能够使本技术实施例所提供的癌细胞分析基因电路可以准确定位一个目标位点,降低脱靶率。这里可以基于jaspar数据库、ncbi数据库中等现有的数据库对预先构建的正向合成启动子和负向启动子的结合位点进行查询和估测,并根据查询结果进行修改从而将正向合成启动子及负向合成启动子的蛋白结合区域均设置得单一。
41.优选地,癌细胞分析基因电路还包括荧光蛋白序列。这样在完成了感染后,即可根据被感染的癌细胞的荧光效应大致筛选出后续需要进一步区分和计数的癌细胞,降低整体辨识所需的工作量,这里可以整个本技术实施例所提供的癌细胞分析基因电路组件中的全部癌细胞分析基因电路均设置为包括一种荧光蛋白序列,如eyfp荧光蛋白序列,也可以是每种癌细胞分析基因电路均包含一种与其他癌细胞分析基因电路有区别的荧光蛋白序列等。
42.作为一种优选的实现方式,如图2所示,本技术实施例所提供的癌细胞分析基因电路中荧光蛋白序列、正向合成启动子、条形码区域和负向合成启动子依次连接。
43.如图2所示,癌细胞分析基因电路还包括lac启动子和lac终止子,荧光蛋白序列、lac启动子、正向合成启动子、条形码区域、负向合成启动子和lac终止子依次连接。更具体地,本技术实施例所提供的癌细胞分析基因电路包括依次连接的3'utr段、荧光蛋白序列、lac启动子、正向合成启动子、条形码区域、cmv启动子、mscarlet序列、wpre、负向合成启动子、lac终止子和3'utr段。
44.根据本发明另一方面,如图1所示,提供一种制备癌细胞分析基因电路的方法,包括如下步骤:
45.步骤1:获取至少两种癌细胞状态下的癌细胞的正向增强子和负向增强子;
46.步骤2:基于每种癌细胞状态对应的正向增强子和负向增强子获得正向合成启动子和负向合成启动子。
47.步骤3:获取条形码区域,将正向增强子、条形码区域和负向增强子依次连接获得癌细胞分析基因电路。在步骤3中,癌细胞分析基因电路还包括荧光蛋白序列,将荧光蛋白序列、正向合成启动子、条形码区域和负向合成启动子依次连接获得癌细胞分析基因电路。
48.步骤1中,本技术实施例中的增强子的获取方式,可以是通过已经探明各种癌细胞状态的癌细胞株的文献记载,也可以是通过联合耐药培养等手段培养出不同癌细胞状态的癌细胞,并从其中分析得到不同癌细胞状态的癌细胞所包含的增强子等,本发明对于增强子的获得方式并不作过多限制,能够获得足以满足制作启动子要求的正向增强子和负向增强子即可。
49.步骤2中,基于正向增强子及负向增强子构建正向合成启动子和负向合成启动子的具体实现方式可以是基于增强子与启动子的核心序列较为接近的本领域的公知常识,利
用如将增强子序列与cpg岛序列重叠并进行蛋白修饰等本领域技术人员常用的技术手段,即可制备包含对应增强子的正向合成启动子及负向合成启动子。本技术对如何合成正向合成启动子及负向合成启动子的具体方式并不做具体限制,其手段为本领域技术人员所熟知。
50.以下,将参考实施例详细描述本发明。然而,根据本说明书的实施例可修改为各种其他形式,并且本说明书的范围不应解释为限于以下描述的实施例。提供本说明书的实施例的目的在于向本领域技术人员更充分地描述本说明书。
51.实施例
52.材料
53.细胞:
54.mhcc97h人高转移性肝癌细胞系,由中科院上海细胞生物研究所究所提供。
55.药品及试剂:
56.doxorubicin(阿霉素),规格:10mg,批号:kfs276,供应商:百奥莱博。
57.sorafenib(索拉非尼)规格:10mg,批号:bay 43-9006,供应商:上海芮晖化工科技有限公司。
58.洛斯维-1640(rpmi-1640)培养基及胎牛血清(fbs),购自美国gibco公司。
59.doxycycline(盐酸强力霉素),规格:10mm/ml,批号:id0390-10mm*1ml(in water),供应商:索莱宝。
60.质粒合成自通用生物(安徽),分类器质粒骨架均使用swb-blasticidin慢病毒骨架,合成启动子载体骨架使用swp-puromycin。
61.lipofectamine 3000,规格:1ml,批号:l3000015,供应商:thermalfisher。
62.慢病毒包装试剂盒,规格:100ml,批号:gm-040801-100,供应商:吉满生物。
63.仪器:
64.cx41倒置相差显微镜和bx51荧光显微镜,均购自日本olympus公司;dtx880酶联免疫检测仪,购自美国beckman公司;751gd紫外分光光度计,购自杭州汇尔仪器有限公司;cytoflex流式细胞仪,购自贝克曼库尔特国际贸易(上海)有限公司。
65.实施方法:
66.1、等质量比例混合8种表型细胞状态辨识器的8种质粒作为目的混合质粒,并使用第三代慢病毒包装系统,在10cm细胞培养皿中,通过4质粒共转染hek293t细胞对细胞状态辨识器混合质粒进行慢病毒包装,转染比例为gag/pol:rev:vsv-g:目的质粒=5:2:3:8。其中,gag/pol为基因组整合蛋白,rev为逆转录蛋白,vsv-g为包装蛋白。
67.2、慢病毒包装成功后,收集慢病毒上清液,0.45μm滤器过滤,去除细胞和碎片。
68.注:过滤器建议使用纤维素醋酸酯或聚醚砜(pes)滤膜(低蛋白结合),不能使用硝酸纤维素滤膜。
69.3、按照4:1的体积比例混合慢病毒上清液(4份)和5x慢病毒浓缩液(1份),4℃放置2小时或者过夜,刚开始时每隔30min混匀一下,混匀进行3次。
70.注:4℃放置的时间越长(如放置过夜),病毒的得率可能会更高;一般4℃条件下病毒颗粒可以在浓缩液里稳定保存几天。
71.4、4℃4000g离心25min。
72.5、小心移除上清,不要剧烈晃动管子,一般可见白色沉淀(有时沉淀不可见)。
73.6、加入适量体积(原上清液体积的1/10)的dmem,使用移液器小心吹打,重悬沉淀物。
74.7、重悬后的病毒以50μl管分装,80℃冰箱保存。
75.注:慢病毒冻存液不能反复冻融,否则病毒滴度会降低。
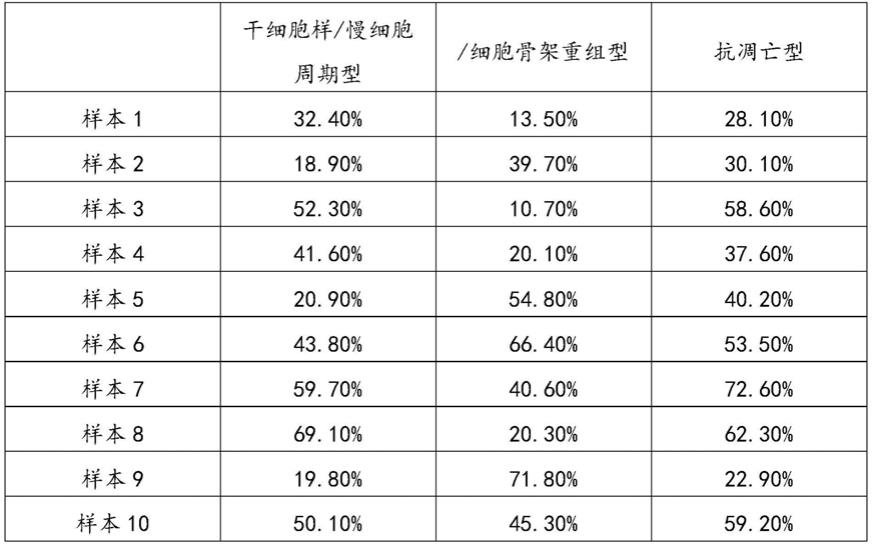
76.使用包装好的慢病毒在六孔板的8个孔中分别使用不同细胞状态辨识器慢病毒感染mhcc97h细胞,感染并抗生素筛选(puromycin抗性筛选,2μg/ml)约10天。之后,使用2μm raf、vegf靶向药sorafenib对这些稳定表达不同细胞状态辨识器的mhcc97h细胞加药处理10天、20天、30天,并通过流式细胞术分析分选表达eyfp荧光蛋白(激发光波长513nm,发射光波长527nm)的细胞,提取这些细胞的基因组,通过设置扩增引物,并对扩增片段进行二代ngs 150bp单端测序,通过bowtie 2同设定好的表型表征barcode序列进行比对及barcode丰度计算,得到每种表型所占比例,以此得到各类细胞状态表型比例数据:表1
[0077][0078]
根据上述数据,以及各亚群最大化覆盖原则,在三启动子配置情况下选择样本7、样本8和样本9的候选启动子作为后续靶向多种耐药亚群治疗性基因电路的驱动元件;在四启动子配置情况下选择样本6、样本7、样本8和样本9的候选启动子作为后续靶向多种耐药亚群治疗性基因电路的驱动元件。
[0079]
本发明通过对癌细胞进行耐药培养,从而获得多个不同的预选启动子,利用预选启动子构建启动子测试慢病毒,并结合不同的细胞表型状态评估器,从而基于癌细胞分别利用细胞表型状态评估器和启动子测试慢病毒进行感染获得双重稳转癌细胞系,并基于该双重稳转癌细胞系的耐药培养结果,判断何种预选启动子能够较高地识别多种亚型的癌细胞系,从而可以将该种预选启动子作为后续所构建的基因电路中的驱动元件。
[0080]
以上描述仅为本技术的较佳实施例以及对所运用技术原理的说明。本领域技术人员应当理解,本技术中所涉及的发明范围,并不限于上述技术特征的特定组合而成的技术方案,同时也应涵盖在不脱离发明构思的情况下,由上述技术特征或其等同特征进行任意
组合而形成的其它技术方案。例如上述特征与本技术中公开的(但不限于)具有类似功能的技术特征进行互相替换而形成的技术方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1