一种心脑血管疾病精准用药的检测试剂盒的制作方法
1.本发明属于医学检验技术领域,具体涉及一种心脑血管疾病精准用药的检测试剂盒。
背景技术:
2.心脑血管疾病是全球范围内死亡的主要原因,并且在发达国家和发展中国家,心脑血管疾病的患病率仍在不断上升。根据世界卫生组织的报告,2016年约有1790万人死于心脏病和中风,占全部死亡人数的31%,到2030年预计2360万人死于心脑血管疾病。目前通过药物维持仍是治疗心脑血管患者重要的方式,但临床上常规使用的抗血小板药、降压药、降脂药等心脑血管药物普遍存在个体差异,药物疗效差、出现不良反应的情况时有发生。因此进行用药前基因检测,预测患者对药物的疗效及不良反应,指导不同患者精准用药具有十分重要的临床意义。
3.基因多态性是心脑血管疾病患者药物疗效个体差异和产生不良反应的主要原因。如硝酸甘油作为抗心绞痛的急救药物,但携带有aldh2突变的患者硝酸脂酶活性会降低10倍,从而使硝酸甘油无法产生一氧化氮,因此难以缓解心脏缺血的症状;抗血小板药物阿司匹林也并非对所有的血栓患者都有效果,部分患者即使服用阿司匹林也不能抑制血小板的聚集和预防血栓形成;美国fda在2010年就曾推荐在使用氯吡格雷前应进行基因检测,并提示氯吡格雷抵抗与cyp2c19功能缺失相关;因slco1b1和apoe单核苷酸多态性(snp)存在,他汀类降脂药物在不同人群中存在用药效果差异及不良反应;降压药物β受体阻断剂敏感性及副作用与cyp2d6和adrb1基因多态性相关。目前市场上仅有针对一种药物或几种高血压药物精准用药产品,但心脑血管病人大多需要多种药物联合治疗,目前尚未有针对心脑血管抗心绞痛、抗血小板、降脂、降压、抗心律失常多种药物检测的产品。
4.目前市场上针对心脑血管用药指导的产品采用技术主要有sanger测序、基因芯片、荧光pcr-扩增曲线等。其中sanger测序操作复杂、检测时间长且检测成本高;基因芯片法准确性低、易污染、检测成本高;荧光pcr-扩增曲线法虽操作简单、成本较低,但用于基因多态性检测准确性较低。
5.另外,传统的荧光pcr-熔解曲线分析法原理是利用不同dna差异具有不同tm值(dna的双螺旋结构降解一半时的温度)的特征,在pcr扩增反应之后,通过逐步提高pcr反应产物的温度,使具有不同tm值的双链dna依次变性为单链dna,从而产生不同形状的熔解曲线,以此来区分不同dna序列。但除靶标位点外, 探针上其它snp位点的存在同样影响dna双链tm值而导致不同的熔解曲线。据研究发现snp位点在人类基因组中极为常见,人类所有群体中存在大约1500万个snp位点(频率大于1%),平均约每300-600bp存在一个snp位点(频率大于1%)。因此紧邻靶标位点的上下游可能存在其他snp位点,如与他汀药物副作用相关的slco1b1*1b位点,此位点上游4bp处存在突变频率为11.457%的snp位点(rs11045819,数据来源ucsc)若忽略此类突变频率较大的snp存在,不可避免假阳性或假阴性出现。然而目前市面上已有利用熔解曲线snp分型的相关检测产品的在探针设计上未考虑其它snp位点的
id no: 19-21所示。
24.更优选地,所述检测cyp2c19*2基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 22-24所示。
25.更优选地,所述检测cyp2c19*17基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 25-27所示。
26.更优选地,所述检测cyp2c19*3基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 28-30所示。
27.更优选地,所述检测slco1b1*5基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 31-33所示。
28.更优选地,所述检测apoe(t388c)基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 34-36所示。
29.更优选地,所述检测apoe(c526t)基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 34、37-38所示。
30.更优选地,所述检测cyp2c9*2基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 39-41所示。
31.更优选地,所述检测cyp2c9*3基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 42-44所示。
32.更优选地,所述检测cyp2d6*10基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 45-47所示。
33.更优选地,所述检测adrb1基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 47-50所示。
34.更优选地,所述检测ace(i/d)基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 51-53所示。
35.更优选地,所述检测add1基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 54-56所示。
36.更优选地,所述检测nppa-as1基因分型的荧光探针和上/下游引物核苷酸序列如seq id no: 57-59所示。
37.本发明具有以下优点:本发明以错配探针结合熔解曲线分析技术为基础,通过检测基因多态性确定心脑血管疾病患者用药的适应性,可为心脑血管患者提供全面的个体化用药指导,与现有检测手段相比,本发明的在熔解曲线分析技术的基础上结合错配探针,特异性高、有效避免假阳性或假阴性的出现,且操作简单、周期短、成本低。
附图说明
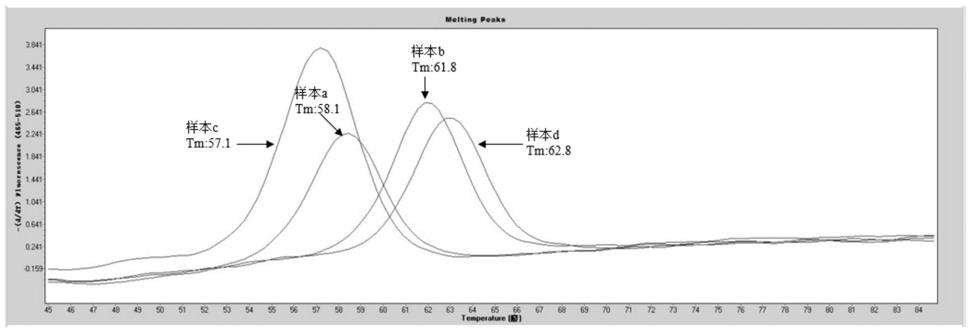
38.图1探针1b-p1体系4种样本熔解曲线图;图2探针1b-p2体系4种样本熔解曲线图;图3探针1b-p3体系4种样本熔解曲线图;图4探针agtr1-p1体系4种样本熔解曲线图;图5探针agtr1-p2体系4种样本熔解曲线图;
图6探针agtr1-p3体系4种样本熔解曲线图;图7为aldh2(rs671)杂合型核酸样本检测结果;图8为itgb3 (rs5918)、il1β (rs16944)、ptgs1 (10306114)、pear1 (rs12041331)各位点杂合型核酸样本检测结果;图9为cyp2c19*2 (rs4244285)、cyp2c19*17 (rs12248560)、cyp2c19*3 (rs4986893)各位点杂合型核酸样本检测结果;图10为slco1b1*5 (rs4149056)、slco1b1*1b (rs72559745)、apoe (t388c, rs429358)、apoe (c526t, rs7412)各位点杂合型核酸样本检测结果;图11为cyp2c9*2 (rs1799853)、cyp2c9*3 (rs1057910)、agtr1 (rs5186)各位点杂合型核酸样本检测结果;图12为cyp2d6*10 (rs1065852)、adrb1 (rs1801253)各位点杂合型核酸样本检测结果;图13为ace (rs4646994)杂合型核酸样本检测结果;图14为add1 (rs4961)杂合型核酸样本检测结果;图15为nppa-as1 (rs5065)杂合型核酸样本检测结果。
具体实施方式
39.下面结合实施例和附图对本发明做进一步说明,但本发明不受下述实施例的限制。
40.实施例1
ꢀꢀ
slco1b1*1b位点引物、错配探针的设计及筛选1. 引物的设计根据slco1b1*1b(rs72559745)设计引物序列如下:上游引物序列:5'
ꢀ‑
ataatggtgcaaataaagggga-3';tm 58.6℃下游引物序列:5'
ꢀ‑ꢀ
tgtcaatattaattcttaccttttccc-3';tm 59.7℃;上述引物进行商业合成,上游引物配制为0.67μm的溶液,下游引物配制为4μm的溶液。
41.2. 错配探针的设计在靶标位点上下游各20bp范围进行snp分析;寻找到一处等位基因频率大于0.1%的snp位点,并在设计探针时引入错配t或g,探针tm值65-70℃,探针距离同方向引物40bp。本次设计3条探针进行筛选及验证错配探针的必要性,探针序列如下:错配为g探针序列:1b-p1:5'-rox-ttcagagcatcagctgggatagtgggaa-bhq2-3';tm 67.4℃错配为t探针序列:1b-p2:5'-rox-ttcagagcatcatctgggatagtgggaa-bhq2-3';tm 65.3℃未设错配探针序列:1b-p3:5'-rox-ttcagagcatcacctgggatagtgggaa-bhq2-3';tm 67.2℃。
42.3. 模板准备准备靶标位点/snp位点均野生(样本a)、靶标位点/snp位点均突变(样本b)、靶标位点野生/snp位点突变(样本c)、靶标位点突变/snp位点野生(样本d)四种样本核酸,稀释
至10ng/μl备用。
43.4. 反应体系及程序单孔体系配制如下:上下游引物各1μl;10
×
pcr buffer
ꢀꢀ
2.5μl;四种模板dna各5μl;2.5mm dntp
ꢀꢀ
2μl;5u/μl taq hot star version
ꢀꢀ
0.2μl;用无核酸酶水补齐至20μl;按如下程序上机:pcr扩增程序95℃预变性300s,95℃变性20s,58℃退火20s,76℃延伸25s,共50个循环,扩增程序结束后直接运行收集熔解曲线程序95℃变性1min,37℃降温180s,45-85℃连续升温(升温速率0.06℃/s)。
44.5. 结果与分析以4种样本(样本a、b、c、d)为模板,含有3种探针的体系获得熔解曲线和对应tm值如图1-3所示:图3中,探针1b-p3体系,样本d和样本a虽有tm值的差异,但样本a和样本b 熔解曲线tm值基本无差异,即若未使用错配探针,样本b会被误判成rs72559745野生型,从而导致假阴性出现。对比图1和图2两种错配探针,探针1b-p2体系中,样本a和样本c/样本b和样本d两组熔解曲线
△
tm≧2℃,且样本a和样本b熔解曲线tm值较接近,容易出现判读错误;而探针1b-p1体系,样本a和样本c/样本b和样本d两组熔解曲线
△
tm≦1℃,此体系中探针受rs11045819影响较小,可较容易区分a/c和b/d样本,因此该体系选取探针1b-p1。
45.实施例2
ꢀꢀ
agtr1位点引物、错配探针的设计及筛选1. 引物的设计根据agtr1(rs5186)设计引物序列如下:上游引物序列:5'
ꢀ‑
aaatcccactcaaacctttcaac-3';tm 59.4℃下游引物序列:5'
ꢀ‑
tagaaaagtcggttcagtccacata-3';tm 60.3℃;上述引物进行商业合成,上游引物配制为0.67μm的溶液,下游引物配制为4μm的溶液。
46.2. 错配探针的设计在靶标位点上下游各20bp范围进行snp分析;寻找到一处等位基因频率大于0.1%的snp位点,并在设计探针时引入错配t或c,探针tm值65-70℃,探针距离同方向引物40bp。本次设计3条探针进行筛选及验证错配探针的必要性,探针序列如下:错配为t探针序列:agtr1-p1:5'-rox-ctgataccaaatgagccttagcttcttttcag-bhq2-3';tm 65.5℃错配为c探针序列:agtr1-p2:5'-rox-ctgataccaaatgagccttagctccttttcag-bhq2-3';tm 67.1℃未设错配探针序列:agtr1-p3:5'-rox-ctgataccaaatgagccttagctacttttcag-bhq2-3';tm 63.8℃。
47.3. 模板准备准备靶标位点/snp位点均野生(样本a)、靶标位点/snp位点均突变(样本b)、靶标位点野生/snp位点突变(样本c)、靶标位点突变/snp位点野生(样本d)四种样本核酸,稀释至10ng/μl备用。
48.4. 反应体系及程序单孔体系配制如下:
上下游引物各1μl;10
×
pcr buffer
ꢀꢀ
2.5μl;四种模板dna各5μl;2.5mm dntp
ꢀꢀ
2μl;5u/μl taq hot star version
ꢀꢀ
0.2μl;用无核酸酶水补齐至20μl;按如下程序上机:pcr扩增程序95℃预变性300s,95℃变性20s,58℃退火20s,76℃延伸25s,共50个循环,扩增程序结束后直接运行收集熔解曲线程序95℃变性1min,37℃降温180s,45-85℃连续升温(升温速率0.06℃/s)。
49.5. 结果与分析以4种样本(样本a、b、c、d)为模板,含有3种探针的体系获得熔解曲线和对应tm值如图4-6所示:图6中,探针agtr1-p3体系,样本b1/d1和样本a1/c1的 tm值的差异不如探针agtr1-p1体系大,若tm值稍有偏移将会导致靶标阴阳性难以区分,从而会有假阳性或假阴性事件的发生,因此舍弃 agtr1-p3探针;对比图4和图5两种错配探针,探针agtr1-p2体系中,样本a1和c1以及样本b1和d1两组熔解曲线
△
tm≧3℃,说明此体系受rs5187影响较大,且样本c1和样本d1区分度不如agtr1-p1体系区分度大;而探针agtr1-p1体系,样本a1/c1和样本b1/d1两组熔解曲线
△
tm≦1℃,此体系中探针受rs5187影响较小,可较容易区分a1/c1和b1/d1样本,因此该体系选取探针agtr1-p1。
50.实施例3
ꢀꢀ
心脑血管疾病精准用药的检测试剂盒及应用按照下表1中序列合成各上、下游引物和探针,装入1ml ep管,与10
×
pcr buffer、dntp、taq hot star version、无核酸酶水和各基因的四种核酸样品(靶标位点/snp位点均野生(样本a)、靶标位点/snp位点均突变(样本b)、靶标位点野生/snp位点突变(样本c)、靶标位点突变/snp位点野生(样本d))组成心脑血管疾病精准用药的检测试剂盒。
51.表1
ꢀꢀ
试剂盒各基因上、下游引物和探针的核苷酸序列
对1例心脑血管疾病患者外周血,使用dna提取试剂盒提取dna,并nandrop定量为532ng/μl,稀释至10ng/μl备用,采用上述检测试剂盒按照表2加样,然后分别加入5μl待测
样本、阴性质控品或各位点的杂合突变型质控品,以无核酸酶水补足至20μl,重复3管。
52.表2
ꢀꢀ
检测体系配制按如下程序进行荧光pcr:95℃预变性300s;95℃变性20s,58℃退火20s,76℃延伸25s,共50个循环; 95℃变性1min,37℃降温180s,45-85℃连续升温(升温速率0.06℃/s)收集荧光信号。各杂合突变型质控品的熔解曲线如图7-15所示。根据样本的tm值并参考表3中结果判读标准对样本进行判读,结果如表4所示。临床医生可根据以上检测结果对该心脑血管疾病患者进行精准用药。
53.表3
ꢀꢀ
各基因分型结果判读标准
表4
ꢀꢀ
样本各基因分型结果
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1