溃疡性结肠炎标志微生物及其应用的制作方法
1.本发明涉及生物技术领域,具体的,本发明涉及溃疡性结肠炎标志微生物及其应用,更具体的,本发明涉及一种试剂盒、试剂在制备试剂盒中的用途、用于预防或者治疗溃疡性结肠炎的药物组合物或者食品组合物、确定个体是否患有溃疡性结肠炎的方法、确定个体是否患有溃疡性结肠炎的装置、一种装置、一种筛选药物的方法。
背景技术:
2.溃疡性结肠炎是一种病因尚不十分清楚的结肠和直肠慢性非特异性炎症性疾病,病变局限于大肠黏膜及黏膜下层。病变多位于乙状结肠和直肠,也可延伸至降结肠,甚至整个结肠。病程漫长,常反复发作。本病见于任何年龄,但20~30岁最多见。溃疡性结肠炎的病因至今仍不明。基因因素可能具有一定地位。有认为溃疡性结肠炎是一种自身免疫性疾病。
3.除少数患者起病急骤外,一般起病缓慢,病情轻重不一。症状以腹泻为主,排出含有血、脓和黏液的粪便,常伴有阵发性结肠痉挛性疼痛,并里急后重,排便后可获缓解。
4.诊断上主要依靠纤维结肠镜检,因为90%~95%患者直肠和乙状结肠受累,因此事实上通过纤维乙状结肠镜检已能明确诊断。镜检中可看到充血、水肿的黏膜,脆而易出血。在进展性病例中可看到溃疡,周围有隆起的肉芽组织和水肿的黏膜,貌似息肉样,或可称为假息肉形成。在慢性进展性病例中直肠和乙状结肠腔可明显缩小,为明确病变范围,还是应用纤维结肠镜作全结肠检查,同时作多处活组织检查以便与克隆结肠炎鉴别。
5.气钡灌肠双重对比造影也是一项有助诊断的检查,特别有助于确定病变范围和严重程度。在钡灌造影中可见到结肠袋形消失,肠壁不规则,假息肉形成以及肠腔变细、僵直。虽然钡剂灌肠检查是有价值的,但检查时应谨慎,避免肠道清洁准备,因为它可使结肠炎恶化。无腹泻的病例检查前给3天流质饮食即可。有腹部征象的病例忌作钡剂灌肠检查,而应作腹部x线平片观察有无中毒性巨结肠、结肠扩张以及膈下游离气体征象。
6.随着人体基因组测序完成及高通量测序技术的高速发展,基因筛查成为溃疡性结肠炎诊断的方向,对于发现溃疡性结肠炎潜在人群很有优势。有研究表明与溃疡性结肠炎相关的多基因在肠道免疫中起重要作用。到目前为止,还没有溃疡性结肠炎患者肠道微生物标记物的相关报道。
技术实现要素:
7.本技术是基于发明人对以下事实和问题的发现和认识作出的:
8.本技术的申请人通过前期大量研究,意外地发现一些微生物可以作为检测溃疡性结肠炎的标志微生物,为早期发现溃疡性结肠炎提供一种非侵入性方法;合理有效地应用标志微生物,扶持肠道有益菌的生长,抑制肠道潜在致病菌,可以治疗或减轻溃疡性结肠炎的临床症状。
9.为此,在本发明的第一方面,本发明提出了一种试剂盒。根据本发明的实施例,所述试剂盒包括适于检测第一微生物集中的至少一种菌种的试剂,所述第一微生物集由以下
菌种组成:远缘链球菌 (streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp. root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp.soil736)。本发明实施例的标志微生物是发明人通过对大量患溃疡性结肠炎个体和大量健康个体的粪便样本中微生物的丰度进行差异比较分析和验证而确定下来的,从而明确了溃疡性结肠炎相关的微生物标志物,根据本发明实施的包含检测所述标志微生物中第一微生物集的至少之一菌种的试剂的试剂盒可以非侵入性的在早期发现或辅助检测溃疡性结肠炎,准确确定个体患有溃疡性结肠炎的概率高低或者处于健康状态的概率高低。
10.在本发明的第二方面,本发明提出了试剂在制备试剂盒中的用途,所述试剂适于检测第一微生物集中的至少一种菌种。根据本发明的实施例,所述试剂盒用于诊断溃疡性结肠炎或检测溃疡性结肠炎的治疗效果,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌 (solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp. soil531)、节杆菌(arthrobacter sp.soil736)。根据本发明具体实施例的试剂制备的试剂盒,可以准确的检测所述第一微生物集中的至少一种菌种,极准确的区分溃疡性结肠炎患者和健康个体,由此,可以有效的在早期进行溃疡性结肠炎诊断,或用于检测治疗过程中溃疡性结肠炎的变化。
11.在本发明的第三方面,本发明提出了一种用于预防或者治疗溃疡性结肠炎的药物组合物或者食品组合物。根据本发明的实施例,含有拟杆菌(bacteroidales bacterium)h5。根据本发明实施例的溃疡性结肠炎标志微生物中拟杆菌(bacteroidales bacterium)h5可以非侵入性的在早期发现或辅助检测溃疡性结肠炎,确定个体患有溃疡性结肠炎的概率高低或者个体处于健康状态的概率高低;同时,提高溃疡性结肠炎高风险人群或已溃疡性结肠炎患者肠道内的所述拟杆菌(bacteroidales bacterium)h5的含量,可以降低患溃疡性结肠炎的概率或减缓、治愈溃疡性结肠炎,因此,所述包含所述拟杆菌(bacteroidalesbacterium)h5的药物或者食品组合物能够用于平衡肠道菌群,有效预防或治疗溃疡性结肠炎。
12.在本发明的第四方面,本发明提出了一种确定个体是否患有溃疡性结肠炎的方法。根据本发明的实施例,包括:(1)确定所述个体的粪便样本中标志微生物的丰度,所述标志微生物包括第一微生物集和拟杆菌(bacteroidales bacterium)h5中的至少一种菌种;(2)将步骤(1)中得到的所述丰度与预定的阈值进行比较,以便确定所述个体是否患有溃疡性结肠炎;其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostocsp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌 (caulobacter sp.root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp.soil736)。根据本发明实施例的方法可以依据个体的粪便样本中的所述标志微生物中的各种菌种的丰度确定个体是否患有溃疡性结肠炎,所述标志微生物是发明人对大量已知状态的粪便样本进行验证,通过差异比较分析各种肠道微生物的丰度,而确定下来的。
13.在本发明的第五方面,本发明提出了一种确定个体是否患有溃疡性结肠炎的装置。根据本发明的实施例,包括:丰度确定单元,用于确定所述个体的粪便样本中标志微生物的丰度,所述标志微生物包括第一微生物集和拟杆菌(bacteroidales bacterium)h5中的至少一种菌种;比较单元,用于将所得到的所述丰度与预定的阈值进行比较,以便确定所述个体是否患有溃疡性结肠炎;其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp. soil736)。所述标志微生物是发明人通过差异比较分析各种肠道微生物在溃疡性结肠炎患者和健康人群的粪便样本中的丰度后经过分析以及对大量已知状态的粪便样本的验证而确定下来的,根据本发明实施例的装置可以准确确定所述个体是否为溃疡性结肠炎的高风险人群或溃疡性结肠炎患者。
14.在本发明的第六方面,本发明提出了一种装置。根据本发明的实施例,包括:计算机可读存储介质,其上存储有计算机程序,所述程序用于第四方面所述的方法;以及一个或者多个处理器,用于执行所述计算机可读存储介质中的程序。根据本发明实施例的装置可以准确确定个体是否为溃疡性结肠炎的高风险人群或溃疡性结肠炎患者。
15.在本发明的第七方面,本发明提出了一种筛选药物的方法。根据本发明的实施例,所述药物用于治疗或者预防溃疡性结肠炎,所述方法包括:将候选药物施用于受试者,检测施用前后,所述受试者粪便中标志微生物的丰度,所述标志微生物包括第一微生物集和拟杆菌(bacteroidales bacterium)h5中的至少一种菌种,其中,满足下列条件至少之一的候选药物适于用于治疗或者预防溃疡性结肠炎:(1) 进行所述施用后,所述第一微生物集中的至少一种菌种的所述丰度降低;和(2)进行所述施用后,所述拟杆菌(bacteroidales bacterium)h5的所述丰度升高;其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostocsp.)dora_2、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.)ccy0110、黄色柄杆菌 (caulobacter sp.)root656、芽孢杆菌(bacillus sp.)soil531、节杆菌(arthrobacter sp.)soil736。根据本发明实施例的方法可以生产或筛选出抑制所述标志微生物中第一微生物集中各种菌种生长,和/ 或促进肠道标志微生物中拟杆菌(bacteroidales bacterium)h5生长的药物,对于辅助减轻溃疡性结肠炎的临床症状具有重要意义。
16.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
17.本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
18.图1是根据本发明实施例的筛选溃疡性结肠炎标志微生物的实验分析流程示意图;以及
19.图2是根据本发明实施例的标志微生物综合指标auc评价结果示意图,其中,
specificity表示特异度,即预测为阳性且实际为阳性,真阳性,纵坐标sensitivity表示敏感度,即真阴性:
20.2a为第一期29个样品数据roc曲线下auc值和置信区间结果图;
21.2b为第二期11个样品数据roc曲线下auc值和置信区间结果图。
具体实施方式
22.下面详细描述本发明的实施例,所述实施例的示例在附图中示出。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
23.此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。在本发明的描述中,“多个”的含义是至少两个,例如两个,三个等,除非另有明确具体的限定。
24.术语“任选地”仅用于描述目的,而不能理解为指示或暗示相对重要性。由此,限定有“任选地”的特征可以明示或者隐含地包括或不包括该特征。
25.生物学标志物是从生物学介质中可以检测到的细胞/生物化学或分子改变。生物学介质包括各种体液、组织、细胞、粪便、头发、呼气等。
26.微生物的丰度是指在某一微生物群体中该种微生物的丰富程度,例如在肠道微生物群体中的该种微生物程度,可表示为该种微生物在该群体中的含量。
27.根据本发明的一个实施方式提供的一种试剂盒,所述试剂盒包括适于检测第一微生物集中的至少一种菌种的试剂,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp. soil531)、节杆菌(arthrobacter sp.soil736)。
28.根据本发明的具体实施方案,所述试剂盒进一步包括适于检测拟杆菌(bacteroidales bacterium)h5 的试剂。
29.根据本发明的具体实施方案,所述试剂盒包括适于检测所述第一微生物集中全部所述菌种的试剂。
30.根据本发明的具体实施方案,所述标志微生物是发明人通过对大量患溃疡性结肠炎个体和大量健康对照个体的粪便样本中的微生物的丰度的差异比较分析、以及验证,而确定下来的,明确了肠道微生物中溃疡性结肠炎相关的微生物标志物。利用包含检测所述标志微生物的试剂的试剂盒能够确定个体处于患有溃疡性结肠炎状态的概率高低或者处于健康状态的概率高低,能够用于非侵入性的早期发现或辅助检测溃疡性结肠炎。
31.根据本发明的具体实施方案,所述适于检测所述第一微生物集和/或拟杆菌(bacteroidales bacterium) h5的试剂不受特别限制,可以检测所述微生物菌种的试剂均包含在本发明的范围内,如通过形态学特征、生理生化反应特征、生态学特征以及血清学反应、对噬菌体的敏感性、分子生物学等方面检测所述微生物菌种的试剂等,具体的,如抗体、酶、核酸分子。
32.本文中,所述微生物形态学特征指:在显微镜下观察微生物外形大小、形状、排列
等,细胞构造,革兰氏染色反应,能否运动、鞭毛着生部位和数目,有无芽孢和荚膜、芽孢的大小和位置,放线菌和真菌的繁殖器官的形状、构造,孢子的数目、形状、大小、颜色和表面特征等。
33.本文中,所述微生物生理生化反应特征指:微生物利用物质的能力、代谢产物的特殊性,如是否产生h2s、吲哚、co2、醇、有机酸,能否还原硝酸盐,能否使牛奶凝固、冻化等、生长环境(适宜生长的温度、湿度、氧气及二氧化碳等气体的浓度、ph、是否耐高渗、是否有嗜盐性等)、与其它生物间的关系(如:共生、寄生、宿主范围及致病情况)等。
34.本文中,所述微生物血清学反应指:利用抗原与抗体的高度敏感特异性反应,来鉴别相似的菌种,或对同种微生物分型,如用已知菌种、型或菌株制成的抗血清,与待鉴定的所述微生物是否发生特异性的血清学反应来鉴定微生物。
35.本文中,分子生物学方法检测微生物主要包括:利用pcr技术、高通量测序等方法。
36.根据本发明提供的试剂在制备试剂盒中的用途,所述试剂适于检测第一微生物集中的至少一种菌种,所述试剂盒用于诊断溃疡性结肠炎或者检测溃疡性结肠炎的治疗效果,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌 (leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp. soil736)。
37.根据本发明的具体实施方案,所述标志微生物是发明人通过对大量患溃疡性结肠炎个体和大量健康对照个体的粪便样本中的微生物的丰度的差异比较分析、以及验证,而确定下来的,明确了肠道微生物中溃疡性结肠炎相关的微生物标志物。利用检测所述标志微生物的试剂能够确定个体患有溃疡性结肠炎的概率高低或者处于健康状态的概率高低,能够用于非侵入性的早期发现或辅助检测溃疡性结肠炎。
38.根据本发明一些具体的实施方案,所述试剂进一步适于检测拟杆菌(bacteroidales bacterium)h5。
39.根据本发明的具体实施例,所述适于检测所述第一微生物集或拟杆菌(bacteroidales bacterium)h5 的试剂不受特别限制,可以检测所述微生物菌种的试剂均包含在本发明的范围内,如通过形态学特征、生理生化反应特征、生态学特征以及血清学反应、对噬菌体的敏感性、分子生物学等方面检测所述微生物菌种的试剂等,具体的,如抗体、酶、核酸分子。
40.本文中,所述微生物形态学特征指:在显微镜下观察微生物外形大小、形状、排列等,细胞构造,革兰氏染色反应,能否运动、鞭毛着生部位和数目,有无芽孢和荚膜、芽孢的大小和位置,放线菌和真菌的繁殖器官的形状、构造,孢子的数目、形状、大小、颜色和表面特征等。
41.本文中,所述微生物生理生化反应特征指:微生物利用物质的能力、代谢产物的特殊性,如是否产生h2s、吲哚、co2、醇、有机酸,能否还原硝酸盐,能否使牛奶凝固、冻化等、生长环境(生长的温度、湿度、氧气及二氧化碳等气体的浓度、ph、是否耐高渗、是否有嗜盐性等)、与其它生物间的关系 (如:共生、寄生、宿主范围及致病情况)等。
42.本文中,所述微生物血清学反应指:利用抗原与抗体的高度敏感特异性反应,来鉴别相似的菌种,或对同种微生物分型,如用已知菌种、型或菌株制成的抗血清,与待鉴定的
所述微生物是否发生特异性的血清学反应来鉴定微生物。
43.本文中,分子生物学方法检测微生物主要包括:利用pcr技术、高通量测序等方法。
44.根据本发明提供的一种确定个体是否患有溃疡性结肠炎的方法,包括步骤(1)和(2)。
45.(1)确定所述个体的粪便样本中的标志微生物的丰度。
46.所述标志微生物包括第一微生物集和拟杆菌(bacteroidales bacterium)h5中的至少一种菌种。其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌 (solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp. soil531)、节杆菌(arthrobacter sp.soil736)。
47.根据本发明的一些具体的实施方案,步骤(1)进一步包括:获得所述个体的粪便样本中的核酸测序数据;将所述测序数据与参考基因组进行比对;基于所述比对的结果,确定所述标志微生物的丰度。
48.根据本发明的具体实施方案,在步骤(1)中,按照下列公式确定所述标志微生物的丰度: ab(s)=ab(us)+ab(ms),其中其中,s表示所述标志微生物的编号,ab(s)表示所述标志微生物s的丰度,ab(us)=us/ls,us为所述测序数据中与所述标志微生物s的参考基因组唯一比对的读段数目,ls为所述标志微生物s的参考基因组的总长度,ms为所述测序数据中与所述标志微生物s的参考基因组非唯一比对的读段的数目,i表示所述非唯一比对读段的编号,coi为所述第i读段对应的丰度系数,co
i,s
表示针对所述标志微生物s,所述非唯一比对的读段i的丰度系数,n为所述非唯一比对的读段i能够比对的微生物的总数,j表示所述非唯一比对的读段i能够比对的微生物的编号。
49.所称的测序数据通过对样本中的核酸序列进行测序得来,测序依据所选的测序平台的不同,可选择但不限于半导体测序技术平台比如pgm、ion proton、bgiseq-100平台,合成边测序的技术平台比如illumina公司的hiseq、miseq序列平台以及单分子实时测序平台比如pacbio序列平台。测序方式可以选择单端测序,也可以选择双末端测序,获得的下机数据是测读出来的片段,称为读段(reads)。
50.比对可以利用已知比对软件进行,例如soap、bwa和teramap等,在比对过程中,一般对比对参数进行设置,设置一个或者一对读段(reads)最多允许有s个碱基错配(mismatch),例如设置s≤2,若reads中有超过s个碱基发生错配,则视为该reads无法比对到(比对上)该组装片段上。所称的获得的比对结果包含各条读段与各物种的参考基因组的比对情况,包括读段是否能够比对上某个或某些物种的参考基因组、只唯一比对到一种物种还是比对到多种物种的参考基因组、比对到物种的参考基因组的位置、比对到物种参考基因组的唯一位置还是多个位置等信息。
51.所称菌种/微生物的参考基因组指预先确定的该微生物物种的序列,可以是预先获得的待测样本所属或者所包含的生物类别的任意参考模板,例如,目标是待测样本中的微生物,参考序列可选择ncbi数据库中的各种微生物的参考基因组和/或hmp、metahit项目公开的dacc肠道基因组,进一步地,也可以预先配置包含更多参考序列的资源库,例如依据待测样本来源的个体的状态、地域等因素选择或是测定组装出更接近的序列作为参考序列。根据本发明的一个实施例,各种微生物的参考基因组从公开的数据库中获得,通常的,一种微生物的参考基因组有多个版本,即一种微生物有多个公开的参考基因组。
52.reads与物种的参考基因组比对,比对上的可以被分为两部分:a)unique reads(u):唯一比对上一个物种的基因组;称这些reads为unique reads。即,如果reads比对上的基因组均来自同一物种,定义这些reads为unique reads。b)multiple reads(m):比对上一个以上物种的基因组,定义为multiple reads。即,如果reads比对上的基因组来自至少两种物种,定义这些reads为multiple reads。
53.(2)丰度比较,以确定个体是否患有溃疡性结肠炎。
54.根据本发明的一个实施例,将步骤(1)中得到的所述丰度与预定的阈值进行比较,以便确定所述个体是否患有酒精性溃疡性结肠炎。
55.根据本发明的一些具体实施例,所述阈值为预先设定的。将标志微生物在待测个体样本中的丰度与所述的阈值比较,基于所述待测个体样本中的丰度是否达到所述阈值,进行待测个体的状态的确定。所述阈值可以为一数值或者数值范围,例如,基于已知患病或健康状态个体中的标志微生物的丰度均值,该微生物对应的阈值可以设为该丰度均值的95%的置信区间(confidence interval)。
56.所述的置信区间是指由样本统计量所构造的总体参数的估计区间。在统计学中,一个概率样本的置信区间是对这个样本的某个总体参数的区间估计。置信区间展现的是这个参数的真实值有一定概率落在测量结果的周围的程度。置信区间给出的是被测量参数的测量值的可信程度,即前面所要求的“一定概率”,这个概率被称为置信水平。
57.根据本发明的一些具体实施例,当步骤(1)中确定的标志微生物的丰度达到所述患酒精性溃疡性结肠炎丰度阈值,未达到所述不患溃疡性结肠炎丰度阈值时,确定所述个体患有溃疡性结肠炎,当(1) 中确定的标志微生物的丰度达到不患溃疡性结肠炎丰度阈值,未达到患溃疡性结肠炎丰度阈值时,确定所述个体不患溃疡性结肠炎。
58.需要说明的是,根据目的或要求不同,可能对确定个体状态结果的可信程度有不同的要求,本领域技术人员可以选择不同的显著性水平或阈值。
59.该方法基于检测个体的粪便样本中的标志微生物中的各种菌种的丰度,分别将检测确定的各种菌种的丰度与其阈值进行比较,依据获得的比较结果能够确定个体为溃疡性结肠炎个体或者为健康个体的概率。为早期发现溃疡性结肠炎提供一种非侵入性的辅助检测或者辅助干预治疗的方法。
60.以上任一实施例中的利用标志微生物确定个体是否患有溃疡性结肠炎的方法的全部或部分步骤,可以利用包含可拆分的相应单元功能模块的装置/系统来施行,或者将方法程序化、存储于机器可读介质,利用机器运行该可读介质来实现。
61.根据本发明提供的一种确定个体是否患有溃疡性结肠炎的装置,该装置包括:丰度确定单元,用于确定所述个体的粪便样本中的所述标志微生物的丰度,所述标志微生物
包括第一微生物集及拟杆菌 (bacteroidales bacterium)h5;比较单元,用于将所得到的所述丰度与预定的阈值进行比较,以便确定所述个体是否患有溃疡性结肠炎;其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcussobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌 (enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp.soil736)。上述对本发明任一实施例的利用标志微生物确定个体是否患有溃疡性结肠炎的方法的技术特征和优点的描述,同样适用本发明这一方面的装置,在此不再赘述。
62.根据本发明的实施例,所述丰度确定单元适于通过下列步骤确定所述丰度:获得所述个体的粪便样本中的核酸测序数据;将所述测序数据与参考基因组进行比对;基于所述比对的结果,确定所述标志微生物的丰度。
63.所称的测序数据通过对样本中的核酸序列进行测序得来,测序依据所选的测序平台的不同,可选择但不限于半导体测序技术平台比如pgm、ion proton、bgiseq-100平台,合成边测序的技术平台比如 illumina公司的hiseq、miseq序列平台以及单分子实时测序平台比如pacbio序列平台。测序方式可以选择单端测序,也可以选择双末端测序,获得的下机数据是测读出来的片段,称为读段(reads)。
64.比对可以利用已知比对软件进行,例如soap、bwa和teramap等,在比对过程中,一般对比对参数进行设置,设置一个或者一对读段(reads)最多允许有s个碱基错配(mismatch),例如设置s≤2,若reads中有超过s个碱基发生错配,则视为该reads无法比对到(比对上)该组装片段上。所称的获得的比对结果包含各条读段与各物种参考的基因组的比对情况,包括读段是否能够比对上某个或某些物种的参考基因组、只唯一比对到一种物种还是比对到多种物种的参考基因组、比对到物种的参考基因组的位置、比对到物种参考基因组的唯一位置还是多个位置等信息。
65.所称微生物的参考基因组指预先确定的该微生物物种的序列,可以是预先获得的待测样本所属或者所包含的生物类别的任意参考模板,例如,目标是待测样本中的微生物,参考序列可选择ncbi数据库中的各种微生物的参考基因组和/或hmp、metahit项目公开的dacc肠道基因组,进一步地,也可以预先配置包含更多参考序列的资源库,例如依据待测样本来源的个体的状态、地域等因素选择或是测定组装出更接近的序列作为参考序列。根据本发明的一个实施例,各种微生物的参考基因组从公开的数据库中获得,通常的,一种微生物的参考基因组有多个版本,即一种微生物有多个公开的参考基因组。
66.reads与物种的参考基因组比对,比对上的可以被分为两部分:a)unique reads(u):唯一比对上一个物种的参考基因组;称这些reads为unique reads。即,如果reads比对上的参考基因组均来自同一物种,定义这些reads为unique reads。b)multiple reads(m):比对上一个以上物种的参考基因组,定义为multiple reads。即,如果reads比对上的参考基因组来自至少两种物种,定义这些reads为multiple reads。
67.根据本发明的一个实施方案,按照下列公式确定所述标志微生物的丰度: ab(s)=ab(us)+ab(ms),其中,s表示所述标志微生物的编号,ab(s)表示所述标志微生物s 的丰度,ab(us)=us/ls,us为所述测序数据中与所述标志微生物s的参考基因组唯一比对的读段
数目,ls为所述标志微生物s的参考基因组的总长度,ms为所述测序数据中与所述标志微生物s的参考基因组非唯一比对的读段的数目,i表示所述非唯一比对读段的编号,coi为所述第i读段对应的丰度系数,co
i,s
表示针对所述标志微生物s,所述非唯一比对的读段i的丰度系数,n为所述非唯一比对的读段i能够比对的微生物的总数,j表示所述非唯一比对的读段i能够比对的微生物的编号。上述对本发明任一实施例的利用标志微生物确定个体是否患有溃疡性结肠炎的方法的技术特征和优点的描述,同样适用本发明这一方面的装置,在此不再赘述。
68.根据本发明提供的一种装置,包括:计算机可读存储介质,其上存储有计算机程序,所述程序用于执行前面所述的一种确定个体是否患有溃疡性结肠炎的方法;以及一个或者多个处理器,用于执行所述计算机可读存储介质中的程序。
69.根据本发明提供的一种筛选药物的方法,所述药物用于治疗或者预防溃疡性结肠炎,所述方法包括:将候选药物施用于受试者,检测施用前后,所述受试者粪便中标志微生物的丰度,所述标志微生物包括第一微生物集和拟杆菌(bacteroidales bacterium)h5中的至少一种菌种,其中,满足下列条件至少之一的候选药物适于用于治疗或者预防溃疡性结肠炎:(1)进行所述施用后,所述第一微生物集中的至少一种菌种的所述丰度降低;和(2)进行所述施用后,所述拟杆菌(bacteroidales bacterium)h5的所述丰度升高;其中,所述第一微生物集由以下菌种组成:远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_2)、屎肠球菌(enterococcusfaecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillussp.soil531)、节杆菌(arthrobacter sp.soil736)。根据本发明实施例的方法可以生产或筛选出抑制所述标志微生物中第一微生物集中各种菌种生长和/或促进肠道标志微生物中拟杆菌(bacteroidalesbacterium)h5生长的药物,对于辅助减轻溃疡性结肠炎的临床症状具有重要意义。
70.利用本发明这一方面的生产或筛选治疗溃疡性结肠炎的药物的方法,通过合理有效地应用确定的溃疡性结肠炎生物标志物进行筛选,能够获得能扶持肠道有益菌的生长和/或抑制肠道潜在致病菌的药物,对于治愈和/或减轻溃疡性结肠炎的临床症状具有重要意义。
71.下面将对实施例作具体介绍。以下实施例中涉及的未特别交待的试剂、序列、软件及仪器,都是常规市售产品。
72.实施例1生物标志物的鉴定
73.本实施例中,发明人通过对18个溃疡性结肠炎患者和11个健康对照的粪便样品进行研究,从而获得肠道菌群微生物微生物群落及功能成分特征。总的来说,发明人通过实验测序得到的179.9gb高质量测序数据构建了溃疡性结肠炎患者参照基因集及1.35g高通量数据构建健康人基因集,并且igc基因集构建一个更加完整的基因集。宏基因组分析显示,42个微生物物种与溃疡性结肠炎疾病密切相关,其中 11个菌在健康人的肠道微生物中富
集,31个菌在溃疡性结肠炎病人的肠道微生物中富集。
74.1、样本收集和dna提取
75.所有样本来自南方医科大学附属医院,实验共采集了18个中国溃疡性结肠炎患者的粪便样品和11 个健康对照的粪便样品,其中每个个体的新鲜粪便样品分成200mg/份,共5份,立即-80℃冰箱冷冻保存。
76.对18个中国溃疡性结肠炎患者的粪便样品和11个健康对照的粪便样品提取总dna。提取方法按照苯酚三氯甲烷处理提取dna方法提取dna。使用乙醇沉淀法对dna进行纯化,测定浓度后保存至
ꢀ‑
20℃。
77.2、构建dna文库及测序
78.dna建库按仪器制造商(illumina)的操作指南进行。对文库进行pe150 bp测序,illumina hiseq2000 (illumina,san diego,ca)平台对29个样品的文库进行测序。每个样本平均产生.9.6gb(sd.
±
0.74gb)测序结果,总计279.6gb测序数据量。
79.参照图1所示的实验流程,鉴定溃疡性结肠炎的相关生物标志物,其中省略的步骤或者细节为本领域技术人员所熟知,几个重要步骤介绍如下面所述。
80.3、微生物物种丰度分析
81.3.1序列优化统计
82.1)首先进行第一期测序,本期测序采集29个样品的数据,获得第一期的29个样品的测序数据以后,对其进行过滤,质控按以下标准进行:a)移除大于5个n碱基的reads;b)去除低质量碱基(q20) 大于50%的reads;c)移除尾部低质量(q20)和n碱基。丢失成对的reads序列被认为是单条reads用于组装。
83.2)由ftp://climb.genomics.cn/pub/10.5524/100001_101000/100064/1.genecatalogs/igc.fa.gz链接下载得到igc基因集。
84.3.2物种丰度分析
85.soapalign 2.21用于匹配针对冗余基因组的paired-end clean reads,这里,所称的冗余基因组来自各数据库中公开的的细菌的参考基因组,比对参数为
–
r 2
–
m 200
–
x 1000。reads与冗余基因组的比对结果,可分为两部分:a)unique reads(u):reads只比对上一个物种的基因组;这些reads被定义为unique reads。即,如果这些基因组来自同一物种,发明人将这些reads定义为unique reads。b)multiple reads(m):如果reads比对上两个及两个以上物种的基因组,定义为multiple reads。即,如果比对上的基因组来自不同物种,发明人定义这些reads为multiple reads。
86.对于物种s,其丰度为ab(s),与特有的u reads和共享的m reads相关,丰度的计算方式如下:
87.ab(s)=ab(us)+ab(ms),
88.其中,s表示所述标志微生物的编号,
89.ab(s)表示所述标志微生物s的丰度,
90.ab(us)=us/ls,
91.us为所述测序数据中与所述标志微生物s的参考基因组唯一比对的读段数目,
92.ls为所述标志微生物s的参考基因组的总长度,
[0093][0094]ms
为所述测序数据中与所述标志微生物s的参考基因组非唯一比对的读段的数目,
[0095]
coi为所述第i读段对应的丰度系数,
[0096][0097]
i表示所述非唯一比对读段的编号,
[0098]
co
i,s
表示针对所述标志微生物s,所述非唯一比对的读段i的丰度系数,
[0099]
n为所述非唯一比对的读段i能够比对的微生物的总数,
[0100]
j表示所述非唯一比对的读段i能够比对的微生物的编号。
[0101]
每个样品中计算得到的物种丰度值,全部除以每个样品的丰度总数后,得到归一化后的物种丰度表。
[0102]
3.3筛选微生物物种标记物
[0103]
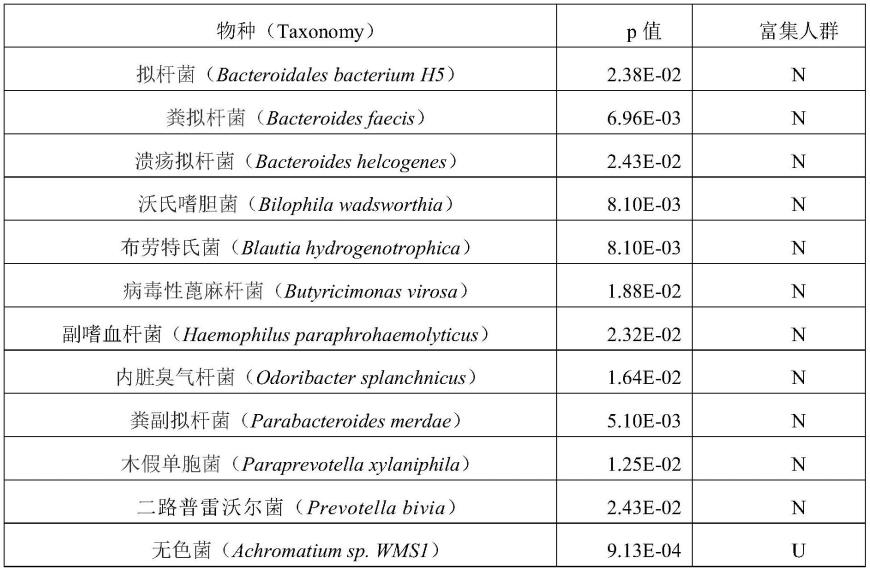
为了获得与溃疡性结肠炎疾病密切相关的肠道微生物物种标记物,发明人利用溃疡性结肠炎患者组(18例)与正常人组(11例)两组肠道微生物物种丰度数据,在物种级别做了一个与疾病相关性的研究。基于得到的物种丰度表,发明人设置标准如下:(1)溃疡性结肠炎患者组或健康人组物种丰度的中位数必须大于0.000001;(2)通过wilcoxon秩和检验进行检验,得到每个物种和溃疡性结肠炎疾病的相关性p值;(3)使用一个相对严格的阈值(p_values《0.025),利用上述参数进行筛选。发明人得到42个与溃疡性结肠炎疾病密切相关的肠道微生物物种,其中,在溃疡性结肠炎(u)患者肠道内中富集的微生物有31个物种,在健康人(n)中富集的有11个物种,这42个微生物物种标记物中的部分结果如表1所示。
[0104]
表1:
[0105]
[0106][0107]
实施例2微生物物种标记物的验证
[0108]
为了验证实施例1中的发现,发明人进一步分析验证群体中的4个健康人及7个溃疡性结肠炎患者的粪便样本中的所述42种菌属的丰度,并根据各物种在健康组及疾病组的
富集情况对所述 42个微生物物种标记物做出删选,验证群体的dna提取、测序以及物种丰度的分析参照实施例1 进行。
[0109]
验证结果如下:对于上述富集在健康人群中的11个物种中,1个在验证集中得到高质量的验证(p值《0.05),验证群体中在健康人富集的微生物物种标志物的p值如下表2所示。
[0110]
表2
[0111]
物种(taxonomy)p值富集人群拟杆菌(bacteroidales bacterium h5)3.76e-02n
[0112]
对于上述富集在溃疡性结肠炎患者中的31个物种中,其中,8个在验证集中得到高质量的验证(p值《0.05),溃疡性结肠炎患者富集的微生物物种标志物验证的p值具体结果如下表3所示,分别为远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌 (leuconostoc sp.dora_2)、屎肠球菌(enterococcus faecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillus sp.soil531)、节杆菌(arthrobacter sp. soil736)。
[0113]
表3
[0114]
物种(taxonomy)p值富集人群远缘链球菌(streptococcus sobrinus)2.26e-02u土壤芽孢杆菌(solibacillus silvestris)2.26e-02u明串珠菌(leuconostoc sp.dora_2)4.24e-02u屎肠球菌(enterococcus faecium)4.24e-02u蓝丝菌(cyanothece sp.ccy0110)4.52e-02u黄色柄杆菌(caulobacter sp.root656)4.24e-02u芽孢杆菌(bacillus sp.soil531)1.21e-02u节杆菌(arthrobacter sp.soil736)1.06e-02u
[0115]
发明人认为,可以将从健康人富集的微生物物种标记物,作为溃疡性结肠炎疾病患病的反向指标,或作为治疗溃疡性结肠炎进行研发的微生物制剂药物菌群成分,或作为检测溃疡性结肠炎、监测溃疡性结肠炎治疗进程的恢复指标;将溃疡性结肠炎患者富集的微生物物种标记物,作为溃疡性结肠炎疾病患病的正向指标,特别用于溃疡性结肠炎疾病非创伤式的检测和诊断。
[0116]
发明人利用这9个微生物物种标记物,构建一个综合指标,估计roc(receiver-operatingcharacteristic)曲线下面积auc,auc越大,表示诊断能力越高,评价综合得分对应其对溃疡性结肠炎的诊断能力。通过对一期(第一阶段)的29个样品和二期(第二阶段)的11个样品进行评测,具体情况如图2所示,都表现出了很好的诊断能力,在一期得到auc=87.4%,如图2a所示,置信区间为74.7.5%-100.0%;二期得到auc=82.1.0%,如图2b所示,置信区间为55.3%-100.0%。
[0117]
实施例3个体状态的检测
[0118]
本实施例中,发明人利用29个粪便样本进行样本来源的个体状态的检测。
[0119]
参照实施例2的方法确定各粪便样本中表3所示的远缘链球菌(streptococcus sobrinus)、土壤芽孢杆菌(solibacillus silvestris)、明串珠菌(leuconostoc sp.dora_
2)、屎肠球菌(enterococcusfaecium)、蓝丝菌(cyanothece sp.ccy0110)、黄色柄杆菌(caulobacter sp.root656)、芽孢杆菌(bacillussp.soil531)、节杆菌(arthrobacter sp.soil736)的丰度,判断各样本中的这8种菌株丰度是否落入各自在疾病对照组或者健康对照组的丰度的95%的置信区间,判定这8种菌种的丰度均落入疾病组的对应区间的样本所对应的个体的状态为溃疡性结肠炎患者,判定8种菌种的丰度均落入健康组的对应区间的样本所对应的个体的状态为非溃疡性结肠炎患者。
[0120]
结果显示,利用本实施例所述方法能够对其中的29个样本进行个体状态判断,而且对这29 个样本中的9个样本对应个体的状态的判断,与记录的该样本来源个体的状态一致。
[0121]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0122]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1