一种抗GUCY2C/CD3双特异性抗体及其用途的制作方法
本技术涉及抗体药物领域,具体地,本技术涉及一种抗gucy2c/cd3双特异性抗体及其用途。
背景技术:
1、胃肠道恶性肿瘤,包括结直肠癌(crc)、胃癌和食管癌,根据2020年的《全球癌症统计报告》显示,全球结直肠癌致死人数占所有癌症致死总数的9.4%,胃癌占7.7%;而在中国,胃癌致死人数占所有癌症致死人数的12.4%,食管癌占10%,结直肠癌占9.5%,可见胃肠道恶性肿瘤是中国乃至全球临床上远未被满足的治疗领域。gucy2c或gcc,即鸟苷酸环化酶2c,属于鸟苷酸环化酶受体家族。研究表明,gucy2c在多种胃肠道癌症中过表达,包括各恶性阶段90%以上的结直肠癌和50%以上的胃或胃-食管交界处癌。生理状态下,gucy2c的表达局限于健康肠道管腔紧密连接的上皮细胞表面,以维持肠道内的稳态。但在病理状态下,肿瘤的发生会破坏肠管腔表面的紧密连接结构,导致gucy2c的暴露,从而可能成为靶向药物优先结合的靶标。
2、重新定向t细胞功能的治疗效果已在多个临床试验中获得证实,如博纳吐单抗(blinatumomab)在血液系统恶性肿瘤治疗中的应用,以及最近临床报告的基于cd3双特异性抗体对实体瘤的有效治疗,如结直肠癌和前列腺癌。基于cd3双特异性抗体,一个臂与肿瘤相关的细胞表面抗原结合,另一臂结合t细胞上的cd3ε蛋白,可有效的用于肿瘤的治疗,因为它们能招募和激活t细胞群特异性靶向肿瘤相关细胞表面过表达的特异性抗原。它们不需要通过t细胞受体(tcr)与mhci类复合体抗原肽结合以激活t细胞,而是通过募集t细胞直接靶向表达细胞表面抗原的肿瘤细胞形成免疫突触激活t细胞,引起细胞毒性t淋巴细胞(ctl)对肿瘤细胞的杀伤作用。
3、因此,为进一步改善gucy2c的抗体抗肿瘤功能,激活t细胞的肿瘤杀伤活性,开发同时靶向gucy2c和cd3的双特异性抗体以治疗gucy2c异常表达的胃肠道恶性肿瘤具有较好的临床应用前景。
技术实现思路
1、本发明的目的在于提供一种抗gucy2c/cd3双特异性抗体及其医药用途。
2、在本发明的第一方面,提供了一种抗gucy2c/cd3双特异性抗体,包含与靶分子a结合的结构域a和与靶分子b结合的结构域b;所述靶分子a和靶分子b选自gucy2c和cd3;所述结构域a和结构域b选自抗gucy2c的抗体或其抗原结合片段,及抗cd3的抗体或其抗原结合片段。
3、在另一优选例中,所述抗体或其抗原结合片段为嵌合抗体或其抗原结合片段,或人源化抗体或其抗原结合片段。
4、在另一优选例中,提供了一种抗gucy2c/cd3双特异性抗体,包含:a)第一结构域a,b)第二结构域b,以及,任选的,还包含c)fc结构域;所述靶分子a和靶分子b选自gucy2c和cd3;所述结构域a和结构域b选自抗gucy2c的抗体或其抗原结合片段和抗cd3的抗体或其抗原结合片段。
5、在另一优选例中,所述第一结构域a和第二结构域b可以是1个、2个、3个或4个。
6、在另一优选例中,所述fc结构域包含2个fc多肽单体,每个fc多肽单体按氨基至羧基顺序包含ch2-ch3,所述fc多肽单体通过二硫键连接。
7、在另一优选例中,所述fc结构域选自同源二聚体的fc结构域或异源二聚体的fc结构域;优选的,所述异源二聚体的fc结构域包含异源二聚修饰。所述异源二聚修饰是指可以诱导fc结构域的异二聚化的修饰方式,包括但不限于杵臼结构(knob-into-hole)修饰、空间位阻修饰、电荷修饰(电荷突变)、氢键作用修饰、疏水作用改变修饰或其组合。更优选的,所述修饰在fc结构域的ch3区。
8、在另一优选例中,所述双特异性抗体包含单体或单体形成的二聚体,所述二聚体可以是同源的或异源的,所述单体从氨基端到羧基端包含选自以下组的结构:
9、结构i:
10、
11、结构ii:
12、
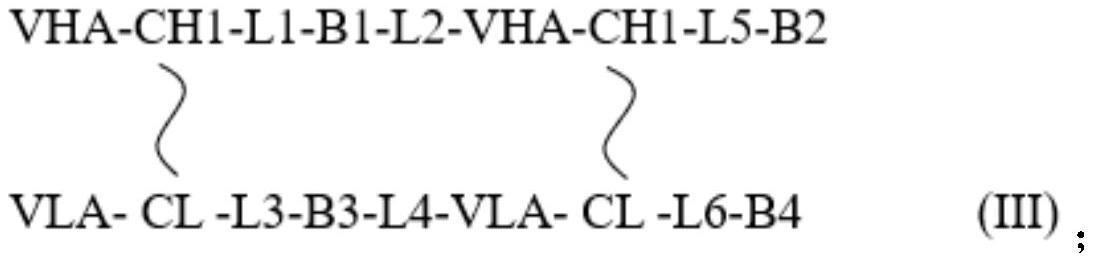
13、结构iii:
14、
15、结构iv:
16、
17、结构v:
18、
19、其中,
20、b1、b2、b3、b4、b5各自独立地为无或与靶分子b结合的抗原结合片段,且至少一个不为无;
21、l1、l2、l3、l4、l5、l6各自独立地为无或键或接头;
22、vha代表与靶分子a结合的重链可变区;vla代表与靶分子a结合的轻链可变区;
23、cl代表轻链恒定区;ch代表重链恒定区;
24、“~”代表二硫键或共价键;“-”代表肽键。
25、在另一优选例中,所述双特异性抗体包含选自以下组的结构:
26、a)结构i的单体形成的同源二聚体;
27、b)结构i与结构ii的单体形成的异源二聚体;
28、c)结构iii的单体;
29、d)结构iv的单体;
30、e)结构v的单体。
31、在另一优选例中,所述抗原结合片段选自scfv、fv、fd、fab、f(ab')2或f(ab')。
32、在另一优选例中,所述双特异性抗体包含1条或2条重链,和1条或2条轻链,所述重链和轻链可以是同源的或是异源的。
33、在另一优选例中,所述重链从氨基端到羧基端包含选自以下组的结构:
34、a)vha-ch1-ch2-ch3-l1-scfvb;
35、b)scfvb-l1-vha-ch1-ch2-ch3;
36、c)vha-ch1-l1-scfvb-ch2-ch3;
37、d)vha-ch1-l1-scfvb;
38、e)vha-ch1;
39、f)vha-ch1-l1-scfvb-l2-vha-ch1;
40、g)vha-ch1-l1-scfvb-l2-vla-cl;
41、h)vla-cl-l1-scfvb-l2-vha-ch1;
42、i)vha-ch1-l1-vha-ch1-l2-scfvb;
43、j)vha-ch1-ch2-ch3;
44、其中,vha是指与靶分子a结合的vh,scfvb是指与靶分子b结合的scfv,l1、l2各自独立地为键或接头。
45、在另一优选例中,所述轻链从氨基端到羧基端包含选自以下组的结构:
46、k)vla-cl;
47、l)scfvb-l3-vla-cl;
48、m)vla-cl-l3-scfvb;
49、n)vla-cl-l3-scfvb-l4-vla-cl;
50、0)vla-cl-l3-vla-cl-l4-scfvb;
51、其中,vla是指与靶分子a结合的vl,scfvb是指与靶分子b结合的scfv,l3、l4各自独立地为键或接头。
52、在另一优选例中,所述的抗gucy2c/cd3双特异性抗体包含选自以下组的结构:
53、结构1:包含2条重链a)和2条轻链k);
54、结构2:包含2条重链b)和2条轻链k);
55、结构3:包含1条重链a)、1条重链j)和2条轻链k),所述重链a)的ch3区包含臼结构修饰,所述重链j)的ch3区包含杵结构修饰;
56、结构4:包含1条重链a)、1条重链j)和2条轻链k),所述重链a)的ch3区包含杵结构修饰,所述重链j)的ch3区包含臼结构修饰;
57、结构5:包含1条重链b)、1条重链j)和2条轻链k),所述重链b)的ch3区包含臼结构修饰,所述重链j)的ch3区包含杵结构修饰;
58、结构6:包含1条重链b)、1条重链j)和2条轻链k),所述重链b)的ch3区包含杵结构修饰,所述重链j)的ch3区包含臼结构修饰;
59、结构7:包含2条重链c)和2条轻链k);
60、结构8:包含1条重链c)、1条重链j)和2条轻链k),所述重链c)的ch3区包含臼结构修饰,所述重链j)的ch3区包含杵结构修饰;
61、结构9:包含1条重链c)、1条重链j)和2条轻链k),所述重链c)的ch3区包含杵结构修饰,所述重链j)的ch3区包含臼结构修饰;
62、结构10:包含1条重链d)和1条轻链k);
63、结构11:包含1条重链e)和1条轻链m);
64、结构12:包含1条重链f)和2条轻链k);
65、结构13:包含1条重链g)、1条重链e)和1条轻链k);
66、结构14:包含2条重链e)和1条轻链n);
67、结构15:包含1条重链h)、1条重链e)和1条轻链k);
68、结构16:包含1条重链i)和2条轻链k);
69、结构17:包含2条重链e)和1条轻链0);
70、结构18:包含2条重链j)和2条轻链l);
71、结构19:包含2条重链j)和2条轻链m)。
72、在另一优选例中,所述抗gucy2c的抗体或其抗原结合片段包含重链互补决定区hcdr1-3和轻链互补决定区lcdr1-3,其中:
73、a)所述hcdr-1氨基酸序列如seq id no:3所示,所述hcdr-2氨基酸序列如seq idno:4所示,所述hcdr-3氨基酸序列如seq id no:5所示;所述lcdr-1氨基酸序列如seq idno:8所示,所述lcdr-2氨基酸序列如seq id no:9所示,所述lcdr-3氨基酸序列如seq idno:10所示;或,
74、b)所述hcdr-1氨基酸序列如seq id no:13所示,所述hcdr-2氨基酸序列如seq idno:14所示,所述hcdr-3氨基酸序列如seq id no:15所示;所述lcdr-1氨基酸序列如seq idno:18所示,所述lcdr-2氨基酸序列如seq id no:19所示,所述lcdr-3氨基酸序列如seq idno:20所示;或,
75、c)所述hcdr-1氨基酸序列如seq id no:23所示,所述hcdr-2氨基酸序列如seq idno:24所示,所述hcdr-3氨基酸序列如seq id no:25所示;所述lcdr-1氨基酸序列如seq idno:28所示,所述lcdr-2氨基酸序列如seq id no:29所示,所述lcdr-3氨基酸序列如seq idno:30所示;或,
76、d)所述hcdr-1氨基酸序列如seq id no:33所示,所述hcdr-2氨基酸序列如seq idno:34所示,所述hcdr-3氨基酸序列如seq id no:35所示;所述lcdr-1氨基酸序列如seq idno:38所示,所述lcdr-2氨基酸序列如seq id no:39所示,所述lcdr-3氨基酸序列如seq idno:40所示;或,
77、e)所述hcdr-1氨基酸序列如seq id no:43所示,所述hcdr-2氨基酸序列如seq idno:44所示,所述hcdr-3氨基酸序列如seq id no:45所示;所述lcdr-1氨基酸序列如seq idno:48所示,所述lcdr-2氨基酸序列如seq id no:49所示,所述lcdr-3氨基酸序列如seq idno:50所示。
78、在另一优选例中,所述抗gucy2c的抗体或其抗原结合片段包含重链可变区vh或其变体和轻链可变区vl或其变体,其中:
79、a)vh的氨基酸序列如seq id no:51所示,vl的氨基酸序列如seq id no:55所示;或,
80、b)vh的氨基酸序列如seq id no:51所示,vl的氨基酸序列如seq id no:57所示;或,
81、c)vh的氨基酸序列如seq id no:53所示,vl的氨基酸序列如seq id no:55所示;或,
82、d)vh的氨基酸序列如seq id no:53所示,vl的氨基酸序列如seq id no:57所示;或,
83、e)vh的氨基酸序列如seq id no:59所示,vl的氨基酸序列如seq id no:63所示;或,
84、f)vh的氨基酸序列如seq id no:61所示,vl的氨基酸序列如seq id no:63所示;或,
85、g)vh的氨基酸序列如seq id no:61所示,vl的氨基酸序列如seq id no:65所示,或,
86、h)vh的氨基酸序列如seq id no:59所示,vl的氨基酸序列如seq id no:65所示。
87、在另一优选例中,所述vh区变体是指与seq id no:51、seq id no:53、seq id no:59、seq id no:61具有至少90%、95%、98%、或99%的氨基酸序列同源性的变体;所述vl区变体是指与seq id no:55、seq id no:57、seq id no:63、seq id no:65具有至少90%、95%、98%、或99%的氨基酸序列同源性的变体。
88、在另一优选例中,所述vh区或vl区包括1-10个氨基酸突变;更优选的,所述突变是取代突变。
89、在另一优选例中,所述抗体或其抗原结合片段包含重链恒定区和轻链恒定区;优选的,所述重链恒定区选自人igg1、人igg2、人igg3或人igg4,所述轻链恒定区选自人κ(kappa)或人λ(lambda)。
90、在另一优选例中,所述人igg1重链恒定区包含如seq id no:109所示的氨基酸序列,所述人κ轻链恒定区包含如seq id no:110所示的氨基序列。
91、在另一优选例中,所述重链恒定区和/或轻链恒定区包含突变的氨基酸;更优选的,所述人igg4重链恒定区包含s228p突变。
92、在另一优选例中,所述抗cd3抗体的抗原结合片段为单价或双价;更优选的,所述抗cd3抗体的抗原结合片段为单价。
93、在另一优选例中,所述抗cd3抗体的抗原结合片段为scfv,所述scfv从氨基端到羧基端包含vh-l1-vl结构或vl-l1-vh结构,所述l1为键或接头。
94、在另一优选例中,所述scfv包含重链互补决定区hcdr1-3和轻链互补决定区lcdr1-3,所述hcdr-1氨基酸序列如seq id no:101所示,所述hcdr-2氨基酸序列如seq idno:102所示,所述hcdr-3氨基酸序列如seq id no:103所示;所述lcdr-1氨基酸序列如seqid no:104所示,所述lcdr-2氨基酸序列如seq id no:105所示,所述lcdr-3氨基酸序列如seq id no:106所示。
95、在另一优选例中,所述scfv包含重链可变区vh和轻链可变区vl,所述vh的氨基酸序列如seq id no:107所示,vl的氨基酸序列如seq id no:108所示。
96、在另一优选例中,所述scfv包含如seq id no:99所示的氨基酸序列。
97、在另一优选例中,上述l1、l2、l3、l4、l5、l6各自独立地为(g4s)n,其中n选自1-6的整数。
98、在另一优选例中,所述靶分子a为gucy2c,所述靶分子b为cd3。
99、在另一优选例中,所述的抗gucy2c/cd3双特异性抗体选自以组:
100、sp4vhl-32h2(结构2):包含氨基酸序列如seq id no:67所示的重链,和氨基酸序列如seq id no:69所示的轻链;或,
101、32h2-sp4vhl-l(结构19):包含氨基酸序列如seq id no:73所示的重链,和氨基酸序列如seq id no:71所示的轻链;或,
102、sp4vhl-32h2-l(结构18):包含氨基酸序列如seq id no:73所示的重链,和氨基酸序列如seq id no:75所示的轻链;或,
103、32h2-sp4vhl(结构1):包含氨基酸序列如seq id no:77所示的重链,和氨基酸序列如seq id no:69所示的轻链;或,
104、32h2fab-sp4vhl(结构10):包含氨基酸序列如seq id no:79所示的重链,和氨基酸序列如seq id no:69所示的轻链;或,
105、32h2ch1-sp4vhl(结构7):包含氨基酸序列如seq id no:81所示的重链,和氨基酸序列如seq id no:69所示的轻链;或,
106、10d7ch1-sp4vhl(结构7):包含氨基酸序列如seq id no:83所示的重链,和氨基酸序列如seq id no:85所示的轻链;或,
107、32h2ch1-sp4vhl-kih(结构9):包含氨基酸序列如seq id no:87所示的第一重链,氨基酸序列如seq id no:89所示的第二重链,和氨基酸序列如seq id no:69所示的轻链;或,
108、32h2ch1-sp4vhl-hik(结构8):包含氨基酸序列如seq id no:91所示的第一重链,氨基酸序列如seq id no:93所示的第二重链,和氨基酸序列如seq id no:69所示的轻链;或,
109、将sp4vhl-32h2、32h2-sp4vhl-l、sp4vhl-32h2-l、32h2-sp4vhl、32h2fab-sp4vhl、32h2ch1-sp4vhl、10d7ch1-sp4vhl、32h2ch1-sp4vhl-kih、32h2ch1-sp4vhl-hik的任一项的氨基酸序列经过一个或多个氨基酸残基的取代、缺失或添加而形成的衍生多肽。
110、在本发明的第二方面,提供了一种多核苷酸分子,所述多核苷酸分子编码根据在本发明的第一方面所述的抗gucy2c/cd3双特异性抗体。
111、在本发明的第三方面,提供了一种表达载体,所述表达载体含有根据本发明的第二方面所述的多核苷酸分子。
112、在另一优选例中,所述表达载体为病毒或质粒。
113、在另一优选例中,所述表达载体选自下组:pcdna3.4,pdr1,pcdna3.1(+),pcdna3.1/zeo(+),pdhfr,ptt5,pdhff,pgm-csf或pcho 1.0。
114、在本发明的第四方面,提供了一种宿主细胞,所述宿主细胞含有根据本发明的第三方面所述的表达载体。
115、在另一优选例中,所述宿主细胞选自下组:cos、cho、ns0、sf9、sf21、dh5α、bl21(de3)、tg1、bl21(de3)、293f或293e细胞。
116、在本发明的第五方面,提供了一种根据本发明的第一方面所述的抗gucy2c/cd3双特异性抗体的制备方法,其特征在于,所述制备方法包括以下步骤:
117、a)在表达条件下,培养根据本发明的第四方面所述的宿主细胞,从而表达抗gucy2c/cd3双特异性抗体;
118、b)分离并纯化步骤a)所述的抗gucy2c/cd3双特异性抗体。
119、在本发明的第六方面,提供了一种药物组合物,其特征在于,所述药物组合物包含有效量的根据本发明的第一方面所述的抗gucy2c/cd3双特异性抗体和一种或多种药学上可接受的载体。
120、在另一优选例中,所述药物组合物为单元剂型。
121、在另一优选例中,所述药物组合物的剂型包括胃肠给药剂型或胃肠外给药剂型。
122、在另一优选例中,所述的胃肠外给药剂型包括玻璃体注射、静脉注射、静脉滴注、皮下注射、局部注射、肌肉注射、瘤内注射、腹腔内注射、颅内注射、或腔内注射。
123、在本发明的第七方面,提供了一种根据本发明的第一方面所述的抗gucy2c/cd3双特异性抗体、或根据本发明的第六方面所述的药物组合物在制备治疗癌症的药物中的用途。
124、在另一优选例中,所述癌症为gucy2c相关癌症;更优选的,所述癌症gucy2c异常表达。
125、在另一优选例中,所述癌症为胃肠道肿瘤或胰腺癌;更优选的,所述胃肠道肿瘤选自直肠癌、结肠癌、小肠癌、胃癌、食管癌和胃-食管交界部癌;进一步更优选的,所述胃肠道肿瘤为恶性肿瘤。
126、在本发明的第八方面,提供了一种治疗癌症的方法,所述方法包括向有需要的受试者施用根据本发明的第一方面所述的抗gucy2c/cd3双特异性抗体、或根据本发明的第六方面所述的药物组合物。
127、在另一优选例中,所述癌症为gucy2c相关癌症;更优选的,所述癌症gucy2c异常表达。
128、在另一优选例中,所述癌症为胃肠道肿瘤或胰腺癌;更优选的,所述胃肠道肿瘤选自直肠癌、结肠癌、小肠癌、胃癌、食管癌和胃-食管交界部癌;进一步更优选的,所述胃肠道肿瘤为恶性肿瘤。
129、在本发明的第九方面,提供了一种免疫偶联物,所述免疫偶联物包括:
130、a)如本发明的第一方面所述的抗gucy2c/cd3双特异性抗体;和b)选自下组的偶联部分:可检测标记物、药物、毒素、细胞因子、放射性核素、或酶。
131、在另一优选例中,所述偶联物部分选自:荧光或发光标记物、放射性标记物、mri(磁共振成像)或ct(电子计算机x射线断层扫描技术)造影剂、或能够产生可检测产物的酶、放射性核素、生物毒素、细胞因子。
132、在另一优选例中,所述免疫偶联物包括抗体-药物偶联物(adc)。
133、在另一优选例中,所述免疫偶联物用于制备治疗癌症的药物组合物。
134、在本发明的第十方面,提供了一种治疗癌症的方法,所述方法包括向有需要的受试者施用如本发明的第九方面所述的免疫偶联物。
135、需要说明的是,实施例中的具体方案或
技术实现要素:
中的优选例均为示例性的给出,不能用于限制本发明。同时,基于抗gucy2c/cd3双特异性抗体发明构思之下的,对其功能元件部分(如抗cd3的抗体或其抗原结合片段、抗gucy2c的抗体或其抗原结合片段)的位置、数量的不同设计或选择所形成的结构方案也在本发明的保护范围之内。例如,根据需要的双特异性抗体的性能(如亲和力、毒性、抗肿瘤活性),抗cd3抗体的抗原结合片段可以是单价、双价、或是多价。抗cd3抗体的抗原结合片段的位置可以是在多肽链的n末端、c末端或中间位置(不在多肽链的n末端或c末端)。
136、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!