基于多重荧光定量ARMS-PCR技术的新冠病毒奥密克戎突变序列检测技术及其应用的制作方法
基于多重荧光定量arms-pcr技术的新冠病毒奥密克戎突变序列检测技术及其应用
技术领域
1.本发明涉及生物技术领域,特别是涉及基于多重荧光定量arms-pcr技术的新冠病毒奥密克戎核酸突变类型检测技术及其应用。
背景技术:
2.自2019年12月起爆发的新型呼吸系统疾病,截止2021年1月中旬已在全球确诊超过九千万例,主要临床症状表现为发热、乏力、干咳。经分离鉴定,确认其病原为一种新型冠状病毒,国际病毒分类学委员会将其命名为“sars-cov-2”。这是目前在人体中发现的第七种冠状病毒,之前主要有6种,其中229e,oc43,nl63,hku1四种致病性较轻,可引起轻微呼吸道疾病,其余两种sars冠状病毒和mers冠状病毒,可引起严重呼吸道疾病。
3.由于新冠肺炎疫情全球持续爆发以及rna病毒更容易在复制过程中突变,新冠病毒突变位点不断出现,相继出现alpha、beta、gamma、delta等世卫组织关注变异株。这对疫苗的预防效果和病毒监测都带来了一定的风险。近日在南非发现了一快速传播的sars-cov-2冠状病毒新变种。在这一变种中发现了超出之前所有变种株所含突变的大量关键突变。受到全球广泛关注,世卫组织将这种变种命名为omicron。该变种的直接参与感染人体细胞的关键蛋白-刺突蛋白突变有已发现的变异突变有32处,而在去年10月报告发现的德尔塔变异株仅有15处突变。刺突蛋白突变的32个,与delta和alpha变异毒株有多处重合,因此,该突变株可能有复制能力增强的特征。其rbd具有k417n、n440k、g446s、s477n、t478k、e484a、q493r、g496s、q498r、n501y、y505h、t547k等突变,是rbd突变最多的突变株,可能会影响抗体识别和疫苗接种。furin切割位点附近有h655y、n679k、p681h突变,可能增强病毒复制能力和感染力。其中涉及s蛋白功能的446g》s、547t》k、496g》s、679n》k关键性新发突变尤为重要。针对新冠病毒检测阳性的病例,确认是否属于新冠病毒奥密克戎突变株及是否具有这四种关键突变类型,对于病毒监测具有重要意义。
4.多种荧光定量arms-pcr检测技术融汇了arms-pcr的灵敏性、dna杂交的特异性、同一管多重或多管快速检测的优点,是目前临床检验中认同程度很高的一种检测技术,已广泛应用于科学研究和临床检测。但目前已上市产品中绝大多数为普通新冠病毒检测产品,没有涉及新冠奥密克戎病毒及新突变类型技术产品。
技术实现要素:
5.鉴于以上所述现有技术的缺点,本发明的目的在于提供一种基于荧光定量arms-pcr技术的新冠病毒(奥密克戎)核酸突变基因类型检测技术及其应用。
6.本发明一方面提供了一种用于检测新冠病毒奥密克戎病毒株核酸s基因突变类型的试剂盒,所述试剂盒包括以下引物和探针组中的任一种或几种,其中每组中的引物都包含正向引物和反向引物,每个所述探针的两端分别标记有荧光报告基团/荧光淬灭基团:
7.a.用于检测s基因突变类型:序列位置23599,序列变化t》g的引物和探针;其中正
向引物的核苷酸序列如:seq id no.1所示,反向引物的核苷酸序列如seq id no.2所示,其中探针的核苷酸序列如seq id no.3所示;
8.b.用于检测s基因突变类型:序列位置23048,序列变化g》a的引物和探针;其中正向引物的核苷酸序列如:seq id no.4所示,反向引物的核苷酸序列如seq id no.5所示,其中探针的核苷酸序列如seq id no.6所示;
9.c.用于检测s基因突变类型:序列位置23202,序列变化c》a的引物和探针;其中正向引物的核苷酸序列如:seq id no.7所示,反向引物的核苷酸序列如seq id no.8所示,其中探针的核苷酸序列如seq id no.9所示;
10.d.用于检测s基因突变类型:序列位置22898,序列变化g》a的引物和探针;其中正向引物的核苷酸序列如:seq id no.10所示,反向引物的核苷酸序列如seq id no.11所示,其中探针的核苷酸序列如seq id no.12所示。
11.新冠病毒的s基因的基因序列参考genbank:mw533315.1和s基因变异基因序列参考genbank:ol672836.1。
12.进一步地,所述试剂盒中含有以上全部四组引物和探针,尤其是当需要被同时检测以上4个突变位点时。例如当需要确定s基因的具体突变类型时,则需要同时检测上述4个位点。
13.进一步地,所述荧光报告基团/荧光淬灭基团选自选自fam、vic或hex、rox、ned、cy3或cy5荧光报告基团/mgb或非mgb的bhq1、bhq2、bhq3、dabcy1、tamra和quencher荧光淬灭基团且试剂盒中各个所述探针上荧光报告基团互不相同。
14.进一步地,所述试剂盒还包括以下组分中的任一种或几种:pcr反应液、酶混合液、阳性对照、阴性对照。
15.进一步地,所述pcr反应液包括缓冲液、mgcl2、dutp和m dntps;所述酶混合液包括taq酶、反转录酶和ung酶,所述的taq酶为热启动taq酶,所述的反转录酶为依赖rna的dna聚合酶,所述的ung酶为尿嘧啶-n-糖基化酶。
16.进一步地,所述阳性对照选自以下任一中或几种:
17.或含有新冠病毒突变序列的假病毒。例如,含有新冠病毒s基因突变序列的非复制型慢病毒。
18.进一步地,所述阴性对照为含有部分新冠病毒的s基因序列的假病毒,例如,含有新冠病毒s基因的非复制型慢病毒。
19.进一步地,所述试剂盒还包括用于检测内参基因的引物探针。
20.进一步地,所述探针包括核苷酸序列如seq id no.13、seq id no.14、seq id no15、所示的多核苷酸中的任一种或几种。每个所述用于检测内参基因的引物与检测对应的突变基因的引物一致。
21.本发明的另一方面提供了如上所述试剂盒用于检测以下任一种或几种新冠病毒核酸s基因突变类型中的用途:s基因突变类型:a.序列位置23599,序列变化t》g,b.序列位置23048,序列变化g》a,c.序列位置23202,序列变化c》a,d.序列位置22898,序列变化g》a。
22.本发明的另一方面提供了如上所述试剂盒在制备检测以下任一种或几种新冠病毒核酸s基因突变类型的产品中的用途:s基因突变类型:a.序列位置23599,序列变化t》g,b.序列位置23048,序列变化g》a,c.序列位置23202,序列变化c》a,d.序列位置22898,序列
变化g》a。
23.如上所述,本发明的关于新冠病毒奥密克戎核酸突变基因检测技术方法,具有以下有益效果:
24.(1)本发明的试剂盒能够同时检测出新冠病毒奥密克戎基因突变类型,填补了现有荧光定量pcr产品只能检测新冠病毒病原体不能检测奥密克戎多种基因突变类型的空白。
25.(2)本发明还具有灵敏度高、特异性好、可重复性强、检测结果快速客观、且可节约成本等优点,在新冠病毒奥密克戎基因新突变类型的体外诊断领域具有极大的应用前景。
26.(3)本试剂盒操作简便且能有效防止污染,arms-pcr荧光检测时间(从标本处理开始)仅为2-3小时,pcr荧光检测是全封闭操作,加入待测样本核酸提取物之后可以不再打开管盖,减少了污染产生的机会。反应液中加入了ung酶,防止了扩增产物的污染。
附图说明
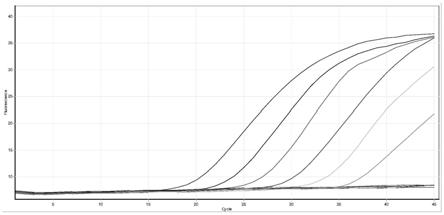
27.图1是新冠病毒s基因突变型446g》s在不同浓度下的扩增曲线图。
28.图2是新冠病毒s基因突变型547t》k在不同浓度下的扩增曲线图。
29.图3是新冠病毒s基因突变型496g》s在不同浓度下的扩增曲线图。
30.图4是新冠病毒s基因突变型679n》k在不同浓度下的扩增曲线图。
31.图5是实施例3中检测试剂盒针对含有446g》s突变型的多种病毒扩增曲线图。
32.图6是实施例3中检测试剂盒针对含有547t》k突变型的多种病毒扩增曲线图。
33.图7是实施例3中检测试剂盒针对含有496g》s突变型的多种病毒扩增曲线图。
34.图8是实施例3中检测试剂盒针对含有679n》k突变型的多种病毒扩增曲线图。
具体实施方式
35.以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。须知,下列实施例中未具体注明的工艺设备或装置均采用本领域内的常规设备或装置。此外应理解,本发明中提到的一个或多个方法步骤并不排斥在所述组合步骤前后还可以存在其他方法步骤或在这些明确提到的步骤之间还可以插入其他方法步骤,除非另有说明;还应理解,本发明中提到的一个或多个设备/装置之间的组合连接关系并不排斥在所述组合设备/装置前后还可以存在其他设备/装置或在这些明确提到的两个设备/装置之间还可以插入其他设备/装置,除非另有说明。而且,除非另有说明,各方法步骤的编号仅为鉴别各方法步骤的便利工具,而非为限制各方法步骤的排列次序或限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容的情况下,当亦视为本发明可实施的范畴。
36.实施例1检测试剂盒及其使用
37.试剂盒包括以下组分:
38.pcr反应液、酶混合液、突变基因多重反应液、内标反应液,阳性对照一、阴性对照;
39.pcr反应液包括10
×
缓冲液、25mm mgcl2、10mm dutp和10mm dntps;酶混合液包括
taq酶、反转录酶和ung酶,突变基因多重反应液及内标反应液上游下游引物、及探针的配比为:4:4:1;上游引物为300nm,下游引物为300nm,探针为100nm。
40.本实施例中使用的新冠病毒突变基因的引物和探针的核苷酸序列可参见表1。
41.表1突变基因多重反应液
42.679nk-ftaggggctgaatatgtcaacaactcseq id no.1679nk-rcgtgcccgccgatgagactseq id no.2679nk
–
px1-ataactagcgcatatacctgcaccaatgggta-y1seq id no.3496gs-ftgagagagatatttcaactgaaatctatcseq id no.4496gs-raacaccataagtgggtcggaaactseq id no.5496gs-px2-cctgcaacaccattacaaggtttgttaccggc
–
y2seq id no.6547tk-fgtgtcaatttcaacttcaatggtttaaaseq id no.7547tk-rccaaattgttggaaaggcagaaactseq id no.8547tk-px3-cacaggtgttcttactgagt
–
y3seq id no.9446gs-fgaattctaacaagcttgattctaaggttaseq id no.10446gs-rggcctgatagatttcagttgaaatatctseq id no.11446gs-px4-ttacctgtatagattgtttaggaa
–
y4seq id no12
43.注:x1、x2、x3、x4、x5、x6、x7、x8为荧光报告基团,y1、y2、y3、y4、y5、y6、y7、y8为荧光淬灭基团。
44.表2内标反应液
45.β-actin-fgcactcttccagccttccttseq id no13β-actin-rcggatgtccacgtcacacttseq id no.14β-actin
–
px1-cctgggcatggagtcctgtggcatc
–
y1seq id no.15
46.注:x1、为荧光报告基团,y1、为荧光淬灭基团。
47.阳性对照:包括以下组分(均为已知基因序列):为含有新冠病毒突变序列的假病毒,是新冠病毒s基因的突变序列的非复制型慢病毒;
48.阴性对照为含有新冠病毒的假病毒,是新冠病毒s基因的非复制型慢病毒。
49.试剂盒的使用
50.一、先进行样本的采集与保存,要求如下:
51.1.咽拭子:用2根聚丙烯纤维头的塑料杆拭子同时擦拭双侧咽扁桃体及咽后壁,将拭子头浸入含3ml采样液的管中,尾部弃去,旋紧管盖。
52.2.鼻拭子:将1根聚丙烯纤维头的塑料杆拭子轻轻插入鼻道内鼻腭处,停留片刻后缓慢转动退出。取另一根聚丙烯纤维头的塑料杆拭子以同样的方法采集另一侧鼻孔。上述两根拭子浸入同一含3ml采样液的管中,尾部弃去,旋紧管盖。
53.该样本(咽拭子/鼻拭子)即为待测样本。样本采集后应及时检测,也可-20℃保存待测,保存期一般不超过4个月,长期保存请置于-70℃。样本避免反复冻融,采用干冰或冰袋低温运输。
54.二、检测方法
55.1.试剂准备(试剂准备区)
56.表3反应液配制1(样本检测):
57.反应液组份加量(μl/反应)pcr反应液5s突变基因多重反应液5酶混合液5总体积15
58.表4反应液配制2(阴性对照):
[0059][0060][0061]
表5反应液配制3(阳性对照):
[0062]
反应液组份加量(μl)/每反应pcr反应液5s突变基因多重反应液5酶混合液5总体积15
[0063]
表6反应液配制4(样本检测):
[0064]
反应液组份加量(μl/反应)pcr反应液5内标反应液5酶混合液5总体积15
[0065]
表7反应液配制5(阴性对照):
[0066]
反应液组份加量(μl)/每反应pcr反应液5内标反应液5酶混合液5总体积15
[0067]
表8反应液配制6(阳性对照):
[0068]
反应液组份加量(μl)/每反应pcr反应液5内标多重反应液5酶混合液5总体积15
[0069]
2.样本处理(样本处理区)(三级防护)
[0070]
进入该实验区缓冲间前须穿戴好三级防护用品,方可进入。穿戴顺序:手卫生
→
戴一次性防护帽
→
戴n95防护口罩(做密合性检测)
→
穿一次性连体防护服
→
穿一次性鞋套
→
穿一次性防水靴套
→
戴第一层乳胶手套(检查密闭性)
→
戴防护目镜或防护面屏
→
戴第二层乳胶手套(检查密闭性)。
[0071]
实验前使用2000mg/l含氯消毒剂进行桌面、台面及地面消毒。消毒液需每天新鲜配制,有效时间不超过24h。标本前处理、提取和加样须在生物安全柜内完成。由2名实验人员共同配合操作,操作过程轻柔,避免飞溅。实验人员操作或处理标本结束,必须脱去外层手套,更换手套后方可将手抽出生物安全柜。生物安全柜内操作由实验员a完成,生物安全柜外操作由实验员b协助完成。提取过程中每进出一次生物安全柜都须用75%乙醇或含醇或醇类复配速干手消毒剂消毒。
[0072]
2.1检查标本(实验员a):转运至实验室的标本转运箱应在生物安全柜内开启。转运箱开启后,使用2000mg/l含氯消毒剂对转运桶内壁和标本采集密封袋进行喷洒消毒。取出标本采集管后应首先检查标本管外壁是否有破损、管口是否泄露。确认无渗漏后,用75%乙醇喷洒、擦拭消毒样品管外表面。如发现渗漏应立即用吸水纸覆盖,并喷洒有效氯含量为5000mg/l的含氯消毒剂进行消毒处理,不得对标本继续检测操作,做好标本不合格记录后需立即进行密封打包,压力蒸汽灭菌处理后销毁。
[0073]
2.2标本灭活处理(实验员b):将标本放入保温箱56℃30min灭活。期间每隔10min将标本轻柔摇匀1次,以保证标本均匀灭活;灭活后标本需静置至室温使气溶胶沉降,随后用75%乙醇擦拭外表,将标本放回生物安全柜内。
[0074]
2.3核酸提取
[0075]
2.3.1实验前,从4℃取出蛋白酶k平衡至室温。
[0076]
2.3.2
[0077]
48人份板:取出1块预封装96深孔板,在第一列和第七列对应数量的样品孔内,每个孔都加入10μl蛋白酶k。
[0078]
96人份板:取出预封装的裂解液板,每个孔都加入10μl蛋白酶k。
[0079]
2.3.3
[0080]
48人份板:将96深孔板移至生物安全柜中,在第一列和第七列对应数量的样品孔内,每个孔加入标本各2000μl。
[0081]
96人份板:每个孔加入标本各2000μl。
[0082]
2.3.4
[0083]
48人份板:加样完成后将96深孔板移至dof-9648仪器中(a1位置在最左上角),插入磁针套,点击“新冠病毒”程序运行核酸提取仪。
[0084]
96人份板:加样完成后按照仪器设置将五块板分别放置在dof-9696pro正确位置,在裂解液板上插上磁针套,点击“校准”,调试完成后点击运行程序进行核酸提取。
[0085]
2.3.5
[0086]
仪器运行结束后,洗脱液板即为提取好的核酸。核酸提取完成后,立即将提取物进行封膜处理。
[0087]
2.3.6在生物安全柜内,向pcr扩增管中加入5μl待测核酸样品,终体积为20μl每
管,盖紧管盖,瞬时低速离心,在rt-pcr仪上进行检测。
[0088]
2.4检测完成后,实验员应用75%乙醇消毒外层手套,并脱下外层手套放入垃圾桶中。将安全柜内产生的医疗垃圾用三层垃圾袋密封,并转移至高压灭菌室消毒灭菌。用75%乙醇擦拭工作台面,2000mg/l的有效氯消毒液喷洒地面。塑料或有机玻璃材质物品消毒使用2000mg/l含氯消毒剂擦拭或喷洒消毒。打开传递窗紫外灯、生物安全柜紫外灯、核酸提取仪紫外灯、移动式紫外消毒车、实验室紫外灯,设置紫外照射60min。
[0089]
2.5实验员实验完毕离开标本制备室时,应在缓冲区按顺序摘脱个人三级防护用品,顺序为:手卫生
→
戴新的一次性乳胶手套
→
摘护目镜,并放入75%乙醇中浸泡消毒
→
脱一次性连体防护服(自上而下,由内而外翻转)
→
脱外层手套
→
手卫生
→
摘n95防护口罩
→
摘一次性防护帽
→
脱一次性鞋套
→
脱手套
→
手卫生。
[0090]
3pcr扩增(319扩增室)(二级防护)
[0091]
进入该实验区操作需穿戴好n95防护口罩、一次性防护帽、本室专用工作服外穿一次性隔离衣、一次性鞋套及乳胶手套(检查密闭性)。
[0092]
表9荧光检测通道选择及扩增循环参数设定
[0093][0094]
注:不选rox校正,淬灭基团选none。
[0095]
设置完毕,保存文件,运行反应程序。
[0096]
三、检验结果分析
[0097]
在仪器正常,阴性参考品、阳性参考品、内标曲线均正常的情况下
[0098]
1.在ct≤36,判断为对应通道病原体为阳性。
[0099]
2.在36<ct≤40,再重复一次实验,结果相同的情况下,判断为阳性。
[0100]
3.在ct>40或无扩增,此次结果判断为阴性。
[0101]
测结果判定为阳性,提示存在相应突变基因,阴性提示无相应突变基因。病原体存在全部四种突变基因,表明样本为新冠病毒奥密克戎(omicron)变异株阳性,建议采取更加严格预防措施。
[0102]
10例模拟样本检测结果与临床预期相符,展示了该试剂盒的灵敏性和特异性,引物探针之间无明显交叉反应。本次实验10例样本为来源于自制模拟样品。
[0103]
实施例2试剂盒的灵敏性试验
[0104]
阳性参考品为新冠病毒s基因的相应突变序列的非复制型慢病毒,通过专业机构合成;10倍梯度稀释至500拷贝每毫升(图中右面起跳的扩增曲线)。
[0105]
采用本发明试剂盒进行检测。
[0106]
检测结果表明:本发明试剂盒对于新冠病毒s基因的相应突变序列(446g》s、547t》k、496g》s、679n》k)的检测具有良好的灵敏性,达到500拷贝每毫升,并且ct值随浓度减少呈
梯度改变。见图1、图2、图3、图4。
[0107]
实施例3试剂盒的特异性试验
[0108]
为了检测本发明核酸检测试剂盒(荧光pcr法)的特异性,用其(荧光pcr法)检测鼻病毒、肠道病毒、腺病毒、呼吸道合胞病毒、流行性感冒病毒(a及b型)、副流感病毒等。
[0109]
检测结果表明:本发明检测试剂盒能特异性扩增相应突变序列(446g》s、547t》k、496g》s、679n》k),而不与呼吸道内其它病毒的核酸发生交叉反应,见图5、图6、图7、图8。
[0110]
以上结果说明本发明的试剂盒在临床上普遍适用,且灵敏度好,特异性高,准确率高,且操作过程省时省力。
[0111]
以上的实施例是为了说明本发明公开的实施方案,并不能理解为对本发明的限制。此外,本文所列出的各种修改以及发明中方法、组合物的变化,在不脱离本发明的范围和精神的前提下对本领域内的技术人员来说是显而易见的。虽然已结合本发明的多种具体优选实施例对本发明进行了具体的描述,但应当理解,本发明不应仅限于这些具体实施例。事实上,各种如上所述的对本领域内的技术人员来说显而易见的修改来获取发明都应包括在本发明的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1