高血压炎症应答基因作为分子标志物在制备新疆哈萨克族原发性高血压诊断试剂中的应用
1.本发明涉及分子生物学诊断技术领域,尤其涉及高血压炎症应答基因作为分子标志物在制备新疆哈萨克族原发性高血压诊断试剂中的应用。
背景技术:
2.新疆哈萨克族是新疆的第二大少数民族,该民族具有其独特的生活习惯和饮食方式(好饮酒,高盐、高脂饮食,谷物、蔬菜、豆制品、不饱和脂肪酸摄入较少),这种独特的生活饮食习惯是造成新疆哈萨克族人群的心血管疾病、糖尿病和肥胖的发病率较高的关键致病因素。原发性高血压作为一种发病原因不明、但血压高于正常值的常见血管疾病,其发病机制与环境因素、生活方式和遗传因素密切相关。据流行病学调查研究显示,2010~2017年新疆哈萨克族人群中原发性高血压的发病率高达40.5%~52.39%。由此可见,该民族原发性高血压患病率较高的原因与其遗传背景、生活习惯和饮食方式的交互作用密切相关。
3.现有研究表明由遗传因素、不良生活习惯和饮食方式引起的免疫细胞介导的低度系统性炎症反应是原发性高血压、动脉粥样硬化、脑中风、心肌梗死和心衰等心血管疾病发生发展及相应靶器官损伤的重要机制。外周血单核细胞是机体内发挥适应性免疫应答的主要细胞类型,近年来研究表明外周血单核细胞的增殖激活、细胞亚群及其功能紊乱与血管内皮的炎性浸润和结构功能损伤、高血压的发生发展以及高血压介导的系统性炎症反应密切相关。然而,高血压等心血管疾病发病过程中由外周血单核细胞介导的系统性炎症反应的分子机制仍不清楚,且目前临床上仍缺乏适用于预测评估新疆哈萨克族高血压发病和病情进展及抗炎药物降压疗效的炎症反应特异性标志物及其组合。
技术实现要素:
4.本发明的目的在于提供高血压炎症应答相关基因作为分子标志物在制备新疆哈萨克族原发性高血压筛查诊断、预后或抗炎降压治疗效果检测试剂中的应用,填补了临床上缺乏适用于预测评估新疆哈萨克族原发性高血压发病和病情进展及抗炎药物降压疗效的炎症反应特异性标志物的空白。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了高血压炎症应答相关基因作为分子标志物在制备新疆哈萨克族原发性高血压筛查诊断、预后或抗炎降压治疗效果检测试剂中的应用,所述高血压炎症应答相关基因包括cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。
7.本发明还提供了高血压炎症应答相关基因作为分子标志物在筛选抗炎降压药物中的应用,所述高血压炎症应答相关基因包括cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。
8.本发明还提供了检测高血压炎症应答相关基因表达水平的试剂在制备新疆哈萨
克族原发性高血压筛查诊断、预后或抗炎降压治疗效果检测试剂中的应用,所述高血压炎症应答相关基因包括cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。
9.本发明还提供了检测高血压炎症应答相关基因表达水平的试剂在筛选抗炎降压药物中的应用,所述高血压炎症应答相关基因包括cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。
10.优选的,所述新疆哈萨克族高血压包括新疆哈萨克族原发性高血压。
11.本发明还提供了一种用于检测高血压炎症应答相关基因表达水平的引物组;所述引物组包括cav1扩增引物、pdgfa扩增引物、vav2扩增引物、igll1扩增引物、myl2扩增引物、myl9扩增引物、alcam扩增引物、hla-dqb1扩增引物、hla-dqa1扩增引物、hla-drb1扩增引物、esam扩增引物、ccl3扩增引物、cxcl5扩增引物和cd79b扩增引物;
12.所述cav1扩增引物包括第一引物和第二引物;
13.所述pdgfa扩增引物包括第三引物和第四引物;
14.所述vav2扩增引物包括第五引物和第六引物;
15.所述igll1扩增引物包括第七引物和第八引物;
16.所述myl2扩增引物包括第九引物和第十引物;
17.所述myl9扩增引物包括第十一引物和第十二引物;
18.所述alcam扩增引物包括第十三引物和第十四引物;
19.所述hla-dqb1扩增引物包括第十五引物和第十六引物;
20.所述hla-dqa1扩增引物包括第十七引物和第十八引物;
21.所述hla-drb1扩增引物包括第十九引物和第二十引物;
22.所述esam扩增引物包括第二十一引物和第二十二引物;
23.所述ccl3扩增引物包括第二十三引物和第二十四引物;
24.所述cxcl5扩增引物包括第二十五引物和第二十六引物;
25.所述cd79b扩增引物包括第二十七引物和第二十八引物;
26.所述第一引物至第二十八引物的核苷酸序列分别如seq id no.1~seq id no.28所示。
27.本发明还提供了一种用于检测高血压炎症应答相关基因表达量的试剂盒,包括上述方案所述引物组和pcr扩增用试剂。
28.本发明提供了高血压炎症应答相关基因作为分子标志物在制备新疆哈萨克族原发性高血压筛查诊断、预后或抗炎降压治疗效果检测试剂中的应用。本技术基于基因芯片、生物信息学分析和实时定量聚合酶链锁反应技术首次获得了新疆哈萨克族原发性高血压患者外周血单核细胞中介导高血压炎症应答的基因表达谱及分子标志物,从免疫学机制为新疆哈萨克族原发性高血压发病的预测诊断、病情进展和抗炎降压疗效评估提供了新的研究证据和分子靶标,并为新疆哈萨克族原发性高血压的干预治疗提供了新的研究思路。
附图说明
29.图1为哈萨克族原发性高血压患者外周血单核细胞中差异表达mrna的聚类分析图和火山图;其中a为6个哈萨克族正常对照和6个哈萨克族原发性高血压患者外周血单核细
drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。
40.本发明提供了检测高血压炎症应答相关基因表达水平的试剂在筛选抗炎降压药物中的应用,所述高血压炎症应答相关基因包括cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5和cd79b中的一种或几种。。
41.本发明利用基因芯片、生物信息学和实时定量聚合酶链锁反应技术筛选新疆哈萨克族原发性高血压患者外周血单核细胞中与高血压炎症应答相关的mrna,为该民族原发性高血压发病的免疫学机制研究、临床诊断和精准防治提供理论依据和特异性分子标志物。
42.在本发明中,所述新疆哈萨克族高血压包括新疆哈萨克族原发性高血压。
43.本发明还提供了一种用于检测高血压炎症应答相关基因表达水平的引物组;所述引物组包括cav1扩增引物、pdgfa扩增引物、vav2扩增引物、igll1扩增引物、myl2扩增引物、myl9扩增引物、alcam扩增引物、hla-dqb1扩增引物、hla-dqa1扩增引物、hla-drb1扩增引物、esam扩增引物、ccl3扩增引物、cxcl5扩增引物和cd79b扩增引物;
44.所述cav1扩增引物包括第一引物和第二引物;
45.所述pdgfa扩增引物包括第三引物和第四引物;
46.所述vav2扩增引物包括第五引物和第六引物;
47.所述igll1扩增引物包括第七引物和第八引物;
48.所述myl2扩增引物包括第九引物和第十引物;
49.所述myl9扩增引物包括第十一引物和第十二引物;
50.所述alcam扩增引物包括第十三引物和第十四引物;
51.所述hla-dqb1扩增引物包括第十五引物和第十六引物;
52.所述hla-dqa1扩增引物包括第十七引物和第十八引物;
53.所述hla-drb1扩增引物包括第十九引物和第二十引物;
54.所述esam扩增引物包括第二十一引物和第二十二引物;
55.所述ccl3扩增引物包括第二十三引物和第二十四引物;
56.所述cxcl5扩增引物包括第二十五引物和第二十六引物;
57.所述cd79b扩增引物包括第二十七引物和第二十八引物;
58.所述第一引物至第二十八引物的核苷酸序列分别如seq id no.1~seq id no.28所示。
59.本发明还提供了一种用于检测高血压炎症应答相关基因表达量的试剂盒,包括上述方案所述引物组和pcr扩增用试剂。
60.下面将结合本发明中的实施例,对本发明中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
61.实施例1
62.以新疆哈萨克族原发性高血压患者的外周血单核细胞为研究对象,采用mrna芯片、生物信息学分析和实时定量聚合酶链锁反应技术初步探索外周血免疫细胞介导的炎症反应在新疆哈萨克族原发性高血压发病过程中的作用,并筛选出新疆哈萨克族原发性高血压患者外周血单核细胞中与高血压炎症应答相关的mrna,为高血压的临床诊断和精准防治
提供特异性分子标志物及基因/药物干预靶点。
63.1对象与方法
64.1.1样本收集
65.选取各60例来源于2018年4月~2019年5月在新疆石河子大学医学院第一附属医院心内科住院部及门诊就诊的哈萨克族高血压患者(男性15例,女性15例)及正常体检人群(男性20例,女性10例),对其进行标准化问诊和体检,并根据以下纳入及排除标准收集入选对象:
66.原发性高血压和正常健康对照纳入标准:a.年龄≥38岁,受试者之间无血缘关系;b.依据2010年世界卫生组织、国际高血压联盟及《2010年中国高血压防治指南》公布的高血压诊断标准,收缩压≥140mmhg和/或舒张压≥90mmhg,且均为初次确诊为原发性高血压或入院前经询问病史已停服降压药物≥2周者;c.既往无高血压病史及降压药物治疗史,非同日测量3次血压,平均收缩压《140mmhg,且平均舒张压《90mmhg的门诊病人为正常血压对照者。
67.排除标准:a.继发性高血压患者及肝肾功能不全者;b.有严重心脑血管疾病、过量饮酒史、风湿性疾病、炎症性肠病、慢性阻塞性肺疾病及近期有手术或创伤史或出现多脏器功能衰竭者和恶性肿瘤患者,近期服用避孕药或其他可能影响血压的药源性疾病患者。c.白大衣高血压者、精神疾病和认知功能障碍患者。本研究通过新疆石河子大学医学院第一附属医院人体伦理委员会审查,研究内容符合helsinki宣言,且本研究所有参与者均签署知情同意书,自愿参与该研究。
68.1.2临床信息采集
69.制定统一问卷,并采集所有入选受试者临床信息,主要包括:年龄、性别、民族、既往病史、高血压及避孕用药史、吸烟、饮酒史等情况。
70.1.3血压测量
71.受试者在血压测量前安静休息至少15min,30min内不允许吸烟、饮酒或饮用咖啡等。受试者取坐位并保持上臂与心脏处于同一水平,使用水银血压计连续测量血压三次,每次间隔不少于5min,取3次血压的平均值为本次血压的测量值。
72.1.4体格检查和血常规生化指标检测
73.受试者体检主要包括身高、体重、体质指数及常规生化指标检测。血常规生生化检测前嘱受试者采血前禁食12h,于清晨空腹抽取受试者肘正中静脉血5ml,分离血清后采用beckmanau-5800全自动生化分析仪,根据标准方法测定各组患者及正常人群中的各项生化指标,包括空腹血糖(fbg)、糖化血红蛋白(ghb)、血清总胆固醇(tc)、甘油三脂(tg)、高密度脂蛋白胆固醇(hdl-c)、低密度脂蛋白胆固醇(ldl-c)和血肌酐(cr)水平。
74.1.5主要试剂
75.人外周血单核细胞分离液北京索莱宝科技有限公司;总rna提取试剂trizol购自美国invitrogen公司;rna纯化试剂盒(qiagen rnaeasy mini kit)购自凯杰生物技术(上海)有限公司;人类lncrna/mrnav4.0基因芯片购自安捷伦科技有限公司;cdna反转录试剂盒(primescript
tm
rt reagent kit)和实时定量聚合酶链锁反应试剂盒(tbpremix ex taq
tm
ii)购自宝日医生物技术(北京)有限公司。
76.1.6外周血单核细胞分离及总rna提取
77.随机抽取符合纳入标准的高血压患者及其正常对照的静脉血5ml,采用ficoll-hypaque密度梯度离心法分离外周血单核细胞,通过台盼蓝染色法检测细胞活性后向外周血单核细胞中加入rna提取试剂trizol置于-80℃冰箱保存备用。经trizol试剂提取各组外周血单核细胞中的总rna后,采用thermo nanodrop nd-2000c核酸/蛋白分析仪(thermo scientific公司)、甲醛变性琼脂糖凝胶电泳和agilent 2100生物分析仪(agilent technologies公司)检测总rna的浓度、纯度及完整性。
78.1.7mrna表达芯片杂交检测
79.在每组受试者中各选择质检合格的6例总rna样本,采用rna clean-up试剂盒纯化总rna,以纯化的rna(200-500ng)为模板合成双链cdna,并以该cdna为模板合成crna,之后使用qiagen rnaeasy mini kit试剂盒纯化crna,然后取5~10μg纯化的crna再次合成含有cyanine 3-dctp荧光标记的cdna,之后采用agilent人类lncrna/mrna v4.0基因芯片于agilent g2545a基因芯片杂交炉(45℃、20rpm)中对片段化后的cnda进行杂交16h;杂交结束后清洗芯片,并立即在agilent g2565ca芯片扫描仪中上机扫描并得到原始图像。最后采用agilent feature extraction(version 11.0.1.1)软件处理原始图像,并采集芯片探针中的荧光信号值。
80.1.8差异表达的mrna功能注释和kegg通路富集分析
81.采用r语言中的“bioconductor”软件包、clusterprofiler r软件包、基因集合富集分析(gene set enrichment analysis,gsea)软件、京都基因与基因组百科全书(kegg orthology basedannotation system,kegg)数据库、基因本体论(gene ontology,go)(http://www.geneongoloty.org/)数据库、生物分子功能注释系统软件(http//:bioinfo.capitalbio.com/mas/)和david软件对外周血单核细胞中表达上调的mrna进行进行功能注释和和kegg信号通路富集分析。首先将表达上调的输入基因集映射到数据库基因中,统计每个go条目中所包括的靶基因个数,并用qvalue、benjamini-hochberg多重假设检验方法进行fdr矫正,计算每个go条目中靶基因富集的显著性,最后挑选出p≤0.05显著富集的生物学功能。此外,利用kegg数据库对差异表达基因进行信号通路富集分析,并用上述统计检验方法计每个信号通路条目中基因富集的显著性,挑选出p≤0.05显著富集的信号通路,最后使用r语言软件包绘制出功能和通路富集的柱状图。
82.1.9实时定量聚合酶链锁反应(quantitative real time polymerase chain reaction,qrt-pcr)
83.采用trizol试剂提取各组外周血单核细胞总rna,并检测总rna浓度、纯度及完整性;取500ng~1μg总rna,采用primescript
tm
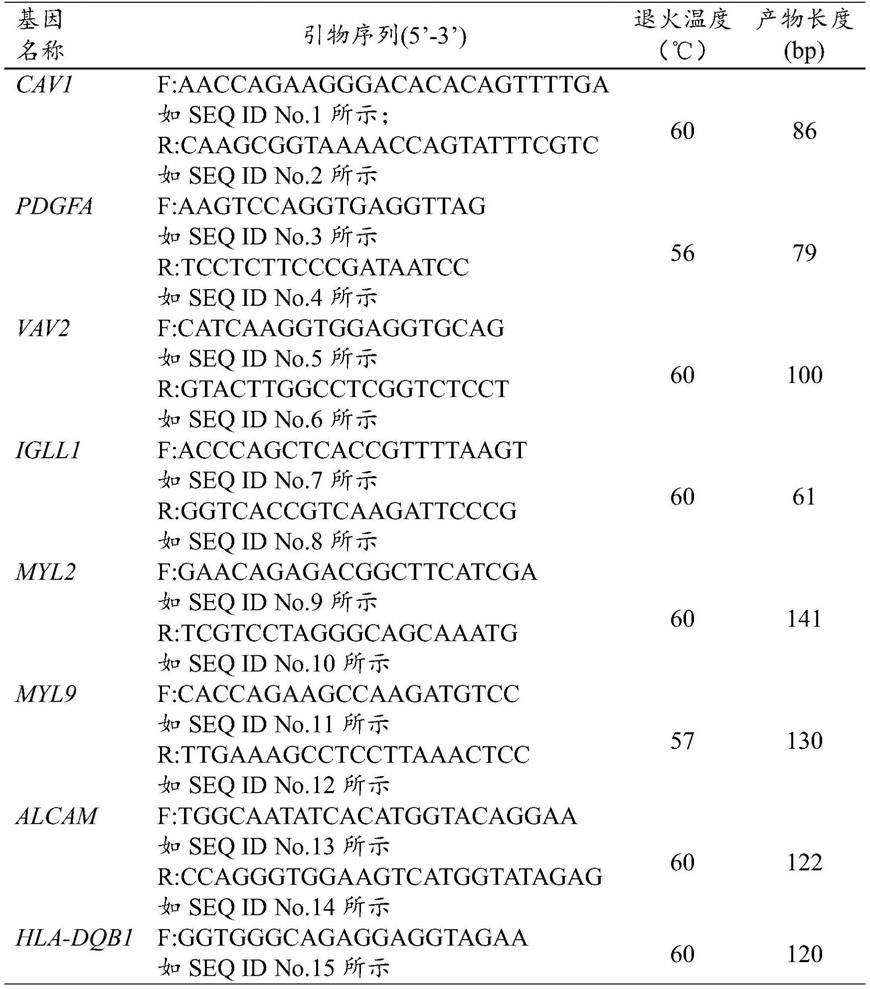
1st strand cdna synthesis kit合成cdna模板。以上述反转录得到的各组cdna样本为模板,采用oligo 7.0和primer 5.0软件设计并由上海生工生物工程有限公司合成的待测基因和内参基因gapdh的特异引物(表1),采用qrt-pcr试剂盒于伯乐公司的cfx96 real-time pcr仪中进行qrt-pcr,反应条件为95℃5min;95℃10s,60℃15s,72℃20s,40个循环。每样本的所有目的基因的检测均设2个平行孔。最后按照公式计算目的基因的相对表达水平。
84.表1 qrt-pcr引物序列
85.[0086][0087]
1.10统计学处理
[0088]
对于芯片数据处理,首先使用agilent genespring gx v13.0软件中的“percentile 75“方法对原始数据进行归一化处理,之后通过箱线图评估芯片扫描质量。采用t检验和benjamini hochberg法校正得到的差异显著性p值和标准化信号值的差异倍数fold change(fc)值筛选出上调或者下调倍数变化值fc≥1.5且p≤0.05的差异表达基因。随后采用cluster 3.0软件对差异表达基因进行层次聚类分析,并用gsea软件、go(http://www.geneongoloty.org/)数据库和生物分子功能注释系统软件(http//:bioinfo.capitalbio.com/mas/)对上调表达mrna进行功能分析。其他数据采用graphpad prism 8.3.0软件进行统计分析,数据统计结果以平均值
±
标准差(mean
±
sd)表示,组间数据比较采用student’s t检验,以p《0.05为差异有统计学意义。
[0089]
2结果
[0090]
2.1哈萨克族原发性高血压患者与哈萨克族正常对照的一般临床指标
[0091]
哈萨克族原发性高血压患者及其正常对照的临床指标如表2所示。其中性别、平均年龄、体质指数(bmi)、吸烟史、饮酒史、空腹血糖、糖化血红蛋白、总胆固醇、甘油三酯、高密
度脂蛋白胆固醇(hdl-c)及低密脂蛋白胆固醇(ldl-c)水平在哈萨克族高血压组和哈萨克族正常对照组间均无显著性差异(p》0.05,表2)。而哈萨克族高血压患者的收缩压和舒张压均显著高于正常对照组(p《0.01,表2)。
[0092]
表2哈萨克族原发性高血压患者及其正常对照的临床资料(n=30)
[0093][0094][0095]
注:计量资料以表示。bmi:体质指数;fbg:空腹血糖;ghb:糖化血红蛋白;tc:总胆固醇;tg:甘油三酯;hdl-c:高密度脂蛋白胆固醇;ldl-c:低密脂蛋白胆固醇。
[0096]
2.2哈萨克族原发性高血压患者外周血单核细胞中差异表达的mrna
[0097]
基因芯片分析结果显示共检测到2549个mrna。在筛选阈值为fc≥1.5、p≤0.05的条件下,与哈萨克族正常对照相比,新疆哈萨克族高血压患者外周血单核细胞中共有522个显著差异表达的mrna,其中上调表达的基因为411个,下调表达的mrna为111个(图1);其中上调表达倍数最高的前15个mrna见表3。
[0098]
表3哈萨克族原发性高血压患者外周血单核细胞中排名前15表达上调的mrna
[0099][0100]
2.3哈萨克族原发性高血压患者外周血单核细胞中上调表达mrna的gsea分析
[0101]
根据p≤0.05的标准,本发明首先对表达上调的mrna进行gsea分析,结果参见表4和图2,结果显示共得到14条基因簇(表4),其中6个基因簇(局部黏附、趋化因子信号通路、白细胞跨内皮迁移、b细胞受体信号通路、细胞因子及其受体相互作用信号通路、t细胞受体信号通路)(图2)可能涉及到高血压炎症应答。
[0102]
表4哈萨克族原发性高血压患者外周血单核细胞中上调表达mrna的gsea分析结果
[0103][0104]
2.4哈萨克族原发性高血压患者外周血单核细胞中上调表达mrna的go功能、kegg信号通路富集分析
[0105]
通过r软件对上调表达的mrna进行go功能和kegg富集分析,结果显示表达上调mrna中与炎症应答相关的生物学过程主要涉及到血小板激活、免疫应答调节、免疫应答激活及其信号转导;细胞组分主要涉及到免疫球蛋白复合体、局部黏附、主要组织相容性ii类蛋白复合体等;分子功能主要涉及到抗原结合、免疫球蛋白受体结合、多肽抗原结合等,见图3~图5。kegg富集分析结果显示哈萨克族原发性高血压患者外周血单核细胞中上调表达的mrna主要参与了局部黏附、细胞黏附分子、合成iga的肠道免疫信号通路、趋化因子信号通路、白细胞跨内皮迁移、细胞因子与其受体相互作用、b细胞受体信号通路等炎症应答相关信号通路(图6),且一些富集通路与gsea分析结果相一致(图2)。
[0106]
2.5哈萨克族原发性高血压炎症应答相关信号通路的共表达网络构建
[0107]
为进一步分析哈萨克族原发性高血压炎症应答相关基因所参与信号通路间的可能相互作用关系,我们对上述kegg富集分析结果中的哈萨克族原发性高血压炎症应答相关信号通路绘制了网络图。结果显示哈萨克族原发性高血压炎症反应过程中t细胞受体信号通路和细胞黏附分子之间、细胞黏附分子和白细胞跨内皮迁移之间、局部黏附和细胞外基质受体间均存在相互作用(图7)。且t细胞受体信号通路可与多个炎症反应相关信号通路(nf-kb、pi3k、mapk、ca
2+
信号通路)产生相互作用(图7)。
[0108]
2.6哈萨克族原发性高血压炎症应答相关分子标志物的筛选
[0109]
对kegg信号通路和gsea分析结果中炎症应答相关的信号通路及其上调表达基因进行归纳整理和交集分析,去除目前无文献报道与炎症应答相关的基因后,最终在上述两种生物信息学分析的交集结果中选定14个在多个炎症应答相关信号通路中均有参与的候选目标差异基因,见表5。
[0110]
表5哈萨克族原发性高血压炎症应答相关信号通路中的表达上调基因
[0111][0112][0113]
2.7哈萨克族原发性高血压炎症应答相关分子标志物的表达水平验证
[0114]
为证实mrna芯片表达数据的可靠性,以及所筛选出的高血压炎症应答相关分子标志物在哈萨克族原发性高血压发病中的作用,采用qrt-pcr在15例哈萨克族原发性高血压患者中对上述筛选的候选分子标志物进行了验证。结果显示,与哈萨克族正常对照相比,哈
萨克族原发性高血压患者外周血单核细胞中参与到局部黏附、细胞黏附分子、合成iga的肠道免疫信号通路、趋化因子信号通路、白细胞跨内皮迁移、细胞因子与其受体相互作用和b细胞受体信号通路的14个炎症应答相关基因(cav1、pdgfa、vav2、igll1、myl2、myl9、alcam、hla-dqb1、hla-dqa1、hla-drb1、esam、ccl3、cxcl5、cd79b)的表达均显著上调(图8,p《0.01),该验证结果与mrna芯片表达数据相一致。
[0115]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1