一种QS21免疫佐剂的制备方法与流程
本发明属于医药生物,具体的,涉及一种qs21免疫佐剂的制备方法。
背景技术:
1、2017年美国疾病控制和预防中心(cdc)免疫实践顾问委员会(acip)发布意见,推荐葛兰素史克重组亚单位疫苗取代默沙东减毒活疫苗用于50岁及以上老年人群的免疫接种。该疫苗中,使用了皂树皂苷21(qs21)作为免疫佐剂。
2、皂树皂苷21(qs21)结构式如下,分子式:c92h148o46,分子量:1990.14,一般性状为无色透明液体。
3、
4、在癌症患者群体中,qs-21剂量在100~200μg范围内具有最佳活性和良好耐受性。在这个剂量范围内的毒性是大多数患者注射部位出现2~10厘米的红斑和硬结,以及偶尔出现轻微的低度流感样症状。此时,超过1000名患者接种了含有100μg剂量的qs-21疫苗,没有剂量限制毒性被报道。
5、在癌症患者群体中100或150μg的剂量的qs-21耐受性相对较好,并且已被证明比其他免疫佐剂更有效地增强对各种抗原的免疫应答。然而,qs-21剂量与免疫效力的相关性表明,如果高剂量可以安全使用,免疫原性可以进一步提高。对于大多数患者群体而言,qs-21相关的副作用限制剂量约为50μg,癌症除外。
6、qs-21浓度低至7~9μg/ml可引起50%引起绵羊红细胞(srbc)溶血,表明qs-21限制剂量相关的副作用约50μg,癌症患者(如黑色素瘤、乳腺癌和前列腺癌)除外。
7、qs-21增强了牛对油佐剂口蹄疫疫苗的早期抗体应答,qs-21剂量750μg/牛。
8、使用相对高剂量的alfq免疫调节剂的两个动物模型(恒河猴和兔)获得的安全性数据表明使用特定的脂质和胆固醇比例的alfq可以减少qs-21介导的细胞溶解和其他毒性不良反应(alfd包含100μg/ml qs-21)。
9、综上,qs-21是一种安全性高,耐受性良好的新型药用佐剂。
10、qs-21的主要作用可以概括为:1)通过作用于抗原提呈细胞(apc)和t细胞,在体内刺激th2体液和th1细胞介导的免疫应答,导致th1细胞因子的释放,参与清除细胞内病原体。2)激活小鼠apc中的nlrp3型炎症小体,随后释放caspase-1依赖的细胞因子il-1β和il-18,它们对th1型应答起重要作用。3)单磷酰脂a(mpla)与脂质体(as01)中的qs-21在早期ifn-γ应答中的独特协同作用机制,促进疫苗免疫原性。
11、以qs-21作为佐剂成份的两种疫苗已经上市:1)带状疱疹疫苗(hz/su)于2017年获得美国食品和药物管理局的许可,并于2018年在欧盟获得营销授权;2)rts,s/as01疟疾疫苗该疫苗于2015年获得欧洲药品管理局批准,可在撒哈拉以南国家进一步实施,供常规使用。
12、但是,目前商品化qs-21供应被少数国际厂商垄断,为了确保疫苗规模化生产时,原辅料供应得到保障。
13、基于此,提出本发明,涉及qs21免疫佐剂的制备方法。
技术实现思路
1、本发明首先涉及一种以半纯化的商品级或食品添加剂级的半纯化皂素为原料,制备皂树皂苷21(qs21)免疫佐剂的制备方法,所述方法包括如下步骤:
2、(1)皂素溶解及过滤,
3、以稀释液对皂素原料进行溶解,然后滤器过滤不溶物;
4、(2)反相粗纯,
5、取步骤(1)得到的皂素过滤样品溶液,按照如下步骤进行反相粗纯:
6、1)上样:上样于unipsn 30-300色谱介质;
7、2)洗脱:以2.5%b到21.25±5.00%b线性梯度洗脱目的峰,并分段收集高纯度的样品,合并粗纯皂素溶液;
8、(3)反相精纯,
9、取步骤(2)得到的粗纯皂素溶液,按照如下步骤进行反相精纯:
10、1)上样:用水稀释样品溶液至乙腈浓度为22%~28%,上样于unips 10-300色谱介质;
11、2)洗脱:10%b到25±5%b线性梯度洗脱目的峰,分段收集高纯度样品并合并;
12、3)合并后的样品重复上述1)~2)步骤1~3次,优选的,重复2次;
13、(4)析出重溶步骤,
14、1)取步骤(3)制备得到的纯化皂素样本溶液,加入2倍体积的水混匀,室温放置后离心收集沉淀;
15、2)向沉淀中加入溶解液,搅拌溶解后,去除有机溶剂样品,优选的,溶解液的加入量与步骤(3)制备得到的纯化皂素样本溶液的量相同;
16、(5)超滤置换步骤,
17、1)取步骤(4)析出重溶后获得的皂素样品溶液,用超滤置换液进行超滤浓缩获得浓缩后的qs21佐剂溶液;优选的,超滤浓缩至原体积的30%~50%;
18、上述步骤(1)~(5)中,
19、稀释液为含30%乙腈、5mm柠檬酸,ph5.0的水溶液;
20、b液为含99%乙腈0.1%tfa的水溶液;
21、溶解液为含5mm组氨酸ph6.0的水溶液;
22、超滤置换液为含5mm组氨酸ph5.0的水溶液。
23、进一步的,所述方法还包括:
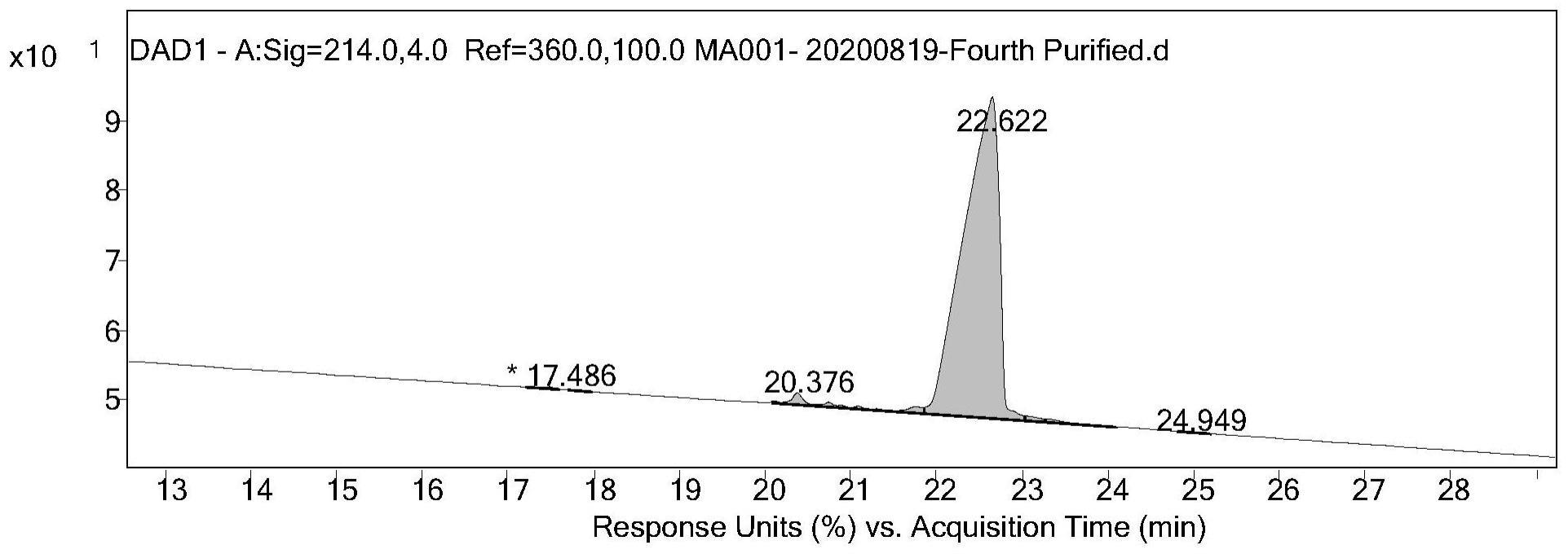
24、(6)分装,对步骤(5)超滤置换后的qs21溶液进行除菌过滤,分装后-70℃以下温度保存。
25、进一步的,本发明所述的皂素原料中,qs21含量不低于8%;水分不高于10%,灰分不高于3%,重金属含量和农药残留符合中国药典标准,使用本发明所述方法纯化qs21的收率不低于50%,最终获得的qs21的纯度,不低于94%。
26、更进一步的,
27、步骤(1)中,按照1:25(w/v)对皂素原料进行溶解,然后以1.0+0.45μm滤器过滤;
28、步骤(2)中,上样载量30~60mg/ml,线性流速90~360cm/h,上样结束后,以a1液冲洗,以2.5%b液冲洗杂质;梯度洗脱时,收集纯度高于30%的样品进行合并;
29、步骤(3)中,上样载量10~50mg/ml,线性流速:100~140cm/h;上样结束后以a2液冲洗,以10%b冲洗杂质,第一次反相精纯收集纯度高于60%的样品,第二次反相精纯收集纯度高于80%的样品,第三次反相精纯收集纯度高于90%的样品,第四次反相精纯收集纯度高于95%的样品;
30、步骤(4)中,室温放置不少于30min,离心参数为:9000~11500g,2~8℃,10min;
31、步骤(5)中,超滤参数为:使用5kd膜包,跨膜压0.2~0.4bar,置换次数10次,以超滤置换液洗滤不低于8倍体积;
32、其中,
33、a1液为含30%乙腈0.1%tfa的水溶液;
34、a2液为含20%乙腈0.1%tfa的水溶液。
35、本发明还涉及所述的qs21免疫佐剂的制备方法在制备疫苗佐剂中的应用。
36、本发明还涉及所述的qs21免疫佐剂的制备方法在制备药品或疫苗中的应用。
37、本发明技术路线的关键技术参数和技术效果在于如下几点:
38、(1)皂素干粉作为原料进行qs-21生产,鉴于qs-21在碱性条件时稳定性较差,选择以ph5.0柠檬酸-柠檬酸钠作为缓冲体系。为了满足后期反相色谱纯化,用含有乙腈的缓冲溶液进行溶解,因此我们选择以30%乙腈5mm柠檬酸ph5.0作为稀释液对皂素进行溶解。
39、(2)色谱柱柱效(理论塔板数),经优化,unipsn 30-300装柱柱效不低于1000n/m,unips 10-300装柱柱效不低于20000n/m,满足最终qs-21产品的质量标准。
40、(3)有机溶剂残留,通过对≥95%的qs-21的反相高效液相色谱图(rp-hplc)进行分析,确定每个杂质峰的去除效果,有机溶剂在超滤置换步骤(连续洗滤不低于8倍体积)最终去除,超滤使用5kd膜包,最终收率不低于70%。
41、(4)多步反相纯化中皂素溶液中乙腈浓度发生一定变化,因此,最后进行析出沉淀时,选择以水稀释至3倍体积,控制乙腈浓度在18%以下,qs-21充分析出,离心收集沉淀。
42、(5)使用本发明技术路线获得的qs21佐剂,收率不低于50%,最终获得的qs21的纯度不低于94%,在刺激免疫功能、毒性以及稳定性等多个方面,都不弱于gsk的qs21佐剂。
- 还没有人留言评论。精彩留言会获得点赞!