一种新型冠状病毒RT-RPA可视化检测引物探针及试剂盒
一种新型冠状病毒rt-rpa可视化检测引物探针及试剂盒
1.本技术要求申请日为2021年7月16日、申请号为2021108064800的中国专利申请的优先权。
技术领域
2.本发明涉及核酸可视化检测技术领域,具体涉及一种新型冠状病毒rt-rpa可视化检测引物探针及试剂盒。
背景技术:
3.新型冠状病毒(sars-cov-2)属于冠状病毒科,冠状病毒属,是一种单股正链的rna病毒。sars-cov-2的实验室检测方法包括病原学检测、血清学检测(igg/igm抗体检测)、核酸检测,但目前sars-cov-2的应用最广泛的实验室确诊方法以核酸检测为主。病毒分离培养是病毒学检测金标准,该方法特异性强,但过程繁琐,耗时长。血清学检测如酶联免疫吸附试验(elisa)、中和试验等虽然也具有良好的可行性,但抗体检测有一定的滞后性,需要在病毒诱导人体免疫应答之后才能检出抗体。而传统的核酸检测方法如rt-pcr,real-time rt-pcr等仍需要专业的仪器设备和实验人员。
4.综上所述,以上方法由于对操作环境和精密设备的需求较高,限制了其应用范围,尚不能在疫病现场或基层实验室实现sars-cov-2快速检测。因此,亟需建立一套快速简便、准确的诊断方法,为sars-cov-2现地快检、病原的监测预警提供新型的检测技术与物质基础。
技术实现要素:
5.本发明的目的是提供一种灵敏度高、特异性强、操作简单快速的新型冠状病毒rt-rpa可视化检测引物探针及试剂盒。
6.第一方面,本发明首先提供一种用于检测sars-cov-2的引物和探针组合。
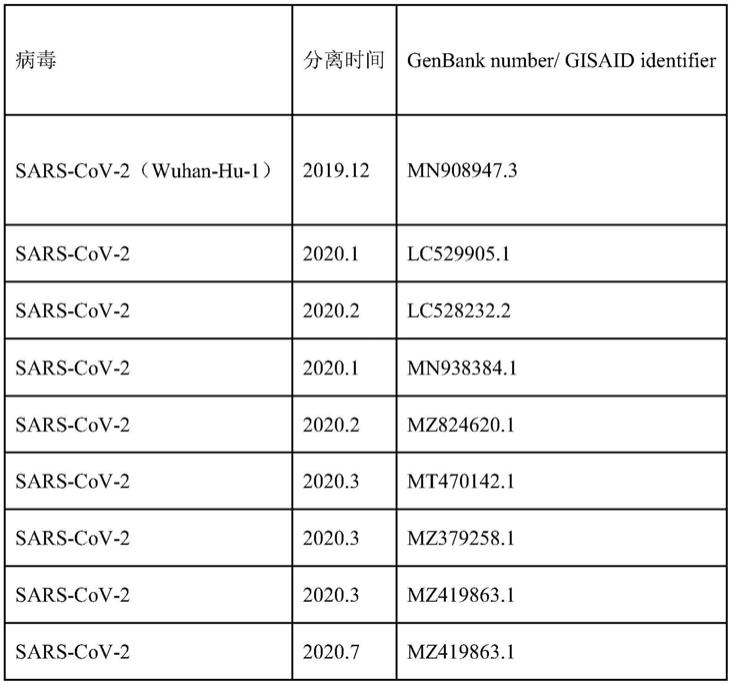
7.本发明通过比对genbank及gisaid数据库上公布的包括现有变异株在内的分离于不同国家、不同地区、不同时间的20株sars-cov-2的基因组,筛选多个保守性较高的基因序列区域。参考株具体信息参见表1。并借鉴文献、国标以及who推荐的sars-cov-2实验室检测靶标,最终确定n蛋白基因的保守区域作为本发明的检测靶标,设计了一种用于rt-rpa可视化方法的sars-cov-2引物和探针,其上游引物n-f序列为:5
’‑
[biotin]ccaaggtttacccaataatactgcgtct-3’,如seq id no.1所示;下游引物n-r序列为:5
’‑
tctttcattttaccgtcaccaccacga-3’,如seq id no.2所示。上游引物的5’端修饰有生物素。探针n-probe:5
’‑
[fitc]aggacaaggcgttccaattaacaccaatag[thf]agtccagatgaccaa[c3-spacer]-3’,如seq id no.3所示。即探针5’端标记异硫氰酸荧光素(fitc),且在距羧基荧光基团的第30个碱基被四氢呋喃thf取代,3’端c3-spacer修饰。
[0008]
表1
[0009]
[0010]
[0011][0012]
第二方面,本发明提供一种新型冠状病毒rt-rpa可视化检测试剂盒,含有seq id no.1-2所示的引物对和seq id no.3所示的探针。
[0013]
所述新型冠状病毒rt-rpa可视化检测试剂盒还含有核苷酸序列如seq id no.4所示的sars-cov-2的n基因全长阳性质粒。
[0014]
所述新型冠状病毒rt-rpa可视化检测试剂盒还含有反转录酶、rna酶抑制剂、重悬缓冲液、重组酶、聚合酶、单链结合蛋白、水解缓冲液、醋酸镁溶液和rnasefree ddh2o中的一种或几种,优选地,所述的试剂盒还含有twistamp
tm nfo kit、rt-raa核酸扩增试剂盒。这些商品化的试剂盒中包括有重组酶、聚合酶冻干粉、单链结合蛋白、水解缓冲液rehydration buffer、280mm醋酸镁溶液。
[0015]
所述新型冠状病毒rt-rpa可视化检测试剂盒包括以下工作步骤:
[0016]
(1)将待测病毒rna和所述的n基因全长阳性质粒,与所述引物和探针组合、反转录酶、rna酶抑制剂、重悬缓冲液和rnasefree ddh2o混匀,加入到装有所述重组酶、聚合酶、单链结合蛋白、水解缓冲液的反应管中,再加入醋酸镁溶液,充分混匀后离心;
[0017]
(2)进行rt-rpa反应;
[0018]
(3)对rt-rpa反应产物使用一次性封闭式核酸可视化检测装置进行检测;优选封闭式核酸可视化检测装置为封闭式胶体金免疫层析试纸条;
[0019]
(4)结果判读,肉眼观察若质控线和检测线位置均出现红色条带,则样品中含有新型冠状病毒;若质控线位置出现红色条带,而检测线位置无条带,则样品中不含新型冠状病毒;若质控线位置没有出现红色条带,则检测结果无效。
[0020]
本发明提供的新型冠状病毒rt-rpa可视化检测试剂盒的工作步骤中,步骤(2)所述rt-rpa反应,其50μl反应体系为:10μm的上、下游引物各2.1μl,10μm的探针0.6μl,rehydration buffer 25μl,rna模板5μl,amv反转录酶5u,ddh2o 12.2μl,混匀后,加入280mm的醋酸镁溶液2.5μl;
[0021]
步骤(2)中反应温度为37-42℃,时间为15-30min,更优选地,反应温度为42℃,反应时间为20min。
[0022]
第三方面,本发明提供了本发明所述的引物和探针组合,所述的新型冠状病毒rt-rpa可视化检测试剂盒在检测新型冠状病毒中的应用。本领域技术人员应当理解,在检测新
型冠状病毒的应用中,存在非疾病诊断目的的检测与鉴定,例如口岸检疫中,检测食品、植物、化妆品、饲料等是否污染新冠病毒,均可采用本发明的试剂盒或本发明的引物和探针采用rt-rpa方法进行。
[0023]
因此本发明还提供了上述的引物和探针组合,所述的新型冠状病毒rt-rpa可视化检测试剂盒在新型冠状病毒流行病学调查、或在非疾病诊断和治疗目的的检测待检样品是否含有新型冠状病毒中的应用。
[0024]
本发明还提供了所述的引物和探针组合在制备检测新型冠状病毒检测试剂中的应用。
[0025]
本发明的有益效果在于:
[0026]
(1)本发明所建立的检测方法能够高特异性检测sars-cov-2。申请人前期分析比对20株sars-cov-2基因序列,筛选了n基因的多个保守区域作为靶标。考虑到冠状病毒n基因相似率较高,本发明将筛选到的靶序列组与sars-cov、mers-cov、hku1、oc43、229e、nl63等冠状病毒进行了序列分析,并最终确定位于sars-cov-2碱基序列的第28399-28581位核苷酸序列为最终检测靶标,以确保引物和探针组的特异性。针对sars-cov-2的n蛋白基因上的靶序列设计了适用于rt-rpa可视化方法的引物和探针组,其靶序列在sars-cov-2n基因中高度保守,并通过特异性试验验证本发明中所使用的引物和探针组与sars-cov、mers-cov、sars-cov-like、hku1、oc43、229e等其他冠状病毒均不存在交叉反应。此外,本发明引入封闭式胶体金试纸,避免了传统等温扩增技术易造成气溶胶污染的问题,且摆脱了对精密设备的依赖,操作过程更加简洁。
[0027]
(2)本发明所建立的检测方法,最低检测限为3.6
×
10-1
copies/μl阳性质粒或1copies/μl新型冠状病毒rna,检测结果稳定可靠。本发明所建立方法相较于who推荐的real-time pcr方法,在将其耗时缩短一半的条件下,灵敏度仍可与其保持同一数量级。(3)本发明试剂盒将rt-rpa技术与封闭式胶体金免疫层析试纸相结合,不需要精密的变温设备,只需在恒温条件下就能获得sars-cov-2靶标基因的有效扩增;通过全封闭式核核酸快速检测装置进行扩增结果的判读,既实现了结果的可视化,又避免了因气溶胶造成的假阳性结果;整个扩增与检测过程在25min内可以完成,大大缩短了常规pcr、real-time pcr、常规rpa的检测时间,实现了疫病现场的快速可视化检测。
附图说明
[0028]
图1为不同浓度质粒标准品评价新型冠状病毒rt-rpa可视化检测方法的敏感性。
[0029]
图2为不同浓度rna标准品评价新型冠状病毒rt-rpa可视化检测方法的敏感性。
[0030]
图3为评价新型冠状病毒rt-rpa可视化检测方法的特异性评价。
[0031]
图4为新型冠状病毒rt-rpa可视化检测方法的临床样品评价。
[0032]
图中control line指代质控线,test line指代检测线。
具体实施方式
[0033]
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别说明,本发明实施例中所用试剂为市售可得。
[0034]
n基因全长阳性质粒购于上海生工生物有限公司;twistamp nfo kits购自
twistdx公司;amv reverse transcriptase、病毒rna/dna提取试剂盒购自宝生物工程(大连)公司;一次性核酸检测装置购自杭州优思达生物技术有限公司,呼吸性病原体试剂盒rp1、rp2购于zeptometrix公司。
[0035]
实施例1 sars-cov-2反转录重组酶聚合酶等温扩增核酸可视化检测方法的建立
[0036]
1、引物和探针的设计与合成
[0037]
本发明人使用软件mega7比对了包括现有变异株在内的不同国家、地区、不同时间分离的20株新冠病毒基因组序列其参考株详细信息参见表1。结合文献、国标以及who推荐的实验室检测靶标,确定n蛋白基因作为本发明的检测靶基因。考虑到冠状病毒属成员n基因相似率较高,因此本发明人将筛选到的保守区域与sars-cov、mers-cov、hku1、oc43、229e、nl63等冠状病毒进行了分析比对,并最终确定位于sars-cov-2碱基序列的第28399-28581位核苷酸序列为最终检测靶标,以确保引物和探针组的特异性。根据rpa引物设计原则前期工作过程中设计并合成了大量引物和探针组合,从中筛选出一对灵敏度高且扩增效率好的引物,及其对应探针。
[0038]
其上游引物n-f序列为:5
’‑
[biotin]ccaaggtttacccaataatactgcgtct-3’,下游引物n-r序列为:5
’‑
tctttcattttaccgtcaccaccacga-3’。探针序列:5
’‑
[fitc]aggacaaggcgttccaattaacaccaatag[thf]agtccagatgaccaa[c3-spacer]-3’,本试剂盒还提供n基因全长阳性质粒,其n基因全长序列如seq id no.4所示。
[0039]
注:fitc:异硫氰酸荧光素;thf:四氢呋喃;c3-spacer:聚合物延伸阻断物。
[0040]
2、rt-rpa-vf检测体系的建立
[0041]
经体外转录获得的sars-cov-2n基因的rna作为rt-rpa-vf检测的模板,使用twist公司的twistamptm nfo kit(twistdx,cambridge,uk)建立rt-rpa-vf扩增方法,反应体系为50μl,10μm的上下游引物各2.1μl,10μm的探针0.6μl,rehydration buffer 25μl,rna 5μl,amv反转录酶5u,ddh2o 12.2μl;将上述47.5μl体系混匀后加入到装有冻干粉的反应管中,吹打至完全溶解,向反应管中加入2.5μl 280mm醋酸镁,混合均匀后置于37℃恒温水浴孵育20min。然后,将反应管装入全封闭式核酸快速检测装置(杭州优思达生物技术有限公司,江苏,中国)进行检测;肉眼观察若质控线和检测线位置均出现红色条带,则样品中含有新冠病毒;若质控线位置出现红色条带,而检测线位置无条带,则样品中不含新冠病毒;若质控线位置没有出现红色条带,则检测结果无效。
[0042]
3、rt-rpa-vf反应温度的优化
[0043]
将浓度为3.6
×
10
10
copies/μl的阳性质粒进行10倍系列稀释至3.6
×
10-3
copies/μl,作为rt-rpa-vf方法的模板。按上述体系分别在37℃、39℃、40℃、42℃条件进行扩增30min,以筛选最适扩增温度。扩增后的产物经一次性核酸可视化检测装置进行检测。结果显示,在42℃条件下,检测模板阳性质粒浓度≥3.6
×
10-1
copies/μl,质控线和检测线均呈现红色条带,即检测结果判定为sars-cov-2阳性。而37℃、39℃、40℃条件下,仅在阳性质粒浓度≥100copies/μl时才呈现sars-cov-2阳性(如图1),因此,最适的反应温度为37~42℃,但最优为42℃。
[0044]
4、rt-rpa-vf反应时间的优化
[0045]
分别将3.6
×
100copies/μl、3.6
×
10-1
copies/μl和3.6
×
10-2
copies/μl的阳性质粒标准品为模板,分别在10min、15min、20min、25min、30min进行扩增,对反应时间进行优
化。经核酸检测装置检测发现扩增时间在20min以上均能检测出0.36copies/μl阳性质粒(如图1)。因此,rt-rpa-vf最优反应时间为20min。
[0046]
实施例2新型冠状病毒反转录重组酶聚合酶扩增核酸可视化检测方法敏感性评价
[0047]
由上海生工生物工程股份有限公司合成的4μg n基因部分序列rna转录本(seq id no.5)作为检测模板评价本方法敏感性,其具体序列信息参见序列表。将rna转录本通过depc水稀释溶解后,经紫外分光光度器测得浓度为226ng/μl。通过下列公式换算rna转录本的拷贝数:rna浓度(copies/μl)=[rna浓度(g/μl)/(体外转录rna长度
×
340)]
×
6.02
×
10
23
。经计算后可知人工合成的rna转录本浓度约为1
×
10
12
copies/μl。
[0048]
分别将rna转录本进行10倍系列稀释,以实施例1建立的rt-rpa-vf检测体系在42℃条件下扩增20min后,以一次性核酸可视化检测装置检测扩增产物,结果显示,rt-rpa-vf方法的检测敏感度为1copies/μl rna转录本。
[0049]
实施例3新型冠状病毒反转录重组酶聚合酶等温扩增核酸可视化检测方法特异性评价
[0050]
分别以sars-cov-2、严重急性呼吸综合征样冠状病毒(sars-cov-like)、mers-cov、猪流行性腹泻病毒(pedv)、猫传染性腹膜炎病毒(fcov)的rna及呼吸性病原体试剂盒rp1、rp2的rna/dna作为检测模板评价实施例1建立的rt-rpv-vf方法的特异性。
[0051]
结果显示,仅sars-cov-2rna的检测结果呈现阳性结果,而其他冠状病毒及呼吸性病原体均呈现阴性(如图3),表明本发明所建立的rt-rpa-vf检测方法与sars-cov-like、mers-cov、hku1、oc43、229e等冠状病毒及其他呼吸性病原体不存在交叉反应,该方法具有较高的特异性。
[0052]
实施例4新型冠状病毒反转录重组酶聚合酶等温扩增核酸可视化检测方法临床样品检测
[0053]
采集sars-cov-2感染的balb/c小鼠和猴呼吸道分泌物,包括balb/c小鼠咽拭子样品7份、食蟹猴咽拭子样品5份。健康balb/c小鼠和食蟹猴呼吸道分泌物各1份,提取上述样品的rna,采用本发明试剂盒进行检测。同时依据中国疾病预防控制中心推荐的real-time rt-pcr,合成相应的引物和探针,对上述样品进行real-time rt-pcr(https://nmdc.cn/resource/ncov/primers/detail/5e9d1386e517ca4ff8006742)方法检测。本发明的检测结果与real-time rt-pcr方法检测结果完全一致,12份sars-cov-2感染的balb/c小鼠和食蟹猴呼吸道样品均为sars-cov-2阳性,2份健康balb/c小鼠和食蟹猴呼吸道样品均为sars-cov-2阴性(如图4),表明本发明的实施例1建立的sars-cov-2反转录重组酶聚合酶等温扩增核酸可视化检测方法及试剂盒在疑似sars-cov-2阳性样品的临床筛查中是可行的,能够满足临床检测的需要。
[0054]
实施例5新型冠状病毒反转录重组酶聚合酶等温扩增核酸可视化检测试剂盒的组装
[0055]
将引物n-f和n-r各210μl、探针n-probe 60μl、阳性质粒100μl,然后与rehydration buffer、醋酸镁、装有酶制剂冻干粉管、一次性封闭式核酸可视化检测装置、八连管组装成96t的新型冠状病毒反转录重组酶聚合酶等温扩增可视化检测试剂盒。
[0056]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因
此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1