一种阿巴帕肽的纯化方法与流程
1.本发明涉及多肽纯化技术领域,尤其涉及一种阿巴帕肽的纯化方法。
背景技术:
2.阿巴帕肽(abaloparatide),是由radius health公司研制的一种新型甲状旁腺激素相关肽(pthrp),它是pth-i受体强有力的选择性激活剂,可以增加骨矿物质含量、骨密度以及骨强度,促进骨骼形成,已于2017年4月28日被fda批准上市,其商品名称为tymlos。阿巴帕肽经皮下注射,用于治疗处于骨折风险或对其它治疗药物无效的绝经后妇女的骨质疏松症,可有效降低新发椎体和非椎体骨折率。甲状旁腺激素(pth)是一种由甲状旁腺主细胞分泌的,调节体内钙和磷代谢的多肽类激素,其c端肽链与pth-ii受体结合可促进骨细胞凋亡、n端肽链与pth-i受体结合可促进骨骼重建。阿巴帕肽由34个氨基酸残基组成,分子式为c
174h300n56o49
,分子量3960,肽链中含有4个lys和三个arg,等电点为9.98,极易结合大量的酸根。其肽链序列如下:
3.ala
1-val
2-ser
3-glu
4-his
5-gln
6-leu
7-leu
8-his
9-asp
10-lys
11-gly
12-lys
13-ser
14-ile
15-gln
16-asp
17-leu
18-arg
19-arg
20-arg
21-glu
22-leu
23-leu
24-glu
25-lys
26-leu
27-leu
28-aib
29-lys
30-leu
31-his
32-thr
33-ala
34-nh2。
4.原研及个参考文献均采用固相合成的方式合成阿巴帕肽,合成过程中会产生大量的杂质,比如氨基酸消旋、氨基酸插入、氨基酸缺失等,现有的纯化方法无法将纯度提高,也无法将单杂降低至0.1%以下,且收率较低,制备成本高。
5.如专利cn 112724241 a1中公开了一种阿巴帕肽的纯化方法。包括以下步骤:步骤一:取阿巴帕肽粗肽进行预处理使其溶于乙腈水溶液中,获得粗肽溶液;步骤二:取所述粗肽溶液,以a1、a2溶液与b溶液的混合溶液进行等度、梯度洗脱,收集洗脱组分,得第一次纯化物;步骤三:取所述第一次纯化物,以a3与b溶液的混合溶液进行转盐等度洗脱,收集洗脱组分,得最终纯化物;步骤四:取最终纯化物经减压旋蒸浓缩、冷冻干燥,得到阿巴帕肽成品;所述a1溶液为10%醋酸水溶液;所述a2溶液为0.1%的tfa的水溶液;所述a3溶液为纯水;所述b溶液为100%乙腈。由于肽链的等电点为9.98,极易集合大量的酸根,所以再使用含有强酸的流动相纯化之后进行转盐,需要用醋酸盐(醋酸铵、醋酸钠或醋酸钾等)缓冲液置换以除去这些酸根。而该专利的公开文件中并没有相应的操作步骤,结果必然导致tfa残留严重。
技术实现要素:
6.针对上述背景技术中,阿巴帕肽纯化效果不理想,消旋杂质及氨基酸插入的杂质控制不力,且tfa残留严重等问题,本发明提供一种阿巴帕肽的纯化方法,能够得到纯度≥99.0%,单杂≤0.10%的醋酸盐样品,氨基酸插入的杂质控制在0.10%以内,tfa未检出,且单次上样量高,生产周期短,废液量少,有利于环保。
7.为实现上述目的,本发明采取的技术方案为:
8.本发明提供一种阿巴帕肽的纯化方法,包括以下步骤:
9.(1)以醋酸盐缓冲液为流动相a1,以乙腈为流动相b对阿巴帕肽粗肽溶液进行梯度洗脱,收集洗脱组分;
10.(2)将步骤(1)收集的洗脱组分转盐:以醋酸溶液为流动相a2,以乙腈为流动相b进行梯度洗脱,收集洗脱组分得到醋酸阿巴帕肽。
11.作为优选地实施方式,步骤(1)中,所述流动相b乙腈的起始体积百分比为15%~25%,截至体积百分比为35%~45%,洗脱时间为50~100min。
12.作为优选地实施方式,步骤(1)中,所述醋酸盐选自醋酸铵、醋酸钠和醋酸钾中的任意一种或任意混合。
13.优选地,步骤(1)中,所述醋酸盐缓冲液的ph值为4.0~8.0。
14.在某些具体的实施方式中,所述醋酸盐缓冲液的ph值为4.0、5.0、6.0、7.0、8.0或它们之间的任意数值的ph。
15.在某些具体的实施方式中,所述醋酸盐缓冲液由醋酸与氨水、氢氧化钠或氢氧化钾混合配制而成。
16.优选地,步骤(1)中,所述醋酸盐缓冲液中以醋酸根的浓度计为5~500mmol/l;进一步优选为20~200mmol/l。
17.在某些具体的实施方式中,所述醋酸盐缓冲液中以醋酸根的浓度计为5mmol/l、50mmol/l、100mmol/l、150mmol/l、200mmol/l、250mmol/l、300mmol/l、400mmol/l、500mmol/l或它们之间的任意数值的浓度。
18.作为优选地实施方式,步骤(1)中,所述对阿巴帕肽粗肽溶液为将阿巴帕肽粗肽溶于乙腈和水的混合溶液;所述乙腈的体积百分比为5%~15%。
19.作为优选地实施方式,步骤(2)中,所述流动相b乙腈的起始体积百分比为5%~15%,截止体积百分比为50%~60%,洗脱时间为30~60min。
20.作为优选地实施方式,步骤(2)中,所述醋酸溶液的浓度为0.05%~5.0%。
21.在某些具体的实施方式中,所述醋酸溶液的浓度为0.05%、0.1%、1.0%、2.0%、3.0%、4.0%、5.0%或它们之间任意数值的浓度。
22.作为优选地实施方式,步骤(2)中,所述梯度洗脱前还包括冲洗,所述冲洗为以所述流动相a2和流动相b进行冲洗。
23.优选地,所述冲洗时间为10~30min。
24.在某些具体的实施方式中,所述冲洗前,需将步骤(1)得到的洗脱组分进行稀释;所述稀释为用水进行稀释,具体为0.8~1.5倍体积的水进行稀释。
25.在本发明的技术方案中,所述纯化方法采用反相制备色谱柱;所述反相制备色谱柱的内装填料选自反相c18、c8和c4中的任意一种;
26.优选地,所述内装填料的粒径为5~10μm;所述内装填料的孔径为5~30nm。
27.作为优选地实施方式,步骤(1)中,所述反相制备色谱柱的上样量为其内装填料质量的1%~10%;优选为3.0%~8.0%。
28.优选地,步骤(2)中,所述反相制备色谱柱的上样量为其内装填料质量的0.5%~5%;优选为1.0%~3.0%。
29.在某些具体的实施方式中,步骤(1)中,所述梯度洗脱还包括前处理,所述前处理
包括过滤和平衡制备色谱柱;所述平衡制备色谱柱为以所述流动相a1和流动相b平衡制备色谱柱,其中流动相b的体积百分比为5%~15%,采用合适的流动相比例使制备色谱柱内的乙腈体积百分比小于初始洗脱梯度,待处理的样品恰好能够吸附在色谱柱又不至于被洗脱。
30.在某些具体的实施方式中,步骤(2)中,还包括后处理,所述后处理包括减压旋蒸和冻干。
31.上述技术方案具有如下优点或者有益效果:
32.本发明提供的阿巴帕肽的纯化方法,首先以醋酸盐缓冲液为流动相a1,乙腈为流动相b对阿巴帕肽粗肽溶液进行梯度洗脱;而后以醋酸为流动相a2,乙腈为流动相b进行转盐,减压旋蒸后冻干即可得到醋酸阿巴帕肽。本发明通过一步纯化加一步转盐即可得到纯度≥99.0%,单杂≤0.10%的合格馏分,将单个杂质控制0.10%以内,且tfa未检出。避免多次纯化而导致有机溶剂消耗量过大,减少纯化的步骤及废液的排放,整个过程操作简单,生产周期短,环境友好,有利于大规模工业化生产。
附图说明
33.图1是实施例1中转盐后冻干精肽的rp-hplc图谱。
34.图2是实施例2中转盐后冻干精肽的rp-hplc图谱。
35.图3是实施例3中转盐后冻干精肽的rp-hplc图谱。
36.图4是实施例4中转盐后冻干精肽的rp-hplc图谱。
37.图5是对比例1中转盐后冻干精肽的rp-hplc图谱。
38.图6是对比例2中转盐后冻干精肽的rp-hplc图谱。
39.图7是对比例3中转盐后冻干精肽的rp-hplc图谱。
40.图8是对比例4中转盐后冻干精肽的rp-hplc图谱。
具体实施方式
41.下述实施例仅仅是本发明的一部分实施例,而不是全部的实施例。因此,以下提供的本发明实施例中的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明的实施例,本领域技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都属于本发明的保护范围。
42.在本发明中,若非特指,所有的设备和原料等均可从市场购得或是本行业常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
43.下述实施例与对比例中,阿巴帕肽粗品为通过基因重组、固相合成、液相合成或固液相结合合成制备得到。
44.实施例1:
45.称取200.0g阿巴帕肽粗品(含阿巴帕肽86.6g),以8l乙腈的体积百分比为10%的乙腈/水溶解,0.45μm滤膜过滤。制备柱为15cm dac,内装3.0kg的c18填料(10μm-,10μm为粒径、为孔径,下述同理)。流动相a1为100mmol/l醋酸铵水溶液,以醋酸调节ph为5.0,流动相b为乙腈。92%a1+8%b平衡10min,流速500ml/min,上样后进行梯度洗脱,洗脱梯度为20%b-40%b/(60min),收集纯度≥95.0%,单杂≤1.0%的馏分,将50.0%≤纯度≤
95.0%或纯度≥95.0%,单杂>1.0%的馏分合并,上样后以a1和b进行梯度洗脱再纯化。
46.将所有合格馏分收集,加入等体积的水稀释,进行转盐。流动相a2为0.5%的醋酸水溶液。上样后以90%a2+10%b冲洗20min,流速500ml/min;而后以a2和b进行梯度洗脱,洗脱梯度为5%b-55%b/(50min),收集纯度≥99.0%,单杂≤0.10%的馏分,旋蒸后冻干得醋酸阿巴帕肽60.8g,纯化回收率为70.2%,纯度为99.86%,最大单杂为0.07%。
47.图1为本实施例中,转盐后的冻干精肽的测试图谱。
48.实施例2:
49.称取210.0g阿巴帕肽粗品(含阿巴帕肽90.9g),以8l乙腈的体积百分比为10%的乙腈/水溶解,0.45μm滤膜过滤。制备柱为15cm dac,内装3.0kg的c8填料(10μm-)。流动相a1为100mmol/l醋酸铵水溶液,以醋酸调节ph为5.5,流动相b为乙腈。92%a1+8%b平衡10min,流速500ml/min,上样后进行梯度洗脱,洗脱梯度为20%b-40%b/(60min),收集纯度≥95.0%,单杂≤1.0%的馏分,将50.0%≤纯度≤95.0%或纯度≥95.0%,单杂>1.0%的馏分合并,上样后以a1和b进行梯度洗脱再纯化。
50.将所有合格馏分收集,加入等体积的水稀释,进行转盐。流动相a2为0.3%的醋酸水溶液。上样后以90%a2+10%b冲洗20min,流速500ml/min;而后以a2和b进行梯度洗脱,洗脱梯度为5%b-55%b/(50min),收集纯度≥99.0%,单杂≤0.10%的馏分,旋蒸后冻干得醋酸阿巴帕肽63.0g,纯化回收率为69.3%,纯度为99.91%,最大单杂为0.06%。
51.图2为本实施例中,转盐后的冻干精肽测试图谱。
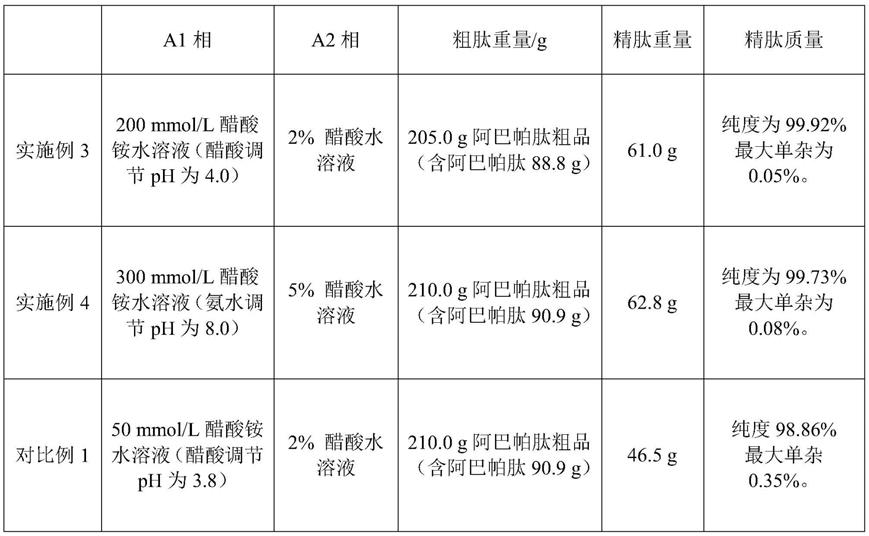
52.实施例3-4、对比例1-4
53.申请人同时进行了以下的实施例和对比例,制备柱均为15cm dac,内装3.0kg的c18填料与上述实施例1和实施例2不同之处,汇总列于表1。
54.表1
55.[0056][0057]
实施例3-4中,转盐冻干后的精肽测试图谱分别见图3和图4;对比例1-4中的转盐冻干后的精肽测试图谱分别由图5-8所示。
[0058]
以上所述仅为本发明的优选实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等效变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1