一种基于糖精衍生物的分子及其制备方法与应用与流程
1.本发明属于有机光电技术领域,具体涉及一种基于糖精衍生物的分子及其制备方法与应用。
背景技术:
2.有机发光二极管(oled)器件由阴极、阳极和中间包夹的有机层(包括电子传输层、发光层、空穴传输层等)构成,器件工作机理为:电子和空穴分别从阴阳两极注入,并分别在功能层中进行迁移,然后电子和空穴在合适的位置形成激子,激子在一定范围内进行迁移,最后激子跃迁至基态发光。
3.由于电子和空穴都存在两种自旋,复合过程是随机的,简单按照自旋量子统计理论来估算,电子和空穴复合产生的三线态激子的数量会是单线态激子的三倍。由于自旋数位为1的三线态激子不能通过辐射跃迁回到自旋数位0的基态,因此占激子总数75%的三线态激子只能以非辐射的形式散发出去,换而言之25%是有机荧光二极管器件最大理论内量子效率上限。为了突破这一理论上限,研究者们开发出了很多理论和方法。
4.其中基于热辅助延迟荧光(tadf)的分子体系可以实现全有机体系对三线态激子的高效利用。通过将分子的homo轨道分布和lumo轨道分布分离,获得最低三线态和最低单线态能量差别非常小的分子。在热量的作用下,分子从 t1态反方向窜越到s1态可以得以实现,从而实现三线态激子的利用,激子利用率(内量子效率)几乎可以到100%。
技术实现要素:
5.针对目前有机半导体薄膜器件,本发明的首要目的在于提供一类基于糖精衍生物受体的分子。该类分子以糖精衍生物作为电子受体单元(a),以芳胺衍生物作为给体单元(d),通过稠环体系连接形成d-π-a的结构,可以实现分子的homo轨道分布和lumo轨道分布分离,降低分子的单线态和三线态能级差。
6.本发明的另一目的在于提供所述一种基于糖精衍生物的分子的制备方法。
7.本发明的再一目的在于提供所述一种基于糖精衍生物的分子在有机电子器件中的应用。
8.本发明目的通过以下技术方案实现:
9.一类基于糖精衍生物的分子,化学结构如式(1)所示:
可彼此连接且可形成环。
17.优选的,l选自苯、萘、蒽、苯并蒽、菲、苯并菲、芘、苝、荧蒽、并四苯、并五苯、联苯、三联苯、四联苯、芴、螺二芴、呋喃、苯并呋喃、异苯并呋喃、噻吩、苯并噻吩、异苯并噻吩、二苯并噻吩、吲哚、异吲哚、咔唑、吲哚并咔唑、茚并咔唑、吡啶、喹啉、异喹啉、吖啶、菲啶、苯并咪唑、嘧啶、吡嗪和三嗪;上述基团可各自被一个或多个基团r2取代(r2的定义同上文相同)。
18.优选的,所述基于糖精衍生物的分子,其化学结构为以下m1~m12所示结构式中的一种:
19.[0020][0021]
一种制备上述基于糖精衍生物的分子的方法,包括:
[0022]
方法a
[0023]
通过在糖精衍生物和芳族或杂芳族环系之间的偶联反应制备一个或多个芳族或杂芳族环系取代的糖精衍生物;卤化后在卤代位置处引入取代基得到基于糖精衍生物的分子;或
[0024]
方法b
[0025]
i)通过在糖精衍生物和卤代芳族或卤代杂芳族环系之间的偶联反应制备一个或多个卤代芳族或杂芳族环系取代的糖精衍生物;
[0026]
ii)使所述取代的糖精衍生物与苯胺衍生物进行偶联反应,得到基于糖精衍生物的分子。
[0027]
进一步地,步骤ii)所述反应的温度为80~120℃,时间为2~36小时;所用溶剂包括甲苯、二甲苯、三甲苯、四氢呋喃、dmf中的一种或一种以上的混合溶剂。
[0028]
该类分子以糖精衍生物作为电子受体单元(a),以芳胺衍生物作为给体单元(d),通过稠环体系连接形成d-π-a的结构,可以实现分子的homo轨道分布和lumo轨道分布分离,降低分子的单线态和三线态能级差。
[0029]
一种含有一种或多种所述基于糖精衍生物的分子的低聚物、聚合物或树枝状大分子,其中一个或多个键合到所述聚合物、低聚物或树枝状大分子的键可位于式(i)中被r1、r2、r3或r4取代的任何期望的位置处。
[0030]
所述的基于糖精衍生物的分子,基于糖精衍生物的分子的低聚物、聚合物或树枝状大分子具良好的加工性,可用于制备有机电子器件。所述有机电子器件优选为有机薄膜晶体管(ofet)、有机发光晶体管(olet)、有机太阳能电池(osc)、有机光电二极管(opd)、有机光电晶体管(opt)、有机发光电化学电池(olec)或有机电致发光二极管器件(oled)。
[0031]
一种制备有机电子器件的方法,将含有所述基于糖精衍生物的分子和/或基于糖精衍生物的分子的低聚物、聚合物或树枝状大分子通过蒸镀、旋涂、喷墨打印或印刷成膜,得到有机电子器件的功能层。
[0032]
与现有技术相比,本发明具有以下优点及有益效果:
[0033]
(1)本发明的基于糖精衍生物的分子,结构简单,成本低廉,有利于批量化生产;
[0034]
(2)本发明的基于糖精衍生物的分子,可以实现分子的homo轨道分布和lumo轨道分布分离,降低分子的单线态和三线态能级差。
附图说明
[0035]
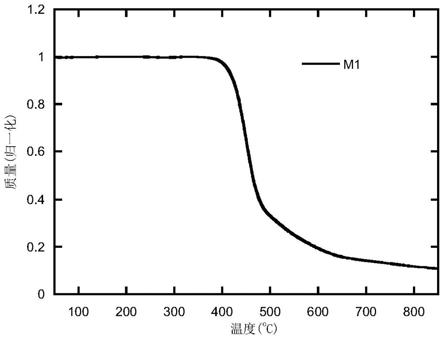
图1为分子m1的热失重测试图;
[0036]
图2为分子m1在ito/pedot:pss/pvk/pvk:m1/csf/al器件结构下的电致发光光谱图。
具体实施方式
[0037]
下面结合实施例和附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
[0038]
实施例1:化合物u1和m1的制备
[0039]
(1)化合物u1的合成
[0040]
在氮气气氛下,将1,4-二溴苯(10mmol)、9,9-二甲基吖啶(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml 甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率79%。1h nmr、
13
cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0041]
合成化合物u1反应方程式如下所示:
[0042][0043]
(2)化合物m1的合成
[0044]
在氮气保护下,将化合物u1(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率81%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0045]
合成化合物m1反应方程式如下所示:
[0046]
[0047]
实施例2:化合物u2和m2的制备
[0048]
(1)化合物u2的合成
[0049]
在氮气气氛下,将1,4-二溴苯(10mmol)、吩噻嗪(10mmol)、醋酸钯(0.5 mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3 (v/v)作淋洗剂柱层析提纯,得固体产物,产率73%。1h nmr、13cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0050]
合成化合物u2反应方程式如下所示:
[0051][0052]
(2)化合物m2的合成
[0053]
在氮气保护下,将化合物u2(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率81%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0054]
合成化合物m2反应方程式如下所示:
[0055][0056]
实施例3:化合物u3和m3的制备
[0057]
(1)化合物u3的合成
[0058]
在氮气气氛下,将1,3-二溴苯(10mmol)、9,9-二甲基吖啶(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml 甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率75%。1h nmr、
13
cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0059]
合成化合物u1反应方程式如下所示:
[0060][0061]
(2)化合物m3的合成
[0062]
在氮气保护下,将化合物u3(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率85%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0063]
合成化合物m3反应方程式如下所示:
[0064][0065]
实施例4:化合物u4和m4的制备
[0066]
(1)化合物u4的合成
[0067]
在氮气气氛下,将1,3-二溴苯(10mmol)、吩噻嗪(10mmol)、醋酸钯(0.5 mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3 (v/v)作淋洗剂柱层析提纯,得固体产物,产率78%。1h nmr、13cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0068]
合成化合物u4反应方程式如下所示:
[0069][0070]
(2)化合物m4的合成
[0071]
在氮气保护下,将化合物u4(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率88%。1h nmr、
13
cnmr、ms和元
素分析结果表明所得到的化合物为目标产物。
[0072]
合成化合物m4反应方程式如下所示:
[0073][0074]
实施例5:化合物u5和m5的制备
[0075]
(1)化合物u5的合成
[0076]
在氮气气氛下,将1,4-二溴代萘(10mmol)、9,9-二甲基吖啶(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12 ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率73%。1h nmr、
13
cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0077]
合成化合物u5反应方程式如下所示:
[0078][0079]
(2)化合物m5的合成
[0080]
在氮气保护下,将化合物u5(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率83%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0081]
合成化合物m5反应方程式如下所示:
[0082][0083]
实施例6:化合物u6和m6的制备
[0084]
(1)化合物u6的合成
[0085]
在氮气气氛下,将1,4-二溴代萘(10mmol)、吩噻嗪(10mmol)、醋酸钯 (0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反
应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7: 3(v/v)作淋洗剂柱层析提纯,得固体产物,产率68%。1h nmr、13cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0086]
合成化合物u6反应方程式如下所示:
[0087][0088]
(2)化合物m6的合成
[0089]
在氮气保护下,将化合物u6(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率63%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0090]
合成化合物m6反应方程式如下所示:
[0091][0092]
实施例7:化合物u7和m7的制备
[0093]
(1)化合物u7的合成
[0094]
在氮气气氛下,将4,7-二溴-2,1,3-苯并噻二唑、9,9-二甲基吖啶(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12 ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率73%。1h nmr、
13
cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0095]
合成化合物u7反应方程式如下所示:
[0096][0097]
(2)化合物m7的合成
[0098]
在氮气保护下,将化合物u7(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:
二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率63%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0099]
合成化合物m7反应方程式如下所示:
[0100][0101]
实施例8:化合物u8和m8的制备
[0102]
(1)化合物u8的合成
[0103]
在氮气气氛下,4,7-二溴-2,1,3-苯并噻二唑、吩噻嗪(10mmol)、醋酸钯(0.5 mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3 (v/v)作淋洗剂柱层析提纯,得固体产物,产率64%。1h nmr、13cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0104]
合成化合物u8反应方程式如下所示:
[0105][0106]
(2)化合物m8的合成
[0107]
在氮气保护下,将化合物u8(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:4(v/v)作淋洗剂柱层析提纯,得固体产物,产率67%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0108]
合成化合物m8反应方程式如下所示:
[0109][0110]
实施例9:化合物u9和m9的制备
[0111]
(1)化合物u9的合成
[0112]
在氮气气氛下,将9,9-二甲基-2,7-二溴芴(10mmol)、9,9-二甲基吖啶(10 mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=7:3(v/v)作淋洗剂柱层析提纯,得固体
产物,产率73%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0113]
合成化合物u9反应方程式如下所示:
[0114][0115]
(2)化合物m9的合成
[0116]
在氮气保护下,将化合物u9(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:2(v/v)作淋洗剂柱层析提纯,得固体产物,产率67%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0117]
合成化合物m9反应方程式如下所示:
[0118][0119]
实施例10:化合物u10和m10的制备
[0120]
(1)化合物u10的合成
[0121]
在氮气气氛下,9,9-二甲基-2,7-二溴芴(10mmol)、吩噻嗪(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml 甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3(v/v)作淋洗剂柱层析提纯,得固体产物,产率74%。1h nmr、13cnmr、 ms和元素分析结果表明所得到的化合物为目标产物。
[0122]
合成化合物u10反应方程式如下所示:
[0123][0124]
(2)化合物m10的合成
[0125]
在氮气保护下,将化合物u10(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2(v/v)作淋洗剂柱层析提纯,得固体产物,产率82%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0126]
合成化合物m10反应方程式如下所示:
[0127][0128]
实施例11:化合物u11、u12和m11的制备
[0129]
(1)化合物u11的合成
[0130]
在氮气气氛下,5,10-二氢吩嗪(10mmol)、溴苯(22mmol)、醋酸钯(0.5 mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3 (v/v)作淋洗剂柱层析提纯,得固体产物,产率75%。1h nmr、
13
cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0131]
(2)化合物u12的合成
[0132]
在氮气保护下,将u11(10mmol)溶于10ml甲苯,避光条件下,将n-溴代丁二酰亚胺(12mmol)分批加入反应中,常温搅拌反应。反应停止,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2(v/v)作淋洗剂柱层析提纯,得固体产物,产率63%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0133]
化合物u11、u12反应方程式如下所示:
[0134][0135]
(2)化合物m11的合成
[0136]
在氮气保护下,将化合物u12(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2(v/v)作淋洗剂柱层析提纯,得固体产物,产率79%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0137]
合成化合物m11反应方程式如下所示:
[0138][0139]
实施例12:化合物m12的制备
[0140]
(1)化合物m12的合成
[0141]
在氮气保护下,将化合物u1(10mmol)、5,6-二氟糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,
冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2 (v/v)作淋洗剂柱层析提纯,得固体产物,产率85%。1h nmr、
13
cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0142]
合成化合物m12反应方程式如下所示:
[0143][0144]
实施例13:化合物m13的制备
[0145]
(1)化合物m13的合成
[0146]
在氮气保护下,将化合物u2(10mmol)、5,6-二氟糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2 (v/v)作淋洗剂柱层析提纯,得固体产物,产率82%。1h nmr、
13
cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0147]
合成化合物m13反应方程式如下所示:
[0148][0149]
实施例14:化合物u13、u14和m14的制备
[0150]
(1)化合物u13的合成
[0151]
在氮气气氛下,5,10-二氢吩嗪(10mmol)、溴苯(10mmol)、醋酸钯(0.5 mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=1:3 (v/v)作淋洗剂柱层析提纯,得固体产物,产率74%。1h nmr、
13
cnmr、ms 和元素分析结果表明所得到的化合物为目标产物。
[0152]
(2)化合物u14的合成
[0153]
在氮气气氛下,u13(10mmol)、1,3-二溴苯(10mmol)、醋酸钯(0.5mmol)、三叔丁基膦(0.4mmol)、叔丁醇钾(15mmol)溶解在12ml甲苯中,加热至 130℃反应30分钟。反应完毕,冷却到室温,用二氯甲烷萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=2:3(v/v) 作淋洗剂柱层析提纯,得固体产物,产率64%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0154]
化合物u13、u14反应方程式如下所示:
[0155][0156]
(3)化合物m14的合成
[0157]
在氮气保护下,将化合物u14(10mmol)、糖精(10mmol)、醋酸钯(1mmol)、三环己基膦(2mmol)、磷酸三钾(15mmol)溶解在10ml甲苯中,加热至110℃反应24h。反应完毕,冷却至室温,用乙酸乙酯萃取产物,饱和氯化钠水溶液洗涤三遍,除去有机相溶剂后,粗产物石油醚:二氯甲烷=3:2(v/v)作淋洗剂柱层析提纯,得固体产物,产率82%。1h nmr、
13
cnmr、ms和元素分析结果表明所得到的化合物为目标产物。
[0158]
合成化合物m14反应方程式如下所示:
[0159][0160]
实施例15:有机发光二极管的制备
[0161]
取预先做好的方块电阻为10ω的氧化铟锡(ito)玻璃,依次用丙酮、洗涤剂、去离子水和异丙醇超声清洗,等离子处理10分钟;在ito上旋涂参杂有聚苯乙烯磺酸的聚乙氧基噻吩(pedot:pss=1:6,w/w)膜,厚度为40nm; pedot:pss膜在真空烘箱里80℃下干燥8小时;随后将聚乙烯咔唑(pvk)的氯苯溶液(1wt.%)旋涂在pedot:pss膜的表面,厚度为20nm,作为空穴传输层;再将pvk:m1~m14(95:5)的二甲苯溶液(1.2wt.%)旋涂在pvk膜的表面,厚度为70nm,作为发光层;最后在发光层上依次蒸镀一层1.5nm厚的csf和 150nm厚的金属al层,器件结构:ito/pedot:pss/pvk/pvk:m1~m14/csf/al。
[0162]
表1聚合物电致发光器件性能
[0163][0164]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1