苯基硅烷的提纯方法与流程
1.本发明涉及提纯技术领域,具体涉及苯基硅烷的提纯方法。
背景技术:
2.二苯基二硅烷(式ia)具有良好的光电、材料性能,应用于光致抗蚀剂、烯烃聚合光引发剂、薄膜光波导器、有机光导电体、紫外线性光学材料等对产品纯度要求更高的领域,但现在针对二苯基硅烷的简便纯化方法未见报道,因此对二苯基硅烷的纯化进行研究具有重要意义。
[0003][0004]
文献j.organomet chem.,2007,692,3559;organometallics,2019,38,2902和dalton t,2020,49,1731中均报道了一种以苯基氯硅烷为原料制备二苯基二硅烷的方法,反应方程式如下所示:
[0005][0006]
上述参考文献均以苯基氯硅烷为原料,但是苯基氯硅烷与水反应极易产生(式ⅱa)所表述的杂质二苯基二硅氧烷,其反应如文献journal of the chemical society perkin transactions i,1998,7,1209中记载,不能满足高纯二苯基硅烷的应用需求,需进行提纯操作,但杂质式ⅱa化合物的沸点与式ia化合物二苯基硅烷的沸点接近,因此通过精馏等方法将二者分离难度很大,效率低,成本高,需改进。
[0007]
技术实现要素:
[0008]
为解决上述至少一个技术缺陷,本发明提供了如下技术方案:
[0009]
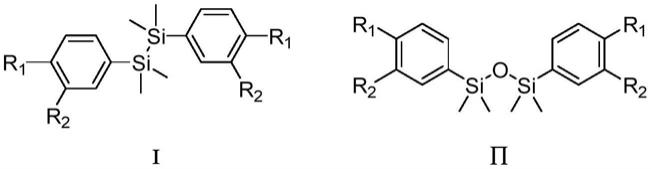
本技术文件公开苯基硅烷的提纯方法,将含式ⅱ化合物的式ⅰ化合物粗品与有机溶剂、三氟化硼络合物混合,在60~100℃下反应3~24h,之后蒸馏排出式ⅱ化合物与三氟化硼络合物反应分解的产物,完成式ⅰ化合物粗品的提纯;
[0010][0011]
其中r1、r2分别独立地选自h,me,ome,cf3或et。
[0012]
本方案在有机溶剂中,将式ⅱ表述的二苯基硅氧烷与三氟化硼络合物反应,使得高沸点杂质二苯基硅氧烷分解成低沸点杂质(与式ⅱ化合物沸点相比),继而通过蒸馏的方式将分解形成的低沸点杂质与式ⅰ化合物分离,完成式ⅰ化合物的提纯。
[0013]
该提纯方法收率高,反应效率高,成本低,且操作安全,符合现在的清洁化生产理念,具有良好的工业应用价值。
[0014]
本方案中,基于二硅醚的硅氧键断裂后一分为二,即与再通过与-f、与-bf2分别形成新的低分子量化合物,以使得高沸点杂质二苯基硅氧烷分解成低沸点杂质。
[0015]
进一步,所述三氟化硼络合物为三氟化硼甲醇络合物、三氟化硼乙醚络合物、三氟化硼四氢呋喃络合物、三氟化硼乙腈络合物中的任意一种或多种。
[0016]
三氟化硼络合物用以提供与二苯基硅氧烷(式ⅱ化合物)反应的bf3。
[0017]
进一步,为了使二苯基硅氧烷(式ⅱ化合物)充分进行分解反应,所述式ⅱ化合物与三氟化硼络合物的摩尔比为1:(1~3)。
[0018]
进一步,式ⅰ化合物粗品与有机溶剂的质量比为1:(1~8),限制硅氧烷与三氟化硼络合物以及有机溶剂等的量比关系,可以提高分解反应程度,目标产物纯度提升。
[0019]
进一步,所述粗品中式ⅰ化合物的含量占比大于等于80%,式ⅱ化合物的含量占比小于20%,以质量计;连同原料残留或其他不可避免的杂质全部成分占比100%。
[0020]
进一步,所述式ⅰ化合物为二苯基四甲基二硅烷。
[0021]
进一步,所述式ⅱ化合物为1,1,3,3-四甲基-1,3-二苯基二硅氧烷。
[0022]
进一步,所述有机溶剂为甲苯、二甲苯中的任意一种,惰性溶剂,更好地去除,同时不对反应进程造成影响。
[0023]
进一步,所述蒸馏压力为-0.1~-0.08mpa,蒸馏温度为80~160℃。式ⅱ化合物与三氟化硼络合物反应后,生成低沸点杂质,进而通过蒸馏的方式将低沸点杂质与高沸点的式ⅰ化合物分离。
附图说明
[0024]
图1是实施例1中二苯基四甲基二硅烷的核磁共振氢谱图;
[0025]
图2是实施例1中二苯基四甲基二硅烷提纯前的气相色谱图及检测表征数据;
[0026]
图3是实施例1中二苯基四甲基二硅烷提纯后的气相色谱图及检测表征数据;
[0027]
图4是实施例2中二苯基四甲基二硅烷提纯前的气相色谱图及检测表征数据;
[0028]
图5是实施例2中二苯基四甲基二硅烷提纯后的气相色谱图及检测表征数据;
[0029]
图6是实施例3中双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷提纯前的气相色谱图及检测表征数据;
[0030]
图7是实施例3中双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷提纯后的气相色谱图及检测表征数据。
[0031]
其中,图2-7的各气相色谱图中,横坐标为min,纵坐标为/pa。
具体实施方式
[0032]
下面结合附图和具体实施例对本发明作进一步说明。
[0033]
如上述文献记载,在氯硅烷制备二硅烷时,极易产生杂质二硅氧烷且二硅氧烷与二硅烷的沸点接近,其中二苯基四甲基二硅烷与1,1,3,3-四甲基-1,3-二苯基二硅氧烷的沸点相差仅20℃,因此,仅仅通过蒸馏等物理方式分离提纯二硅烷的难度较高。
[0034]
鉴于此,本发明将含二苯基二硅氧烷的二苯基四甲基二硅烷粗品与有机溶剂、三氟化硼络合物混合,通过二苯基二硅氧烷与三氟化硼络合物发生分解反应,由高沸点杂质分解为低沸点杂质,该低沸点杂质与目标产物二苯基四甲基二硅烷的沸点相差大,通过蒸馏即可分离排出。
[0035]
对于有机溶剂,选用不参与该分解反应的溶剂类型,如惰性有机溶剂,例如苯基有机溶剂,优选甲苯或二甲苯,方便分离重复使用。
[0036]
以下以具体实施例进行展示。
[0037]
实施例1
[0038]
将100g杂质化合物ⅱa含量为11.2%的二苯基四甲基二硅烷(化合物ⅰa)粗品、8.5g三氟化硼乙醚络合物和800ml甲苯混合并搅拌升温,在70℃下保温反应4h,反应结束后,-0.1mpa下升温至80℃通过蒸馏将低沸点杂质与二苯基四甲基二硅烷分离,即得二苯基四甲基二硅烷精品83.6g。
[0039]
二苯基四甲基二硅烷提纯前的气相色谱图如图2所示,其提纯前的纯度为83.5%,杂质化合物ⅱa的含量为11.2%。二苯基四甲基二硅烷提纯后的气相色谱图如图3所示,其提纯后的纯度为99.9%。
[0040][0041]
本实施例的二苯基四甲基二硅烷的核磁共振氢谱图如图1所示,由图1可知:1h nmr(400mhz,cdcl3)δ7.40
–
7.34(m,1h),7.33
–
7.26(m,1h),0.34
–
0.30(m,3h)。
[0042]
实施例2
[0043]
将1kg杂质化合物ⅱa含量为9.4%的二苯基四甲基二硅烷(化合物ⅰa)粗品液、120g三氟化硼乙醚络合物和2l甲苯混合并搅拌升温,在80℃下保温反应8h,反应结束后,-0.1mpa下升温至85℃通过蒸馏将低沸点杂质与二苯基四甲基二硅烷分离,即得二苯基四甲
基二硅烷精品897.9g。
[0044]
二苯基四甲基二硅烷提纯前的气相色谱图如图4所示,其提纯前的纯度为89.7%,杂质化合物ⅱa的含量为9.4%。二苯基四甲基二硅烷提纯后的气相色谱图如图5所示,其提纯后的纯度为99.9%。
[0045]
实施例3
[0046]
将150g杂质化合物ⅱb含量为7.6%的双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷(化合物ⅰb)粗品液、14.0g三氟化硼乙醚络合物和600ml甲苯混合并搅拌升温,在80℃下保温反应5h,反应结束后,-0.09mpa下升温至120℃通过蒸馏将低沸点杂质与双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷分离,即得双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷精品138.1g。
[0047]
双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷提纯前的气相色谱图如图6所示,其中,其提纯前的纯度为92.0%,杂质化合物ⅱb的含量为7.6%。双(4-甲氧基苯基)-1,1,2,2-四甲基二硅烷提纯后的气相色谱图如图7所示,其提纯后的纯度为99.9%。
[0048][0049]
实施例4
[0050]
将200g杂质化合物ⅱc含量为11.7%的二(3-甲氧基苯基)-1,1,2,2-四甲基二硅烷(化合物ⅰc)粗品液、18.0g三氟化硼甲醚络合物和500ml甲苯混合并搅拌升温,在90℃下保温反应6h,反应结束后,-0.09mpa下升温至130℃通过蒸馏将低沸点杂质与二(3-甲氧基苯基)-1,1,2,2-四甲基二硅烷分离,即得精品174.3g,经检测,其纯度为99.5%;其中,二(3-甲氧基苯基)-1,1,2,2-四甲基二硅烷提纯前的纯度为86.7%。
[0051][0052]
实施例5
[0053]
将500g杂质化合物ⅱd含量为10.7%的双(4-甲基苯基)-1,1,2,2-四甲基二硅烷(化合物ⅰd)粗品液、50g三氟化硼乙醚络合物和900ml二甲苯混合并搅拌升温,在90℃下保温反应10h,反应结束后,-0.08mpa下升温至160℃通过蒸馏将低沸点杂质与双(4-甲基苯基)-1,1,2,2-四甲基二硅烷分离,即得双(4-甲基苯基)-1,1,2,2-四甲基二硅烷精品432.5g,经检测,其纯度为99.2%;其中,双(4-甲基苯基)-1,1,2,2-四甲基二硅烷提纯前的纯度为85.8%。
[0054][0055]
以上仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1