一种固液合成亮丙瑞林的方法与流程
1.本发明涉及医药合成技术领域,具体涉及一种固液合成亮丙瑞林的方法。
背景技术:
2.亮丙瑞林,英文名leuprorelin,化学名:5-氧代-脯氨酰-组氨酰-色氨酰-丝氨酰-酪氨酰-d-亮氨酰-亮氨酰-精氨酰-n-乙基-脯氨酰胺,cas号∶53714-56-0,肽序∶pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet,分子式∶c
61h88n16o14
,分子量:1209.41,为促性腺激素类药物,绒毛状固体,临床上常用于子宫内膜异位症;伴有月经过多、下腹痛、腰痛及贫血等的子宫肌瘤;绝经前乳腺癌,且雌激素受体阳性患者;前列腺癌;中枢性性早熟症。亮丙瑞林是1974年由日本武田化工的fujinomasahiko等人首先发现促黄体激素释放激素的九肽酰胺类似物,具有很好的活性,并且发明合成工艺。其先后在日本、德国、美国等国家申请专利,专利号分别为jp19740027442、de2446005、us4008209等。随后,又有一些研究机构和个人发表了一些合成工艺,专利号为ep1088555、ep1777232、us5480868、cn1865280等。
3.在现有技术中,申请号为cn200910104993.6提供本发明公开了一种固相法和液相法结合合成亮丙瑞林的新工艺,申请号为cn201610927544.1公开了一种亮丙瑞林的合成制备方法报道了一种采用氯树脂固相合成亮丙瑞林的工艺。申请号为cn201810363465.1的一种亮丙瑞林的固相合成方法,采用hmbalinker偶联amresin得到hmbalinkeramresin,再将合成的二肽应用到固相合成中,得到全保护的肽树脂:将肽树脂用乙胺溶液氨解得到末端乙胺化的全保护肽,经三氟乙酸脱保护得到粗肽;将粗肽经过高效液相色谱制备得到高质量的精肽。该方案提供的亮丙瑞林的固相合成方法,使用氨解得到末端酰氨基,使用了哌啶为脱帽试剂,价格价高,属于液体易制毒试剂,不易管理,容易变质。cn202011087409.3一种多肽固液片段合成亮丙瑞林的方法,以哌嗪作为脱帽试剂用ctc树脂合成片段,结合液相法合成亮丙瑞林,采用7+2的方法,合成7肽用全固相法合成,成本较大,随着肽链的延长,收率变低,因此为了克服收率变低和降低成本,本发明采用固液法相结合,用5+2+2片段缩合的合成路线。
技术实现要素:
4.因此,本发明要解决的技术问题在于克服现有技术中产品收率低、纯度不高的缺陷,从而提供一种固液合成亮丙瑞林的方法。
5.本发明提供的一种固液合成亮丙瑞林的方法,包括以下步骤:
6.s1、用固相法合成化合物1∶
7.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-oh;
8.s2、用液相法合成化合物2:d-leu-leu-ome;
9.s3、用液相法合成化合物3:h-arg(pbf)-pro-nhet;
10.s4、在液相中合成化合物4:
11.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome;
12.s5、在液相中合成化合物5:
13.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh;
14.s6、液相法合成化合物6:boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet
15.s7、合成亮丙瑞林粗品:pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet。
16.优选地,步骤s1中,化合物1通过多肽固相法从c到n末端的顺序合成,其步骤包括:
17.1)以ctc树脂为固相载体;
18.氨基酸单体为boc-pyr-oh,fmoc-his(boc)-oh,fmoc-trp(boc)-oh,fmoc-ser(tbu)-oh,fmoc-tyr(tbu)-oh;
19.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic或dcc中的任意一种;
20.脱帽试剂为5wt%哌嗪/dmf溶液;
21.从c到n末端依次合boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂;
22.2)用体积分数为1%的三氟乙酸/二氯甲烷溶液切割,浓缩后用水析出,得到化合物1:boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-oh。
23.优选地,步骤s2中,化合物2通过液相法合成:
24.以fmoc-d-leu-oh,h-leu-ome为氨基酸单体;
25.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic或dcc中的任意一种;
26.活化剂为hosu或hobt;
27.有机碱为diea或tea;
28.依次合成:
29.1)fmoc-d-leu-leu-ome;
30.2)d-leu-leu-ome。
31.优选地,步骤s3中,化合物3通过液相法合成:
32.以fmoc-arg(pbf)-oh,h-pro-nhet.hcl为氨基酸单体;
33.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic或dcc中的任意一种;
34.活化剂为hosu或hobt;
35.有机碱为diea或tea;
36.依次合成:
37.1)fmoc-arg(pbf)-pro-nhet.hcl;
38.2)h-arg(pbf)-pro-nhet。
39.优选地,步骤s4中,化合物4通过液相法合成:
40.以化合物1和化合物2为合成片段;
41.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic或dcc中的任意一种;
42.活化剂为hosu或hobt;
43.有机碱为diea或tea;
44.化合物1和化合物2的摩尔比为1∶1.1~1∶1.5,化合物2和缩合剂、活化剂及有机碱的摩尔比=1∶1∶1∶1。
45.优选地,步骤s5中,化合物5通过液相法合成:
46.取甲醇和化合物4反应,缓慢加入2m naoh,反应2-4h,过滤、洗涤、干燥得化合物5;
47.其中,naoh和化合物4的摩尔比为1.5∶1~20∶1;
48.优选地,步骤s6中,化合物6通过液相法合成:
49.以化合物5和化合物3为合成片段;
50.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic或dcc中的任意一种;
51.活化剂为hosu或hobt;
52.有机碱为diea或tea;
53.化合物5和化合物3的摩尔比为1∶1.1~1∶1.5,化合物3和缩合剂、活化剂及有机碱的摩尔比=1∶1∶1∶1。
54.进一步地,步骤s7中,由化合物6获得粗品的步骤如下:
55.1)取烧瓶,称化合物6投入,加入切肽试剂(tfa∶tis∶h2o=95∶2.5∶2.5)切割,得到含有亮丙瑞林粗品的tfa溶液;
56.2)浓缩tfa溶液至少量,加入乙醚;
57.3)离心,真空干燥得亮丙瑞林三氟乙酸盐粗品。
58.优选地,使用后的树脂回收步骤如下:
59.1)将树脂用dmf洗涤;
60.2)甲醇洗涤,抽去滤液,真空干燥;
61.3)另配置二氯亚砜的dcm溶液,加入装有树脂的固相合成反应器中,反应2h后,抽去反应液,dcm洗涤,甲醇洗涤干燥备用。
62.本发明技术方案,具有如下优点:
63.一种固液合成亮丙瑞林的方法,制得的亮丙瑞林粗品纯度达到90%以上,多肽固相合成法和液相合成法结合的方法,利用固相合成法合成较难的化合物1,采用固相合成法,使得操作简单,可以实现自动化生产,树脂可以回收利用,降低成本。液相法合成较简单的化合物2和化合物3,降低了成本,化合物2(d-leu-leu)纯度高,和化合物1反应后的七肽片段纯度更好,提高了后续合成中间品的纯度,从而提高了产品粗品的纯度。
附图说明
64.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还根据这些附图获得其他的附图。
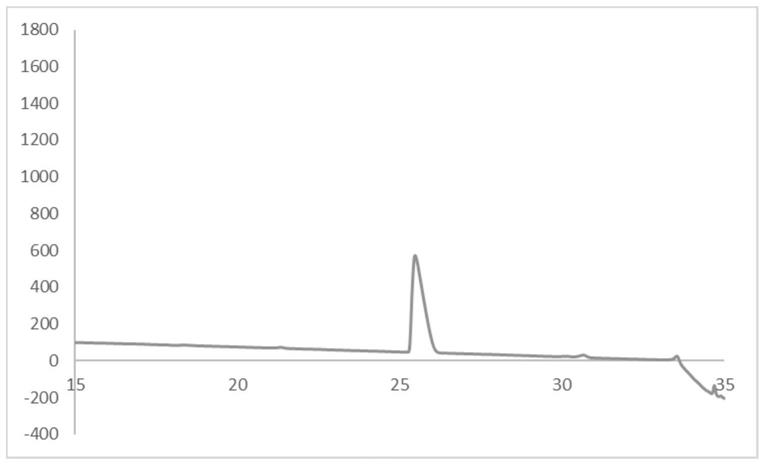
65.图1是本发明实施例1中化合物2的hplc色谱图;
66.图2是本发明实施例1中化合物4的hplc色谱图;
67.图3是本发明实施例1中地洛瑞林粗品的hplc色谱图。
具体实施方式
68.实施例1
69.一种固液合成亮丙瑞林的方法,包括以下步骤:
70.s1、用多肽固相法合成化合物1:
71.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-oh;
72.s2、用多肽液相法合成化合物2:d-leu-leu-ome;
73.s3、用多肽液相法合成化合物3:h-arg(pbf)-pro-nhet;
74.s4、在液相中合成化合物4:
75.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome;
76.s5、在液相中合成化合物5:
77.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh;
78.s6、液相法合成化合物6:
79.boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet
80.s7、合成亮丙瑞林粗品:pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet。
81.步骤s1中,化合物1通过固相法从c到n末端的顺序合成,其步骤包括:
82.1)以ctc树脂为固相载体;
83.boc-pyr-oh、fmoc-his(boc)-oh、fmoc-trp(boc)-oh、fmoc-ser(tbu)-oh、fmoc-tyr(tbu)-oh为氨基酸单体;
84.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
85.脱帽试剂为5wt%哌嗪/dmf溶液;
86.从c到n末端依次合成:boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂;
87.具体包括如下步骤:
88.1a)tyr(tbu)-ctc树脂的合成:称取25gctc树脂(取代度1mmol/g)于250ml固相合成反应其中,取fmoc-tyr(tbu)-oh(30mmol)于250ml三角瓶中,100ml量筒量取dcm 100ml,摇匀,加diea150ml,摇匀溶解,倒入反应器开始反应,30min后,补加diea50mmol,甲醇50ml,再反应20min,用抽滤装置抽去反应液,用dmf洗4次;量取200ml5wt%哌嗪/dmf溶液,倒入反应器中,反应20分钟,抽去反应液,dmf洗涤4次;取树脂于玻璃管中,加入异丙醇,vortex5秒,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤3次,茚三酮检验呈阳性得tyr(tbu)-ctc树脂。
89.1b)ser(tbu)-tyr(tbu)-ctc树脂的合成:得到tyr(tbu)-ctc树脂后,向反应体系中加入fmoc-ser(tbu)-oh(50mmol)、缩合剂hbtu(50mmol)和有机碱tea(50mmol),溶剂为dmf,反应时间为2h,反应完成后,用dmf洗涤4次;取200ml5wt%哌嗪/dmf溶液,导入反应器中,反应20分钟,抽去反应液,dmf洗涤4次;取树脂于玻璃管中,加入异丙醇,vortex5秒,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤3次,茚三酮检验呈阳性得ser(tbu)-tyr(tbu)-树脂。
90.1c)trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂的合成:得到ser(tbu)-tyr(tbu)-ctc树脂,取fmoc-trp(boc)-oh(50mmol)于250ml三角瓶中,缩合剂hbtu(50mmol)和有机碱tea(50mmol),溶剂为dmf,反应时间为2h,反应完全后,用抽滤装置抽去反应液,用dmf洗4次;量取200ml5wt%哌嗪/dmf溶液,导入反应器中,反应20分钟,抽去反应液,dmf洗涤4次;取树脂于玻璃管中,加入异丙醇,vortex5秒,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤3次,茚三酮检验呈阳性得trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂。
91.1d)his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂的合成:得到trp(boc)-ser
(tbu)-tyr(tbu)-ctc树脂后,向反应体系中加入fmoc-his(boc)-oh(50mmol)、缩合剂hbtu(50mmol)和有机碱tea(50mmol),溶剂为dmf,反应时间为2h,反应完成后,用dmf洗涤4次;取200ml5wt%哌嗪/dmf溶液,入倒反应器中,反应20分钟,抽去反应液,dmf洗涤4次;取树脂于玻璃管中,加入异丙醇,vortex5秒,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤3次,茚三酮检验呈阳性得his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂。
92.1e)boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂的合成:
93.在his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂的基础上,向反应体系中加入boc-pyr-oh(50mmol)、缩合剂hbtu(50mmol)和有机碱tea(50mmol),溶剂为dmf,反应时间为2h,反应完成后,用dmf洗涤4次;取200ml5wt%哌嗪/dmf溶液,倒入反应器中,反应20分钟,抽去反应液,dmf洗涤4次;取树脂于玻璃管中,加入异丙醇,vortex5秒,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤3次,茚三酮检验呈阳性得boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-ctc树脂。
94.2)用1wt%三氟乙酸/二氯甲烷溶液切割,浓缩后用水析出,得到化合物1:boc-pyr-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-oh。
95.步骤s2中,化合物2通过液相法合成:
96.以fmoc-d-trp(boc)-oh,h-leu-ome为氨基酸单体;
97.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
98.活化剂为hosu或hobt;
99.有机碱主要为diea或tea;
100.依次合成:
101.1)fmoc-d-leu-leu-ome;
102.2)d-leu-leu-ome。
103.具体包括以下步骤:
104.以fmoc-d-leu-oh(50mmol),h-leu-ome(55mmol)为氨基酸单体,按照摩尔比为1:1.1投料,用dmf完全溶解后;加入缩合剂(dcc)、活化剂(hobt)和有机碱(tea);h-leu-ome与缩合剂、活化剂、有机碱的摩尔比为1:1:1:1,反应完全后,过滤反应液,用0.5m盐酸水溶液析出,过滤得固体,然后用纯化水洗至中性,真空干燥后,溶于200ml二乙胺,浓缩,加入石油醚析出,过滤,收集固体,真空干燥,得到化合物2。
105.化合物2的hplc检测条件为:
106.流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
107.检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
108.梯度:0-30min,10%b-50%b。
109.其结果参照图1,收率:80%,纯度:97.6%。
110.优选地,步骤s3中,化合物3通过液相法合成:
111.以fmoc-arg(pbf)-oh,h-pro-nhet.hcl为氨基酸单体;
112.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
113.活化剂为hosu或hobt;
114.有机碱主要为diea或tea;
115.依次合成:
116.1)fmoc-arg(pbf)-pro-nhet.hcl;
117.2)h-arg(pbf)-pro-nhet。
118.以fmoc-arg(pbf)-oh(50mmol),h-pro-nhet.hcl(55mmol)为氨基酸单体,按照摩尔比为1:1.1投料,用dmf完全溶解后;加入缩合剂(dcc 55mol)、活化剂(hobt55mmol)和有机碱(tea 55mmol);fmoc-arg(pbf)-oh与缩合剂、活化剂、有机碱的摩尔比为1:1.1:1.1:1.1,反应完全后,过滤反应液,用0.5m盐酸水溶液析出,过滤的固体,然后用纯化水洗至中性,真空干燥,得fmoc-arg(pbf)-pro-nhet.hcl,加入二乙胺180ml,浓缩至少量,,加入石油醚析出固体,过滤,真空干燥,得化合物3。
119.步骤s4中,化合物4通过液相法合成:
120.以化合物1和化合物2为合成片段;
121.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
122.活化剂为hosu或hobt;
123.有机碱主要为diea或tea;
124.化合物1和化合物2的摩尔比为1∶1.1,化合物2和缩合剂、活化剂及有机碱的摩尔比=1∶1∶1∶1。
125.具体包括:
126.称取化合物1(10mmol)和化合物2(12mmol)于100ml圆底烧瓶中,用40mldmf溶解,冷浴10min,加入dcc(12mmol),开始反应,1.5h后,hplc检测化合物1反应完全。过滤,固体用dmf洗涤3次,滤液加入冷的0.5m盐酸溶液,析出产物固体,固体过滤,纯划水洗涤至中性,收集固体,干燥,即得。
127.化合物4的hplc检测条件为:
128.流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
129.检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
130.梯度:0-30min,50%b-90%b。
131.其结果参照图2,收率:90.1%,纯度:90.3%。
132.步骤s5中,化合物5通过液相法合成:
133.取甲醇60ml溶解化合物4,冰浴下,缓慢加入2m naoh 10ml,反应6h,加入0.5m盐酸溶液200ml,过滤、纯化水洗涤至中性、干燥得化合物5;
134.步骤s6中,化合物6通过液相法合成:
135.以化合物5和化合物3为合成片段;
136.缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
137.活化剂为hosu或hobt;
138.有机碱主要为diea或tea;
139.化合物5和化合物3的摩尔比为1∶1.1,化合物3和缩合剂、活化剂及有机碱的摩尔比=1∶1∶1∶1。
140.称取化合物5(6mmol)和化合物3(7.2mmol)于100ml圆底烧瓶中,用30ml dmf溶解,冷浴10min,加入bop(7.2mmol),开始反应,1h后,hplc检测化合物1反应完全。过滤,固体用dmf洗涤3次,滤液加入冷的0.5m盐酸溶液,析出产物固体,固体过滤,纯划水洗涤至中性,收集固体,干燥即得。
141.步骤s7中,由化合物6获得粗品的步骤如下:
142.1)取烧瓶,称化合物6投入,加入20ml切肽试剂(tfa:tis:h2o=95:2.5:2.5)切割,得到含有亮丙瑞林粗品的tfa溶液;
143.2)浓缩tfa溶液至少量,加入乙醚;
144.3)离心,真空干燥得亮丙瑞林三氟乙酸盐粗品。
145.亮丙瑞林粗品的hplc检测条件为:
146.流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
147.检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
148.梯度:0-30min,50%b-90%b。
149.其结果参照图3,收率85.2%,纯度93.3%。
150.实施例2
151.与实施例1的区别在于,步骤s4中化合物1和化合物2的摩尔比为1:1.5;步骤s6中化合物5和化合物3的摩尔比为1∶1.5。其余同实施例1。
152.所得亮丙瑞林粗品收率为83.3,纯度90.1%。
153.实施例3
154.与实施例1的区别在于,采用步骤s1中使用后的树脂回收后合成化合物1。回收步骤如下:
155.1)将树脂用dmf洗涤;
156.2)甲醇洗涤,抽去滤液,真空干燥;
157.3)另配置二氯亚砜的dcm溶液,加入装有树脂的固相合成反应器中,反应2h后,抽去反应液,dcm洗涤,甲醇洗涤干燥备用。其余同实施例1。
158.所得亮丙瑞林三氟乙酸盐粗品收率为82.9%,纯度90%。
159.对比例1
160.与实施例1的区别在于,步骤s1中脱保护试剂为4wt%哌嗪/dmf溶液,其余同实施例1。所得粗品收率为74.4%,纯度77.5%。
161.对比例2
162.与实施例1的区别在于,步骤s1中脱保护试剂为5wt%哌啶/dmf溶液,其余同实施例1。所得粗品收率为75.5%,纯度76.4%。
163.显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1