HSD17B13基因多态性在中重度MAFLD诊断中的应用
hsd17b13基因多态性在中重度mafld诊断中的应用
技术领域
1.本发明属于生物医药领域,涉及hsd17b13基因多态性在中重度mafld诊断中的应用,具体的涉及snp为rs72613567。
背景技术:
2.非酒精性脂肪性肝病(nonalcoholic fatty liver disease,nafld)是一组高度异质性疾病,与多种机体代谢功能障碍密切相关,在2020年3月,国际专家共识建议将nafld改为代谢相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease,mafld)(薛苗,范建高.代谢相关脂肪性肝病新定义的国际专家共识简介[j].临床肝胆病杂志,2020,36(06):1224-1227.)。nafld/mafld的全球患病率估计为24-30%。超重/肥胖及代谢综合症(metabolic syndrome,mets)这些与nafld/mafld密切相关疾病的流行,使得其患病率更高,预计在接下来的10年,其严重状态的非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,nash)的发病率将激增至56%(huang daniel q,el-serag hashem b,loomba rohit,global epidemiology of nafld-related hcc:trends,predictions,risk factors and prevention[j].nat rev gastroenterol hepatol,2020,undefined:undefined.)。随着nafld/mafld及nash的患病率的迅速增长,该病及其所致的终末期肝脏病所带来的公共卫生负担也在飞速增加,然而目前临床上尚无针对nafld/mafld安全有效的治疗方案,由此可见,提高早期诊断率尤为重要。目前肝活检仍是nafld/mafld患者诊断、分级和分期的金标准,然而肝脏活检也有自身的局限性,比如采样误差风险、观察者间和观察者内差异率高、并发症风险高等。故而,努力寻找安全、有效、可推广的非侵入性诊断的方法显得尤为重要。
[0003]
hsd17b13主要表达于肝细胞脂滴(lipiddroplet,ld)表面,是一种新型的小鼠和人类肝脏特异性ld表面相关蛋白(suw,maoz,liuy,et al.role of hsd17b13 in the liver physiology and pathophysiology[j].mol cell endocrinol,2019,489:119-125.)hsd17b13最初被命名为短链脱氢酶/还原酶9,于2007年首次在人类肝脏cdna文库中克隆发现。现hsd17b13被列入17-hsd家族,该家族在类固醇代谢中发挥重要作用,hsd17b13同17-hsd家族其他成员一样,具有nad(p)+/nad(p)h结合位点(tgxxgxg)和一个在n-端的酶促活性位点(yxxxk)。hsd17b13亚细胞定位于肝细胞ld表面,蛋白质组学研究显示hsd17b13在肝细胞中大量表达,组织分布研究显示hsd17b13在肾脏肺脑骨骼肌卵巢和睾丸中仅有非常低的表达水平,表明其在肝脏中发挥重要作用(suw,wangy,jiax,et al.comparative proteomic study reveals17-hsd13 as apathogenic protein in nonalcoholic fattyliver disease[j].procnatl acadsci usa,2014,111(31):11437-11442.)。
[0004]
hsd17b13作为一种新型肝脏特异性ld表面蛋白,在脂肪性肝病进展中具有重要意义。目前关于hsd17b13在肝脏疾病的作用机制仍需进一步探究。本技术拟通过检测受试者的基因型,筛选与mafld相关的基因型,从而为不同亚型的mafld的诊断提供分子基础。
技术实现要素:
[0005]
为了弥补现有技术的不足,本发明的目的在于提供一种用于判断中重度mafld的snp标志物,通过检测snp基因型来判断中重度mafld患者的预后。
[0006]
为了实现上述目的,本发明采用了如下技术方案:
[0007]
本发明提供了检测样本中snp标志物的试剂在制备判断中重度mafld的产品中的应用,所述snp为rs72613567。
[0008]
进一步,当rs72613567发生插入缺失突变时,患者存在患中重度mafld的风险或患中重度mafld。
[0009]
进一步,相比非mafld和轻度mafld受试者,中重度mafld受试者中rs72613567发生插入缺失突变的频率增加。
[0010]
进一步,相比非肥胖型轻度mafld受试者,非肥胖型中重度mafld受试者中rs72613567发生插入缺失突变的频率增加。
[0011]
进一步,检测样本中snp标志物的试剂包括通过直接测序、单碱基延伸、等位基因特异性探针杂交、等位基因特异性引物延伸、等位基因特异性扩增(allele-specific pcr,as-pcr))、等位基因特异性核苷酸掺入、5'核酸酶消化、分子信标测定、寡核苷酸连接测定、大小分析和单链构象多态性(sscp)方法检测rs72613567基因型的试剂。
[0012]
进一步,所述样本选自血液、组织。
[0013]
进一步,所述样本为血液。
[0014]
本发明提供了用于判断中重度mafld的产品,所述产品包括检测受试者样本中snp位点rs72613567基因型的试剂。
[0015]
进一步,所述试剂包括引物或探针。
[0016]
进一步,所述探针包括与rs72613567突变进行特异性杂交的突变型探针。
[0017]
进一步,所述探针还包括与hsd17b13中rs72613567突变以外区域杂交的通用型探针。
[0018]
进一步,所述产品还包括处理样本的试剂。
[0019]
进一步,所述产品还包括检测mafld的常规指标的试剂。
[0020]
进一步,所述产品包括试剂盒、芯片。
[0021]
本发明提供了rs72613567在构建预测中重度mafld的计算模型中的应用。
[0022]
本发明的优点和有益效果:
[0023]
本发明首次发现了snp位点rs72613567的基因型与中重度mafld相关,通过检测rs72613567的基因型,可以判断受试者是否患有中重度mafld或存在患中重度mafld的风险。
具体实施方式
[0024]
术语“样本”或“样品”是指含有或假定含有靶核酸的任何组合物。这包括从个体分离的组织或流体的样品,例如,皮肤、血浆、血清、脊髓液、淋巴液、滑液、尿液、泪液、血细胞、器官,并且也表示从取自个体的细胞建立的体外培养物的样品,包括福尔马林固定的石蜡包埋的组织(ffpet)和从其分离的核酸。样品还可以包括无细胞材料,诸如含有无细胞dna(cfdna)级分。样品还可以指处理的组织或生物流体,例如,纯化或部分纯化的核酸。
[0025]
术语“核酸”、“多核苷酸”和“寡核苷酸”可以互换使用以指单一核苷酸的多聚体或聚合物。“寡核苷酸”是有时用于描述较短多核苷酸的术语。寡核苷酸可以包含至少6个核苷酸,例如至少约10-12个核苷酸,或至少约15-30个核苷酸,例如,对应于指定的核苷酸序列的区域。术语“核苷酸”通常是指单体或单碱基。
[0026]
术语“引物”是指这样的寡核苷酸:其与靶核酸中的序列杂交,且能够充当沿着核酸的互补链合成(在适合于这样的合成的条件下)的起始点。当在适当条件下暴露于核酸聚合酶时,正向引物和反向引物设定扩增子的边界并产生扩增产物。如本文所用,术语“探针”是指与靶核酸中的序列杂交且经常可检测地标记的寡核苷酸。探针可以具有修饰(诸如3
’‑
端修饰,其使探针不可被核酸聚合酶延伸)和一种或多种非天然存在的标记物(例如,荧光团、生色团,其任选地与猝灭剂组合)。具有相同序列的寡核苷酸可以在一种测定中充当引物且在不同的测定中充当探针。
[0027]
如本文所用,术语“靶序列”、“靶核酸”或“靶标”是指待检测或分析的样品中的核酸序列的部分。术语靶标包括靶序列的所有变体,例如,一种或多种突变型变体和野生型变体。
[0028]
术语“测序”是指确定靶核酸中核苷酸序列的任何方法。
[0029]
术语“snp”(单核苷酸多态性)是指dna中的单个碱基位置,在该单个碱基位置上存在一个群体的不同的等位基因或替代的核苷酸。该snp位置通常前接和后接所述等位基因的高度保守序列(例如,在种群中小于1/100或1/1000的成员中不同的序列)。对于在每个snp位置的等位基因,个体可以是纯合的或杂合的。本发明的snp位点以“rs
‑”
方式命名,本领域技术人员能够根据上文的rs-命名,从适合的数据库和相关的信息系统如单核苷酸多态性数据库(dbsnp)中确定其确切的位置、核苷酸序列。
[0030]
术语“基因型”指存在于个体或样品中的等位基因的同一性。典型地,其指与感兴趣的特定基因相关的个体的基因型;在多倍体个体中,其指个体携带有基因等位基因的何种组合。
[0031]
术语“患者”和“受试者”是指可以或不可以被诊断患有疾病或针对疾病治疗、但是是医学护理的受试者的个体。
[0032]
本发明提供了hsd17b13中变体rs72613567在中重度mafld中发生插入缺失突变的频率发生变化,提供了该突变可以赋予中重度mafld诊断的证据。
[0033]
在一些实施方案中,通过直接测序、单碱基延伸、等位基因特异性探针杂交、等位基因特异性引物延伸、等位基因特异性扩增(allele-specific pcr,as-pcr))、等位基因特异性核苷酸掺入、5'核酸酶消化、分子信标测定、寡核苷酸连接测定、大小分析或单链构象多态性(sscp)方法来检测样本中的snp。
[0034]
sscp是指单链dna由于碱基序列不同可引起空间构象差异,这种差异会导致相同或相近长度单链dna电泳迁移率的不同,从而可以通过非变性聚丙烯酰胺凝胶电泳进行有效地检测。pcr-sscp是将sscp用于pcr扩增产物的基因突变检测的方法,pcr扩增的dna片段在变性剂条件下,通过高温处理使双链dna扩增片段解旋并且维持单链状态,进一步进行非变性聚丙烯酰胺凝胶电泳。目前,pcr-sscp技术被广泛应用于分子生物学的各个领域。
[0035]
as-pcr的原理是由于taq dna聚合酶对位于引物3'末端的单个碱基的错配无法修复,当引物3'末端的碱基与snp位点的等位基因互补配对时,才能发生扩增反应;当引物3'
末端的碱基与snp位点的等位基因不互补配对时,则扩增反应不能发生。目前,已出现了基于as-pcr改良的一些方法,如四引物扩增受阻突变体系pcr(tetra-primer amplification refractory mutation system pcr,tetra-primer arms-pcr)、片段长度差异等位基因特异pcr(fragment length discrepant allele specific pcr,fldas-pcr)、多等位基因特异扩增(pcr amplification of multiple specific alleles,pmasa)等。
[0036]
直接测序检测snp是最直接可靠的方法,检出率高达100%,代表测序技术有焦磷酸测序(pyrosequencing)、taqman技术、微测序(snapshot)等。该方法通过比对不同样本中的同一基因或是基因片段的pcr扩增产物的测序结果,或是重测序分析已定位的序列标签位点(sts)及表达序列标签(est)来检测snp。可以将pcr产物纯化回收后通过连接到载体上进行测序,也可以对pcr产物直接进行测序。通过序列的比对,就能够准确地检测snp的突变类型和位置。
[0037]
本领域技术人员可选择任一种或几种方法(不限于上述的方法)来检测snp位点,只要可以实现snp位点的检测。
[0038]
用于从生物样品分离核酸的方法是已知的,例如,如sambrook等人,molecular cloning,alaboratory manual,cold springs harbor press(cold springs harbor,n.y.1989)中所述,并且几种试剂盒是可商购的(例如,来自roche的高纯rna分离试剂盒、高纯病毒核酸试剂盒和magnapure lc总核酸分离试剂盒)。在一些实施方案中,制备dna并将其用作本发明公开的扩增和检测方法的模板。在一些实施方案中,制备rna。当rna用作通过pcr扩增的模板时,需要逆转录步骤来制备cdna。然后可以使用dna聚合酶诸如taq、taq衍生物或其它热稳定聚合酶来实施扩增。
[0039]
在一些实施方案中,通过用突变特异性寡核苷酸引物(例如,等位基因特异性引物)的等位基因特异性pcr检测hsd17b13基因中的rs72613567位点的突变的方法。等位基因特异性引物通常具有与靶序列(例如,突变型序列)匹配且与替代序列(例如野生型序列)错配的3'-末端。任选地,等位基因特异性引物可以含有与野生型和突变型靶序列的内部错配。
[0040]
在一些实施方案中,所述方法进一步包括使用等位基因特异性pcr来以任何组合检测患者样品中的一种或多种hsd17b13突变。可以使用突变位点的任一侧上的扩增引物或用与涵盖特定融合产物的融合点的序列互补的一个引物来检测融合产物。在一些实施方案中,使用与涵盖突变位点的序列互补(杂交)的标记探针检测基因突变。在一些实施方案中,标记的探针与hsd17b13的序列互补,并且基于与该探针杂交的扩增产物的尺寸或存在来检测突变。
[0041]
在一些实施方案中,进一步提供了用于用特异性探针检测hsd17b13基因中的rs72613567位点突变的方法。该探针可用于许多核酸检测技术,例如southern或northern杂交、实时pcr或ngs。一种典型的突变特异性的检测探针在实施检测的反应条件下与靶序列(例如,突变型序列)形成稳定的杂交物,并且不与替代序列(例如,在相同位点的野生型序列)形成稳定的杂交物。对于成功的探针杂交,所述探针需要与靶序列具有至少部分互补性。通常,靠近探针的中心部分的互补性比在探针末端处的互补性更关键。在一些实施方案中,所述探针具有特定结构,包括蛋白-核酸(pna)、锁定核酸(lna)、分子信标探针或可以包括于自探测引物中(whitcombe等人,(1999)nat.biotechnol.8:804-807)。
可以用放射性标记物、荧光标记物或生色团标记物(任选地与猝灭部分(例如bhq)组合)来标记探针。例如,可以通过实时等位基因特异性的聚合酶链式反应来检测突变,其中探针与扩增产物的杂交导致探针的酶促消化和消化产物的检测。通过检测由核酸双链体形成引起的荧光变化或通过检测探针和靶标之间的杂交物的特征性解链温度,也可以检测探针和靶标之间的杂交。在一些实施方案中,所述方法进一步包括使用杂交探针来以任何组合检测患者样品中的一种或多种基因突变。
[0042]
本发明提供了用于判断中重度mafld的产品,所述产品包括检测样本中snp位点rs72613567基因型的试剂。
[0043]
在一些实施方案中,所述产品可以是试剂盒、芯片或试纸。
[0044]
在一些实施方案中,本发明中的芯片包括:固相载体;以及有序固定在所述固相载体上的寡核苷酸探针,所述的寡核苷酸探针特异性地对应于rs72613567所在的序列。
[0045]
所述固相载体可采用基因芯片领域的各种常用材料,例如包括但不限于塑料制品、微颗粒、膜载体等。所述塑料制品可通过非共价或物理吸附机制与抗体或蛋白抗原相结合,最常用的塑料制品为聚苯乙烯制成的小试管、小珠和微量反应板;所述微颗粒是由高分子单体聚合成的微球或颗粒,其直径多为微米,由于带有能与蛋白质结合的功能团,易与抗体(抗原)形成化学偶联,结合容量大;所述膜载体包括硝酸纤维素膜、玻璃纤维素膜及尼龙膜等微孔滤膜。
[0046]
在一些实施方案中,所述产品为试剂盒。所述试剂盒含有检测hsd17b13基因中的rs72613567位点突变的一种或两种所必需的试剂。在一些实施方案中,所述试剂盒包含寡核苷酸,诸如对突变型序列特异性(即,能够区分野生型序列与突变型序列)的探针和扩增引物,或用于捕获rs72613567位点突变位于其中的hsd17b13基因的部分的捕获探针。在一些实施方案中,所述试剂盒含有检测dna或相应mrna序列中的rs72613567位点突变所必需的试剂。例如,所述试剂盒进一步包含进行扩增和检测测定所必需的试剂,诸如pcr、实时pcr、定量pcr、逆转录(例如,用于rt-pcr)和/或转录介导的扩增(tma)的组分。在一些实施方案中,可检测地标记所述突变特异性寡核苷酸。在一些实施方案中,所述试剂盒包含用于标记和检测标记物的试剂。例如,如果所述寡核苷酸用生物素标记,则所述试剂盒可以包含具有酶及其生色底物的链霉抗生物素蛋白试剂。在一些实施方案中,所述试剂盒进一步包括用于检测中重度mafld基因中的至少一种或多种突变的试剂。
[0047]
在一些实施方案中,所述试剂盒包含用于检测mrna中的rs72613567位点突变的试剂。该实施方案与用于检测dna中的突变的试剂盒共享元件,并且进一步包含用于基于rna的检测的试剂,包括以下中的一种或多种:具有逆转录酶活性的dna聚合酶,或逆转录酶,具有rna酶h活性的酶,和寡-dt捕获试剂。
[0048]
在一些实施方案中,所述试剂盒包含用于检测hsd17b13蛋白中rs72613567位点突变的试剂。所述试剂盒可以包含对突变型hsd17b13蛋白、但不对野生型hsd17b13蛋白特异性的抗体。在一些实施方案中,所述试剂盒含有用于检测来自患者的血液(例如,血浆或血清)样品中的突变型蛋白的试剂。在一些实施方案中,所述试剂盒包括用于检测来自患者的组织样品中的突变体的试剂。
[0049]
在一些实施方案中,所述试剂盒进一步包括热稳定dna聚合酶、逆转录酶、具有两种活性的酶和/或酶的活性所必需的任何辅因子。在一些实施方案中,所述试剂盒进一步提
供了可用于核酸扩增中的额外试剂,例如,dntp和/或缓冲试剂。在一些实施方案中,所述试剂盒进一步包括一次性组件,诸如管、多孔板或毛细管芯片等。
[0050]
在一些实施方案中,所述试剂盒进一步包含引物和至少一种探针,其用于检测来自患者的样品中的内部对照,例如,持家基因。在一些实施方案中,所述试剂盒进一步包含至少一种阳性对照,例如,通过试剂盒组分可检测的每种hsd17b13突变的阳性对照。在一些实施方案中,所述试剂盒进一步包含阴性对照,例如,野生型hsd17b13人dna或rna。
[0051]
本发明提供了rs72613567在构建预测中重度mafld的计算模型中的应用。
[0052]
在一些实施方案中,所述计算模型以rs72613567的基因型作为输入变量。
[0053]
在一些实施方案中,所述计算模型还以其他与中重度mafld相关的标志物作为输入变量。
[0054]
下面结合具体的实施例进一步说明本发明,本发明的实施例仅用于解释本发明,并不意味着限制本发明的保护范围。
[0055]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0056]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0057]
实施例 研究与mafld相关的snp位点
[0058]
1、研究对象
[0059]
纳入于吉林大学第一医院按照标准诊断为mafld的患者376例。同时选取对照组无肝病患者82例。
[0060]
纳入标准:
[0061]
(1)年龄≥18周岁;(2)具有完整的临床资料:血压、身高、年龄、体重、血常规、肝功、血脂、空腹血糖、肾功、肝脏影像学检查或者肝脏活检、fibroscan等;(3)男性饮酒折合乙醇量小于30克/每天,女性小于20克/每天。
[0062]
排除标准:
[0063]
(1)甲肝、乙肝、丙肝或其他病毒性肝病患者;(2)药物性肝损伤或自身免疫性肝病患者;(3)存在肝细胞癌或肝细胞癌可能(甲胎蛋白》100ng/ml且影像学提示肝脏恶性占位可能;或甲胎蛋白持续3个月》100ng/ml;(4)合并其他系统恶性肿瘤及恶性血液系统疾病;(5)既往或计划行肝脏移植者;(6)临床资料不全者。
[0064]
肥胖定义:本研究分别将bmi《25kg/m2,25kg/m2《bmi《30kg/m2,bmi》30kg/m2的nafld人群定义为非肥胖型mafld、肥胖型mafld、严重肥胖型mafld。
[0065]
2、使用mri-pdff检测脂肪含量(lfc)
[0066]
每位参与者均接受mri-pdff检查。参与者接受腹部磁共振成像(mri)(ge discovery 750 3.0t mr)。使用mri-pdff,通过mri迭代分解水和脂肪,利用回波不对称性和最小二乘估计(理想iq)精确测量(ge discovery 750 3.0tmr)。在轴向ideal iq检查中覆盖整个肝脏。关键参数如下:采集矩阵=256
×
256,回波时间=3,重复时间=6ms,翻转角度=3,视野=480mm,厚度=9mm。单次屏气,采集时间=19秒。将284mm2的方形感兴趣区(roi)分别手动放置在右后段、右前段、左外侧段和左内段的单层上。避免了肝脏病灶、大血管、伪影和胆管。测量四个rols部分的脂肪分数,以代表肝脏的脂肪分数。在ideal iq扫描后自动执行在线后处理,并在图像列表中生成定量脂肪分数图。然后将图像传输到工作站(aw4.5,ge医疗系统)以测量肝脂肪。具有mri-pdff值的参与者lfc≥5.1%诊断为mafld,
5.2~14.0%为轻度mafld,≥14.1%建议中度和重度mafld。
[0067]
3、血液基因组dna的提取
[0068]
使用qiagen dneasy血液试剂盒从上述队列中个体的血液中提取基因组dna。使用quibt3评估dna的纯度和浓度。
[0069]
4、基因型检测
[0070]
检测表1所述基因的snp位点,检测方法如下:
[0071]
以dna为模板,荧光定量pcr检测目的基因,taqman探针法检测snp,加入10ng基因组dna检测每个反应。除pnpla3外,其他所有snp均处于hardy-weinberg平衡。
[0072]
表1检测位点
[0073]
genersw/vadipoqrs1501299g/tpnpla3rs738409c/grasgrp1rs7403531c/tuqcc1rs878639a/gmboat7rs641738c/tnos3rs2070744c/taplnrrs948847g/thsd17b13rs72613567-/afam13ars9991328c/t
[0074]
5、数据分析
[0075]
对所获取的9个snp分型按不同的分组分别进行卡方检验,探讨9个snp的分型不同mafld分组的关系,p《0.05意味该snp与疾病有联系。logistic回归分析用于计算snp分型对疾病的危险程度(or),or大于1提示是脂肪肝的危险因素,or<1提示是脂肪肝的保护因素,分析的过程中校正了年龄,性别,bmi。
[0076]
6、结果
[0077]
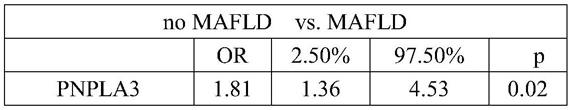
不同基因的基因型与不同分组mafld之间的相关性如表2-12所示,rs738409(pnpla3)、rs72613567(hsd17b13)、rs878639(uqcc1)与中重度mafld显著相关(表3)。rs641738(mboat7)与非肥胖型mafld显著相关(表4)。rs72613567(hsd17b13)与非肥胖型中重度mafld显著相关(表5)。
[0078]
在纳入的所有人群中,hsd17b13基因rs72613567位置发生插入变异的有120人,未发生变异的有340人,lfc呈现显著性差异(表6)。在未发生变异的所有人群中,no-mild mafld(非mafld和轻度mafld)占比74.12%,在发生插入变异的所有人群中,no-mild mafld占比为56.67%(表7)。在纳入的非肥胖型人群中,发生插入变异的有52人,未发生变异的有134人(表8)。在未发生变异的非肥胖型人群中,非肥胖型轻度mafld占比为70.90%;在发生插入变异的非肥胖型人群中,非肥胖型轻度mafld占比为51.90%(表9)。
[0079]
在非肥胖型人群中,mboat7基因rs641738位置发生基因型变异的有39人,未发生变异的有203人,lfc呈现显著性差异(表10)。在未发生变异的非肥胖型人群中,non-obese no mafld的占比为26.1%;在发生变异的非肥胖型人群中,non-obese no mafld的占比为7.7%(表11)。
[0080]
在纳入的所有人群中,uqcc1基因rs878639位置发生变异的有137人,未发生变异的有323人;在未发生变异的所有人群中,no-mild mafld占比66.56%,在发生插入变异的所有人群中,no-mild mafld占比为76.64%(表12)。
[0081]
表2 snp与mafld的相关性分析
[0082][0083][0084]
表3 snp与中重度mafld的相关性分析
[0085][0086]
表4 snp与非肥胖型mafld的相关性分析
[0087][0088]
表5 snp与非肥胖型中重度mafld的相关性分析
[0089][0090][0091]
表6所有人群中rs72613567(hsd17b13a)不同表型的lfc
[0092][0093]
表7 rs72613567(hsd17b13a)在中重度mafld中的表型
[0094][0095]
表8非肥胖型mafld人群中rs72613567(hsd17b13a)不同表型的lfc
[0096][0097]
表9 rs72613567(hsd17b13a)在非肥胖型中重度mafld中的表型
[0098][0099]
表10非肥胖型人群中rs641738(mboat7)不同表型的lfc
[0100][0101]
表11 rs641738(mboat7)在非肥胖型mafld中的表型
[0102][0103]
表12 rs878639(uqcc1)在中重度mafld中的表型
[0104][0105]
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1