骨骼肌3D成型装置的制作方法
骨骼肌3d成型装置
技术领域
1.本实用新型涉及生物领域,特别是涉及一种骨骼肌3d成型装置。
背景技术:
2.二维细胞培养是目前体外细胞研究的主要方法,但二维细胞体外培养模型与细胞在体内真实的生长环境以及生长方式存在很大差异,因此二维细胞培养较难反映体内细胞的真实情况。三维细胞培养是一种模拟体内细胞立体生长环境的体外细胞培养技术,可以有效模拟细胞外基质,为细胞的生长提供导向支持。
3.如公开号为cn109294910a的中国发明公开专利说明书提出了一种近场细胞3d打印装置及其打印方法,包括3d打印成型机构和臂式机器人3d 打印运动机构,所述的3d成型机构包括近场模块,挤出-喷射集成模块和光固化模块,所述近场模块设置有带孔导电圆片和正极,所述臂式机器人 3d打印运动机构与所述挤出-喷射集成模块连接,所述运动机构包括多轴臂式机器人,以及集成在多轴臂式机器人内部的震动阻尼装置。该装置在近场静电作用下,能够实现对墨水的精确控制和成型,实现10nm~100μm 墨水细度控制和高尺寸样品3d打印;打印时震动幅度小,打印误差小,精度可达10μm,可实现精确走位和高自由度3d打印。
4.但是,上述装置仅能针对近场细胞进行打印,然而当需要构建骨骼肌细胞时就变得不适用,而且无论是电场电极、电/磁变流体等均无法提供骨骼肌所需要的生长环境,因此有必要提出一种骨骼肌3d成型装置以解决上述问题。
技术实现要素:
5.实用新型目的:为了克服现有技术中存在的不足,本实用新型提供一种骨骼肌细胞3d成型装置。
6.技术方案:为实现上述目的,本实用新型的骨骼肌3d成型装置,包括:
7.分别沿水平和竖直方向阵列设置的多个电极丝;
8.成对设置的脉冲输出电极,其中一个所述脉冲输出电极电连接所述电极丝并用以对所述电极丝输出脉冲电流,其中另一个所述脉冲输出电极用以与所述细胞组织块连接;
9.细胞悬液挤压模块,用以挤出细胞悬液,所述细胞悬液挤压模块被配置为沿所述电极丝轴线方向运动,并可沿竖直方向移动;
10.设置于所述细胞悬液挤压模块运动方向后侧的基质挤压模块,用以挤出基质,所述基质挤压模块被配置为与所述细胞悬液挤压模块同向且同步运动。
11.进一步地,还包括用以容纳细胞培养液的容器,所述多个电极丝设于所述容器内。
12.进一步地,还包括剪断机构,所述剪断机构用以在所述细胞悬液挤压模块和所述基质挤压模块完成打印后,剪断至少一个所述电极丝。
13.进一步地,所述细胞悬液挤压模块包括输出细胞悬液的悬液打印针头,所述悬液打印针头插设于所述电极丝之间的缝隙内,所述基质挤压模块包括输出基质的基质打印针
头,所述基质打印针头设于所述悬液打印针头前侧。
14.进一步地,还包括驱动机构,包括:
15.设置有所述悬液打印针头和所述基质打印针头的第一驱动组件,所述第一驱动组件驱动所述悬液打印针头和所述基质打印针头沿竖直方向运动;
16.与所述第一驱动组件连接的第二驱动组件,所述第二驱动组件驱动所述第一驱动组件沿电极丝水平两侧方向运动;
17.与所述第二驱动组件连接的第三驱动组件,所述第三驱动组件驱动所述第二驱动组件沿电极丝轴线方向运动。
18.进一步地,还包括电极丝移动机构,用以驱使所述电极丝两端分别向电极丝轴线方向相反移动。
19.进一步地,各相邻所述电极丝间距不大于1mm且大于0.5mm。
20.进一步地,所述电极丝直径小于0.1mm。
21.进一步地,所述细胞悬液挤出压力被配置为大于5kpa,小于等于20kpa。
22.进一步地,所述细胞悬液挤出速度被配置为不大于40mm/s。
23.有益效果:通过上述方案,本实用新型骨骼肌3d成型装置用于构建骨骼肌类组织,利用基质挤压模块和细胞悬液挤压模块进行细胞组织的打印,在打印的同时或者打印完成后,可以利用电极丝对细胞组织进行电流刺激,更好地模拟了骨骼肌生长过程中的电信号刺激,提供了阻力训练,生长更为接近体内生长真实情况,结构较为简单,相比于现有方案,不但提升了细胞组织的生长效果,还提高了自动化水平和降低了生产制造难度。
附图说明
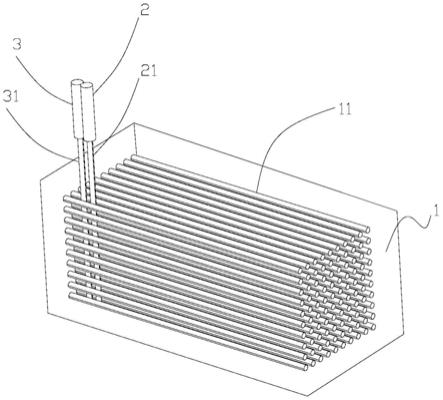
24.附图1为本实用新型骨骼肌3d成型装置的立体结构示意图;
25.附图2为图1所示骨骼肌3d成型装置的设有剪断机构实施例的平面结构示意图;
26.附图3为图1所示骨骼肌3d成型装置的电极丝移动机构部分结构示意图;
27.附图4为另一实施例中的骨骼肌3d成型装置平面结构示意图;
28.附图5为图1所示骨骼肌3d成型装置的驱动机构结构示意图。
具体实施方式
29.为了使本实用新型的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本实用新型进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本实用新型,并不用于限定本实用新型。基于本实用新型中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本实用新型保护的范围。
30.需要说明的是,在本实用新型中涉及“第一”、“第二”等的描述仅用于描述目的,而不能理解为指示或暗示其相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。另外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本实用新型要求的保护范围之内。
31.参见附图1-图4所示本实用新型骨骼肌3d成型装置的一个实施例,包括:电极丝
11、脉冲输出电极6、细胞悬液挤压模块3和基质挤压模块。多个电极丝11分别沿水平和竖直方向阵列设置。
32.脉冲输出电极6成对设置,其中一个所述脉冲输出电极62电连接所述电极丝并用以对所述电极丝11输出脉冲电流,其中另一个所述脉冲输出电极61用以与需要成型的细胞组织块5连接,用以对所述电极丝11两端输出脉冲电流,预设频率为根据细胞生长的状态和种类而定,在此不作限定。具体地,脉冲输出电极61为一块水平放置的金属板,位于电极丝11下方,还可以起到用以放置细胞组织块5的作用。
33.细胞悬液挤压模块3用以挤出细胞悬液,所述细胞悬液挤压模块3被配置为沿所述电极丝11轴线方向运动,并可沿竖直方向移动。
34.基质挤压模块2设置于所述细胞悬液挤压模块3运动方向后侧,用以挤出基质,所述基质挤压模块2被配置为与所述细胞悬液挤压模块3同向且同步运动。细胞悬液,又称生物墨水,是可用于3d打印的具备悬浮细胞的培养液。基质为适宜细胞生长的凝胶态物质,在细胞悬液之前打印以方便细胞生长。
35.通过上述方案,本实用新型骨骼肌3d成型装置用于构建骨骼肌类组织,利用基质挤压模块2和细胞悬液挤压模块3进行细胞组织的打印,在打印的同时或者打印完成后,可以利用电极丝11对细胞组织进行电流刺激,更好地模拟了骨骼肌生长过程中的电信号刺激,提供了阻力训练,生长更为接近体内生长真实情况,结构较为简单,相比于现有方案,不但提升了细胞组织的生长效果,还提高了自动化水平和降低了生产制造难度。
36.具体地,电极丝11可以为多根,或者一根或几根弯折呈多个平行排列的电极丝11形态,以减少所须的电极丝11排列布置工作,这样的结构变化依旧落入本实用新型的保护范围之内。
37.作为对本实施例进一步地优化,还包括用以容纳细胞培养液的容器1,所述多个电极丝11设于所述容器1内。将电极丝11直接放置入容器1内,无需移动骨骼肌3d成型装置,即可实现细胞培养的全流程工作,大大提升了工作效率。
38.在其他实施例中,还包括剪断机构4,所述剪断机构4用以在所述细胞悬液挤压模块3和所述基质挤压模块2完成打印后,剪断至少一个所述电极丝11。具体地,剪断机构4为设置在电极丝11一侧的剪刀4,由操作人员操作进行剪断,并在剪断后移动操控电极丝移动机构9,将电极丝11被剪断的一端移动至细胞组织块5内,如图3所示。在其他实施例中,剪断机构4为液压或者气压驱动,这样的结构变化依旧落入本实用新型的保护范围之内。通过设置剪断机构4,可以无需取出细胞组织块,即可实现针对电极丝11的剪断工作,以方便细胞培养液从被剪断的电极丝11所形成的间隙中进入,提升了细胞和培养液间的物质交换水平。在某些实施例中,可以全部剪断电极丝11,在另一些实施例中,也可以部分剪断,可以根据频率和细胞生长需要而定,在此不作赘述。
39.作为对本实施例进一步地优化,所述细胞悬液挤压模块3包括输出细胞悬液的悬液打印针头31,所述悬液打印针头31插设于所述电极丝11之间的缝隙内,所述基质挤压模块2包括输出基质的基质打印针头21,所述基质打印针头21设于所述悬液打印针头31前侧。
40.具体地,为提升骨骼肌3d打印的自动化水平,本实施例还包括驱动机构,包括:
41.设置有所述悬液打印针头31和所述基质打印针头21的第一驱动组件 71,所述第一驱动组件71驱动所述悬液打印针头31和所述基质打印针头 21沿竖直方向运动;
42.与所述第一驱动组件71连接的第二驱动组件72,所述第二驱动组件 72驱动所述第一驱动组件71沿电极丝11水平两侧方向运动;
43.与所述第二驱动组件72连接的第三驱动组件73,所述第三驱动组件 73驱动所述第二驱动组件72沿电极丝11轴线方向运动。
44.如此,则实现了基质挤压模块2和细胞悬液挤压模块3在竖直、水平和纵深三个方向上的移动,使得骨骼肌3d成型装置可以按预先设置好的程序和速度培育骨骼肌细胞组织块。需要注意的是,所有现有技术中的驱动组件均可实施在本实用新型骨骼肌3d成型装置上进行应用,包括但不限于丝杆螺母组件、齿轮齿条组件、齿轮链条组件、气缸组件和/或液压组件。在其他实施例中,悬液打印针头31和所述基质打印针头21也可以分开设置,只需要保证悬液打印针头31和所述基质打印针头21的打印顺序为基质打印在前,细胞悬液打印在后即可。
45.在本实施例中,还包括电极丝移动机构9,用以驱使所述电极丝11两端分别向电极丝11轴线方向相反移动。同样的,所有现有技术中可驱使两个物体沿直线相反运动的驱动组件均可应用于本实施例中,在此不作赘述。在有的实施例中,仅设置电极丝移动机构9而不设置剪断机构4,通过利用电极丝11的移动而拉断电极丝11,并形成一定的间隙,从而实现电极丝11 的一分为二,以引导所述培养液经所述被剪断电极丝11移动后留下的空隙进入所述细胞组织块5内。
46.作为对本实施例进一步地优化,为避免细胞悬液挤出压力过大而导致细胞破裂,所述细胞悬液挤出压力被设置为不大于40kpa。优选地,所述细胞悬液挤出压力大于5kpa,小于等于20kpa,在此区间范围内,可保证细胞悬液具备良好的挤出速率,且不会发生细胞破裂现象。
47.作为对本实施例进一步地优化,为避免挤出速度过快而导致细胞悬液分布不均,所述细胞悬液挤出速度被设置为不大于120mm/s。优选地,所述细胞悬液挤出速度不大于40mm/s,在此区间范围内,可保证细胞均匀致密排布,且不会因为细胞分布过密而导致的细胞无法存活的现象。
48.作为对本实施例进一步地优化,为保证细胞组织块内细胞生长间距,所述电极丝11直径小于0.1mm,使得细胞组织块内细胞分布更为贴近真实情况。优选地,各相邻所述电极丝11间距不大于1mm且大于0.5mm。以提供细胞组织块更好的生长空间。
49.以上所述仅是本实用新型的优选实施方式,应当指出:对于本技术领域的普通技术人员来说,在不脱离本实用新型原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本实用新型的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1