具有肌腱再生效果的皮肤来源成纤维细胞及其用途的制作方法
1.本发明涉及一种具有肌腱再生效果的皮肤来源成纤维细胞及包含其作为有效成分的用于肌腱再生和治疗的药学组合物。
背景技术:
2.肌腱(tendon)是连接肌肉和骨骼(bone)并将从肌肉产生的力量传递到骨骼来引起关节运动的结缔组织,其由肌腱细胞(tenocyte)和胶原蛋白(collagen)等细胞外基质(extra cellular matrix,ecm)组成。肌腱细胞是肌腱特异性成纤维细胞,在肌腱基质的产生及保持中发挥作用。外伤引起的肌腱损伤在运动或工作、日常生活中也经常发生,即使是轻微的外伤,也会发生因老化而发生退行性变化导致的肌腱炎症或部分撕裂等。
3.肩袖撕裂(rotator cuff tear)是指围绕肩胛骨并有助于手臂自由移动的冈上肌(supraspinatus)、冈下肌(infraspinatus)、小圆肌(teres minor)及肩胛下肌(subscapularis)这四块肌肉的肌腱(tendon)由于诸如老化现象之类的原因而部分或全部别撕裂。肩袖撕裂约占肩部病变的70%,并且随着老龄化及运动人群的增加等,其发病率也在增加。目前为止的治疗方法大部分为手术缝合,但由于缝合后再撕裂率高,因而需要开发替代治疗方法。
4.虽然目前已存在使用肌腱细胞的自体来源细胞治疗剂作为相似细胞治疗剂,但其缺点是需要伴随对患者正常肌腱组织的采集手术以获得细胞治疗剂的原料细胞。
5.相反,若可以将成纤维细胞用作治疗剂,则成纤维细胞能够以相对非侵入性的方式轻松采集,并且可以制成确保质量标准的现成品(ready-made)形式,以便在需要时可以立即使用,从而可以解决使用上述自体来源肌腱细胞的细胞治疗剂而产生的问题。因此,需要开发一种使用除同种来源肌腱细胞之外的成纤维细胞的肌腱损伤治疗剂。
技术实现要素:
6.技术问题
7.本发明人为了开发一种使用成纤维细胞的肌腱损伤治疗剂而付出努力,以解决上述问题。通过确认来源于人皮肤,并且选自波形蛋白、i型胶原蛋白、iii型胶原蛋白、v型胶原蛋白、纤连蛋白及弹性蛋白中的一种或以上蛋白质的表达比肌腱细胞增加的成纤维细胞具有肌腱再生效果,从而完成了本发明。
8.技术方案
9.为了解决上述问题,本发明的一方面提供一种具有肌腱再生效果的成纤维细胞(皮肤来源成纤维细胞),来源于皮肤且所述成纤维细胞内的选自波形蛋白、i型胶原蛋白、iii型胶原蛋白、v型胶原蛋白、纤连蛋白及弹性蛋白中的一种或以上蛋白质的表达与肌腱细胞相比有增加。
10.在本说明书中,“成纤维细胞(fibroblast)”是指在各种组织中发现的高度多样化的中胚层细胞,根据美国国立卫生研究院数据库的医学主题词表(mesh),其定义为“结缔组
织细胞,其分泌富含胶原蛋白及聚合物物质(connective tissue cells which secrete an extracellular matrix rich in collagen and other macromolecules)”。
11.在本说明书中,“肌腱(tendon)”是连接肌肉和骨骼并将从肌肉产生的力量传递到骨骼来引起关节运动的结缔组织,i型胶原蛋白占肌腱重量的85-95%,iii型胶原蛋白约占5%以内,蛋白多糖约占5%以内。并且,纤连蛋白、弹性蛋白等在组织中提供坚固的细胞支架(cell scaffold)。
12.本发明人使用了能够以相对非侵入性的方式获得自体或同种(allogenic)细胞的成纤维细胞,以解决使用自体来源肌腱细胞的细胞治疗剂的问题。具体地,将从供体分离的正常皮肤组织切碎,并通过分解细胞基质等来仅分离成纤维细胞。上述供体可以是通过适宜性评估被评估为适合细胞库建立的人,并且可以不限于特定供体。因此,本发明的皮肤来源成纤维细胞可以来源于自体或同种。同种来源成纤维细胞是指来源于其他人的成纤维细胞。
13.从供体分离的成纤维细胞在37%及10%的co2条件下开始原代培养,与普通细胞培养不同,将10%的co2用于细胞培养,以保持细胞培养基的ph7.4。当细胞在培养皿中以汇合前(pre-confluent)密集度填充至70%至80%程度时,进行传代培养,在第2代建立主细胞库,在第6代建立工作细胞库。
14.因此,根据本发明的一具体例,上述皮肤来源成纤维细胞经过2代或以上传代培养,优选地,可以经过6代或以上培养,并且在ph6.5至ph8.0的培养基中传代培养。
15.并且,根据本发明的一具体例,上述皮肤来源成纤维细胞的每代细胞增殖水平(群体倍增水平(population doubling level))的范围为2.5至5.0,并且即使继续传代培养,该值也保持在规定水平。相反,当继续传代培养时,人肌腱细胞的细胞增殖水平显著降低(图2)。其中,一次传代是指将细胞接种(seeding)在培养皿中后,以汇合前(pre-confluent)密集度培养约6天的细胞。
16.根据本发明的一具体例,上述皮肤来源成纤维细胞可能具有增加的细胞因子及信号传递物质的表达,据报道,这些细胞因子及信号传递物质参与细胞外基质形成及组织再生促进。具体地,与肌腱细胞相比,tgf-β(转化生长因子-β(transforming growth factor-β))分泌增加,并且参与erk(细胞外信号调节激酶(extracellular-signal regulated kinase))信号传递的p-erk1/2(磷酸化细胞外信号调节激酶1/2(phosphorylated extracellular-signal regulated kinase 1/2))的表达及i型胶原蛋白的表达也增加。
17.并且,本发明的皮肤来源成纤维细胞即使在长期保存后解冻,其细胞存活率仍为约70%或以上,并且确认到作为细胞外基质的胶原蛋白每106个单位细胞含有0.10μg或以上,因此细胞质量也非常优秀。
18.因此,本发明的另一方面提供一种用于改善或治疗肌腱疾病的药学组合物,其包含上述具有肌腱再生效果的成纤维细胞作为有效成分。
19.根据本发明的一具体例,肌腱疾病可以选自肩袖撕裂、跟腱疾病、肌腱炎、肌腱损伤及肌腱松解,优选地,可以是肩袖撕裂。
20.本发明人在向肩袖撕裂动物模型注入具有肌腱再生效果的成纤维细胞的结果,确认到肌肉组织再生至与没有肩袖撕裂的正常组相似的水平(图8)。
21.并且,为了确认肌腱再生机制,在用具有肌腱再生效果的成纤维细胞的裂解物处
理肌腱细胞的结果,确认到参与erk信号传递的p-erk1/2的表达显著增加,并且i型胶原蛋白的表达也增加(图9)。
22.上述用于改善或治疗肌腱疾病的药学组合物可以进一步包含透明质酸(hyaluronic acid)、海藻酸(alginate)、纤维蛋白(fibrin)等辅助剂,这些辅助剂为能够增强药效的聚合物载体。这种聚合物载体必须是生物相容的,其可以帮助细胞传递,在不影响细胞存活率的情况下改善物性,从而增强药效。
23.并且,上述用于改善或治疗肌腱疾病的药学组合物可以进一步包含作为细胞冷冻保护剂的dmso(二甲亚砜(dimethyl sulfoxide)),dmso能够以细胞冷冻培养基的2%至15%的浓度包含在内。dmso通过在细胞冷冻时的冰形成过程中改变非渗透性细胞外溶液的浓度来防止脱水。
24.并且,除了有效成分之外,上述用于改善或治疗肌腱疾病的药学组合物还可以进一步包含药学上可接受的载体。上述组合物所包含的药学上可接受的载体通常用于制剂的制备,包括乳糖、葡萄糖、蔗糖、山梨糖醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、海藻酸,明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁和矿物油等,但不限于此。
25.上述用于改善或治疗肌腱疾病的药学组合物优选非口服给药。在非口服给药的情况下,可以通过皮下注入、肌肉注入、腹腔注入、内皮给药、局部给药等方式给药,也可以直接注射到患部。
26.以成人为准,上述用于改善或治疗肌腱疾病的药学组合物的合适剂量范围为100-100000000(102至108)cells/kg。术语“药学有效率”是指足以预防肌腱损伤或治疗受损肌腱的量。
27.上述组合物可以根据本发明所属技术领域的普通技术人员容易实施的方法,通过使用药学上可接受的载体和/或赋形剂配制来制备成单位容量形式,或者可以通过投入于多容量容器中来制备。并且,上述组合物可以作为单独的治疗剂给药或与其他治疗剂组合给药,可以与现有治疗剂依次或同时给药。并且可以一次给药或根据需要追加给药,可以与缝合等外科手术联合使用或单独给药。
28.能够以细胞治疗剂形式提供包含上述具有肌腱再生效果的成纤维细胞作为有效成分的用于改善或治疗肌腱疾病的药学组合物。上述“细胞治疗剂”是指“为了恢复细胞的组织和功能,活的自体通过在体外增殖和筛选同种或异种细胞或通过其他方法改变细胞的生物学特性等一系列行为来用于治疗、诊断及预防的药品”。
29.并且,本发明提供一种肌腱疾病的改善或治疗方法,其包括将权利要求1的具有肌腱再生效果的成纤维细胞或权利要求8的用于改善或治疗肌腱疾病的药学组合物给予需要治疗的个体的步骤。肌腱疾病的类型、药学组合物或成纤维细胞的剂量、给药方法与上述用于改善或治疗肌腱疾病的药学组合物中的描述相同。
30.发明的效果
31.本发明一例的具有肌腱再生效果的同种皮肤来源成纤维细胞在细胞在形态学上与肌腱细胞相似,作为成纤维细胞标志物的波形蛋白的表达水平高,表达大量的细胞外基质蛋白,可通过作用于tgf-β、erk信号传递机制来增加胶原蛋白的合成,从而可以有效再生受损的肌腱。
附图说明
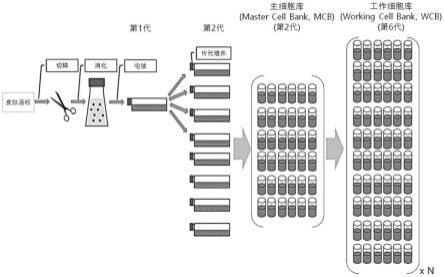
32.图1为使用本发明一例的皮肤来源成纤维细胞来建立人源同种皮肤成纤维细胞库的示意图。
33.图2为根据人源肌腱细胞(a)及皮肤来源成纤维细胞(b)的传代培养确认细胞增殖水平(population doubling level,pdl)的结果。
34.图3为使用相差显微镜确认体外培养的肌腱细胞和主细胞库及工作细胞库的皮肤来源成纤维细胞的结果。
35.图4为在体外培养的肌腱细胞和工作细胞库的皮肤来源成纤维细胞中确认波形蛋白的表达水平的结果。
36.图5为在工作细胞库的皮肤来源成纤维细胞中确认作为角质细胞标志物的角蛋白(keratin;k14)及泛细胞角蛋白(pan-cytokeratin)的表达水平的结果。
37.图6为通过流式细胞分析方法确认工作细胞库的皮肤来源成纤维细胞中的波形蛋白表达细胞比例的结果。
38.图7为通过荧光显微镜(a)及蛋白质印迹(b)确认体外培养的肌腱细胞和工作细胞库的皮肤来源成纤维细胞中的细胞外基质蛋白的表达水平的结果。
39.图8为通过组织学分析方法确认在将皮肤来源成纤维细胞注入到肩袖撕裂动物模型中后肌腱组织的恢复程度的结果。
40.在图9中,a部分为确认皮肤来源成纤维细胞中分泌的tgf-β水平的结果,b部分为在用皮肤来源成纤维细胞的细胞裂解物处理肌腱细胞后信号传递分子的表达变化的结果。
41.图10为从基因水平上确认在用皮肤来源成纤维细胞的细胞裂解物处理肌腱细胞后信号传递分子的表达变化的结果。
具体实施方式
42.以下将通过实施例更加详细地描述一个或以上的具体例。然而,这些实施例用于示例性地描述一个或以上的具体例,并且本发明的范围不限于这些实施例。
43.实施例1:培养皮肤来源成纤维细胞
44.将从供体分离的正常皮肤组织切碎,并通过分解来仅分离成纤维细胞。分离的成纤维细胞在含有10%胎牛血清(fetal bovine serum,fbs)的达尔伯克改良伊格尔培养基(dulbecco's modified eagle's medium,dmem)/f12(invitrogen,美国)中进行原代培养(primary culture),培养条件保持在37℃、10%co2的潮湿环境。以约5天至6天的间隔传代培养后,在第2代(passage)建立主细胞库(master cell bank,mcb)。然后,以约5天至6天的间隔进一步传代培养,并在第6代中获得大量工作细胞库(working cell bank,wcb)(图1)。当培养皿中的细胞填充至70~80%程度时,使用胰蛋白酶(trypsin)-edta分离细胞来进行细胞传代培养。在大多数体外(in vitro)细胞培养中,将5%co2用作气体组合物,但在本发明中,使用10%co2,以将培养基的ph准确保持在7.4。
45.细胞库以如下方式冷冻和保存。首先将第2代至第10代的细胞和含有少于10%的二甲基亚砜(dimethyl sulfoxide,dmso)(一种细胞用冷冻保护剂)的冷冻培养基进行混合。然后,将悬浮状态的1-10x106个细胞分株到玻璃剂型的安瓶中,用异丙醇(isopropanol)逐渐降温的同时将细胞冷冻,并且最终在-15℃以下的冰箱或液氮中长期保
存。
46.以下,将本实施例中获得的人皮肤来源成纤维细胞称为“皮肤来源成纤维细胞”。
47.实施例2:确认皮肤来源成纤维细胞的特性
48.2-1.皮肤来源成纤维细胞的增殖及形态学特性
49.将实施例1中获得的皮肤来源成纤维细胞在相同培养条件下从第2代培养至第10代,并通过计数初始铺板时的细胞数和获得细胞后的总细胞数来计算细胞的倍增时间(doubling time)。结果,从第2代至第10代平均需要30小时,并且对于两种不同的培养基表现出相似的值。
50.并且,根据以下数学式1确认细胞增殖水平(population doubling level,pdl)的结果,计算出实施例1中获得的皮肤来源成纤维细胞每次传代2.7个至4.5个(图2,下端图表;n=3,平均标准偏差)。该结果与体外培养时肌腱细胞的短的细胞寿命相反(图2,上端图表;n=3,平均标准偏差),并且是应用成纤维细胞的细胞治疗剂的重要优点之一。
51.数学式1
52.pdl=(log(nh)-log(ni))/log 2
53.nh:最终获得的细胞数;ni:初始铺板细胞数。
54.并且,在从实施例1中制备的主细胞库及工作细胞库中确认皮肤来源成纤维细胞的形态的结果,确认到本发明的皮肤来源成纤维细胞保持类似于肌腱细胞的成纤维细胞固有的纺锤(spindle)形态(图3)。
55.2-2.确认波形蛋白的表达
56.培养的肌腱细胞和皮肤来源成纤维细胞用针对成纤维细胞标记的波形蛋白的一抗和绿色荧光物质(fitc)结合二抗处理后,通过荧光显微镜观察。细胞核用dapi(4,6-二脒基-2-苯基吲哚(4,6-diamidino-2-phenylindole))染色。
57.结果,确认到工作细胞库的皮肤来源成纤维细胞表现出成纤维细胞固有特征,并且以与肌腱细胞相似或更高的水平表达波形蛋白(图4)。
58.2-3.确认均质性
59.为了确认工作细胞库的皮肤来源成纤维细胞的混合性及均质性,使用角质细胞标志物角蛋白(keratin;k14)及泛细胞角蛋白(pan-cytokeratin)抗体对细胞进行染色,然后通过荧光显微镜观察并进行流式细胞分析。细胞核用dapi染色。
60.结果,在作为定性观察的荧光显微镜观察中,没有检测到角质细胞标记物(图5)。并且,在作为定量分析的流式细胞分析中,确认到被分类为作为成纤维细胞标志物的波形蛋白表达细胞的细胞平均为98.5%,从而确认到构成工作细胞库的大多数皮肤来源成纤维细胞表现出成纤维细胞特征(图6)。
61.2-4.确认细胞外基质蛋白
62.在工作细胞库的皮肤来源成纤维细胞中确认了作为代表性细胞外基质的胶原蛋白等的表达水平。皮肤来源成纤维细胞用针对细胞外基质蛋白的每种一抗和绿色荧光物质(fitc)结合二抗处理后,通过荧光显微镜观察。
63.确认结果,可知皮肤来源成纤维细胞中i型、iii型及iv型胶原蛋白、纤连蛋白(fibronectin)及弹性蛋白(elastin)的表达水平很高(图7)。
64.实施例3:确认皮肤来源成纤维细胞的质量
65.将冷冻保存中的细胞库的皮肤来源成纤维细胞解冻后,进行再培养并确认了质量。结果,再培养的皮肤来源成纤维细胞表现出优异的解冻率、细胞存活率,从而确认到无论冷冻期限如何,均保持细胞质量(表1)。
66.表1
[0067][0068][0069]
并且,在进行符合韩国食品药品安全部细胞治疗审批标准的外源病毒阴性试验及微生物残留试验的结果,确认到上述细胞库中没有外源病毒和微生物残留。
[0070]
实验例1:确认对肩袖撕裂的疗效
[0071]
1-1.临床前疗效
[0072]
以如下方式确认工作细胞库的皮肤来源成纤维细胞对肩袖撕裂的疗效。
[0073]
对20周龄新西兰白兔(new zealand white rabbits)的肩部实施双侧冈上肌撕裂(bilateral supraspinatus tears),6周后,向对照组注入生理盐水(saline),并向实验组注入107个皮肤来源成纤维细胞后缝合。缝合12周后,确认兔的体重及其他无异常,然后处死兔,摘除肩腱,脱钙(decalcification)来制备石蜡块。将石蜡块用马松三色(masson's trichrome)染色后进行组织学分析。
[0074]
分析结果,与注入生理盐水的对照组相比,注入皮肤来源成纤维细胞的实验组中,可以观察到与没有肩袖撕裂的正常组相似水平的对齐且致密的肌腱组织排列(图8)。在图8中,以染成蓝色的部分为胶原蛋白,染成红色的部分为肌肉、细胞质及角蛋白。
[0075]
1-2.确认疗效机制
[0076]
为了确认本发明一例的皮肤来源成纤维细胞对肩袖撕裂的疗效机制,分析了据报道参与细胞外基质形成及组织再生促进的细胞因子及信号传递物质。
[0077]
培养人源肌腱细胞和工作细胞库的皮肤来源成纤维细胞,并通过elisa(酶联免疫吸附试验,enzyme-linked immunosorbent assay)定量tgf-β(转化生长因子-β(transforming growth factor-β))的水平,结果,皮肤来源成纤维细胞(hf)每1x106个细胞分泌692pg的tgf-β,从而表现出比肌腱细胞(ht)更高的分泌量(图9的a部分)。
[0078]
并且,用皮肤来源成纤维细胞的细胞裂解物处理肌腱细胞并经过24小时后,通过蛋白质印迹确认了参与信号传递的细胞信号分子。结果,可知与对照组相比,在用皮肤来源成纤维细胞裂解物处理的实验组(hf lysate)中,p-erk 1/2(磷酸化细胞外信号调节激酶1/2(phosphorylated extracellular-signal regulated kinase 1/2))的表达显著增加,并且i型胶原蛋白的表达也增加(图9的b部分)。并且,在基因水平上也可以确认细胞信号分子的表达增加(图10)。
[0079]
本实验例的结果表明,本发明的皮肤来源成纤维细胞通过erk信号传递来增加i型胶原蛋白的表达,最终表现出肌腱再生效果(图9及图10)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1