用于制备塔格糖的组合物和利用其制备塔格糖的方法与流程
1.本发明涉及用于制备塔格糖的组合物和利用其制备塔格糖的方法。
背景技术:
2.塔格糖是一种天然甜味剂,少量存在于如牛奶、奶酪、可可以及甜味天然水果(如苹果和橘子)等食物中。塔格糖的卡路里是1.5kcal/g,为糖的1/3,其血糖指数(gi)是3,为糖的5%。然而,塔格糖具有与糖类似的物理性质,具有多种健康功能,同时具有与糖类似的甜味,因此可以作为一种既能满足健康又能满足口感的代糖应用于各种产品中。
3.制备塔格糖的传统已知或常用方法包括以半乳糖为主要原料的化学方法(催化反应)和生物方法(异构酶反应)(pct wo 2006/058092)。然而,由于乳糖的价格取决于国际市场原奶和乳糖的生产、需求和供应,因此乳糖作为半乳糖的基本原料,在传统的塔格糖制备方法中被用作主要原料,其稳定的供应是有限的。因此,需要一种以广义糖类(糖、葡萄糖、果糖等)为原料的塔格糖生产系统。
4.因此,目前正在应用一种以果糖为原料,通过谷氨酸棒状杆菌(corynebacterium glutamicum)为基础的细胞反应生产塔格糖的技术。当果糖加入产生塔格糖转化酶的细胞时,果糖通过细胞反应转变成塔格糖以产生塔格糖。为了提高塔格糖转化的效率,首先需要增加细胞中塔格糖转化酶的量。为此,细胞内塔格糖转化酶的高表达系统是绝对必要的。
技术实现要素:
5.技术问题
6.本发明人为增加果糖-4-差向异构酶(一种塔格糖的转化酶)的表达进行了深入研究,结果发现一种表达显著增加的果糖-4-差向异构酶的突变的多核苷酸,从而完成本发明。
7.技术方案
8.本发明提供一种突变的多核苷酸,其编码kosmotoga oelia衍生的果糖-4-差向异构酶;或其变体。
9.本发明提供一种包含突变的多核苷酸的载体。
10.本发明提供一种棒状杆菌属(corynebacterium sp.)微生物,其表达kosmotoga oelia衍生的果糖-4-差向异构酶或其变体,所述微生物包含突变的多核苷酸或包含突变的多核苷酸的载体。
11.本发明提供一种产生果糖-4-差向异构酶的方法,所述方法包括在培养基中培养棒状杆菌属微生物,所述微生物包含突变的多核苷酸或者包含突变的多核苷酸的载体。
12.本发明提供用于产生塔格糖的组合物,其包含棒状杆菌属微生物,所述微生物包含突变的多核苷酸或者包含突变的多核苷酸的载体;或所述微生物的培养物。
13.本发明提供一种制备塔格糖的方法,所述方法包括使棒状杆菌属微生物;或所述微生物的培养物与果糖接触,所述微生物包含突变的多核苷酸或包含所述突变的多核苷酸
的载体。
14.本发明提供棒状杆菌属微生物用于产生塔格糖的用途,所述微生物包含突变的多核苷酸或者包含突变的多核苷酸的载体。
15.有益效果
16.与未突变的多核苷酸相比,本发明的突变的多核苷酸具有显著更高的果糖-4-差向异构酶或其变体的表达水平,因此,当从包含所述突变的多核苷酸的微生物中产生酶时,经济效率较高。
附图说明
17.图1为突变的多核苷酸表达的果糖-4-差向异构酶的表达水平,其中e是空质粒,wt是#7_h4_ko(knf4e),变体是#7_h4_ko(knf4e)变体;
18.图2为通过突变的多核苷酸表达的果糖-4-差向异构酶的塔格糖转化率;
19.图3为突变的多核苷酸表达的果糖-4-差向异构酶变体的表达水平,其中1是空白,2是#7_h4_ko(knf4e),3是#7_h4_ko(knf4e)_变体,4是#7_h4_ko(knf4e)_变体_3aa突变(n97y,t124w,n367v),5是#7_h4_ko(knf4e)_变体_1aa突变(t124w);
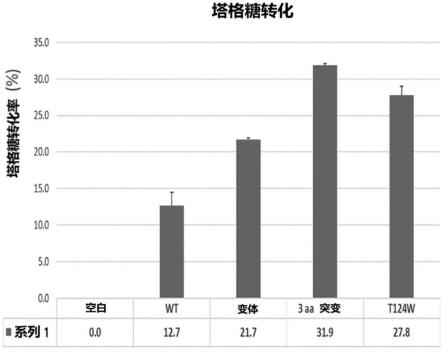
20.图4为通过突变的多核苷酸表达的果糖-4-差向异构酶变体的塔格糖转化率;
21.图5为通过向新阿波罗栖热袍菌(thermotoga neapolitana)衍生的果糖-4-差向异构酶变体施用核苷酸突变获得的突变的多核苷酸表达水平,其中con是空质粒,wt是h4_tn_初始,变体2是h4_tn_变体_2,cj是muxae,变体1是h4_tn_变体_1。
22.图6为通过向新阿波罗栖热袍菌衍生的果糖-4-差向异构酶变体施用核苷酸突变获得的突变的多核苷酸引起的塔格糖转化率。
具体实施方式
23.本发明详细描述如下。同时,本发明内容公开的各描述和实施方式还可应用于其他描述和实施方式。即,本发明内容所公开不同要素的全部组合在本发明范围内。而且,本发明的范围不限制于以下具体的描述。另外,本领域技术人员应理解或能够确定仅使用常规实验的本文描述的本发明的特定实施方式的许多等同物。此外,这些等同物应理解为在本发明范围内。
24.为实现本发明的目的,本发明一个方面提供突变的多核苷酸,其编码kosmotoga oelia衍生的果糖-4-差向异构酶;或其变体。
25.突变的多核苷酸可以是其中任意一种或多种编码氨基酸的多核苷酸在编码果糖-4-差向异构酶;或其变体的多核苷酸中修饰,但不限于此。特别地,突变的多核苷酸可包括以下任意一种或多种突变:i)编码亮氨酸(l)的多核苷酸选自ctc、ctg、ctt和ttg;ii)编码异亮氨酸(i)的多核苷酸选自atc和att;iii)编码苏氨酸(t)的多核苷酸选自act、acg和acc;iv)编码精氨酸(r)的多核苷酸选自cgt、cgc和cgg;或v)编码甘氨酸(g)的多核苷酸选自ggc、ggt和gga,并且可包括i)-v)的所有突变,但不限于此。
26.此外,突变的多核苷酸还可包括以下任意一种或多种突变:vi)编码缬氨酸(v)的多核苷酸选自gta、gtc、gtg和gtt;vii)编码丝氨酸(s)的多核苷酸选自tca、tct、tcc和agc;viii)编码丙氨酸(a)的多核苷酸选自gcg、gct、gcc和gca;或ix)编码谷氨酰胺(q)的多核苷
酸选自cag和caa,但不限于此。
27.更特别地,突变的多核苷酸可包括以下任意一种或多种突变:i)编码亮氨酸(l)的多核苷酸选自ctc、ctg、ctt和ttg;ii)编码异亮氨酸(i)的多核苷酸选自atc和att;iii)编码苏氨酸(t)的多核苷酸选自act、acg和acc;iv)编码精氨酸(r)的多核苷酸选自cgt、cgc和cgg;v)编码甘氨酸(g)的多核苷酸选自ggc、ggt和gga;vi)编码缬氨酸(v)的多核苷酸选自gta、gtc、gtg和gtt;vii)编码丝氨酸(s)的多核苷酸选自tca、tct、tcc和agc;viii)编码丙氨酸(a)的多核苷酸选自gcg、gct、gcc和gca;或ix)编码谷氨酰胺(q)的多核苷酸选自cag和caa,但不限于此。
28.突变的多核苷酸可引入棒状杆菌属微生物并在其中表达。特别地,在引入突变的多核苷酸的棒状杆菌属微生物中,微生物中所表达果糖-4-差向异构酶的表达水平或所产生塔格糖的量可增加。更特别地,相较未引入突变的多核苷酸的棒状杆菌属微生物,即引入未突变的多核苷酸的棒状杆菌属微生物或野生型棒状杆菌属微生物,其果糖-4-差向异构酶的表达水平和所产生塔格糖的量可增加。
29.一般来说,每个微生物都有一个编码氨基酸的核酸序列。例如,在kosmotoga属微生物衍生的野生型蛋白中,seq id no:1核酸序列翻译成seq id no:2氨基酸序列。
30.因此,本发明中,编码kosmotoga属微生物衍生野生型蛋白的基因突变,使得在棒状杆菌属微生物中适当地进行翻译。突变可以是以下任意一种或多种,例如选自:ttt(编码苯丙氨酸(f)的多核苷酸)突变成ttc和ttc突变成ttt;选自:ttg(编码亮氨酸(l)的多核苷酸)突变成ctc,ctt突变成ctc,ttg突变成ctg,ctt突变成ctg,cta突变成ctg,ttg突变成ctt,ctc突变成ctt,tta突变成ctt,ctt突变成ttg,ctg突变成ttg,ctc突变成ttg,cct突变成ttg,和tta突变成ttg;选自:att(编码异亮氨酸(i)的多核苷酸)突变成atc,ata突变成atc,atc突变成att和ata突变成att;选自:gtt(编码缬氨酸(v)的多核苷酸)突变成gta,gtc突变成gta,gtt突变成gtc,gta突变成gtc,gta突变成gtg,gtt突变成gtg,gta突变成gtt;选自:agc(编码丝氨酸(s)的多核苷酸)突变成tca,tct突变成tca,agc突变成tct,agc突变成tcc,agt突变成tcc,tca突变成tcc,tct突变成tcc,tca突变成agc和tcg突变成agc;选自:tat(编码酪氨酸(y)的多核苷酸)突变成tac,tac突变成tat;选自:cat(编码组氨酸(h)的多核苷酸)突变成cac和cac突变成cat;选自:caa(编码谷氨酰胺(q)的多核苷酸)突变成cag;选自:aat(编码天冬酰胺(n)的多核苷酸)突变成aac和aac突变成aat;选自:aag(编码赖氨酸(k)的多核苷酸)突变成aaa和aaa突变成aag;选自:gat(编码天冬氨酸(d)的多核苷酸)突变成gac,和gac突变成gat;选自:gaa(编码谷氨酸(e)的多核苷酸)突变成gag,和gag突变成gaa;选自:tgc(编码半胱氨酸(c)的多核苷酸)突变成tgt,和tgt突变成tgc;选自:aga(编码精氨酸(r)的多核苷酸)突变成cgt,agg突变成cgt,cga突变成cgt,aga突变成cgc,cga突变成cgc,cgg突变成cgc,cgt突变成cgc,aga突变成cgg,cga突变成cgg和cgt突变成cgg;选自:gga(编码甘氨酸(g)的多核苷酸)突变成ggc,ggg突变成ggc,ggt突变成ggc,gga突变成ggt,ggc突变成ggt,ggg突变成ggt,ggc突变成gga,ggg突变成gga,ggt突变成gga;选自:cca(编码脯氨酸(p)的多核苷酸)突变成ccc,ccg突变成ccc,cct突变成ccc,cca突变成cct,ccc突变成cct,ccg突变成cct,ccc突变成ccg,ccg突变成cca和cct突变成cca;选自:aca(编码苏氨酸(t)的多核苷酸)突变成act,aca突变成acg,act突变成acc和aca突变成acc;或选自:gca(编码丙氨酸(a)的多核苷酸)突变成gct,gcc突变成gct,gcg突变成gct,gcg突变成gcc,
gca突变成gcc,gct突变成gcc,gcc突变成gca,gcg突变成gca和gct突变成gca,但不限于此。
31.如本文所用,术语“多核苷酸”是指作为核苷酸聚合物的一定长度或更长的dna或rna链,其中核苷酸单体以长链形状共价连接。
32.如本文所用,术语“突变的多核苷酸”是指通过用其他核苷酸取代构成多核苷酸的任意一个或多个核苷酸而突变的多核苷酸。突变的多核苷酸可与术语如突变体多核苷酸和多核苷酸突变酶互换使用。
33.如本文所用,术语“果糖-4-差向异构酶”是指显示果糖-4-差向异构化活性的酶,其使得果糖的4位碳差向异构,从而使果糖转变成塔格糖。为实现本发明目的,果糖-4-差向异构酶可无限制地包括任意酶,只要其是使用果糖作为底物,能够产生塔格糖,且可与“d-果糖-4-差向异构酶”互换使用。例如,已知数据库kegg(京都基因和基因组百科全书(kyoto encyclopedia of genes and genomes))中的二磷酸塔格糖醛缩酶或二磷酸塔格糖醛缩酶ii类辅助蛋白ec 4.1.2.40可纳入果糖-4-差向异构酶,只要其显示将作为底物的果糖转变成塔格糖的活性。二磷酸塔格糖醛缩酶已知是使用d-塔格糖1,6-二磷酸作为底物,生成磷酸甘油酮和d-甘油醛3-磷酸的酶,如下面的[方案1]所示。
[0034]
[方案1]
[0035]
d-塔格糖1,6-二磷酸《=》磷酸甘油酮+d-甘油醛3-磷酸
[0036]
例如,塔格糖-6-磷酸激酶(ec 2.7.1.144)可纳入果糖-4-差向异构酶,只要其显示将作为底物的果糖转变成塔格糖的活性。塔格糖-6-磷酸激酶已知是使用adp和d-塔格糖6-磷酸作为底物,生成adp和d-塔格糖1,6-二磷酸的酶,如下面的[方案2]所示。
[0037]
[方案2]
[0038]
atp+d-塔格糖6-磷酸《=》adp+d-塔格糖1,6-二磷酸
[0039]
关于果糖-4-差向异构酶的活性,从作为底物的果糖到塔格糖的转化率(转化率=塔格糖重量/初始果糖重量
×
100)可以是0.01%或更多,特别地0.1%或更多,更特别地0.3%或更多。更特别地,转化率可以是0.01%-100%范围,或0.1%-50%范围,但不限于此。
[0040]
本发明中编码果糖-4-差向异构酶的多核苷酸可包括seq id no:1核酸序列,特别地可基本由seq id no:1核酸序列组成,更特别地可由seq id no:1核酸序列组成,但不限于此。
[0041]
seq id no:1是编码果糖-4-差向异构酶的核酸序列。seq id no:1核酸序列可包括与其具有80%、85%、90%、95%、96%、97%、98%或99%或更高同源性或相同性的核酸序列组成的多核苷酸。显然,由其中一些序列缺失、修饰、取代或添加的核酸序列组成的多核苷酸也包括在本发明的seq id no:1核酸序列范围内,只要该核酸序列具有这类同源性或相同性且显示对应seq id no:1的功效。
[0042]
换言之,即使当其在本发明中描述为“由特定seq id no所示核酸序列组成的多核苷酸”或“具有特定seq id no所示核酸序列的多核苷酸”时,显然,由其中一些序列缺失、修饰、取代或添加的核酸序列组成的多核苷酸也可用于本发明,只要其显示与由对应seq id no:核酸序列组成的多核苷酸相同或对应的活性。例如,显然“由seq id no:1核酸序列组成的多核苷酸”可属于“由seq id no:1核酸序列组成的多核苷酸”,只要其显示与该多核苷酸相同或对应的活性。
[0043]
本发明的果糖-4-差向异构酶可包括seq id no:2氨基酸序列,特别地可基本由seq id no:2氨基酸序列组成,更特别地可由seq id no:2氨基酸序列组成,但不限于此。
[0044]
seq id no:2是编码果糖-4-差向异构酶的氨基酸序列,seq id no:2氨基酸序列可包括与其具有80%、85%、90%、95%、96%、97%、98%或99%或更高同源性或相同性的氨基酸序列组成的多肽。显然,由其中一些序列缺失、修饰、取代或添加的氨基酸序列组成的多肽也包括在本发明的seq id no:2氨基酸序列范围内,只要该氨基酸序列具有这类同源性或相同性且显示对应seq id no:2的功效。
[0045]
本发明的kosmotoga oelia衍生的果糖-4-差向异构酶变体可以是kosmotoga oelia衍生的果糖-4-差向异构酶氨基酸序列中的任意一个或多个氨基酸被取代并显示果糖-4-差向异构酶活性的变体,但不限于此。氨基酸取代可以是特定取代1-20个氨基酸、1-15个氨基酸、1-12个氨基酸、1-10个氨基酸、1-9个氨基酸或1-7个氨基酸。例如,氨基酸取代可包括任意一种或多种选自以下的取代:a)用酪氨酸(y)取代97位对应的氨基酸,b)用色氨酸(w)取代124位对应的氨基酸和c)用缬氨酸(v)取代367位对应的氨基酸,但不限于此。
[0046]
如本文所用,术语“酶变体”指蛋白,其中蛋白的功能或性质得以维持,而一个或多个氨基酸保守取代和/或修饰与所述序列不同。酶变体与所鉴定序列差异数个氨基酸取代、缺失或添加。这种酶变体一般可如下鉴定:修饰蛋白的氨基酸序列中的一个或多个氨基酸并评估修饰蛋白的性质。换言之,酶变体的能力相较天然蛋白可增加、不变或减少。一些酶变体可包括其中一个或多个部分例如n-末端前导序列或跨膜结构域被去除的酶变体。其他酶变体可包括从成熟蛋白n-和/或c-末端移除一部分的酶变体。对于术语“酶变体”,可使用修饰、修饰蛋白、修饰多肽、突变体、突变蛋白质、分歧、变体等,酶变体不限于此,只要其是用于突变意义的术语。
[0047]
为实现本发明的目的,在酶变体中,修饰蛋白活性可相较自然出现的野生型或未修饰蛋白增加,但酶变体不限于此。
[0048]
如本文所用,术语“保守取代”指一种氨基酸用显示类似结构和/或化学特性的另一氨基酸取代。例如,酶变体可具有一种或多种保守取代,而仍保留一种或多种生物活性。这类氨基酸取代一般可基于残基极性、电荷、溶解度、疏水性、亲水性和/或两亲性方面的相似性而发生。例如,在带电氨基酸中,带正电(碱性)氨基酸包括精氨酸、赖氨酸和组氨酸,带负电(酸性)氨基酸包括谷氨酸和天冬氨酸。不带电氨基酸中,非极性氨基酸包括甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、苯丙氨酸、色氨酸和脯氨酸,极性或亲水氨基酸包括丝氨酸、苏氨酸、半胱氨酸、酪氨酸、天冬酰胺和谷氨酰胺,非极性氨基酸中的芳族氨基酸包括苯丙氨酸、色氨酸和酪氨酸。
[0049]
酶变体可包括对多肽二级结构和性质影响极小的氨基酸缺失或添加。例如,多肽可在蛋白n-末端缀合信号(或前导)序列,其参与共翻译或翻译后的蛋白转移。多肽可缀合其他序列或接头以能够鉴定、纯化或合成多肽。
[0050]“用另一氨基酸取代”不受限制,只要氨基酸不同于取代前的氨基酸。换言之,用另一氨基酸取代不受限制,只要对应seq id no:2氨基酸序列97位的氨基酸天冬酰胺(n)用天冬酰胺以外的氨基酸残基取代,对应124位的氨基酸苏氨酸(t)用苏氨酸以外的氨基酸残基取代,或对应367位的氨基酸天冬酰胺(n)用天冬酰胺以外的氨基酸残基取代。在本发明中,当表示为“特定氨基酸被取代”时,显然氨基酸用不同于取代前的氨基酸取代,即使没有单
独指明氨基酸用另一氨基酸取代。
[0051]
酶变体可以是其中,对应seq id no:2氨基酸序列97位、124位和367位的氨基酸中一个或多个氨基酸用不同于取代前的氨基酸取代。或者,酶变体可具有不带电氨基酸并用不同于取代前的氨基酸取代,但不限于此。
[0052]
特别地,酶变体可包括选自以下的任意一种或多种取代:在seq id no:2氨基酸序列中,a)用另一氨基酸取代97位对应的氨基酸,b)用另一氨基酸取代124位对应的氨基酸和c)用另一氨基酸取代367位对应的氨基酸。更特别地,酶变体可以是其中,a)用酪氨酸(y)取代97位对应的氨基酸,b)用色氨酸(w)取代124位对应的氨基酸和c)用缬氨酸(v)取代367位对应的氨基酸。
[0053]
本发明提供的果糖-4-差向异构酶变体可以指酶变体,其具有上述果糖-4-差向异构化能力的蛋白特定位置处氨基酸被取代,因而显示果糖-4-差向异构化能力和/或果糖-4-差向异构化能力的稳定性相较突变前的蛋白增加。
[0054]
酶变体可包括seq id no:5或seq id no:7氨基酸序列,但不限于此。
[0055]
酶变体可包括对应seq id no:2的97位、124位或367位的氨基酸用另一氨基酸取代,与seq id no:5或seq id no:7氨基酸序列具有至少80%、90%、95%、96%、97%、98%或99%或更多或100%序列同源性,并显示果糖-4-差向异构化活性。
[0056]
酶变体可包括seq id no:5或seq id no:7氨基酸序列或与该氨基酸序列有80%或更多同源性或相同性的氨基酸序列,且在对应氨基酸序列97位、124位或367位的氨基酸中有一个或多个固定氨基酸,但不限于此。特别地,本发明的酶变体可包括多肽,其与seq id no:5或seq id no:7氨基酸序列具有至少80%、90%、95%、96%、97%、98%或99%或更多同源性或相同性。显然本发明范围也包括具有某一氨基酸序列的蛋白,其中除了对应97位、124位或367位的一些序列缺失、修饰、取代或添加,只要氨基酸序列具有这类同源性或相同性且显示对应该蛋白的功效。
[0057]
本发明的突变的多核苷酸可以是编码单一氨基酸的任意一个或多个多核苷酸在编码果糖-4-差向异构酶的seq id no:1核酸序列中突变,或编码果糖-4-差向异构酶变体的核酸序列,其中果糖-4-差向异构酶的氨基酸序列中的任意一个或多个氨基酸被取代,但不限于此。特别地,突变可包括以下一种或多种突变:i)编码亮氨酸(l)的多核苷酸选自ctc、ctg、ctt和ttg;ii)编码异亮氨酸(i)的多核苷酸选自atc和att;iii)编码缬氨酸(v)的多核苷酸选自gta、gtc、gtg和gtt;iv)编码丝氨酸(s)的多核苷酸选自tca、tct、tcc和agc;v)编码苏氨酸(t)的多核苷酸选自act、acg和acc;vi)编码丙氨酸(a)的多核苷酸选自gct、gcc和gca;vii)编码谷氨酰胺(q)的多核苷酸选自cag;viii)编码精氨酸(r)的多核苷酸选自cgt、cgc和cgg;或ix)编码甘氨酸(g)的多核苷酸选自ggc、ggt和gga,但不限于此。
[0058]
多核苷酸突变不受特定限制,只要其在一定范围内进行,其中仅密码子改变,但编码果糖-4-差向异构酶的氨基酸序列不变。特别地,在seq id no:1核酸序列中,i)在6位、12位、36位、47位、82位、89位、94位、126位、128位、134位、145位、156位、157位、159位、172位、209位、219位、253位、278位、289位、295位、299位、306位、313位、320位、333位、352位、359位、362位、368位、378位、382位、389位、391位、407位、408位、415位、422位和424位任意一个或多个位置编码亮氨酸(l)的多核苷酸可选自ctc、ctg、ctt和ttg及突变;ii)在9位、17位、32位、48位、76位、80位、87位、88位、112位、115位、150位、178位、195位、227位、242位、257
位、263位、288位、309位、379位、387位、392位、403位、413位、416位和420位任意一个或多个位置编码异亮氨酸(i)的多核苷酸可选自atc和att及突变;iii)在34位、35位、44位、45位、51位、62位、65位、154位、180位、198位、206位、210位、254位、270位、274位、296位、317位、373位、380位、384位、390位、421位和431位任意一个或多个位置编码苏氨酸(t)的多核苷酸可选自act,acg和acc及突变;iv)在29位、70位、109位、116位、133位、153位、163位、173位、205位、225位、247位、249位、251位、300位、330位、348位、351位、354位、361位、363位、372位、404位、409位和419位任意一个或多个位置编码精氨酸(r)的多核苷酸可选自cgt、cgc和cgg及突变;v)在16位、20位、43位、59位、60位、63位、81位、90位、91位、95位、101位、122位、139位、170位、179位、186位、187位、192位、218位、224位、234位、238位、267位、285位、292位、319位、345位和406位任意一个或多个位置编码甘氨酸(g)的多核苷酸可选自ggc、ggt和gga及突变;vi)在10位、21位、24位、31位、46位、55位、73位、149位、175位、177位、182位、197位、200位、207位、226位、229位、230位、231位、235位、264位、282位、286位、291位、325位、327位、328位、371位、375位和423位任意一个或多个位置编码缬氨酸(v)的多核苷酸可选自gta、gtc、gtg和gtt及突变;vii)在11位、23位、26位、75位、104位、131位、168位、171位、194位、199位、269位、307位、308位、322位、357位、393位和414位任意一个或多个位置编码丝氨酸(s)的多核苷酸可选自tca、tct、tcc和agc及突变;viii)在27位、39位、50位、67位、77位、107位、111位、119位、121位、130位、135位、151位、155位、161位、164位、169位、188位、213位、222位、228位、250位、256位、275位、277位、287位、294位、298位、302位、305位、331位、353位、374位和430位任意一个或多个位置编码丙氨酸(a)的多核苷酸可选自gcg、gct、gcc和gca及突变;和ix)在7位、13位、15位、54位、57位、102位、106位、189位、201位、232位和273位任意一个或多个位置编码谷氨酰胺(q)的多核苷酸可选自cag和caa及突变,但多核苷酸突变不限于此。
[0059]
当选自构成酶的氨基酸序列中的苏氨酸(t)、天冬氨酸(d)、丝氨酸(s)和谷氨酸(e)的任意一个或多个氨基酸连续排列成两个相同氨基酸时,编码相同氨基酸中第一氨基酸的多核苷酸与编码第二氨基酸的多核苷酸可彼此不同,但不限于此。
[0060]
当选自构成酶的氨基酸序列中的脯氨酸(p)和缬氨酸(v)的任意一个或多个氨基酸连续排列成三个或更多相同氨基酸时,编码相同氨基酸的多核苷酸中编码至少两个氨基酸的多核苷酸可彼此相同,但不限于此。
[0061]
果糖-4-差向异构酶变体包括任意一种或多种选自以下的取代:在seq id no:2氨基酸序列中,a)用酪氨酸(y)取代97位对应的氨基酸,b)用色氨酸(w)取代124位对应的氨基酸和c)用缬氨酸(v)取代367位对应的氨基酸,在97位编码酪氨酸(y)的多核苷酸可以是tac,在124位编码色氨酸(w)的多核苷酸可以是tgg,在367位编码缬氨酸(v)的多核苷酸可以是gtt,但果糖-4-差向异构酶变体不限于此。
[0062]
突变的多核苷酸可具有选自以下的任意一种或多种核酸序列:seq id no:3、seq id no:4和seq id no:6,但不限于此。
[0063]
seq id no:3核酸序列可编码构成果糖-4-差向异构酶的seq id no:2氨基酸序列,seq id no:4核酸序列可编码构成果糖-4-差向异构酶变体的seq id no:5氨基酸序列,seq id no:6核酸序列可编码构成果糖-4-差向异构酶变体的seq id no:7氨基酸序列,但不限于此。
[0064]
特别地,在kosmotoga oelia衍生的果糖-4-差向异构酶的氨基酸序列(由seq id no:3核酸序列编码)中,seq id no:4和seq id no:6核酸序列可用适当碱基取代以实现选自以下的任意一种或多种氨基酸取代:a)用酪氨酸(y)取代97位对应的氨基酸,b)用色氨酸(w)取代124位对应的氨基酸和c)用缬氨酸(v)取代367位对应的氨基酸,但不限于此。用合适碱基取代可以是如上所述,在97位用tac取代编码酪氨酸(y)的多核苷酸,在124位用tgg取代编码色氨酸(w)的多核苷酸,在367位用gtt取代编码缬氨酸(v)的多核苷酸,但不限于此。
[0065]
由seq id no:3核酸序列编码的kosmotoga oelia衍生的果糖-4-差向异构酶的氨基酸序列,可翻译成seq id no:2氨基酸序列,但不限于此。
[0066]
本发明的突变的多核苷酸定义为具有选自以下的任意一种或多种核酸序列:seq id no:3、seq id no:4和seq id no:6,但不排除在seq id no:3、seq id no:4或seq id no:6核酸序列或者可能天然发生的突变或其沉默突变之前和之后加入无义序列,本领域技术人员清楚了解多核苷酸对应本发明的突变的多核苷酸,只要其显示与包括seq id no:3、seq id no:4或seq id no:6核酸序列的多核苷酸相同或对应的活性。作为一个具体示例,本发明的突变的多核苷酸可以是由以下组成的多核苷酸:seq id no:3、seq id no:4或seq id no:6核酸序列或与该核酸序列有80%、85%、90%、95%、96%、97%、98%或99%或更高同源性或相同性的核酸序列。显然,由其中一些序列缺失、修饰、取代或添加的核酸序列组成的多核苷酸也包括在本发明突变的多核苷酸范围内,只要该核酸序列具有这类同源性或相同性且显示对应突变的多核苷酸的功效。
[0067]
突变的多核苷酸可包括编码显示果糖-4-差向异构酶活性的蛋白的任意多核苷酸序列,其通过与从已知基因序列制备的探针杂交,例如在严格条件下与构成突变的多核苷酸的全部或部分核酸序列互补的序列,但不限于此。“严格条件”指多核苷酸之间能够发生特异性杂交的条件。这些条件在文献中有具体描述(j.sambrook et al.,molecular cloning,a laboratory manual,2nd edition,cold spring harbor laboratory press,cold spring harbor,new york,1989;f.m.ausubel et al.,current protocols in molecular biology,john wiley&sons,inc.,new york)。其示例包括某一条件,其中相互杂交的基因具有高同源性或相同性,即基因具有70%或更多、80%或更多、特别是85%或更多、特别是90%或更多、更特别是95%或更多、更加特别97%或更多、尤其特别99%或更多同源性或相同性,同源性或相同性低于此的基因彼此不杂交,或者某一条件,其进行一次洗涤,特别是2-3次,盐浓度和温度对应60℃、1x ssc和0.1%sds,特别是60℃、0.1x ssc和0.1%sds,更特别地是68℃、0.1x ssc和0.1%sds,这是常规southern杂交的洗涤条件。
[0068]
杂交需要两种多核苷酸具有互补序列,尽管碱基间的错配是可能的,这取决于杂交严格程度。术语“互补”用于描述能够相互杂交的核苷酸碱基之间的关系。例如,对于dna,腺苷与胸腺嘧啶互补,胞嘧啶与鸟嘌呤互补。因此,本发明也包括与基本相似多核苷酸序列以及整个序列互补的分离的多核苷酸片段。
[0069]
特别地,有同源性或相同性的多核苷酸可用杂交条件检测,包括在55℃ tm值和上述条件下的杂交步骤。tm值可以是60℃、63℃或65℃,但不限于此且可由本领域技术人员根据目的适当调整。
[0070]
用于杂交多核苷酸的合适严格性取决于多核苷酸长度和互补程度,并且参数为本
领域公知的。
[0071]
如本文所用,术语“同源性”或“相同性”指两种给定氨基酸序列或核酸序列彼此相关的程度且可表示为百分数。术语“同源性”和“相同性”通常可互换使用。
[0072]
保守多核苷酸或多肽的序列同源性或相同性通过标准对齐算法确定,由所用程序确定的默认间隙罚分可一起使用。基本上,同源或相同序列在中等或高严格条件下可彼此杂交至通常约50%、60%、70%、80%或90%或更多的整个序列或全长序列。对于杂交,多核苷酸也考虑包含简并密码子而不是密码子的多核苷酸。
[0073]
任意两种多核苷酸或多肽序列是否具有同源性、相似性或相同性,可用例如如pearson et al.(1988)proc.natl.acad.sci.usa 85:2444中的默认参数和已知计算机算法如“fasta”程序确定。或者,needleman
–
wunsch算法(needleman和wunsch,1970,j.mol.biol.48:443
–
453)如emboss包的needleman算法(emboss:the european molecular biology open software suite,rice et al.,2000,trends genet.16:276
–
277)(5.0.0或之后的版本)中实施的,可用于确定同源性、相似性或相同性(包括gcg程序包(devereux,j.et al.,nucleic acids research 12:387(1984)),blastp,blastn,fasta(atschul,s.f.et al.,j molec biol 215:403(1990);guide to huge computers,martin j.bishop,ed.,academic press,san diego,1994,and carillo et al.(1988)siam j applied math 48:1073)。例如,来自国家生物技术信息中心(national center for biotechnology information)的blast或clustalw可用于确定同源性、相似性或相同性。
[0074]
多核苷酸或多肽的同源性、相似性或相同性可通过比较序列信息来确定,例如用gap计算机程序如needleman et al.(1970),j mol biol.48:443,例如在smith和waterman,adv.appl.math(1981)2:482中已知。总之,同源性、相似性或相同性可定义为,在gap程序中将排列相似的符号(即核苷酸或氨基酸)的数量除以两种序列中较短序列中符号总数所得到的值。gap程序的默认参数可包括(1)二元比较矩阵(包含值1表示相同性和值0表示非相同性)和gribskovet al.(1986)nucl.acids res.14:6745(或ednafull(ncbi nuc4.4的emboss版)替代矩阵)的权重比较矩阵,如schwartz和dayhoff,eds.,atlas of protein sequence and structure,national biomedical research foundation,pp.353
–
358(1979)所公开;(2)各间隙的3.0罚分和对于每个间隙中每个符号的额外0.10罚分(或10的间隙开放罚分,0.5的间隙延伸罚分);和(3)末端间隙没有罚分。因此,如本文所用,术语“同源性”或“相同性”指序列之间的相关性。
[0075]
本发明的另一方面提供包含本发明突变的多核苷酸的载体。
[0076]
突变的多核苷酸如上所述。
[0077]
如本文所用,术语“载体”指包含编码靶多肽的多核苷酸的核酸序列的dna制品,其可操作连接合适控制序列,使得靶多肽能在合适宿主中表达。控制序列可包括能够起始转录的启动子,控制这类转录的任意操纵子序列,编码合适mrna核糖体结合位点的序列和控制转录及翻译终止的序列。转化入合适宿主细胞后,载体可独立于宿主基因组而复制或发挥功能,且可自身整合入基因组。
[0078]
载体可采用本发明的突变的多核苷酸可操作连接的形式。
[0079]
如本文所用,术语“可操作连接”一般指碱基表达控制序列和编码靶蛋白的核酸序列可操作连接以执行功能,从而影响编码核酸序列的表达。与载体的可操作连接可用本领
域已知的遗传重组技术构建,位点特异性dna剪切和连接可用本领域的裂解和连接酶等构建。
[0080]
本发明所用载体没有特别限制,可使用本领域已知任意载体。常用载体示例包括天然或重组状态的质粒、粘粒、病毒和噬菌体。例如,pwe15、m13、mbl3、mbl4、ixii、ashii、apii、t10、t11、charon4a、charon21a等可用作噬菌体载体或粘粒载体,phcp(韩国专利公开号10-2018-0092110)、pbr系统、puc系统、pbluescript ii系统、pgem系统、ptz系统、pcl系统、pet系统等可用作质粒载体。特别地,可使用pdz、pacyc177、pacyc184、pcl、peccg117、puc19、pbr322、pmw118和pcc1bac载体等。
[0081]
例如,编码靶多肽的多核苷酸可通过用于胞内染色体插入的载体来插入染色体。多核苷酸插入染色体可由本领域已知任意方法实施,例如同源重组,但不限于此。载体还可包含用于确定多核苷酸是否插入染色体的选择标记。选择标记用于选择转化有载体的细胞,即确认靶核酸分子是否插入,可使用赋予选择性表型如药物抗性、营养缺陷型、细胞毒素剂抗性或表面多肽表达的标记。在用选择性试剂处理的环境中,只有表达选择标记的细胞存活或显示其他表达性状,因此可选择转化细胞。本发明的另一方面是提供一种棒状杆菌属微生物,其表达kosmotoga oelia衍生的果糖-4-差向异构酶或其变体,所述微生物包含本发明的突变的多核苷酸或包含突变的多核苷酸的载体。
[0082]
突变的多核苷酸、载体、果糖-4-差向异构酶和果糖-4-差向异构酶变体如上所述。
[0083]
如本文所用,术语“表达kosmotoga oelia衍生的果糖-4-差向异构酶或其变体的微生物”指产生kosmotoga oelia衍生的果糖-4-差向异构酶或其变体的能力天然弱的微生物,或通过向不具有产生果糖-4-差向异构酶或其变体的能力的亲代菌株赋予产生kosmotoga oelia衍生的果糖-4-差向异构酶或其变体的能力而获得的微生物。为实现本发明的目的,微生物特定是表达果糖-4-差向异构酶或其变体的微生物,包含突变的多核苷酸或包含突变的多核苷酸的载体,且突变的多核苷酸可包括以下突变:i)编码亮氨酸(l)的多核苷酸选自ctc、ctg、ctt和ttg;ii)编码异亮氨酸(i)的多核苷酸选自atc和att;iii)编码苏氨酸(t)的多核苷酸选自act、acg和acc;iv)编码精氨酸(r)的多核苷酸选自cgt、cgc和cgg;v)编码甘氨酸(g)的多核苷酸选自ggc、ggt和gga;vi)编码缬氨酸(v)的多核苷酸选自gta、gtc、gtg和gtt;vii)编码丝氨酸(s)的多核苷酸选自tca、tct、tcc和agc;viii)编码丙氨酸(a)的多核苷酸选自gcg、gct、gcc和gca;和ix)编码谷氨酰胺(q)的多核苷酸选自cag和caa,但不限于此。
[0084]
微生物可以是通过向宿主细胞引入包含突变的多核苷酸的载体的方法构建的重组微生物。转化载体的方法可包括向细胞引入多核苷酸的任意方法,可选择本领域已知的合适标准技术来完成。例如,所述方法能包括电穿孔、磷酸钙共沉淀、逆转录病毒感染、显微注射、deae
–
葡聚糖、阳离子脂质体法和热激法,但不限于此。
[0085]
如本文所用,术语“转化”指向宿主细胞引入包含编码靶蛋白的多核苷酸的载体,从而多核苷酸编码的蛋白可在宿主细胞中表达。
[0086]
转化基因可包括插入宿主细胞染色体的形式和位于染色体外的形式,只要其能在宿主细胞中表达。基因包括dna和rna作为多核苷酸,且任何基因可无限制地使用,只要其能引入宿主细胞并在宿主细胞中表达。例如,基因可以表达盒形式引入宿主细胞,其是包括自身表达所需全部元件的多核苷酸构建体。表达盒通常能包括与基因可操作连接的启动子、
转录终止信号、核糖体结合位点和翻译终止信号。表达盒可采用能够自复制的重组载体形式。基因可以自身形式或多核苷酸构建体形式引入宿主细胞,并可操作地连接宿主细胞中表达所需的序列。
[0087]
如本文所用,术语“从而表达多核苷酸或多肽/表达多核苷酸或多肽”指将靶多核苷酸或多肽引入微生物或修饰,从而在微生物中表达的状态,以及当多核苷酸或多肽是微生物中存在的蛋白时,与修饰前的固有活性或活性相比,多核苷酸或多肽的活性增强的状态。
[0088]
特别地,“引入多肽(或蛋白)”指与靶多肽的修饰前固有活性或活性相比,显示活性提高,或微生物显示微生物最初不具有的特定多肽的活性。例如,编码特定多肽的多核苷酸引入微生物的染色体,或包含编码特定多肽的多核苷酸的载体引入微生物且显示特定多肽活性。“活性增强”指与微生物所具有的特定多肽修饰之前的固有活性或活性相比,活性得到提高。“固有活性”指当微生物特性通过天然或人为因素引起的基因突变而改变时,亲代菌株在转化前原有的特定多肽活性。
[0089]
特别地,本发明的活性增强可以是
[0090]
1)编码蛋白或其酶变体的基因胞的内拷贝数增加;
[0091]
2)向编码蛋白或其酶变体的基因的表达控制序列引入突变;
[0092]
3)用显示强活性的序列取代编码蛋白或其酶变体的基因的表达控制序列;
[0093]
4)用突变的多核苷酸取代染色体上编码天然蛋白的基因;
[0094]
5)向编码蛋白或其酶变体的基因额外引入突变,以提高蛋白或其酶变体活性;
[0095]
6)向微生物引入蛋白或其酶变体;或
[0096]
7)两种或更多选自上面1)-6)的组合,但不限于此。
[0097]
在上面,基因的拷贝数增加不受特别限制,而可以以基因可操作连接载体的形式进行,或可通过基因插入宿主细胞染色体来进行。特别地,载体(与本发明的突变的多核苷酸可操作连接)能够独立于宿主而复制和发挥功能,可引入宿主细胞。或者,载体(与突变的多核苷酸可操作连接)能够插入突变的多核苷酸到宿主细胞染色体,可引入宿主细胞染色体。插入突变的多核苷酸到染色体可通过本领域已知的任何方法实现,例如通过同源重组。
[0098]
其次,修饰表达控制序列以增加突变的多核苷酸表达,不特定限于此,但可以通过缺失、插入或者非保守或保守取代核酸序列或其组合来诱导序列突变,以进一步增强表达控制序列活性,或通过用显示更强活性的核酸序列取代表达控制序列来进行。表达控制序列不特定限于此,可包括启动子、操纵子序列、编码核糖体结合位点的序列、控制转录和翻译终止的序列等。
[0099]
强启动子可连接突变的多核苷酸表达单元的上部,而不是原始启动子,但启动子不限于此。已知强启动子示例包括cj1-cj7启动子(韩国专利号10-0620092)、iac启动子、trp启动子、trc启动子、tac启动子、lambda噬菌体pr启动子、pl启动子、tet启动子、gapa启动子、spl7启动子、spl13(sm3)启动子(韩国专利号10-1783170)、o2启动子(韩国专利号10-1632642)、tkt启动子和ycca启动子,但启动子不限于此。
[0100]
修饰染色体上的突变的多核苷酸序列不特定限于此,但可以通过缺失、插入或者非保守或保守取代核酸序列或其组合来诱导表达控制序列突变,以进一步提高突变的多核苷酸活性,或通过用突变的多核苷酸序列取代该突变的多核苷酸序列以进一步增强活性来
进行。
[0101]
基于野生型或未修饰微生物菌株中多肽的表达、活性或浓度,这种引入靶多肽(或蛋白)和增强活性可以是增加对应多肽的表达、活性或浓度,但不限于此。
[0102]
如本文所用,术语“未修饰微生物”不排除包括在微生物中可能天然出现的突变的菌株,但是指天然菌株本身,或不包含突变的多核苷酸和编码靶多肽基因的微生物,或未用包含突变的多核苷酸和编码靶多肽基因载体转化的微生物。
[0103]
为实现本发明的目的,靶多肽可以是果糖-4-差向异构酶或其变体,但不限于此。
[0104]
重组微生物可包括原核微生物和真核微生物,只要其是包含本发明突变的多核苷酸或包含突变的多核苷酸的载体并因此能产生果糖-4-差向异构酶或其变体的微生物。重组微生物可包括属于例如埃希氏菌(escherichia)属、欧文氏菌(erwinia)属、沙雷氏菌(serratia)属、普罗威登斯菌(providencia)属、棒状杆菌(corynebacterium)属和短杆菌(brevibacterium)属的微生物菌株,特别是棒状杆菌属。例如,棒状杆菌属可以是谷氨酸棒杆菌(corynebacterium glutamicum)、产氨棒杆菌(corynebacterium ammoniagenes)、corynebacterium crudilactis、corynebacterium deserti、有效棒杆菌(corynebacterium efficiens)、帚石南棒杆菌(corynebacterium callunae)、corynebacterium stationis、corynebacterium singulare、corynebacterium halotolerans、纹带棒杆菌(corynebacterium striatum)、corynebacterium pollutisoli、corynebacterium imitans、corynebacterium testudinoris或corynebacterium flavescens,更特别是谷氨酸棒杆菌,但重组微生物不限于此。
[0105]
为实现本发明的目的,重组微生物可以是产生比野生型或未修饰微生物菌株更大量的果糖-4-差向异构酶或其变体的微生物。
[0106]
本发明的微生物可包括除了引入核酸或载体外,通过各种已知方法能够表达本发明的果糖-4-差向异构酶或其变体的所有微生物。
[0107]
本发明的另一方面是提供产生果糖-4-差向异构酶或其变体的方法,所述方法包括在培养基中培养棒状杆菌属的微生物,所述微生物包含本发明所述的突变的多核苷酸或包含所述突变的多核苷酸的载体。
[0108]
突变的多核苷酸、载体、果糖-4-差向异构酶、果糖-4-差向异构酶变体和微生物如上所述。
[0109]
为实现本发明的目的,棒状杆菌属微生物是可表达kosmotoga oelia衍生的果糖-4-差向异构酶或其变体的微生物,但不限于此。
[0110]
如本文所用,术语“培养”指在适当控制的环境条件下培养微生物。本发明的培养工艺可根据本领域已知适当培养基和培养条件实施。这种培养工艺可根据选定菌株由本领域技术人员方便地调整和使用。特别地,培养可以是分批培养、连续培养和补料分批培养,但不限于此。
[0111]
如本文所用,术语“培养基”指混合培养微生物所需的营养物作为主要成分的材料,并提供生存和发育所必要的包括水在内的营养物和生长因子。特别地,作为用于培养本发明微生物的培养基和其他培养条件,可使用任意培养基,而没有任何特别限制,只要其是常规用于培养微生物的培养基。本发明的微生物能在常规培养基中培养,所述培养基包含适当碳源、氮源、磷源、无机化合物、氨基酸和/或维生素等,处于需氧条件下,同时控制温
4-差向异构酶或其变体的微生物,但不限于此。
[0125]
产生塔格糖的组合物还可包含果糖,但不限于此。
[0126]
本发明中产生塔格糖的组合物还可包含任意适当赋形剂,其常用于产生塔格糖的组合物。例如,这类赋形剂可以是防腐剂、湿润剂、分散剂、悬浮剂、缓冲剂、稳定剂或等渗剂,但不限于此。
[0127]
本发明中产生塔格糖的组合物还可包含金属离子或金属盐。在一个实施方案中,所述金属离子或金属盐的金属可以是含二价阳离子的金属。特别地,本发明的金属可以是镍(ni)、铁(fe)、钴(co)、镁(mg)或锰(mn)。更特别地,金属盐可以是mgso4、feso4、niso4、nicl2、mgcl2、coso4、mncl2或mnso4。
[0128]
本发明的另一方面提供一种制备塔格糖的方法,所述方法包括使棒状杆菌属微生物;或所述微生物的培养物与果糖接触,所述微生物包含本发明的突变的多核苷酸或包含所述突变的多核苷酸的载体。
[0129]
突变的多核苷酸、载体、果糖-4-差向异构酶、果糖-4-差向异构酶变体和微生物如上所述。
[0130]
为实现本发明的目的,棒状杆菌属微生物是可表达kosmotoga oelia衍生的果糖-4-差向异构酶或其变体的微生物,但不限于此。
[0131]
使棒状杆菌属微生物或微生物的培养物与果糖接触的步骤可以是使棒状杆菌属微生物或微生物的培养物接触果糖以将果糖转变成塔格糖的步骤,但不限于此。
[0132]
果糖-4-差向异构酶变体可用作果糖-4-差向异构酶以从果糖制备塔格糖,但不限于此。
[0133]
例如,本发明的接触可在ph 5.0-ph 9.0条件和30℃-80℃温度条件和/或持续0.5小时-48小时下进行。特别地,本发明的接触可在ph 6.0-ph 9.0条件或ph 7.0-ph 9.0条件下进行。本发明的接触可在35℃-80℃、40℃-80℃、45℃-80℃、50℃-80℃、55℃-80℃、60℃-80℃、30℃-70℃、35℃-70℃、40℃-70℃、45℃-70℃、50℃-70℃、55℃-70℃、60℃-70℃、30℃-65℃、35℃-65℃、40℃-65℃、45℃-65℃、50℃-65℃、55℃-65℃、30℃-60℃、35℃-60℃、40℃-60℃、45℃-60℃、50℃-60℃或55℃-60℃温度条件下进行。本发明的接触可进行0.5小时-36小时、0.5小时-24小时、0.5小时-12小时、0.5小时-6小时、1小时-48小时、1小时-36小时、1小时-24小时、1小时-12小时、1小时-6小时、3小时-48小时、3小时-36小时、3小时-24小时、3小时-12小时、3小时-6小时、6小时-48小时、6小时-36小时、6小时-24小时、6小时-12小时、12小时-48小时、12小时-36小时、12小时-24小时、18小时-48小时、18小时-36小时或18小时-30小时。
[0134]
本发明的接触可在金属离子或金属盐存在下进行。可以使用的金属离子或金属盐与上述方面的那些相同。
[0135]
本发明的制备方法还可包括分离和/或纯化所制备塔格糖的步骤。分离和/或纯化可以通过本发明技术领域常用方法实施。作为非限制性示例,可使用透析、沉淀、吸附、电泳、离子交换层析和分级结晶。纯化可以仅通过一种方法或者两种或更多方法实施。
[0136]
本发明的制备方法还可包括在分离和/或纯化步骤之前或之后实施脱色和/或脱盐的步骤。通过脱色和/或脱盐,可以获得质量优异的塔格糖。
[0137]
作为另一示例,本发明的制备方法还可包括在果糖转化成塔格糖步骤、分离和/或
纯化步骤或本发明的脱色和/或脱盐步骤后,使塔格糖结晶的步骤。结晶可以通过常用结晶方法实施。例如,结晶可通过冷却结晶法实施。
[0138]
本发明的制备方法还可包括在结晶步骤前浓缩塔格糖的步骤。浓缩可以增加结晶效率。
[0139]
作为另一示例,本发明的制备方法还可包括在本发明的分离和/或纯化步骤后,使未反应果糖接触本发明的酶、表达酶的微生物或微生物培养物的步骤;在本发明的结晶步骤后,再利用从分离和/或纯化步骤中得到的母液;或其组合。
[0140]
实施例
[0141]
在下文中,将参照实施例和实验实施例更详细地描述本发明。然而,这些实施例和实验实施例用于阐明本发明的目的,本发明范围不限于这些实施例和实验实施例。
[0142]
实施例1:验证表达自突变的多核苷酸的kosmotoga oelia衍生的果糖-4-差向异构酶的表达水平
[0143]
为了增加棒状杆菌菌株(谷氨酸棒杆菌(c.glutamicum))中韩国专利公开号10-2018-0111678a已知的kosmotoga oelia衍生的果糖-4-差向异构酶的基因表达效率,构建突变的多核苷酸的果糖-4-差向异构酶基因(seq id no:3)。加入6x his-标签序列以用于果糖-4-差向异构酶基因构建期间的分离。
[0144]
作为质粒,phcp质粒用于高拷贝数,其中orfa2(parb)的21位突变成腺嘌呤(a)(韩国专利公开号10-2018-0092110a)。本发明中,尝试获得比现有phcp拷贝数更高的质粒。为此,随机改变和筛选98bp序列,该序列是phcp的ctrna部分。因此,最终鉴定ctrna部分第22个核苷酸用c(胞嘧啶)取代的多核苷酸和第79个核苷酸用c(胞嘧啶)取代的多核苷酸。含有此的高拷贝数质粒名为phcp7载体(seq id no:8),并用载体构建含有果糖-4-差向异构酶基因序列的质粒。
[0145]
各突变果糖-4-差向异构酶基因插入phcp7载体,转化入棒状杆菌菌株(谷氨酸棒杆菌atcc13032)。转化的棒状杆菌菌株在10ml bhi培养基(包含25μg/ml卡那霉素(km))中30℃,200rpm搅拌下培养24小时。之后,培养基以1/100体积比置于50ml新鲜bhi培养基(包含25μg/ml km)并在30℃,200rpm搅拌下培养24小时。
[0146]
培养的菌株在o.d 600nm为4时回收,悬浮于300μl pbs,在冰桶中超声波处理(以50%脉冲和20%幅度,总共7分钟)。通过离心破裂菌株获得的上清与5x样品缓冲液混合,100℃加热5分钟。混合物在12%sds-page上加样后,采用考马斯亮蓝的染色液和脱色液鉴定蛋白。为分析蛋白表达水平,总蛋白中果糖-4-差向异构酶的表达水平用凝胶分析仪程序确认。
[0147]
结果,如图1所示,证实表达突变的多核苷酸表达的果糖-4-差向异构酶的表达水平相较果糖-4-差向异构酶野生型(突变前)多核苷酸(wt)表达的表达水平增加约6%或更多。
[0148]
实施例2:验证表达自突变的多核苷酸的果糖-4-差向异构酶的塔格糖转化率
[0149]
在3,500rpm和4℃持续10分钟,45ml的实施例1中所培养棒状杆菌菌株培养液进行离心,随后用10ml tris-hcl(ph 8.0)缓冲液洗涤。之后,在与上面相同的条件下实施离心并测重。将相当于回收菌株总反应体积20%重量的量接种于2ml管,在60℃进行30分钟的加热预处理。塔格糖转化反应中待加入的coso4或niso4也接受加热预处理。菌株和含底物
(30%果糖)的50mm tris-hcl(ph 8.0)及3mm coso4或niso4一起混合,60℃反应2小时。反应完成后,样品在13,000rpm和4℃离心10分钟以回收上清,上清通过hplc分析。对于hplc,采用aminex hpx-87h柱,其使用5mm h2so4溶剂,分析产生的塔格糖量。
[0150]
结果,如图2所示,证实表达自突变的多核苷酸的果糖-4-差向异构酶的转化率为约22%,这比wt(#7_ko(knf4e))高多至7%。
[0151]
实施例3:验证表达自突变的多核苷酸的果糖-4-差向异构酶变体的表达水平
[0152]
进行实验以确认即使实施例1的kosmotoga oelia衍生的果糖-4-差向异构酶中的一些氨基酸序列突变,其表达水平是否增加。分别构建通过在果糖-4-差向异构酶基因(seq id no:3)中突变氨基酸获得的两种酶变体(n97y、t124w、n367v突变:seq id no:4,t124w突变:seq id no:6)的基因序列,其是突变的多核苷酸。含有酶变体(seq id no:4)的菌株名为谷氨酸棒杆菌cf01-0014,在2019年10月18日保藏于韩国微生物保藏中心,该中心是布达佩斯条约下的受托机构,登录号为kccm12610p。
[0153]
各突变果糖-4-差向异构酶基因插入phcp7载体,将其引入棒状杆菌菌株,按照实施例1的方法通过western印迹确认菌株中两种酶变体的表达水平。
[0154]
结果,如图3所示,证实表达自突变的多核苷酸的果糖-4-差向异构酶n97y、t124w、n367v变体(泳道4)的表达水平相较wt(泳道2)增加约8%,t124w变体(泳道5)的表达水平相较果糖-4-差向异构酶野生型(突变前)多核苷酸(wt)增加约12%或更多,证实表达水平与表达自突变的多核苷酸的果糖-4-差向异构酶(泳道3)相似。
[0155]
实施例4:验证表达自突变的多核苷酸的果糖-4-差向异构酶变体的塔格糖转化率
[0156]
实施例3中两种酶变体的塔格糖转化率通过实施例2的方法确认。
[0157]
结果,如图4所示,证实n97y、t124w、n367v变体(3aa突变)的塔格糖转化率为约32%,相较wt增加19%。t124w变体的塔格糖转化率也高达27.8%。
[0158]
对比例1:验证应用相同核苷酸突变的新阿波罗栖热袍菌衍生的果糖-4-差向异构酶的表达水平和塔格糖转化率
[0159]
构建了突变的多核苷酸变体2和变体1(seq id no:12和13),其中与实施例1那些相同的核苷酸突变应用于编码从韩国专利公开号10-2017-0015250a已知的新阿波罗栖热袍菌衍生的果糖-4-差向异构酶(己糖醛酸c4-差向异构酶,seq id no:9)的变体(seq id no:10)的核酸序列(seq id no:9),将这些插入phcp载体,将这些引入棒状杆菌菌株,随后通过实施例1和2的方法确认表达水平和塔格糖转化率。
[0160]
结果,如图5所示,表达自突变的多核苷酸的果糖-4-差向异构酶变体(变体1/tn_变体_1,变体2/tn_变体_2,cj)的表达水平低于wt,果糖-4-差向异构酶变体的塔格糖转化率也低于wt(图6)。
[0161]
特别地,在韩国专利公开号10-2017-0015250a中,果糖-4-差向异构酶变体显示的活性高于野生型(突变前)果糖-4-差向异构酶,但证实当酶变体的多核苷酸突变时,活性低于野生型(突变前)果糖-4-差向异构酶,因而表达水平显著减少。
[0162]
因此,证实本发明所述核苷酸突变对kosmotoga oelia衍生的酶是有效的。
[0163]
基于上面描述,本领域技术人员应理解本发明可以不同具体形式实施,而不改变其技术精神或基本特征。因此,应理解上述实施方案并非限制性的,而是在所有方面都是示例性的。本发明范围由所附权利要求定义,而不是其之前的描述,因此落入权利要求的范围
或这些范围的等同物的所有变化和修改旨在被权利要求所涵盖。
[0164]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1