外核苷酸焦磷酸酶/磷酸二酯酶1(ENPP1)抑制剂及其使用方法与流程
外核苷酸焦磷酸酶/磷酸二酯酶1(enpp1)抑制剂及其使用方法
技术领域
1.本发明一般涉及外核苷酸焦磷酸酶/磷酸二酯酶(enpp1)的抑制剂。本发明涉及含有式1或式2化合物的药物组合物以及使用这些化合物或组合物治疗 enpp1过度表达的各种类型的人类癌症、心血管、糖尿病、肥胖、非酒精性脂肪性肝炎、青光眼、抗病毒、抗菌和抗纤维化治疗剂的方法。本发明还涉及制备化合物和其药物盐的方法。
背景技术:
2.外核苷酸焦磷酸酶/磷酸二酯酶(enpp)家族成员包含七种同种型,enpp1-7,其为ii型跨膜糖蛋白或胞外酶。来自370多个蛋白质靶标的质谱和蛋白质组学分析表明,胞外蛋白enpp1是表现出高水解活性的热门基因之一。atp是经鉴定的enpp1的底物,其水解为amp和ppi。cd73将amp转化为腺苷和无机磷酸(pi)。动力学实验数据表明enpp1能够水解atp。这些外核苷酸酶参与胞外核苷酸中的焦磷酸(ppi)和磷酸二酯键的水解;如三磷酸、寡核苷酸,并且其产生核苷5'-单磷酸。关键的同种型之一,enpp1(浆细胞膜糖蛋白-1,pc-1)参与许多生理过程,如发育、形成和运输,以及病理生理病状。相对于正常乳腺上皮,已经在乳腺癌中检测到enpp1表达异常,这是其在骨转移(在大约80%病例中发生)、霍奇金氏淋巴瘤、肝细胞癌、滤泡性淋巴瘤、成胶质细胞瘤以及其它恶性肿瘤组织中发展潜力的证据。
3.最近的报道表明,环状二核苷酸(cdn),enpp1的底物,通过干扰素基因的sting依赖性活化来刺激先天免疫。sting路径活化的enpp1抑制对于肿瘤控制是关键的,类似于检查点抑制剂,如抗pd-1或pd-l1的抑制,所述检查点抑制剂是用于各种癌症的有希望的免疫疗法。另外,enpp1中的突变与若干种病症相关,包含婴儿动脉钙化(婴儿期广泛性动脉钙化或gaci)、脊柱的后纵韧带的骨化以及胰岛素信号传导和抗性。enpp1表达在骨和软骨中很高,并且涉及肺和肾纤维化。还发现enpp1的表达与星形细胞肿瘤的等级之间的相关性。另一项研究报道需要enpp1来维持成胶质细胞瘤干细胞样细胞的未分化和增殖状态。因此,enpp1是开发新型抗癌、心血管、糖尿病、肥胖、非酒精性脂肪性肝炎、青光眼和抗纤维化治疗剂的有吸引力的药物靶点。
4.根据对mda-mb231细胞的直接结合测定和体外细胞功效两者进一步研究了enpp1活性的重要性。enpp1的基于sirna的敲低在细胞特异性和体内实验两者中均显著降低其催化活性。这些实验证明,enpp1活性在用sirna治疗后被消除。这进一步支持此靶标在某些疾病中的有效性。最近已经显示,内源 cgamp的二硫代磷酸酯类似物对enpp1磷酸二酯酶的水解具有抗性,并且特别是环状二核苷酸(cdn)在通过抑制enpp1活性和同时抑制sting活化反应的机制诱导人thp1细胞中的ifn-β分泌方面更有效。
5.有充分证据表明enpp1表达相对于正常乳腺上皮在人原发性乳腺肿瘤中是显著的,其中在乳腺-骨转移中观察到最高水平。这些数据不仅支持enpp1在乳腺-骨转移中的潜在作用,而且支持作为乳腺癌的潜在预后标志物。最近,enpp1 显示在肺癌中上调。肺癌细胞系hcc827和a549中enpp1的敲低导致抑制结肠形成、体外锚定非依赖性生长和体内致瘤
性。这些来自靶标验证实验的结果清楚地支持enpp1在开发新型癌症免疫疗法方面的药理作用。
6.此外,enpp1活性还涉及由细菌和/或病毒引起的疾病,并且因此enpp1 的调节剂可以用于治疗细菌和/或病毒疾病和病状。
技术实现要素:
7.在一个方面,本发明涉及如下式i或式ii化合物:
[0008][0009]
其中
[0010]
x是n或cr11;
[0011]
y选自包括-cr4r5-、-nr6-、-n(ch2)mo-、-o-、-s-、-s(o)-、-s(o)2、芳基和杂芳基的基团;其中m是2或3;
[0012]
l选自包括c1-c5烷基和c1-c5烯基的基团;
[0013]
每个r1、r2和r3独立地选自包括氢、卤素、cn、ora、-c(=o)nrbrc、
ꢀ‑
nrbrc、-c(=o)rd、芳基、杂芳基、环烷基和杂环烷基的基团。
[0014]
每个ra独立地选自包括氢、低级烷基、-(ch2)n-c(=o)nrbrc、芳烷基、芳基、杂芳基、杂环烷基和环烷基的基团;
[0015]
其中n是1到3之间的整数
[0016]
每个rb和rc独立地选自包括氢、低级烷基和低级芳基、杂环烷基或环烷基的基团;
[0017]
每个rd独立地选自包括-ore和低级烷基的基团;
[0018]
每个re独立地选自包括氢、低级烷基和低级芳基的基团;
[0019]
r11独立地选自包括氢、卤素、cooet、cooh和cn的基团;
[0020]
r4、r5和r6独立地选自包括氢和低级烷基的基团;
[0021]
或其异构体、水合物、溶剂化物、多晶型物、互变异构体或药学上可接受的盐。
[0022]
式ii的化合物如下:
[0023][0024]
其中
[0025]
x是n或cr11;
[0026]
z是c或n;
[0027]
w选自包括c1-c5烷基、-c(=o)-(ch2)n-、-(c1-c5烷基)-n-的基团;nh 和直接键如下:
[0028]
每个r1、r2和r3独立地选自包括氢、卤素、cn、ora、-c(=o)nrbrc、
ꢀ‑
nrbrc、-c(=o)rd、芳基、杂芳基、环烷基和杂环烷基的基团。
[0029]
每个ra独立地选自包括氢、低级烷基和-(ch2)n-c(=o)nrbrc、芳烷基、芳基、杂芳基、杂环烷基、环烷基的基团;
[0030]
其中n是1到3之间的整数;
[0031]
每个rb和rc独立地选自包括氢、低级烷基和低级芳基、杂环烷基或环烷基的基团;
[0032]
每个rd独立地选自包括-ore和低级烷基的基团;
[0033]
每个re独立地选自包括氢、低级烷基和低级芳基的基团;
[0034]
r11独立地选自包括氢、卤素、cooet、cooh和cn的基团;
[0035]
r7、r8和r9独立地选自包括h、卤素和低级烷基的基团;并且r8和r9 也可以在具有1个或2个原子的7元环上形成桥,如下:
[0036][0037]
r10独立地选自包括氢和cf3的基团;
[0038]
或其异构体、水合物、溶剂化物、多晶型物、互变异构体或药学上可接受的盐。
[0039]
本发明包含任何化合物或结构,其包括上述取代基的任何组合。
[0040]
在一个优选的实施方式中,式i中的y是吡啶基。
[0041]
在一个优选的实施方式中,式i或式ii中的x是c-cn。
[0042]
在一个优选的实施方式中,式i中的y是nr6。
[0043]
在一个优选的实施方式中,在式i和式ii的化合物中,r1、r2和r3选自包括ch3o和h的基团。
[0044]
在一个优选的实施方式中,在式ii化合物中,z是n。
[0045]
在一个优选的实施方式中,在式ii化合物中,w选自包括-4,5-咪唑、2-恶唑、3-吡咯;吡唑和噻唑的基团。
[0046]
在一个优选的实施方式中,在式ii化合物中,x是n。
[0047]
在一个优选的实施方式中,在式ii化合物中,x是c-cn。
[0048]
在一个优选的实施方式中,在式ii化合物中,r7、r8和r9独立地选自包括h和卤素的基团。
[0049]
在一个优选的实施方式中,在式ii化合物中,r7是卤素,更优选f。
[0050]
在一个优选的实施方式中,
[0051]
该化合物具有式i;
[0052]
x是n;
[0053]
y选自包括吡啶基、c1-c5烷基、o、n和s的基团;
[0054]
l是任选取代的c1-c5烷基;和
[0055]
r1和r2都是ch3o。
[0056]
在另一个优选的实施方式中,
[0057]
该化合物具有式ii;
[0058]
x是n;
[0059]
z是n;
[0060]
w选自任选取代的包括c1-c5烷基、-c(=o)-(ch2)-、-(任选取代的c1-c5 烷基)-n的基团;和直接键;和
[0061]
r1和r2都是ch3o。
[0062]
所提供的化合物的实施例包含:
[0063]
[0064]
[0065]
[0066]
[0067]
[0068][0069]
本发明还包含所述化合物的水合物、溶剂化物、多晶型物、异构体、互变异构体、所述化合物的药学上可接受的盐以及所述互变异构体的药学上可接受的盐。
[0070]
本发明还提供了药物制剂、包含化合物的药物、制备药物制剂、药物、化合物的方法以及用所提供的药物制剂和化合物治疗患者的方法。
[0071]
通过基于结构的、计算对接和结合自由能来鉴定本发明的化合物。
[0072]
还公开了药物组合物,其包括治疗有效量的所公开化合物以及药学上可接受的载体。
[0073]
还公开了用于制备所公开化合物的合成方法。在另外的方面,公开了所公开的合成方法的产物。
[0074]
还公开了用于治疗哺乳动物中与enpp1活性功能障碍相关的病症的方法,所述方法包括向所述哺乳动物施用治疗有效量的所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物的步骤。
[0075]
还公开了用于抑制哺乳动物的enpp1活性的方法,所述方法包括向所述哺乳动物施用治疗有效量的至少一种所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物的步骤。
[0076]
还公开了用于抑制至少一个细胞的enpp1活性的方法,所述方法包括使所述至少一个细胞与有效量的至少一种所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物接触的步骤。
[0077]
还公开了通过引发哺乳动物的免疫疗法反应来治疗与所述哺乳动物的 enpp1活性功能障碍相关的病症的方法,所述方法包括向所述哺乳动物施用治疗有效量的所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物,其中所述化合物引起在治疗与enpp1活性相关的所述病症中有益的免疫疗法应答。这种病症可以是但不限于由涉及enpp1活性的细菌和/或病毒引起的任何类型的癌症或任何疾病。本发明化合物可治疗的疾病和状况包括但不限于癌症、心血管疾病、糖尿病、肥胖、非酒精性脂肪性肝炎、青光眼、纤维化抗病毒药物、抗菌和抗纤维化治疗剂。
[0078]
还公开了药物组合物,其包括药学上可接受的载体和有效量的所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物。
[0079]
还公开了试剂盒,其包括至少一种所公开化合物、或其药学上可接受的盐、互变异构体、异构体、水合物、溶剂化物或多晶型物。
[0080]
还公开了用于制造药物的方法,所述方法包括将至少一种所公开化合物或至少一种所公开产品与药学上可接受的载体或稀释剂组合。在另外的方面,本发明涉及所公开化合物在制造用于治疗与enpp1活性功能障碍相关的病症的药物中的用途。在另外的方面,本
发明涉及所公开化合物在制造用于治疗不受控细胞增殖病症的药物中的用途。
[0081]
还公开了所公开化合物或所公开产品在制造用于治疗与哺乳动物的enpp1 功能障碍相关的病症的药物中的用途。
[0082]
尽管可以以特定的法定类别,如系统法定类别来描述和要求保护本发明的方面,但是这仅是为了方便起见,并且本领域的技术人员将理解,可以以任何法定类别来描述和要求保护本发明的每个方面。除非另有明确说明,否则不旨在将本文中所阐述的任何方法或方面解释为要求以特定顺序执行其步骤。因此,在方法权利要求在权利要求书或说明书中未具体陈述步骤被限制为特定顺序的情况下,在任何方面,绝不旨在推断顺序。这适用于任何可能的用于解释的非表达基础,包含关于步骤安排或操作流程的逻辑的事项、从语法组织或标点得到的普通含义或在说明书中描述的方面的数量或类型。
附图说明
[0083]
图1显示了本发明化合物对转染的hek293t细胞裂解物的enpp抑制图。
[0084]
图2显示了hpac细胞中的免疫渗透测定结果。
[0085]
图3显示了化合物015-hcl在大鼠中的pk简介。
[0086]
图4a显示了化合物015-hcl对肿瘤的体内抑制。
[0087]
图4b显示了化合物015-hcl与放射治疗组合对肿瘤的体内抑制。
具体实施方式
[0088]
定义
[0089]
如本文所使用的,包含有机化合物的化合物的命名法可以使用通用名称、 iupac、iubmb或cas命名法建议给出。当存在一个或更多个立体化学特征时,可以采用用于立体化学的cahn-ingold-prelog规则来指定立体化学优先级、e/z 规范等。如果给出名称,本领域的技术人员可以容易地确定化合物的结构,通过使用命名惯例的化合物结构的系统性降低或通过可商购获得的软件,如 chemdraw
tm
(美国剑桥软件公司)。
[0090]
如在说明书和所附权利要求书中所使用的单数形式“一个(a)”、“一种(an)”以及“所述(the)”包含复数指示物,除非上下文另外清楚地指明。因此,例如,提及“官能团”、“烷基”或“残基”包含两种或更多种此类官能团、烷基或残基等的混合物。
[0091]
在本文中,范围可以表示为从“约”一个特定值和/或到“约”另一个特定值。当表达这种范围时,另外的方面包含从一个特定值和/或到另一个特定值。类似地,当通过使用先行词“约”来将值表示为近似值时,应当理解的是所述特定值形成了另外的方面。还应当理解,每个范围的端值在与其它端值相关和独立于其它端值的情况下均为重要的。还应理解,本文公开了多个值,并且每个值在本文中还被公开为“约”为除了所述值本身之外的所述特定值。例如,如果公开了值“10”,则还公开了“约10”。还应理解,还公开了两个特定单元之间的每个单元。例如,如果公开了10和15,则还公开了11、12、13和14。
[0092]
在说明书和最后的权利要求书中对组合物中的特定元素或组分的重量份的提及,表示所述组合物或物品中的元素或组分与任何其它元素或组分之间的重量关系,对此表达为重量份。因此,在含有2重量份的组分x与5重量份的组分y的化合物中,x和y以2:5的重量比存在,并且不管化合物中是否还含有其它组分都以该比率存在。
[0093]
除非具体地相反地指出,否则组分的重量百分比(wt%)基于包含所述组分的制剂或组合物的总重量。
[0094]
如本文所使用的,术语“enpp1”是指外核苷酸焦磷酸酶/磷酸二酯酶。
[0095]
如本文所使用的,术语“任选的”或“任选地”意指随后描述的事件或情况可以发生或可以不发生,并且所述描述包含所述事件或情况发生的实施例以及事件或情况没有发生的实施例。
[0096]
如本文所使用的,术语“受试者”可以是脊椎动物,如哺乳动物、鱼、鸟、爬行动物或两栖动物。因此,本文公开的方法的受试者可以是人、非人灵长类动物、马、猪、兔、狗、绵羊、山羊、牛、猫、豚鼠或啮齿动物。所述术语不指示具体的年龄或性别。因此,旨在涵盖成人及新生的受试者以及胎儿,无论是男性还是女性。在一方面,所述受试者是哺乳动物。患者是指患有疾病或病症的受试者。术语“患者”包含人类和牲畜受试者。在公开的方法的一些方面,在施用步骤之前,已经诊断出受试者需要治疗与enpp1功能障碍相关的不受控细胞增殖病症。在公开的方法的一些方面,在施用步骤之前,已经诊断出受试者需要抑制enpp1。
[0097]
如本文所使用的,术语“治疗”是指对患者的医疗管理,旨在治愈、改善、稳定或预防疾病、病理病状或病症。此术语包含积极治疗,即特异性针对疾病、病理病状或病症的改善的治疗,并且还包含病因治疗,即针对相关疾病、病理病状或病症的病因的去除的治疗。另外,此术语包含姑息性治疗,即设计用于缓解症状而非治愈疾病、病理病状或病症的治疗;预防性治疗,即针对最小化或部分或完全抑制相关疾病、病理病状或病症的发展的治疗;以及支持性治疗,即用于补充针对相关疾病、病理病状或病症的改善的另一种特异性疗法的治疗。在各个方面中,术语涵盖对受试者,包含哺乳动物(例如,人)的任何治疗,并且包含:(i)防止疾病在可能倾向于患有疾病但尚未被诊断为患有疾病的受试者身上发生;(ii)抑制疾病,即遏制其发展;或(iii)缓解疾病,即使疾病消退。在一方面,所述受试者是哺乳动物,如灵长类动物,并且在另外的方面,所述受试者是人。术语“受试者”还包含家养动物(例如,猫、狗等)、家畜(例如,牛、马、猪、绵羊、山羊等)以及实验室动物(例如,小鼠、兔、大鼠、豚鼠、果蝇、斑马鱼等)。
[0098]
如本文所使用的,术语“预防(prevent)”或“预防(preventing)”是指排除、避免、消除、阻止、停止或阻碍某些事情发生,尤其是通过提前动作。应当理解,除非另外明确指明,否则在本文所使用的降低、抑制或预防的情况下,还明确公开了其它两个词语的使用。
[0099]
如本文所使用的,术语“诊断的”意指已经经受由技术人员(例如,医师)进行的身体检查,并且发现患有可以通过本文公开的化合物、组合物或方法诊断或治疗的病状。例如,“诊断患有不受控细胞增殖病症”意指已经经受由技术人员(例如,医师)进行的身体检查,并且发现患有可以通过可以抑制enpp1的化合物或组合物诊断或治疗的病状。作为另外的实施例,“诊断为需要抑制enpp1”是指已经经受由技术人员(例如,医师)进行的身体检查,并且发现患有特征在于 enpp1功能障碍的病状。如本文所讨论的,这种诊断可以参考病症,如不受控细胞增殖、癌症等病症。例如,“诊断为需要治疗与enpp1功能障碍相关的不受控细胞增殖的一种或更多种病症”意指已经经受由技术人员(例如,医师)进行的身体检查,并且发现患有与enpp1功能障碍相关的不受控细胞增殖的一种或多种病症。
[0100]
如本文所使用的,短语“鉴定为需要治疗病症”等是指基于对治疗所述病症的需要来选择受试者。例如,基于技术人员的早期诊断,受试者可以被鉴定为需要治疗病症(例如,
与enpp1的功能障碍相关的病症)并且此后经受对所述病症的治疗。经考虑,在一方面,鉴定可以由与作出诊断的人不同的人进行。还经考虑,在另外的方面,可以由随后进行施用的人进行施用。
[0101]
如本文所使用的,术语“施用(administering)”和“施用(administration)”是指向受试者提供药物制剂的任何方法。此类方法是本领域的技术人员熟知的,并且包含但不限于口服施用、透皮施用、通过吸入施用、鼻腔施用、局部施用、阴道内施用、眼内施用、耳内施用、脑内施用、直肠施用、舌下施用、口腔施用、尿道内施用以及肠胃外施用,包含注射,如静脉内施用、动脉内施用、肌内施用和皮下施用。施用可以是连续或间歇的。在各个方面,可以治疗地施用制剂;即施用制剂以治疗现有疾病或病状。在另外的各个方面,可以预防性施用制剂;即施用以预防疾病或病状。
[0102]
如本文所使用的术语“接触”是指以这种方式使所公开化合物与细胞、靶受体或其它生物实体带到一起,所述方式使得化合物可以直接地或间接地影响靶标 (例如,受体、细胞等)的活性;即通过与靶标本身相互作用;即通过与靶标的活性所依赖的另一个分子、辅因子、因子或蛋白质相互作用。
[0103]
如本文所使用的,术语“有效量(effectiveamount)”和“有效量(amounteffective)”是指足以实现期望结果或对不期望病状具有影响的量。例如,“治疗有效量”是指足以实现期望治疗结果或对不期望症状具有影响但通常不足以引起不良副作用的量。任何特定患者的具体治疗有效剂量水平将取决于多种因素,包含:所治疗的病症和病症的严重程度;所采用的特定组合物;患者的年龄、体重、总体健康、性别和饮食;施用时间;施用途径;所采用的具体化合物的排泄率;治疗的持续时间;与所采用的特定化合物组合或同时使用的药物以及医学领域熟知的类似因素。例如,以比实现期望治疗效果所需的剂量水平低的剂量水平开始使用化合物并且逐渐增加剂量直到期望效果得以实现完全处于本领域的技术范围内。如果需要,出于施用的目的,有效每日剂量可以分成多个剂量。因此,单个剂量组合物可以含有此类量或其约数以组成每日剂量。在任何禁忌症的情况下,可以由个别医师调整剂量。剂量可以变化,并且可以每天一次或更多次剂量施用来施用,持续一天或数天。可以在文献中找到针对给定类别的药物产品的适当剂量的指导。在另外的各个方面,可以以“预防有效量”施用制剂;即用于预防疾病或病状的有效量。
[0104]
如本文所使用的,“ec
50”旨在指生物过程或过程的组分的50%激动作用或活化所需要的物质(例如,化合物或药物)的浓度,包含蛋白质、亚基、细胞器、核糖核蛋白等。在一方面,ec
50
可以是指体内50%激动作用或活化所需要的物质的浓度,如本文其它地方进一步定义的。在一个另外的方面,ec
50
是指激动剂或活化剂的浓度,所述浓度引起基线与最大反应之间的一半处的应答。
[0105]
如在此所使用的,“ic
50”旨在指生物过程或过程的组分的50%抑制所需要的物质(例如,化合物或药物)的浓度,包含蛋白质、亚基、细胞器、核糖核蛋白等。例如,ic
50
可以指体内50%抑制所需要的物质的浓度或体外测量的抑制,如本文其它地方进一步定义的。可替代地,ic
50
是指物质的半最大(50%)抑制浓度(ic)。可以在细胞系中测量抑制,如an3ca、bt-20、bt-549、hct116、her218、 mcf7、mda-mb-231、mda-mb-235、mda-mb-435s、mda-mb-468、panc-1、 pc-3、sk-n-mc、t-47d和u-87mg。
[0106]
术语“药学上可接受的”描述了不是生物学上或在其它方面不期望的材料,即不会
引起不可接受水平的不期望的生物效应或以有害方式相互作用的材料。
[0107]
本文所使用的术语“稳定的”是指这样的化合物:所述化合物在经受允许其被生产、被检测并且在某些方面被回收、被纯化并且被用于本文公开的目的中的一个或更多个目的条件时,其基本上不会发生变化。
[0108]
如本文所使用的,术语“衍生物”是指一种化合物,其结构衍生自母体化合物 (例如,本文公开的化合物)的结构,并且其结构与本文公开的结构十分类似,并且基于这种类似性,本领域的技术人员预期所述化合物表现出与所要求保护的化合物相同或类似的活性和效用,或作为前体诱导与所要求保护的化合物相同或类似的活性和效用。示例性衍生物包含盐、酯、酰胺、酯或酰胺的盐和母体化合物的n-氧化物。
[0109]
如本文所使用的,术语“药学上可接受的载体”是指无菌水性或非水性溶液、分散体、悬浮液或乳液,以及用于在即将使用之前重构成无菌可注射溶液或分散体的无菌粉末。合适的水性和非水性载体、稀释剂、溶剂或媒剂的实施例包含水、乙醇、多元醇(如甘油、丙二醇、聚乙二醇等)、羧甲基纤维素及其合适的混合物、植物油(如橄榄油)和可注射有机酯,如油酸乙酯。可以例如通过使用包衣材料(如卵磷脂),在分散体的情况下通过维持所需的粒度以及通过使用表面活性剂来维持恰当的流动性。这些组合物还可以含有佐剂,如防腐剂、润湿剂、乳化剂以及分散剂。可以通过包含各种抗细菌剂和抗真菌剂,如对羟基苯甲酸酯、氯丁醇、苯酚、山梨酸等来确保防止微生物的作用。还可以令人期望的是包含等渗剂,如糖、氯化钠等。可注射药物形式的延长吸收可以通过包含延迟吸收的药剂(如单硬脂酸铝和明胶)来实现。通过在可生物降解的聚合物,如聚丙交酯-聚乙交酯、聚(原酸酯)和聚(酸酐)中形成药物的微胶囊基质来制备可注射储库型形式。根据药物与聚合物的比率以及所采用的特定聚合物的性质,可以对药物释放的速率进行控制。储库型可注射制剂还通过将药物截留在与身体组织相容的脂质体或微乳液中来制备。可注射制剂可以例如通过滤过细菌截留过滤器,或通过掺入呈无菌固体组合物形式的灭菌剂来灭菌,这些无菌固体组合物可以在即将使用前溶解或分散于无菌水或其它无菌可注射介质中。合适的惰性载体可以包含糖,如乳糖。期望地,至少按重量计95%的活性成分颗粒的有效粒度处于0.01到10微米范围内。
[0110]
在说明书和最后的权利要求书中所使用的化学物种的残基是指在特定反应方案或后续制剂或化学产品中作为化学物种的所得产物的部分,而无论所述部分实际上是否从化学物种中获得。因此,聚酯中的乙二醇残基是指聚酯中的一个或更多个-och2ch2o-单元,无论乙二醇是否用于制备聚酯。类似地,聚酯中的癸二酸残基是指聚酯中的一个或更多个-co(ch2)8co-部分,无论残基是否通过使癸二酸或其酯反应以获得聚酯而获得的。
[0111]
如本文所使用的,术语“经取代的”预期包含有机化合物的所有可允许的取代基。在广泛的方面,可允许的取代基包含有机化合物的无环和环状、支链和无支链、碳环和杂环、芳香族和非芳香族的取代基。说明性取代基包含例如以下描述的那些取代基。对于适当的有机化合物,可允许的取代基可以是一个或更多个并且可以是相同或不同的。出于本公开的目的,杂原子(如氮)可以具有本文描述的有机化合物的氢取代基和/或任何可允许的取代基,这些取代基将满足杂原子的化合价。本公开不旨在以任何方式受限于有机化合物的可允许的取代基。而且,术语“取代”或“被
……
取代”包含隐含条件:这种取代与经取代的原子和取代基的所允许化合价一致,并且所述取代导致稳定的化合物,例如不会自发地经
历转化(如通过重排、环化、消除等)的化合物。还经考虑,在某些方面,除非明确相反地指明,否则单独的取代基可以进一步任选地被取代(即,进一步被取代或未被取代)。
[0112]
在定义各种术语时r1,、r2、r3等和ra、rb、rc、rd在本文中用作通用符号以表示各种特定取代基。这些符号可以是任何取代基,不限于本文公开的那些取代基,并且当在一种情况下这些符号被定义为某些取代基时,在另一种实施例其可以被定义为一些其它取代基。
[0113]
如本文所使用的术语“烷基”是具有1到24个碳原子的支链或无支链的饱和烃基团,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、仲戊基、新戊基、己基、庚基、辛基、壬基、癸基、十二烷基、十四烷基、十六烷基、二十烷基、二十四烷基等。烷基团可以是环状或非环状的。烷基团可以是支链或无支链的。烷基团还可以是经取代的或未经取代的。例如,烷基团可以被一个或更多个基团取代,包含但不限于烷基、环烷基、烷氧基、氨基、醚、卤化物、羟基、硝基、甲硅烷基、磺基-氧代或硫醇,如本文所述。“低级烷基团”是含有一到六个(例如,一到四个)碳原子的烷基团。
[0114]
例如,“c1-c3烷基团”可以选自甲基、乙基、正丙基、异丙基和环丙基,或选自其子集。在某些方面,“c1-c3烷基团”可以任选地被进一步取代。作为另外的实施例,“c1-c4烷基团”可以选自甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基和环丁基,或选自其子集。在某些方面,“c1-c4 烷基团”可以任选地被进一步取代。作为另外的实施例,“c1-c6烷基团”可以选自甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、正戊基、异戊基、仲戊基、叔戊基、新戊基、环戊基、正己基、异己基、3-甲基戊烷、2,3-二甲基丁烷、新己烷和环己烷,或选自其子集。在某些方面,“c1-c6烷基团”可以任选地被进一步取代。作为另外的实施例,“c1-c8烷基团”可以选自甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、正戊基、异戊基、仲戊基、叔戊基、新戊基、环戊基、正己基、异己基、3-甲基戊烷、2,3-二甲基丁烷、新己烷、环己烷、庚烷、环庚烷、辛烷和环辛烷,或选自其子集。在某些方面,“c1-c8烷基团”可以任选地被进一步取代。作为另外的实施例,“c1-c12烷基团”可以选自甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、正戊基、异戊基、仲戊基、叔戊基、新戊基、环戊基、正己基、异己基、3-甲基戊烷、2,3
‑ꢀ
二甲基丁烷、新己烷、环己烷、庚烷、环庚烷、辛烷、环辛烷、壬烷、环壬烷、癸烷、环癸烷、十一烷、环十一烷、十二烷和环十二烷,或选自其子集。在某些方面,“c1-c12烷基团”可以任选地被进一步取代。
[0115]
贯穿本说明书,“烷基”通常用于指未经取代的烷基团和经取代的烷基团两者;然而,经取代的烷基团在本文中还通过鉴定烷基团上的一个或多个特定取代基而被具体提及。例如,术语“卤化烷基”或“卤代烷基”具体地是指被一或更多个卤离子(例如,氟离子、氯离子、溴离子或碘离子)取代的烷基团。术语“烷氧基烷基”具体地是指被一个或更多个烷氧基团取代的烷基团,如下文所述。术语“烷基氨基”具体地是指如下所述的被一个或更多个氨基团等取代的烷基团。当在一种情况下使用“烷基”并且在另一种实施例使用特定术语如“烷基醇”时,这并不意味着暗示术语“烷基”也未指特定术语如“烷基醇”等。
[0116]
这种实践也用于本文所述的其它基团。也就是说,尽管术语如“环烷基”是指未经取代和经取代的环烷基部分两者,但是所述经取代的部分可以另外在本文中具体地鉴定;例如,特定的经取代的环烷基可以被称为例如“烷基环烷基”。类似地,经取代的烷氧基可以具体地被称为例如“卤化烷氧基”,特定的经取代的烯基可以为例如“烯基醇”等。再次,使用
通用术语如“环烷基”和特定术语如“烷基环烷基”的实践不意味着暗示通用术语也不包含特定术语。
[0117]
如本文所使用的术语“环烷基”是由至少三个碳原子构成的非芳香族的碳基环。环烷基团的实施例包含但不限于环丙基、环丁基、环戊基、环己基、降冰片基等。术语“杂环烷基”是如以上定义的环烷基团的一种类型,并且包含在术语“环烷基”的含义内,其中环的碳原子中的至少一个碳原子被杂原子替代,所述杂原子如但不限于氮、氧、硫或磷。环烷基团和杂环烷基团可以是经取代的或未经取代的。环烷基团和杂环烷基团可以被一个或更多个基团取代,所述基团包含但不限于烷基、环烷基、烷氧基、氨基、醚、卤化物、羟基、硝基、甲硅烷基、磺基-氧代、腈、磺酰胺或硫醇,如本文所述。
[0118]
如本文所使用的术语“芳基”是含有任何碳基芳香族基团的基团,包含但不限于苯、萘、苯基、联苯基、苯氧基苯等。术语“芳基”还包含“杂芳基”,其被定义为含有芳香族基团的基团,所述芳香族基团具有并入芳香族基团的环内的至少一个杂原子。杂环原子的实施例包含但不限于氮、氧、硫以及磷。同样,也包含在术语“芳基”中的术语“非杂芳基”定义了含有未含有杂原子的芳香族基团的基团。芳基团可以是取代的或未取代的。芳基团可以被一个或更多个基团取代,所述一个或更多个基团包含但不限于烷基、环烷基、烷氧基、烯基、环烯基、炔基、环炔基、芳基、杂芳基、醛、氨基、羧酸、酯、醚、卤化物、羟基、酮、叠氮化物、硝基、甲硅烷基、磺基-氧代、腈、磺酰胺或硫醇,如本文所述。术语“联芳基”是特定类型的芳基团并且包含在“芳基”的定义中。联芳基是指如在萘中通过稠环结构结合在一起或如在联苯中通过一个或更多个碳-碳键连接的两个芳基团。
[0119]
如本文所使用的术语“卤素”、“卤化物”和“卤基”是指卤素氟、氯、溴和碘。还经考虑,在各个方面,卤素可以选自氟、氯、溴和碘。例如,卤素可以选自氟、氯和溴。作为另外的实施例,卤素可以选自氟和氯。作为另外的实施例,卤素可以选自氯和溴。作为另外的实施例,卤素可以选自溴和碘。作为另外的实施例,卤素可以选自氯、溴和碘。在一方面,卤素可以是氟。在另外的方面,卤素可以是氯。在仍另外的方面,卤素是溴。在又另外的方面,卤素是碘。
[0120]
还经考虑,在某些方面,可以使用拟卤素(例如,三氟甲磺酸酯、甲磺酸酯、甲苯磺酸酯、对溴苯磺酸酯等)代替卤素。例如,在某些方面,卤素可以被拟卤素替代。作为另外的实施例,拟卤素可以选自三氟甲磺酸酯、甲磺酸酯、甲苯磺酸酯和对溴苯磺酸酯。在一方面,拟卤素是三氟甲磺酸酯。在另外的方面,拟卤素是甲磺酸酯。在另外的方面,拟卤素是甲苯磺酸酯。在另外的方面,拟卤素是对溴苯磺酸酯。
[0121]
如本文所使用的术语“杂环”是指单环和多环的芳香族或非芳香族环系,其中环成员中的至少一个环成员不是碳。杂环包含氮杂环丁烷、二噁烷、呋喃、咪唑、异噻唑、异噁唑、吗啉、噁唑、噁唑(包含1,2,3-噁二唑、1,2,5-噁二唑和1,3,4
‑ꢀ
噁二唑)、哌嗪、哌啶、吡嗪、吡唑、哒嗪、吡啶、嘧啶、吡咯、吡咯烷、四氢呋喃、四氢吡喃、四嗪(包含1,2,4,5-四嗪)、四唑(包含1,2,3,4-四唑和1,2,4,5-四唑)、噻二唑(包含1,2,3-噻二唑、1,2,5-噻二唑和1,3,4-噻二唑)、噻唑、噻吩、三嗪(包含1,3,5-三嗪和1,2,4-三嗪)、三唑(包含1,2,3-三唑、1,3,4-三唑)等。
[0122]
如本文所使用的术语“羟基”由式-oh表示。
[0123]
如本文所使用的“r
1”、“r
2”、“r
3”、“r
n”(其中n是整数)可以独立地具有以上列出的
基团中的一个或更多个基团。例如,如果r1是直链烷基团,则烷基的氢原子之一可以任选地被羟基团、烷氧基团、烷基团、卤化物等取代。根据所选择的基团,第一基团可以并入第二基团内,或可替代地,第一基团可以是第二基团的侧基(即,连接)。例如,对于短语“包括氨基团的烷基团”,氨基团可以并入烷基团的主链内。可替代地,氨基团可以与烷基团的主链连接。所选择的一个或多个基团的性质将确定第一基团是嵌入第二基团还是与第二基团连接。
[0124]
如本文所述,本发明的化合物可以含有“经任选取代的”部分。通常,除非另有明确说明,化学基团可以被取代,无论是否明确说明它是“任选地被取代的”。通常,术语“经取代的”,无论前面是否有术语“任选地”,都意味着指定部分的一个或更多个氢被合适的取代基替代。除非另有指明,否则“经任选取代的”基团可以在所述基团的每个可取代位置处具有合适的取代基,并且在任何给定结构中的多于一个位置可以被多于一个选自指定组的取代基取代时,在每个位置处,取代基可以相同或不同。本发明所设想的取代基组合优选地是使稳定或化学上可行的化合物形成的取代基组合。还经考虑,在某些方面,除非明确相反地指明,否则个别取代基可以进一步被任选地取代(即,进一步被取代或未被取代)。
[0125]
本文所述的化合物可以含有一个或更多个双键,并且因此可能产生顺式/反式(e/z)异构体,以及其它构象异构体。除非相反地说明,否则本发明包含所有这些可能的异构体,以及这些异构体的混合物。
[0126]
除非相反地说明,否则具有仅以实线而不是楔形或虚线示出的化学键的式涵盖了每种可能的异构体,例如每种对映异构体和非对映异构体,以及异构体的混合物,如外消旋混合物或非外消旋混合物。本文所述的化合物可以含有一个或更多个不对称中心,并且因此可能产生非对映异构体和光学异构体。除非相反地说明,否则本发明包含所有这些可能的非对映异构体及其外消旋混合物、其基本上纯的拆分对映异构体、所有可能的几何异构体及其药学上可接受的盐。还包含立体异构体的混合物以及分离的特定立体异构体。在用于制备此类化合物的合成过程的进程期间,或在使用本领域的技术人员已知的外消旋化或差向异构化过程中,这些过程的产物可以是立体异构体的混合物。
[0127]
所有对映异构体均通过sfc柱分离,且立体化学仍不确定。
[0128]
许多有机化合物以具有旋转平面偏振光平面的能力的光学活性形式存在。在描述光学活性化合物时,前缀d和l或r和s用于表示分子围绕其一个或多个手性中心的绝对构型。前缀d和/或(+)和(-)用于表示化合物对平面偏振光的旋转符号,其中(-)或/表示化合物是左旋的。前缀为(+)或d的化合物是右旋的。对于给定的化学结构,被称为立体异构体的这些化合物是相同的,除了其是彼此不能叠加的镜像之外。特定的立体异构体也可以被称为对映异构体,并且此类异构体的混合物通常称为对映异构体混合物。对映异构体的50:50混合物被称为外消旋混合物。
[0129]
本文所述的许多化合物可以具有一个或更多个手性中心,并且因此可以以不同的对映异构体形式存在。如果需要,手性碳可以用星号(*)表示。当与手性碳的键在所公开的式中被描绘为直线时,应理解手性碳的(r)和(s)构型两者,以及因此对映异构体和其混合物两者均包含在式内。如本领域中所使用的,当期望指定关于手性碳的绝对构型时,与手性碳的键之一可以被描绘为楔形(与平面上方的原子的键),并且另一个可以被描绘为短平行线的串联或楔形(与平面下方的原子的键)。cahn-inglod-prelog系统可以用于将(r)或(s)
构型分配给手性碳。
[0130]
如
[0131]
本文所述的化合物包括处于其天然同位素丰度和处于非天然丰度两者的原子。所公开化合物可以是同位素标记的或同位素取代的化合物,所述化合物与所描述的那些化合物相同,但是事实是一个或更多个原子被具有与通常在自然界中发现的原子质量或质量数不同的原子质量或质量数的原子替代。可以并入到本发明的化合物中的同位素的实施例分别包含氢、碳、氮、氧、磷、氟和氯的同位素,如2h、3h、
13
c、
14
c、
15
n、
18
o、
17
o、
35
s、
18
f和
36
cl。化合物进一步包括其前药,并且含有上述同位素和/或其它原子的其它同位素的所述化合物或所述前药的药学上可接受的盐在本发明的范围内。本发明的某些同位素标记的化合物(例如其中并入放射性同位素,如3h和
14
c的那些)在药物和/或底物组织分布测定中是有用的。氚化的同位素(即,3h)和碳-14同位素(即,
14
c)因其易于制备和可检测性而特别优选。进一步地,使用较重的同位素,如氘(即,2h)的取代可以得到由更大代谢稳定性产生的某些治疗优点,例如体内半衰期增加或剂量需求降低,并且因此在一些情况可能是优选的。本发明的同位素标记的化合物和其前药通常可以通过实施以下程序制备:用可容易获得的同位素标记的试剂取代非同位素标记的试剂。
[0132]
本发明中描述的化合物可以作为溶剂化物存在。在某些情况下,用于制备溶剂化物的溶剂是水性溶液,并且因此溶剂化物通常被称为水合物。化合物可以作为水合物存在,所述水合物可以例如通过从溶剂或水性溶液中结晶而获得。就此而言,一个、两个、三个或任何任意数量的溶剂化物或水分子可以与根据本发明的化合物组合以形成溶剂化物和水合物。除非相反地说明,否则本发明包含所有这些可能的溶剂化物。
[0133]
还应理解,本文所述的某些化合物可以作为互变异构体的平衡存在。例如,具有α-氢的酮可以以酮形式和烯醇形式的平衡存在。
[0134][0135]
同样,具有n-氢的酰胺可以以酰胺形式和亚胺酸形式的平衡存在。除非相反地说明,否则本发明包含所有这些可能的互变异构体。
[0136]
已知化学物质形成以不同顺序状态存在的固体,所述顺序状态被称为多晶型形式或修饰。多晶型物质的不同修饰在其物理性质上可能有很大不同。根据本发明的化合物可以以不同的多晶型形式存在,其中特定修饰可能是亚稳定的。除非相反地说明,否则本发明
包含所有这些可能的多晶型形式。
[0137]
在一些方面,化合物的结构可以由下式表示:
[0138][0139]
其被理解为等效于下式:
[0140][0141]
其中n通常是整数。即,rn应理解为表示五个独立的取代基,r
n(a)
、r
n(b)
、 r
n(c)
、r
n(d)
、r
n(e)
。“独立的取代基”意指每个r取代基可以被独立地定义。例如,如果在一个实施例中r
n(a)
为卤素,则在所述实施例中r
n(b)
不一定为卤素。
[0142]
本文公开的某些材料、化合物、组合物和组分可以商购获得或使用本领域的技术人员通常已知的技术容易地合成。例如,在制备所公开化合物和组合物中使用的起始材料和试剂是可从商业供应商,如西格玛-奥德里奇化学公司(密尔沃基,威斯康星州)、阿克洛斯有机物公司(莫里斯平原,新泽西州)、飞世尔科技公司(匹兹堡,宾夕法尼亚州)或西格玛公司(圣路易斯,密苏里州)获得的或通过本领域的技术人员已知的方法遵循以下参考文献中所阐述的程序制备的:如《费塞尔与菲泽有机合成试剂》,第1-17卷(约翰
·
威利父子出版公司,1991);《罗氏德碳化合物化学》,第1-5卷和增刊(塞维尔科学出版社,1989);《有机反应》,第1-40卷(约翰
·
威利父子出版公司,1991);《玛奇高等有机化学》,(约翰
·
威利父子出版公司,第4版);以及《拉罗克综合有机转化》(vch出版社公司,1989)。
[0143]
除非另有明确说明,否则不旨在将本文中所阐述的任何方法解释为要求以特定顺序执行其步骤。因此,在方法权利要求实际上不叙述其步骤所遵循的顺序或者在权利要求书或说明书中没有另外具体地说明步骤被限制为特定顺序的情况下,绝不旨在任何方面推断顺序。这适用于任何可能的用于解释的非表达基础,包含:关于步骤安排或操作流程的逻辑问题;从语法组织或标点得到的普通含义;以及说明书中描述的实施方式的数量或类型。
[0144]
公开了用于制备本发明的组合物的组分以及在本文公开的方法内所使用的组合物本身。本文中公开了这些和其它材料,并且应理解,当公开了这些材料的组合、子集、相互作用、基团等时,尽管无法明确地公开对这些化合物的每种各种单独和集体组合和排列的具体引用,但在本文中具体地设想和描述了每一种组合和排列。例如,如果公开和讨论了特定化合物,并且讨论了可能对包含所述化合物的多个分子进行的许多修饰,则除非具体地相反地指明,否则具体地涵盖所述化合物中的每个组合和排列以及可能的修饰。因此,如果公开了一类分子a、b和c以及一类分子d、e和f,并且公开了组合分子a-d的实施例,则即使每个并未单独地叙述,但单独地和共同地考虑每个分子,这意味着视为公开了组合a-e、a-f、b-d、b-e、b-f、c-d、c-e和c-f。同样,还公开了这些的任何子集或组合。因此,例如,将认为a-e、b-f和c-e的子基团是公开的。此概念适用于本技术的所有方面,包含但不限于制备和使用本发明的组合物的方法中的步骤。因此,如果存在可以执行的各种另外的步骤,应理解,这些另外的步骤中的每个步骤可以用本发明的方法的任何具体实施方式或实施方式的组
合来执行。
[0145]
应理解,本文公开的组合物具有某些功能。本文公开了用于执行所公开功能的某些结构要求,并且应理解,存在可以执行与所公开结构相关的同一功能的多种结构,并且这些结构通常将实现同一结果。
[0146]
化合物
[0147]
在一方面,本发明涉及可用作enpp1抑制剂的化合物。此外,在一方面,本发明的化合物可用于治疗不受控细胞增殖病症。在另外的方面,不受控细胞增殖病症是癌症或肿瘤。在仍另外的方面,不受控细胞增殖病症与enpp1功能障碍相关,如本文进一步所述。
[0148]
在另一方面,本发明的化合物可用于治疗细菌或病毒来源的疾病。因此,在一方面,本发明提供了一种治疗由细菌或病毒引起的疾病的方法,所述方法包括向受试者施用治疗有效量的本发明的化合物。
[0149]
经考虑,每个所公开衍生物可以任选地被进一步取代。还经考虑,本发明可以任选地省略任何一种或更多种衍生物。应理解,所公开化合物可以通过所公开方法来提供。还应理解,所公开化合物可以在所公开的使用方法中使用。
[0150]
结构
[0151]
在一个方面,本发明涉及如下式i或式ii化合物:
[0152][0153]
其中
[0154]
x是n或cr
11
;
[0155]
y选自包括-cr4r
5-、-nr
6-、-n(ch2)mo-、-o-、-s-、-s(o)-、-s(o)2、芳基和杂芳基的基团;其中m是2或3;
[0156]
l选自包括c
1-c5烷基和c
1-c5烯基的基团;
[0157]
每个r1、r2和r3独立地选自包括氢、卤素、cn、ora、-c(=o)nrbrc、-nrbrc、
ꢀ‑
c(=o)rd、芳基、杂芳基、环烷基和杂环烷基的基团。
[0158]
每个ra独立地选自包括氢、低级烷基、-(ch2)
n-c(=o)nrbrc、芳烷基、芳基、杂芳基、杂环烷基和环烷基的基团;
[0159]
其中n是1到3之间的整数;
[0160]
每个rb和rc独立地选自包括氢、低级烷基和低级芳基、杂环烷基或环烷基的基团;
[0161]
每个rd独立地选自包括-ore和低级烷基的基团;
[0162]
每个re独立地选自包括氢、低级烷基和低级芳基的基团;
[0163]r11
独立地选自包括氢、卤素、cooet、cooh和cn的基团;
[0164]
r4、r5和r6独立地选自包括氢和低级烷基的基团;
[0165]
或其异构体、水合物、溶剂化物、多晶型物、互变异构体或药学上可接受的盐。
[0166]
式ii的化合物如下:
[0167][0168]
其中
[0169]
x是n或cr
11
;
[0170]
z是c或n;
[0171]
w选自包括c
1-c5烷基、-c(=o)-(ch2)
n-、-(c
1-c5烷基)-n-的基团;nh和直接键如下:
[0172]
每个r1、r2和r3独立地选自包括氢、卤素、cn、ora、-c(=o)nrbrc、-nrbrc、
ꢀ‑
c(=o)rd、芳基、杂芳基、环烷基和杂环烷基的基团。
[0173]
每个ra独立地选自包括氢、低级烷基和-(ch2)
n-c(=o)nrbrc、芳烷基、芳基、杂芳基、杂环烷基、环烷基的基团;
[0174]
其中n是1到3之间的整数;
[0175]
每个rb和rc独立地选自包括氢、低级烷基和低级芳基、杂环烷基或环烷基的基团;
[0176]
每个rd独立地选自包括-ore和低级烷基的基团;
[0177]
每个re独立地选自包括氢、低级烷基和低级芳基的基团;
[0178]r11
独立地选自包括氢、卤素、cooet、cooh和cn的基团;
[0179]
r7、r8和r9独立地选自包括h、卤素和低级烷基的基团;并且r8和r9也可以在具有1个或2个原子的7元环上形成桥,如下:
[0180]r10
独立地选自包括氢和cf3的基团;
[0181]
或其异构体、水合物、溶剂化物、多晶型物、互变异构体或药学上可接受的盐。
[0182]
本发明包含任何化合物或结构,其包括上述取代基的任何组合。
[0183]
在一个优选的实施方式中,式i中的y是吡啶基。
[0184]
在一个优选的实施方式中,式i或式ii中的x是c-cn。
[0185]
在一个优选的实施方式中,式i中的y是nr6。
[0186]
在一个优选的实施方式中,在式i和式ii的化合物中,r1、r2和r3选自包括ch3o和h的基团。
[0187]
在一个优选的实施方式中,在式ii化合物中,z是n。
[0188]
在一个优选的实施方式中,在式ii化合物中,w选自包括-4,5-咪唑、2-恶唑、3-吡咯;吡唑和噻唑的基团。
[0189]
在一个优选的实施方式中,在式ii化合物中,x是n。
[0190]
在一个优选的实施方式中,在式ii化合物中,x是c-cn。
[0191]
在一个优选的实施方式中,在式ii化合物中,r7、r8和r9独立地选自包括h 和卤素的基团。
[0192]
在一个优选的实施方式中,在式ii化合物中,r7是卤素,更优选f。
[0193]
在一个优选的实施方式中,在式ii化合物中,r8和r9都是卤素。
[0194]
在一个优选的实施方式中,
[0195]
该化合物具有式i;
[0196]
x是n;
[0197]
y选自包括吡啶基、c
1-c5烷基、o、n和s的基团;
[0198]
l是任选取代的c
1-c5烷基;和
[0199]
r1和r2都是ch3o。
[0200]
在另一个优选的实施方式中,
[0201]
该化合物具有式ii;
[0202]
x是n;
[0203]
z是n;
[0204]
w选自任选取代的包括c
1-c5烷基、-c(=o)-(ch2)-、-(任选取代的c
1-c5烷基)-n的基团;和直接键;和
[0205]
r1和r2都是ch3o。
[0206]
所提供的化合物的实施例包含:
[0207]
[0208]
[0209]
[0210]
[0211]
[0212][0213]
本发明还提供了一种药物组合物,其包括治疗有效量的任何本发明的化合物以及药学上可接受的载体。
[0214]
本发明还提供了一种用于治疗哺乳动物的不受控细胞增殖病症的方法,所述方法包括向所述哺乳动物施用有效量的任何本发明的化合物的步骤。
[0215]
本发明还提供了一种用于降低哺乳动物的enpp1活性的方法,所述方法包括向所述哺乳动物施用有效量的任何本发明化合物的步骤。
[0216]
本发明还提供了一种用于抑制哺乳动物的enpp1活性的方法,所述方法包括向所述哺乳动物施用有效量的任何本发明的化合物的步骤。
[0217]
制备化合物的方法
[0218]
在一方面,本发明涉及制备可用作enpp1抑制剂的化合物的方法。在另外的方面,所公开的制备方法的产物是enpp1活性的调节剂。
[0219]
除了文献中已知的、实验部分中例示的或本领域的技术人员清楚的其它标准操作之外,本发明的化合物可以通过使用如以下方案中所示的反应来制备。为了清楚起见,显示了具有单个取代基的实施例,其中在本文公开的定义下允许多个取代基。
[0220]
除了文献中或本领域的技术人员已知的其它标准操作之外,用于产生本发明的化合物的反应还通过使用如以下反应方案所示的反应来制备。提供以下实施例以使得本发明可以被更充分地理解,所述实施例仅是说明性的并且不应被解释为限制性的。
[0221]
在一方面,所公开化合物包括本文所述的合成方法的产物。在另外的方面,所公开化合物包括通过本文所述的合成方法产生的化合物。在仍另外的方面,本发明包括一种药物组合物,其包括治疗有效量的所公开方法的产物以及药学上可接受的载体。在仍另外的方面,本发明包括一种用于制造药物的方法,所述方法包括将任何所公开化合物中的至少一种化合物或所公开方法中的至少一种产物与药学上可接受的载体或稀释剂组合。
[0222]
在没有说明反应条件和成分的量的情况下,据信确定其处于本领域的技术范围内。经考虑,每个所公开方法可以进一步包括另外的步骤、操作和/或组分。还可以设想,本发明可以任选地省略任何一个或更多个步骤、操作和/或组分。应理解,所公开的方法可用于提供所公开的化合物。还应理解,所公开方法的产物可以用于所公开的使用方法中。
[0223]
药物组合物
[0224]
在一方面,本发明涉及包括所公开化合物的药物组合物。即,可以提供包括治疗有效量的至少一种所公开化合物或所公开方法的至少一种产物以及药学上可接受的载体的药物组合物。
[0225]
在另外的方面,本发明涉及包括药学上可接受的载体和有效量的所公开合成方法的产物的药物组合物。在另外的方面,有效量是治疗有效量。在另外的方面,有效量是预防
有效量。在另外的方面,化合物是所公开化合物。
[0226]
在某些方面,所公开药物组合物包括作为活性成分的所公开化合物(包含其一种或多种药学上可接受的盐)、药学上可接受的载体以及任选地其它治疗剂成分或佐剂。本发明组合物包含适于口服施用、直肠施用、局部施用和肠胃外(包含皮下、肌内和静脉内)施用的那些组合物,但是在任何给定情况下最合适的途径将取决于特定宿主和施用活性成分的病状的性质和严重程度。药物组合物可以方便地以单位剂型呈现并且可以通过药学领域熟知的任何方法制备。
[0227]
如本文所使用的,术语“药学上可接受的盐”是指由药学上可接受的无毒碱或酸制备的盐。当本发明的化合物是酸性的时,其对应的盐可以方便地由药学上可接受的无毒碱(包含无机碱和有机碱)制备。衍生自此类无机碱的盐包含铝、铵、钙、铜(-ic和-ous)、铁、亚铁、锂、镁、锰(-ic和-ous)、钾、钠、锌等盐。特别优选的是铵盐、钙盐、镁盐、钾盐和钠盐。衍生自药学上可接受的有机无毒碱的盐包含伯胺、仲胺和叔胺以及环状胺和经取代胺,如天然存在的和合成的经取代胺的盐。可以由其形成盐的其它药学上可接受的有机无毒碱包含离子交换树脂,例如精氨酸、甜菜碱、咖啡因、胆碱、n,n'-二苄基乙二胺、二乙胺、2
‑ꢀ
二乙氨基乙醇、2-二甲基氨基乙醇、乙醇胺、乙二胺、n-乙基吗啉、n-乙基哌啶、葡糖胺、葡萄糖胺、组氨酸、海巴胺、异丙胺、赖氨酸、甲基葡糖胺、吗啉、哌嗪、哌啶、聚胺树脂、普鲁卡因、嘌呤、可可碱、三乙胺、三甲胺、三丙胺、氨丁三醇等。
[0228]
如本文所使用的,术语“药学上可接受的无毒酸”包含无机酸、有机酸以及由其制备的盐,例如乙酸、苯磺酸、苯甲酸、樟脑磺酸、柠檬酸、乙磺酸、富马酸、葡萄糖酸、谷氨酸、氢溴酸、盐酸、羟乙基磺酸、乳酸、马来酸、苹果酸、扁桃酸、甲磺酸、粘酸、硝酸、扑酸、泛酸、磷酸、琥珀酸、硫酸、酒石酸、对甲苯磺酸等。优选的是柠檬酸、氢溴酸、盐酸、马来酸、磷酸、硫酸和酒石酸。
[0229]
在实践中,根据常规药物混配技术,本发明的本发明化合物或其药学上可接受的盐可以作为活性成分与药物载体紧密混合。载体可以采取多种形式,这取决于对于施用而言,例如口服或肠胃外(包含静脉内)所期望的制剂的形式。因此,本发明的药物组合物可以作为适于口服施用的离散单位呈现,如各自含有预定量的活性成分的胶囊、扁囊剂或片剂。进一步地,组合物可以作为粉末、颗粒、溶液、水性液体中的悬浮液、非水性液体、水包油乳液或油包水液体乳液存在。除了以上阐述的常见剂型之外,还可以通过控制释放装置和/或递送装置来施用本发明的化合物和/或其一种或多种药学上可接受的盐。组合物可以通过任何制药方法制备。通常,此类方法包含使活性成分与构成一种或更多种必需成分的载体结合的步骤。通常,组合物通过使活性成分与液体载体或细粉状固体载体或两者均匀且紧密混合来制备。然后可以将产品方便地成型为所期望的外观。
[0230]
因此,本发明的药物组合物可以包含药学上可接受的载体和本发明的化合物或所述化合物的药学上可接受的盐。本发明的化合物或其药学上可接受的盐也可以与一种或更多种其它治疗活性化合物组合包含在药物组合物中。
[0231]
所采用的药物载体可以是例如固体、液体或气体。固体载体的实施例包含乳糖、白土、蔗糖、滑石粉、明胶、琼脂、果胶、阿拉伯胶、硬脂酸镁和硬脂酸。液体载体的实施例是糖浆、花生油、橄榄油和水。气态载体的实施例包含二氧化碳和氮气。
[0232]
在制备用于口服剂型的组合物时,可以使用任何方便的药物介质。例如,水、乙二
醇、油、醇、调味剂、防腐剂、着色剂等可以用于形成口服液体制剂,如悬浮液、酏剂和溶液;而如淀粉、糖、微晶纤维素、稀释剂、制粒剂、润滑剂、粘合剂、崩解剂等载体可以用于形成口服固体制剂,如粉末、胶囊和片剂。因为易于施用,片剂和胶囊是优选的口服剂量单位,由此采用固体药物载体。任选地,可以通过标准的水性或非水性技术来对片剂进行包衣。
[0233]
含有本发明的组合物的片剂可以通过压制或模制,任选地用一种或更多种辅助成分或佐剂来制备。可以通过在合适的机器中压制任选地与粘合剂、润滑剂、惰性稀释剂、表面活性剂或分散剂混合的呈自由流动形式的活性成分(如粉末或颗粒)来制备。可以通过在合适的机器中模制用惰性液体稀释剂润湿的粉末状化合物的混合物来制造模制片剂。
[0234]
本发明的药物组合物包括作为活性成分的本发明的化合物(或其药学上可接受的盐)、药学上可接受的载体和任选地一种或更多种另外的治疗剂或佐剂。本发明组合物包含适于口服施用、直肠施用、局部施用和肠胃外(包含皮下、肌内和静脉内)施用的组合物,但是在任何给定情况下最合适的途径将取决于特定宿主和施用活性成分的病状的性质和严重程度。药物组合物可以方便地以单位剂型呈现并且可以通过药学领域熟知的任何方法制备。
[0235]
适于肠胃外施用的本发明的药物组合物可以制备为活性化合物在水中的溶液或悬浮液。可以包含合适的表面活性剂,例如羟丙基纤维素。还可以在甘油、液体聚乙二醇和其混合物中以及在油中制备分散体。进一步地,可以包含防腐剂以防止微生物的有害生长。
[0236]
适于可注射使用的本发明的药物组合物包含无菌水性溶液或分散体。此外,组合物可以呈无菌粉末的形式,用于临时制备此类无菌可注射溶液或分散体。在所有情况下,最终的可注射形式必须是无菌的并且为了易于注射必须是有效流体。药物组合物在制造和储存条件下必须是稳定的;因此,优选地应抗微生物(如细菌和真菌)的污染作用而保存。载体可以是溶剂或分散介质,其含有例如水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇)、植物油和其合适的混合物。
[0237]
本发明的药物组合物可以呈适于局部使用的形式,例如气雾剂、乳膏、软膏、洗剂、撒粉剂、漱口水、漱口剂等。进一步地,组合物可以呈适合用于透皮装置的形式。这些制剂可以利用本发明的化合物或其药学上可接受的盐通过常规加工方法来制备。作为实施例,通过使亲水材料和水与约5wt%到约10wt%的化合物一起混合来制备乳膏或软膏,以产生具有所期望稠度的乳膏或软膏。
[0238]
本发明的药物组合物可以呈适于直肠施用的形式,其中载体是固体。优选混合物形成单位剂量栓剂。合适的载体包含可可脂和本领域常用的其它材料。栓剂可以通过首先使组合物与一种或多种软化或熔融的载体混合,然后在模具中冷却和成型来方便地形成。
[0239]
除了上述载体成分之外,以上所述的药物制剂视情况可以包含一种或多种另外的载体成分,如稀释剂、缓冲剂、调味剂、粘合剂、表面活性剂、增稠剂、润滑剂、防腐剂(包含抗氧化剂)等。此外,可以包含其它佐剂以使制剂与预期受体的血液等渗。含有本发明的化合物和/或其药学上可接受的盐的组合物也可以以粉末或液体浓缩物形式制备。
[0240]
在治疗需要抑制或负调节enpp1蛋白活性的病状中,适当的剂量水平通常将为约0.01到500mg每kg患者体重每天,并且可以以单剂量或多剂量施用。优选地,剂量水平将为约0.1到约250mg/kg每天;更优选地0.5到100mg/kg 每天。合适的剂量水平可以为约0.01到250mg/kg每天、约0.05到100mg/kg 每天或约0.1到50mg/kg每天。在此范围内,剂量可以为
0.05到0.5、0.5到5.0 或5.0到50mg/kg每天。对于口服施用,组合物优选地以含有1.0到1000毫克活性成分,具体地1.0、5.0、10、15、20、25、50、75、100、150、200、250、 300、400、500、600、750、800、900和1000毫克活性成分的片剂形式提供,以对待治疗患者的剂量进行对症调整。化合物可以根据1到4次每天,优选地一次或两次每天的方案施用。可以调整这种给药方案以提供最佳的治疗反应。
[0241]
然而,应理解,任何特定患者的特定剂量水平将取决于多种因素。这些因素包含患者的年龄、体重、总体健康、性别和饮食。其它因素包含施用的时间和途径、排泄速率、药物组合以及经受疗法的特定疾病的类型和严重程度。
[0242]
本发明进一步涉及一种用于制造用于抑制或负调节哺乳动物(例如,人)的enpp1蛋白活性(例如,治疗不受控细胞增殖病症或与enpp1功能障碍相关的一种或多种神经退行性病症)的药物的方法,所述方法包括将一种或更多种所公开化合物、产物或组合物与药学上可接受的载体或稀释剂组合。因此,在一方面,本发明涉及一种用于制造药物的方法,所述方法包括将至少一种所公开化合物或至少一种所公开产品与药学上可接受的载体或稀释剂组合。
[0243]
所公开的药物组合物可进一步包含其他治疗活性化合物,其通常用于治疗上述病理状况。
[0244]
应理解,所公开组合物可以由所公开化合物制备。还应理解,所公开组合物可以在所公开的使用方法中使用。
[0245]
使用化合物和组合物的方法
[0246]
所公开的化合物可作为单一药剂或与一种或更多种其他药物组合使用,用于治疗、预防、控制、改善或降低上述疾病、紊乱和条件的风险,其中式i或ii 化合物或其他药物对这些疾病、紊乱和条件具有效用,其中将药物组合在一起比单独使用任何一种药物更安全或更有效。因此,可以通过途径并且以常用的量将一种或多种其它药物与所公开化合物同时地或顺序地施用。当所公开化合物与一种或更多种其它药物同时使用时,含有此类药物和所公开化合物的单位剂型的药物组合物是优选的。然而,组合疗法也可以根据重叠时间表施用。还设想的是,一种或更多种活性成分与所公开化合物的组合将比作为单一试剂更有效。
[0247]
本发明的药物组合物和方法可进一步包含如本文所述的其他治疗活性化合物,其通常用于治疗上述病理状况。
[0248]
治疗方法
[0249]
本文公开的化合物可用于治疗、预防、改善、控制多种病症或降低其风险,其中患者或受试者将受益于enpp1的抑制或负调节。在一方面,提供了一种治疗或预防受试者的病症的方法,所述方法包括以有效剂量和有效量向所述受试者施用至少一种所公开化合物;至少一种所公开的药物组合物;和/或至少一种所公开产品以治疗所述受试者的所述病症的步骤。
[0250]
还提供了一种用于治疗受试者的一种或多种病症的方法,对于所述病症,预测enpp1抑制是有益的,所述方法包括以有效剂量和有效量向所述受试者施用至少一种所公开化合物;至少一种所公开的药物组合物;和/或至少一种所公开产品以治疗所述受试者的所述病症的步骤。
[0251]
在一方面,提供了一种用于治疗不受控细胞增殖病症的方法,所述方法包括:以有效剂量和有效量向受试者施用至少一种所公开化合物;至少一种所公开的药物组合物;和/或至少一种所公开产品以治疗所述受试者的所述病症。在另外的方面,提供了一种用于治疗或预防神经退行性病症的方法,所述方法包括:以有效剂量和有效量向受试者施用至少一种所公开化合物;至少一种所公开的药物组合物;和/或至少一种所公开产品以治疗所述受试者的所述病症。还提供了一种用于治疗哺乳动物的病症的方法,所述方法包括向所述哺乳动物施用至少一种所公开化合物、组合物或药物的步骤。
[0252]
本发明涉及化学组合物通过施用一种或更多种所公开化合物或产品来治疗患者(优选地人)的疾病或病症的用途,其中预测enpp1抑制具有治疗效果,如不受控细胞增殖病症(例如,癌症)和神经退行性病症,如阿尔茨海默氏病、亨廷顿氏病和帕金森氏病、由细菌和/或病毒(包括dna和rna病毒)引起的疾病。
[0253]
本发明的化合物还可以用于免疫疗法。在一个实施方式中,本发明的化合物通过免疫疗法治疗不受控细胞增殖病症和/或由细菌和/或病毒引起的疾病,这意味着所述化合物引发免疫疗法反应,这导致这些疾病的治疗。
[0254]
本文公开的化合物可用于治疗、预防、改善、控制多种不受控细胞增殖病症或降低其风险。
[0255]
还提供了所公开化合物、组合物或药物的使用方法。在一方面,使用方法涉及病症的治疗。在另外的方面,所公开化合物可以作为单一药剂或与一种或更多种其它药物组合用于治疗、预防、控制、改善化合物或其它药物对其具有效用的上述疾病、病症和病状或降低其风险,其中药物组合在一起比任一单独的药物更安全或更有效。因此,可以通过途径并且以常用的量将一种或多种其它药物与所公开化合物同时地或顺序地施用。当所公开化合物与一种或更多种其它药物同时使用时,含有此类药物和所公开化合物的单位剂型的药物组合物是优选的。然而,组合疗法也可以根据重叠时间表施用。还设想的是,一种或更多种活性成分与所公开化合物的组合可以比作为单一试剂更有效。
[0256]
可用所提供的化合物治疗的病症的实施例包含不受控细胞增殖病症。在又另外的方面,不受控细胞增殖病症是癌症。在又另外的方面,癌症是白血病。在甚至另外的方面,癌症是肉瘤。在仍另外的方面,癌症是实体瘤。在又另外的方面,癌症是淋巴瘤。
[0257]
应理解,癌症是指或描述哺乳动物中通常以不受调节的细胞生长为特征的生理病状。癌症可以具有多重耐药性(mdr)或药物敏感性。癌症的实施例包含但不限于癌、淋巴瘤、胚细胞瘤、肉瘤和白血病。此类癌症的更具体的实施例包含乳腺癌、前列腺癌、结肠癌、鳞状细胞癌、小细胞肺癌、非小细胞肺癌、胃肠癌、胰腺癌、宫颈癌、卵巢癌、腹膜癌、肝癌,例如肝癌、膀胱癌、结肠直肠癌、子宫内膜癌、肾癌和甲状腺癌。
[0258]
在各个方面,癌症的另外实施例是基底细胞癌、胆道癌;骨癌;脑和cns 癌症;绒毛膜癌;结缔组织癌;食道癌;眼癌;头颈癌;胃癌;上皮内肿瘤;喉癌;淋巴瘤,包含霍奇金淋巴瘤和非霍奇金淋巴瘤;黑色素瘤;骨髓瘤;神经母细胞瘤;口腔癌(例如,唇、舌、嘴和咽);视网膜母细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;肉瘤;皮肤癌;胃癌;睾丸癌;子宫癌;泌尿系统癌症,以及其它癌和肉瘤。
[0259]
在另外的方面,癌症是血液学癌症。在仍另外的方面,血液学癌症选自急性髓性白血病(aml)、急性淋巴细胞白血病(all)、慢性髓性白血病(cml)、慢性淋巴细胞白血病
(cll)、毛细胞白血病、慢性粒单核细胞白血病(cmml)、幼儿粒单细胞白血病(jmml)、霍奇金淋巴瘤、非霍奇金淋巴瘤、多发性骨髓瘤、孤立性骨髓瘤、局限性骨髓瘤和髓外骨髓瘤。在仍另外的方面,癌症选自慢性淋巴细胞白血病、小淋巴细胞淋巴瘤、b细胞非霍奇金淋巴瘤和大b细胞淋巴瘤。
[0260]
在另外的方面,癌症是脑癌。在仍另外的方面,脑癌选自神经胶质瘤、成神经管细胞瘤、原始神经外胚层肿瘤(pnet)、听神经瘤、神经胶质瘤、脑膜瘤、垂体腺瘤、神经鞘瘤、cns淋巴瘤、原始神经外胚层肿瘤、颅咽管瘤、脊索瘤、成神经管细胞瘤、脑神经母细胞瘤、中枢神经细胞瘤、松果体细胞瘤、松果体母细胞瘤、非典型畸胎样横纹肌样瘤、软骨肉瘤、软骨瘤、脉络丛癌、脉络丛乳头状瘤、颅咽管瘤、胚胎发育不良性神经上皮瘤、神经节细胞瘤、生殖细胞瘤、成血管细胞瘤、血管外皮瘤和转移性脑瘤。在又另外的方面,神经胶质瘤选自室管膜瘤、星形细胞瘤、少突神经胶质瘤和少突星形细胞瘤。在甚至另外的方面中,神经胶质瘤选自幼儿毛细胞性星形细胞瘤、室管膜下巨细胞性星形细胞瘤、神经节神经胶质瘤、室管膜下瘤、多形性黄色星形细胞瘤、间变性星形细胞瘤、多形性成胶质细胞瘤、脑干神经胶质瘤、少突神经胶质瘤、室管膜瘤、少突星形细胞瘤、小脑星形细胞瘤、婴儿促纤维增生型星形细胞瘤、室管膜下巨细胞性星形细胞瘤、弥散性星形细胞瘤、混合型神经胶质瘤、视神经胶质瘤、脑神经胶质瘤、多灶性神经胶质细胞瘤、多中心多形性成胶质细胞瘤、副神经节瘤和神经节神经胶质瘤。
[0261]
在一方面,癌症可以是选自以下的癌症:血液癌、脑癌、泌尿生殖道癌、胃肠道癌、结肠癌、直肠癌、乳腺癌、肾癌、淋巴系统癌、胃癌、肺癌、胰腺癌和皮肤癌。在另外的方面,癌症选自前列腺癌、多形性成胶质细胞瘤、子宫内膜癌、乳腺癌和结肠癌。在另外的方面,癌症选自乳腺癌、卵巢癌、前列腺癌、头癌、颈癌和肾癌。在仍另外的方面,癌症选自血液癌、脑癌、泌尿生殖道癌、胃肠道癌、结肠癌、直肠癌、乳腺癌、肝癌、肾癌、淋巴系统癌、胃癌、肺癌、胰腺癌和皮肤癌。在又另外的方面,癌症选自肺癌和肝癌。在甚至另外的方面,癌症选自乳腺癌、卵巢癌、睾丸癌和前列腺癌。在仍另外的方面,癌症是乳腺癌。在又另外的方面,癌症是卵巢癌。在甚至另外的方面,癌症是前列腺癌。在仍另外的方面,癌症是睾丸癌。
[0262]
在各个方面,与enpp1功能障碍相关的病症包含神经退行性病症。在另外的方面,神经退行性疾病选自阿尔茨海默氏病、帕金森氏病和亨廷顿氏病。
[0263]
化合物可进一步用于预防、治疗、控制、改善本文所述的疾病、病症和病状或降低其风险的方法中。化合物与其它药剂的组合可进一步用于预防、治疗、控制、改善上述疾病、病症和病状或降低其风险的方法中。
[0264]
本发明进一步涉及施用enpp1抑制剂,以改善在不受控细胞增殖病症(包含癌症)的背景下的治疗结果。即,在一方面,本发明涉及共治疗方法,其包括向哺乳动物施用有效量和剂量的与癌症疗法有关的至少一种本发明化合物的步骤。
[0265]
在另外的方面,在癌症疗法的背景下,施用改善了治疗结果。与癌症疗法有关的施用可以是连续的或间歇的。施用不需要与疗法同时进行并且可以在疗法之前、期间和/或之后进行。例如,癌症疗法可以在施用化合物之前或之后的 1天、2天、3天、4天、5天、6天、7天内提供。作为另外的实施例,癌症疗法可以在施用化合物之前或之后的1周、2周、3周或4周内提供。作为仍另外的实施例,认知或行为疗法可以在所施用化合物的1个、2个、3个、4个、5 个、6个、7个、8个、9个或10个半衰期的时间段内在施用之前或之后提供。
[0266]
在一方面,所公开化合物可以与一种或更多种其它药物组合用于治疗、预防、控制、改善所公开化合物或其它药物可以对其具有效用的疾病或病状或降低其风险,其中药物组合在一起比任一单独的药物更安全或更有效。因此,可以通过途径并且以常用的量将此类一种或多种其它药物与本发明的化合物同时地或顺序地施用。当本发明的化合物与一种或更多种其它药物同时使用时,含有此类其它药物和所公开化合物的单位剂型的药物组合物是优选的。然而,组合疗法还可以包含其中根据不同的重叠时间表施用所公开化合物和一种或更多种其它药物的疗法。还经考虑,当与一种或更多种其它活性成分组合使用时,所公开化合物和其它活性成分可以以比在各自单独使用时更低的剂量使用。在一个实施方式中,本发明涉及一种组合疗法,其中式i或式ii化合物与放射疗法一起使用。可以在施用本发明化合物之前或之后同时进行放射治疗。
[0267]
因此,药物组合物包含除了本发明的化合物之外含有一种或更多种其它活性成分的那些。
[0268]
上述组合不仅包含所公开化合物与一种其它活性化合物的组合,还包含所公开化合物与两种或更多种其它活性化合物的组合。同样,所公开化合物可以与其它药物组合使用,所述其它药物用于预防、治疗、控制、改善所公开化合物对其有用的疾病或病状或降低其风险。因此,可以通过途径并且以常用的量将此类其它药物与本发明的化合物同时地或顺序地施用。当本发明的化合物与一种或更多种其它药物同时使用时,除了所公开化合物之外还含有此类其它药物的药物组合物是优选的。因此,药物组合物包含除了本发明的化合物之外还含有一种或更多种其它活性成分的那些。
[0269]
所公开化合物与第二活性成分的重量比可以改变并且将取决于每种成分的有效剂量。通常,将使用各自的有效剂量。因此,例如,当本发明的化合物与另一种药剂组合时,所公开化合物与另一种药剂的重量比的范围通常为约1000:1 到约1:1000,优选地约200:1到约1:200。本发明的化合物与其它活性成分的组合通常也将处于上述范围内,但是在每种情况下,应使用每种活性成分的有效剂量。
[0270]
在此类组合中,所公开化合物和其它活性剂可以单独或联合施用。另外,一种要素的施用可以在一种或多种其它药剂的施用之前、同时或之后。
[0271]
因此,主题化合物可以单独使用或与已知对受试者适应症有益的其它药剂或影响受体或酶的其它药物组合使用,所述受体或酶提高所公开化合物的功效、安全性、便利性或降低其不想要的副作用或毒性。主题化合物和其它药剂可以以伴随疗法中或固定组合的方式共同施用。
[0272]
在一方面,化合物可以与抗癌治疗剂或其它已知的治疗剂组合使用。
[0273]
在治疗需要抑制或负调节enpp1的病状中,适当的剂量水平通常将为约 0.01到1000mg每kg患者体重每天,其可以以单剂量或多剂量施用。优选地,剂量水平将为约0.1到约250mg/kg每天;更优选地约0.5到约100mg/kg每天。合适的剂量水平可以为约0.01到250mg/kg每天、约0.05到100mg/kg每天或约0.1到50mg/kg每天。在此范围内,剂量可以为0.05到0.5、0.5到5或5到 50mg/kg每天。对于口服施用,组合物优选地以含有1.0到1000毫克活性成分,具体地1.0、5.0、10、15、20、25、50、75、100、150、200、250、300、400、 500、600、750、800、900和1000毫克活性成分的片剂形式提供,以对待治疗患者的剂量进行对症调整。化合物可以根据1到4次每天,优选地一次或两次每天的方案施用。可以调整这种剂量方案
以提供最佳的治疗反应。然而,应理解,用于任何特定患者的具体剂量水平和剂量频率可以变化,并且将取决于多种因素,包含所采用的具体化合物的活性、所述化合物的代谢稳定性和作用时间长度、年龄、体重、总体健康、性别、饮食、施用模式和时间、排泄速率、药物组合、特定病状的严重程度和经受疗法的宿主。
[0274]
因此,在一方面,本发明涉及用于以调节或活化enpp1活性反应的有效量抑制或负调节至少一个细胞中的enpp1的方法,例如在所述至少一个细胞中,所述方法包括使所述至少一个细胞与至少一种本发明的化合物接触的步骤。在另外的方面,细胞是哺乳动物,例如人。在另外的方面,在接触步骤之前已经从受试者分离细胞。在另外的方面,接触是通过向受试者施用进行的。
[0275]
不受控细胞增殖病症的治疗
[0276]
在一方面,本发明涉及一种用于治疗哺乳动物的不受控细胞增殖病症的方法,所述方法包括向所述哺乳动物施用有效量的至少一种所公开化合物或所公开的制备化合物、或其药学上可接受的盐、水合物、溶剂化物或多晶型物的方法的产品的步骤,由此治疗不受控细胞增殖病症。
[0277]
在仍另外的方面,有效量是治疗有效量。在又仍另外的方面,有效量是预防有效量。
[0278]
在另外的方面,哺乳动物是人。在又另外的方面,方法进一步包括鉴定需要治疗不受控细胞增殖病症的哺乳动物的步骤。在仍另外的方面,在施用步骤之前,已经诊断哺乳动物需要治疗不受控细胞增殖病症。
[0279]
在另外的方面,不受控细胞增殖病症是癌症。在又另外的方面,癌症是白血病。在甚至另外的方面,癌症是肉瘤。在仍另外的方面,癌症是实体瘤。在又另外的方面,癌症是淋巴瘤。在甚至另外的方面,癌症选自慢性淋巴细胞白血病、小淋巴细胞淋巴瘤、b细胞非霍奇金淋巴瘤和大b细胞淋巴瘤。在仍另外的方面,癌症选自血液癌、脑癌、泌尿生殖道癌、胃肠道癌、结肠癌、直肠癌、乳腺癌、肝癌、肾癌、淋巴系统癌、胃癌、肺癌、胰腺癌和皮肤癌。在又另外的方面,癌症选自肺癌和肝癌。在甚至另外的方面,癌症选自乳腺癌、卵巢癌、睾丸癌和前列腺癌。在仍另外的方面,癌症是乳腺癌。在又另外的方面,癌症是卵巢癌。在甚至另外的方面,癌症是前列腺癌。在仍另外的方面,癌症是睾丸癌。
[0280]
实施例
[0281]
实验
[0282]
提出以下实施例以便为本领域的普通技术人员提供如何制备和评价本文要求保护的化合物、组合物、制品、装置和/或方法的完整公开和描述,并且旨在纯粹是本发明的示例性说明而不旨在限制诸位发明人所认为的其发明的内容的范围。虽然已经做出努力确保关于数字(例如,量、温度等)的准确性,但是仍应考虑一些误差和偏差。除非另外指明,否则份数为按重量计份数,温度是以c 为单位或处于环境温度下,并且压力处于或接近大气压。
[0283]
在以下实施例中说明了用于制备本发明的化合物的若干种方法。起始材料和必需的中间体在一些情况下是可商购获得的,或可以根据文献程序或如本文中所展示来制备。
[0284]
合成本发明的以下示例性化合物。本文提供实施例以说明本发明,并且不应被解释为以任何方式限制本发明。根据iupac命名惯例,实施例通常以游离碱形式进行描绘。然而,所述实施例中的一些实施例以盐的形式获得或分离。
[0285]
所述实施例中的一些实施例是作为一种或更多种对映异构体或非对映异构体的外消旋混合物获得的。本领域的技术人员可以分离化合物以分离单独的对映异构体。分离可以通过将化合物的外消旋混合物偶联到对映体地纯的化合物以形成非对映异构体混合物,随后通过标准方法(例如,分级结晶或色谱法)分离单独的非对映体来进行。还可以通过使用手性固定相的色谱方法直接分离化合物的外消旋或非对映体混合物。
[0286]
实验化学
[0287]
合成方案、方法和程序:
[0288]
总体方案1
[0289][0290][0291]
实施例1:(n-(3-((6,7-二甲氧基喹唑啉-4-基)氧基)丙基)磺酰胺的合成:
[0292]
步骤1:叔丁基(n-(3-羟丙基)氨磺酰基)氨基甲酸的合成
[0293][0294]
在0℃下,向二氯甲烷(20ml)中的3-氨基丙烷-1-醇1(500mg,6666mmol) 的搅拌溶液中添加二异丙基乙胺(1.9ml,9999mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)-亚基)-n-甲基甲酰胺2(2.25g,7.385mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过100-200硅胶柱色谱纯化,通过在二氯甲烷中的3%甲醇洗脱,得到半纯化合物。用石油醚中的50%乙酸乙酯洗涤该半纯品,得到的(n-(3-羟丙基)氨磺酰基)氨基甲酸叔丁基3(650mg,2.559mmol,38%产率)为灰白色固体。
[0295]
1h nmr(400mhz,dmso)δ10.77(s,1h),7.45(t,1h),4.44(t,1h),3.40(d, 2h),2.91(d,2h),1.60-1.57(t,2h),1.41(s,9h)
[0296]
通过使用上述一般程序合成以下化合物。
[0297][0298][0299]
步骤2:叔丁基(n-(3-((6,7-二甲氧基喹唑啉-4-基)氧基)丙基)氨磺酰基)氨基甲酸的合成
[0300][0301]
向二氯甲烷(20ml)中的叔丁基(n-(3-羟丙基)氨磺酰)氨基甲酸酯4(900mg,3.897mmol)的搅拌溶液中添加60%nah(212mg,5.314mmol),然后回流搅拌30分钟。然后在室温下加入4-氯-6,7-二甲氧基喹唑啉3(795mg,3.542mmol),再次在回流下搅拌16小时。通过tlc监测反应进程。反应完成后,向反应混合物中加入水(200ml)并用乙酸乙酯(2
×
100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗化合物通过100-200硅胶柱层析纯化,通过100%乙酸乙酯洗脱,得到呈淡黄色固体的叔丁基(n-(3-((6,7-二甲氧基喹唑啉-4-基)氧基)丙基)氨磺酰基)氨基甲酸5(700mg,1.583mmol,44%产率)。1hnmr(400mhz,dmso)δ10.85(s,1h),8.60(s,1h),7.71(s,1h),7.31(d,2h),4.55(t,2h),3.92(d,6h),3.12(d,2h),2.01(m,2h),1.37(s,9h)。lc-ms:m/z:442.9(m+1)
[0302]
通过使用上述一般程序合成以下化合物。
[0303]
[0304][0305]
步骤3:(n-(3-((6,7-二甲氧基喹唑啉-4-基)氧基)丙基)磺酰胺)的合成
[0306][0307]
在0℃下,向1,4-二氧六环(2ml)中的叔丁基(n-(3-(6,7-二甲氧基喹唑啉-4
‑ꢀ
基)氧基)丙基)氨磺酰)氨基甲酸酯(200mg,0.452mmol)搅拌溶液中添加4m hcl 到二氧六环(8ml),然后在室温下搅拌3小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过制备型prep-hplc 方法纯化粗化合物,得到淡黄色固体形式的(n-(3-(6,7-二甲氧基喹唑啉-4-基)氧基)丙基)磺胺)(目标-12)(120mg,0.35mmol,78%产率)纯化合物。1h nmr(400 mhz,dmso)δ8.93(s,1h),7.42(d,2h),6.57(bs,2h),4.67(t,2h),3.96(d,6h), 3.10(t,2h),2.06(t,2h)。
[0308]
通过使用上述一般程序合成以下化合物。
[0309][0310]
[0311]
化合物052也基于实施例1的一般程序制备。
[0312][0313]
1h nmr(400mhz,dmso)δ8.93(s,1h),7.42(d,2h),6.57(bs,2h),4.67(t, 2h),3.96(d,6h),3.10(t,2h),2.06(t,2h)。lcms 342.9;mw 378.83。
[0314]
总体方案2:
[0315]
[0316][0317]
实施例2:n-(3-((6,7-二甲氧基喹唑啉-4-基)氨基)丙基磺酰胺盐酸盐
[0318]
步骤1:n1-(6,7-二甲氧基喹唑啉-4-基)丙烷-1,3-二胺
[0319][0320]
在室温下,向4-氯-6,7-二甲氧基喹唑啉(2g,8.9mmol)在四氢呋喃(20ml)中的搅拌溶液中添加丙烷-1,3-二胺(3.7ml,44.50mmol),并在室温下搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过grace反相色谱纯化,通过在水中洗脱 40%乙腈,得到的n1-(6,7-二甲氧基喹唑啉-4-基)丙烷-1,3-二胺的纯化合物(50 0mg,1.908mmol,21%产率)为浅棕色固体。1h nmr(400mhz,dmso)8.3(s, 1h),8.0(brs,1h),7.57(s,1h),7.05(s,1h),3.86(s,6h),3.55-3.46(m,2h),2.64(t, 3h),1.75-1.68(m,2h)。
[0321]
1.98(s,2h),1.15(d,9h)。
[0322]
通过使用上述一般程序合成以下化合物
[0323][0324]
步骤2:叔丁基(n-(3-((6,7-二甲氧基喹唑啉-4-基)氨基)丙基)氨磺酰基)氨基甲酸的合成
[0325][0326]
在室温下,向n1-(6,7-二甲氧基喹唑啉-4-基)丙烷-1,3-二胺(500mg,1.90mmol)在二氯甲烷(40ml)中的搅拌溶液中添加二异丙基乙胺(1.65ml,9.50mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚偏基)-n-甲基甲酰胺氯化物(640mg,1.90mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过用二氯甲烷中的2%甲醇洗脱来纯化粗制化合物,得到的(n-(3-((6,7-二甲氧基喹唑啉-4-基)氨基)丙基)氨磺酰基)氨基甲酸叔丁基(600mg,1.36mmol,71%产率)为黄色固体。1hnmr(400mhz,dmso)10.83(s,1h),8.31(s,1h),7.89(t,1h),7.60(s,
1h),7.54 (s,1h),7.06(s,1h)3.87(s,6h),3.55-3.50(m,2h),2.98-2.93(m,2h),1.82(t,2h), 1.36(s,9h)。lcms:(m+h+):m/z:441.9
[0327]
通过上述一般程序合成以下化合物
[0328][0329][0330]
步骤3:n-(3-((6,7-二甲氧基喹唑啉-4-基)氨基)丙基)磺酰胺盐酸盐的合成
[0331]
将4m hcl在二氧六环(2ml)中加入1,4-二氧六环(0.5ml)中的叔丁基 (n-(3-(6,7-二甲氧基喹唑啉-4-基)氨基)丙基)氨磺酰)氨基甲酸酯(200mg,0.453 mmol)在室温下搅拌溶液,然后在50℃下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶
剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc纯化,得到的纯化合物(n-(3-((6,7-二甲氧基喹唑啉-4-基)氨基)丙基) 磺酰胺盐酸盐(100mg,0.293mmol,65%产率)为灰白色固体。1h nmr(400mhz, dmso)14.42(brs,1h),9.99(s,1h),8.79(s,1h),8.02(s,1h),7.23(s,1h),6.61(s, 1h),6.53(s,1h),3.94(s,6h),3.73-3.71(m,2h),2.97-2.96(m,2h),1.90-1.86(m, 2h)。lcms:(m+h+):m/z:341.9
[0332]
通过上述一般程序合成以下化合物:
[0333][0334][0335]
化合物055也通过上述一般程序合成:
[0336][0337]
1h nmr 400mhz,dmso)14.42(brs,1h),9.99(s,1h),8.79(s,1h),8.02(s, 1h),7.23(s,1h),6.61(s,1h),6.53(s,1h),3.94(s,6h),3.73-3.71(m,2h), 2.97-2.96(m,2h),1.90-1.86(m,2h)。lcms 341.9。mw.377.84
[0338]
化合物006的合成
[0339][0340]
步骤1:4-((3-氨基丙基)氨基)-6,7-二甲氧基喹啉-3-腈(3)的合成
[0341][0342]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(150mg,0.60mmol)在thf(15ml)中的搅拌溶液中添加丙烷-1,3-二胺2(223mg,3.02mmol),然后在50℃下搅拌反应混合物20小时。通过tlc监测反应进程。反应完成后,反应混合物完全蒸出并吸附在硅藻土上,使用acn/水系统
进行反相grace处理,得到的4-((3-氨基丙基) 氨基)-6,7-二甲氧基喹啉-3-腈(250mg)为白色固体。
[0343]
分析数据:1h nmr(400mhz,dmso):δ8.37(s,1h),8.19(brs,1h),7.9(brs, 1h),7.78(s,1h),7.22(s,1h),3.99-3.89(m,7h),3.83(q,2h),2.87(t,2h),1.99(t, 2h)。
[0344]
步骤2:叔丁基(n-(3-((3-氰基-6,7-二甲氧基喹啉-4-基)氨基)丙基)氨磺酰基) 氨基甲酸(5)的合成
[0345][0346]
向dcm(10ml)中的4-(3-氨基丙基)氨基)-6,7-二甲氧基喹啉-3-碳腈3(150 mg,0.52mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶
ꢀ‑
4(1h)-亚基)-n-甲基甲酰胺氯化物4(193mg,0.57mmol),然后在相同温度下添加dipea(0.3ml,0.78mmol)。将反应混合物在室温下搅拌16小时。通过tlc 监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。通过在dcm 中洗脱2-3%meoh,通过combi-flash色谱法纯化粗产物,得到的叔丁基(n-(3-((3
‑ꢀ
氰基-6,7-二甲氧基喹啉-4-基)氨基)丙基)氨磺酰基)氨基甲酸酯5(100mg)为白色固体。
[0347]
分析数据:lcms:(m+h)
+
:m/z:466.2
[0348]
第3步:化合物006的合成:
[0349][0350]
在0℃下,向二氯甲烷(3ml)中的叔丁基(n-(3-(3-(3-氰基-6,7-二甲氧基喹啉
ꢀ‑
4-基)氨基)丙基)氨磺酰)氨基甲酸酯5(95mg,0.40mmol)的搅拌溶液中添加4mhcl到二氧六环(2ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc纯化,得到的化合物006(10mg)为白色固体。
[0351]
分析数据:1h nmr(400mhz,dmso)δ:8.33(s,1h),7.79(t,1h),7.59(s, 1h),7.21(s,1h),6.60(brs,2h),6.53(brs,2h),3.90-3.89(m,6h),3.78(q,2h), 2.99(q,2h),1.92(p,2h)。
[0352]
lcms:(m+h)
+
:m/z:366.2。
[0353]
化合物007的合成:
[0354][0355]
步骤1:4-((4-氨基丁基)氨基)-6,7-二甲氧基喹啉-3-腈3的合成:
[0356][0357]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(200mg,0.80mmol)在thf(8ml)中的搅拌溶液中添加丁烷-1,4-二胺2(411mg,4.03mmol),然后在50℃下搅拌反应混合物20小时。通过tlc监测反应进程。反应完成后,反应混合物完全蒸出并吸附在硅藻土上,使用acn/水系统进行反相grace处理,得到的4-((4-氨基丁基) 氨基)-6,7-二甲氧基喹啉-3-腈3(220mg)为白色固体。
[0358]
分析数据:1h nmr(400mhz,dmso):δ8.37(s,2h),8.32(s,1h),7.67(s, 1h),7.21(s,1h),3.90-3.89(m,7h),3.76(t,2h),2.79(t,2h),1.78-1.73(m,2h), 1.67-1.64(m,2h)。
[0359]
步骤2:叔丁基(n-(4-((3-氰基-6,7-二甲氧基喹啉-4-基)氨基)丁基)氨磺酰基) 氨基甲酸5的合成:
[0360][0361]
向dcm(10ml)中的4-(4-氨基丁基)氨基)-6,7-二甲氧基喹啉-3-碳腈3(220 mg,0.73mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶
ꢀ‑
4(1h)-亚基)-n-甲基甲酰胺氯化物4(296mg,0.88mmol),然后在相同温度下添加dipea(0.4ml,2.19mmol)。将反应混合物在室温下搅拌16小时。通过tlc 监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。通过在dcm 中洗脱2-3%meoh,通过combi-flash色谱法纯化粗品,得到的叔丁基(n-(4-((3
‑ꢀ
氰基-6,7-二甲氧基喹啉-4-基)氨基)丁基)氨磺酰基)氨基甲酸酯5(100mg)为白色固体。
[0362]
分析数据:1h nmr(400mhz,dmso):δ8.46-8.44(m,1h),8.31(s,1h), 7.82(t,1h),7.60-7.57(m,2h),7.20(s,1h),3.90-3.89(m,6h),3.72(q,2h), 2.92-2.91(m,2h),1.73-1.70(m,2h),1.58-1.54(m,2h)。
[0363]
lcms:(m+h)
+
:m/z:480
[0364]
步骤3:化合物007的合成:
[0365][0366]
在0℃下,向二氯甲烷(3ml)中的叔丁基(n-(4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)氨基)氨磺酰)氨基甲酸酯(100mg,0.20mmol)的搅拌溶液中添加4m hcl到二氧六环(1ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc纯化,得到化合物007(10mg),为白色固体。
[0367]
分析数据:1h nmr(400mhz,dmso)δ:8.35-8.31(m,2h),7.86(t,1h),7.60 (s,1h),7.20(s,1h),6.50(t,2h),6.46(s,1h),3.90-3.89(m,6h),3.73(q,2h),2.90 (q,2h),1.75-1.71(m,2h),1.61-1.53(m,2h)。
[0368]
lcms:(m+h)
+
:m/z:380.24。
[0369]
化合物008的合成方案:
[0370][0371]
步骤1:4-((5-氨基戊基)氨基)-6,7-二甲氧基喹啉-3-腈3的合成:
[0372][0373]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(200mg,0.80mmol)在thf(8ml)中的搅拌溶液中添加丁烷-1,4-二胺2(411.2mg,4.03mmol),然后在50℃下搅拌反应混合物20小时。通过tlc监测反应进程。反应完成后,反应混合物完全蒸出并吸附在硅藻土上,使用acn/水系统进行反相grace处理,得到的4-((5-氨基戊基) 氨基)-6,7-二甲氧基喹啉-3-腈3(200mg)为白色固体。
[0374]
分析数据:1h nmr(400mhz,dmso):δ8.48(s,1h),8.30(s,1h),7.98(brs, 1h),7.66(s,1h),7.19(s,1h),3.90-3.89(m,6h),3.72-3.71(m,2h),2.60-2.56(m, 2h),1.73-1.66(m,2h),1.48-1.21(m,4h)。
[0375]
lcms:(m+h)
+
:m/z:315.23
[0376]
步骤2:叔丁基(n-(5-((3-氰基-6,7-二甲氧基喹啉-4-基)氨基)戊基)氨磺酰基) 氨基甲酸5的合成:
[0377][0378]
向dcm(10ml)中的4-(5-氨基戊基)氨基)-6,7-二甲氧基喹啉-3-碳腈3(220 mg,0.63mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶
ꢀ‑
4(1h)-亚基)-n-甲基甲酰胺氯化物4(266mg,0.76mmol),然后在相同温度下添加dipea(0.17ml,0.95mmol)。将反应混合物在室温下搅拌16小时。通过tlc 监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。通过在dcm 中洗脱2-3%meoh,通过combi-flash色谱法纯化粗品,得到的叔丁基(n-(5-((3
‑ꢀ
氰基-6,7-二甲氧基喹啉-4-基)氨基)戊基)氨磺酰基)氨基甲酸酯5(130mg)为白色固体。
[0379]
分析数据:1h nmr(400mhz,dmso):δ10.75(s,1h),8.31(s,1h),7.82(t, 1h),7.60(s,1h),7.51(brs,1h),7.20(s,1h),3.90-3.89(m,6h),3.71(q,2h),2.87 (q,2h),1.72-1.64(m,2h),1.58-1.47(m,2h),1.22(m,2h)。
[0380]
lcms:(m+h)
+
:m/z:494.2
[0381]
步骤3:化合物008的合成:
[0382][0383]
在0℃下,向二氯甲烷(4ml)中的叔丁基(n-(5-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)氨基)氨基甲酸酯(130mg,0.20mmol)的搅拌溶液中添加4m hcl到二氧六环 (1.5ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc纯化,得到的化合物008(10mg)为白色固体。
[0384]
分析数据:1h nmr(400mhz,dmso)δ:8.31(s,1h),8.12(s,1h),7.84(t, 1h),7.60(s,1h),7.20(s,1h),6.45-6.44(m,3h),3.90-3.89(m,6h),3.72(q,2h), 2.86(q,2h),3.01(t,2h),1.73-1.65(m,2h),1.55-1.48(m,2h),1.43-1.40(m,2h)
[0385]
lcms:(m+h)
+
:m/z:394.2.
[0386]
化合物009和010的合成方案
[0387][0388]
n1-(7-(苄氧基)-6-甲氧基喹唑啉-4-基)丁烷-1,4-二胺(3)的合成
[0389][0390]
在室温下,向7-(苄氧基)-4-氯-6-甲氧基喹唑啉(1)(1g,3.33mmol)在四氢呋喃(20ml)中的搅拌溶液中添加丁烷-1,4-二胺2(1.5g,16.66mmol),并在室温下搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过grace反相色谱纯化,通过在水中洗脱40%乙腈,得到的纯化合物n1-(7-(苄氧基)-6-甲氧基喹唑啉-4-基)丁烷-1,4-二胺(3)(1g,0.284mmol,85%产率)为浅棕色粘稠液体。
[0391]
分析数据:1h nmr(400mhz,dmso)δ8.29(s,1h),7.95-7.98(m,1h),7.59 (s,1h),7.32-7.48(m,5h),7.15(s,1h),5.22(s,2h),3.87(s,3h),3.47-3.51(m,2h), 2.56-2.59(m,2h),1.62-1.66(m,2h),1.41-1.44(m,2h)。
[0392]
lcms:(m+h
+
):m/z:353.2
[0393]
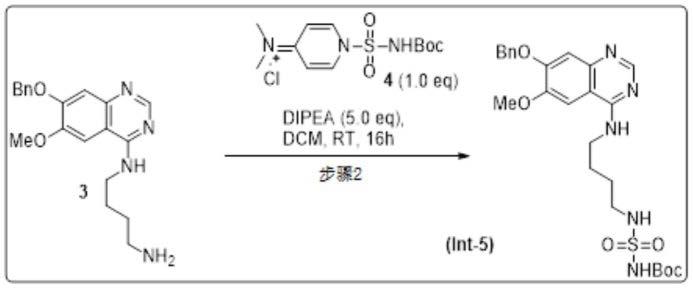
叔丁基(n-(4-((7-(苄氧基)-6-甲氧基喹唑啉-4-基)氨基)丁基)氨磺酰基)氨基甲酸(int-5)的合成
[0394][0395]
在室温下,向n1-(7-(苄氧基)-6-甲氧基喹唑啉-4-基)丁烷-1,4-二胺(3)(1.0g, 2.84mmol)在二氯甲烷(20ml)中的搅拌溶液中添加二异丙基乙胺(1.5ml,8.52 mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺4(957mg,2.84mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过用dcm中的10%meoh洗脱来纯化粗制化合物,得到的(int-5)(1.1g,2.07mmol,73%产率)为浅黄色固体。
[0396]
分析数据:1h nmr(400mhz,dmso)δ10.83(br s,1h),8.3(s,1h),7.93(brs, 1h),7.59-7.561(m,2h),7.46-7.61(d,2h),7.32-7.42(m,3h),7.16(s,1h),5.226(s, 2h),4.03(s,1h),3.88(s,3h),3.46-3.50(m,2h),2.89-2.93(m,2h),1.62-1.66(m, 2h),1.52-1.54(m,2h),1.38(s,9h)。
[0397]
lcms:(m+h)
+
:m/z:532.2
[0398]
叔丁基(n-(4-((7-羟基-6-甲氧基喹唑啉-4-基)氨基)丁基)氨磺酰基)氨基甲酸 (int-6)的合成
[0399][0400]
向叔丁基(n-(4-(7-(苄基氧基)-6-甲氧基喹唑啉-4-基)氨基)氨磺酰)氨基甲酸酯(5)-(1g,1.88mmol)在甲醇(15ml)和乙酸乙酯(2.5ml)中的搅拌溶液中添加10%钯/碳(100mg),并在室温下在气球氢气氛下搅拌反应混合物6小时。通过tlc 监测反应进程。反应完成后,反应混合物通过硅藻土过滤并用含5%甲醇的二氯甲烷(100ml)洗涤硅藻土床。减压浓缩滤液,得到的叔丁基(n-(4-((7-羟基-6-甲氧基喹唑啉-4-基)氨基)丁基)氨磺酰基)氨基甲酸(6)(800mg,1.81mmol,96%产率)为淡黄色固体。
[0401]
分析数据:1h nmr(400mhz,dmso)δ10.13(br s,1h),8.24(s,1h),7.83 (brs,1h),7.54-7.57(m,2h),6.92(s,1h),3.87(s,3h),3.45-3.50(m,2h),2.88-2.93 (m,2h),1.59-1.65(m,2h),1.50-1.53(m,2h),1.38(s,9h)。
[0402]
lcms:(m+h
+
):m/z:442.2
[0403]
化合物009的制备
[0404][0405]
在室温下,向int-6(100mg,0.226mmol)在1,4-二氧六环(1.0ml)中的搅拌溶液中添加4m hcl在二氧六环(2.0ml)中。将反应混合物在室温下搅拌6小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的化合物009的纯化合物(50 mg,0.146mmol,64%产率)为灰白色固体。
[0406]
分析数据:1h nmr(400mhz,dmso-d6)δ14.27(brs,1h),11.41(s,1h),9.80 (s,1h),8.70(s,1h),7.94(s,1h),7.19(s,1h),6.47-6.51(m,3h),3.93(s,3h), 3.61-3.68(m,2h),2.87-2.92(m,2h),1.66-1.71(m,2h),1.49-1.57(m,2h), 1.23-1.28(m,2h)。
[0407]
lcms:(m+h)
+
:m/z:342.1
[0408]
化合物010的制备
[0409][0410]
在室温下,向int-5(100mg,0.188mmol)在1,4-二氧六环(1.0ml)中的搅拌溶液中添加4m hcl在二氧六环(2.0ml)中。将反应混合物在室温下搅拌6小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的纯int-5化合物(50mg,1.16mmol,61%产率)为灰白色固体。
[0411]
分析数据:1h nmr(400mhz,dmso)δ8.3(s,1h),8.14(s,2h),7.92(m,1h), 7.6(s,1h),7.47-7.49(d,2h),7.39-7.41(t,2h),7.35-7.37(m,1h),7.17(s,1h),6.45 (s,1h),5.23(s,2h),3.89(s,3h),3.50-3.51(m,2h),2.89-2.94(m,2h),1.66-1.70 (m,2h),1.54-1.56(m,2h)。
[0412]
lcms:(m+h)
+
:m/z:432.2
[0413]
化合物011的合成方案
[0414][0415]
4-((4-((n-(叔丁氧基羰基)氨磺酰基)氨基)丁基)氨基)-6-甲氧基喹唑啉-7-基三氟甲磺酸酯(int-5)
[0416][0417]
在0℃下,向int-6(500mg,1.13mmol)在二氯甲烷(20ml)中的搅拌溶液中添加三乙胺(0.475ml,3.39mmol)和1,1,1-三氟-n-苯基-n-(三氟甲基)磺酰基)甲磺酰胺2(445mg,1.24mmol),然后在室温下搅拌4小时。通过tlc监测反应进程。反应完成后,在减压下完全蒸馏掉有机溶剂,将水(200ml)加入粗品中并用二氯甲烷(2
×
200ml)分配。用盐水溶液(200ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过combi-flash色谱法纯化,用石油醚中的70%乙酸乙酯洗脱,得到的4-((4-((n-(叔丁氧基羰基)氨磺酰基)氨基)丁基)氨基)-6-甲氧基喹唑啉-7-基三氟甲磺酸盐int-5(450mg,0.785mmol,69%两步产率)为淡黄色固体。
[0418]
lcms:(m+h
+
):m/z:574.1
[0419]
化合物011的制备
[0420]
[0421]
在密封管中,将叔丁基5-(4,4,4,5,5-四甲基-1,3,2-二氧苯甲醛-2-基)-1-吡唑-1
‑ꢀ
羧酸(33mg,0.113mmol)和氟化铯(40mg,0.26mmol)添加到4-(4-(叔丁氧羰基) 氨磺酰)氨基)丁基)氨基)-6-甲氧基喹唑啉-7-基三氟甲烷磺酸int-5(50mg,0.349 mmol)在二氧六环(2ml)和水(05ml)中的搅拌溶液中。然后将反应混合物脱气 30分钟。然后再次脱气5分钟加入四(三苯基膦)钯(0)(100mg,0.0087mmol),并在100℃搅拌反应混合物5小时。通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100 ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。粗品经制备型hplc方法纯化,得到的(化合物011)(10mg,0.127 mmol,29%)为灰白色固体。
[0422]
分析数据:1h nmr(400mhz,dmso)δ12.96(brs,1h),8.39(s,1h),8.23 (brs,1h),8.13(s,2h),7.74(s,2h),6.88(d,1h),6.495(t,1h),6.46(s,2h),4.0(s, 3h),3.53-3.58(q,2h),2.90-2.95(q,2h),1.66-1.72(m,2h),1.55-1.59(m,2h)。
[0423]
lcms:(m+h
+
):m/z:392.1
[0424]
总体方案3
[0425][0426][0427]
实施例3:n-(4-((6,7-二甲氧基喹唑啉-4-基)硫代)丁基)磺酰胺盐酸盐
[0428]
步骤1:6,7-二甲氧基喹唑啉-4-硫醇的合成
[0429][0430]
在室温下,向4-氯-6、7-二甲氧基喹唑啉(500mg,2.2mmol)在乙醇(5ml) 中的搅拌溶液中添加硫脲(338mg,4.44mmol),并在回流下搅拌反应混合物4 小时。通过tlc监测反应进程。反应完成后,使反应混合物在室温下沉降。通过过滤收集形成的固体,其为所需化合物6,7-二甲氧基喹唑啉-4-硫醇(400mg, 1.801mmol,80%产率)为浅棕色固体。1h nmr(400mhz,dmso)δ13.67(s,1h), 8.09-8.10(s,1h),7.90(s,1h),7.16(s,1h),3.93(s,3h),3.89(s,3h)。lcms:(m+h) +:m/z:222.9
[0431]
步骤2:2-(4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁基)异吲哚啉-1,3-二酮的合成
[0432][0433]
向dmf(10ml)中6,7-二甲氧基喹唑啉-4-硫醇(1g,4.5mmol)的搅拌溶液中添加碳酸钾(684mg,4.95mmol)和2-(4-溴丁基)异吲哚啉-1,3-二酮(1.27g,4.5mmol),然后在90℃下搅拌6小时。通过tlc监测反应进程。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分出有机层,水洗,减压浓缩,得到的纯2-(4-((6,7-二甲氧基喹唑啉-4-基)硫代)丁基)异二氢吲哚-1,3-二酮化合物(800mg, 1.891mmol,42%产率)为浅棕色固体。1h nmr(400mhz,dmso)δ8.75(s,1h), 7.81-7.82(m,4h),7.26(s,1h),7.13(s,1h),3.95(s,3h),3.91(s,3h),3.61(t,2h), 3.30-3.36(m,2h),1.75(m,4h)。lcms:(m+h)+:m/z:424.2。
[0434]
通过上述程序合成以下化合物
[0435][0436]
步骤3:4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁胺的合成
[0437][0438]
在室温下,向2-(4-(6,7-二甲氧基喹唑啉-4-基)硫代丁基)异吲哚啉-1,3-二酮 (1.1g,2.60mmol)在乙醇(30ml)中的搅拌溶液中添加90%水合肼(0.163ml,5.2 mmol),然后回流搅拌反应混合物2小时。通过tlc监测反应进程。反应完成后,将反应混合物冷却至室温,形成沉淀。通过过滤收集固体,得到的4-((6,7
‑ꢀ
二甲氧基喹唑啉-4-基)硫代)丁-1-胺(700mg,2.389mmol,92%产率)为浅棕色固体。1h nmr(400mhz,dmso)δ8.81(s,1h),7.29(s,1h),7.16(s,1h),3.95(s, 3h),3.92(s,3h),3.35(t,2h),2.67(t,2h),1.77-1.71(m,2h),1.62-1.56(m,2h)。 lcms:(m+h)+:m/z:294.1
[0439]
通过上述程序合成以下化合物
[0440][0441][0442]
步骤4:叔丁基(n-(4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁基)氨磺酰基)氨基甲酸酯
[0443][0444]
在室温下,向4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁-1-胺5(550mg,1.87mmol) 在二氯甲烷(20ml)中的搅拌溶液中添加二异丙基乙胺(1.6ml,9.38mmol)和 n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚乙基)-n-甲基甲酰胺氯化物4(337mg, 1.87mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。使用组合快速柱色谱法纯化粗化合物,通过在石油醚中洗脱60%乙酸乙酯,得到的叔丁基(n-(4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁基)氨磺酰基)氨基甲酸酯6(150mg,0.317mmol,17%产率)为白色固体。
[0445]
分析数据:1h nmr(400mhz,dmso)δ:10.79(s,h),8.82(s,1h),7.62-7.59 (t,1h),7.30(s,1h),7.17(s,1h),3.95(s,3h),3.93(s,3h),3.34(t,2h),2.94-2.90(m, 2h),1.77-1.70(m,2h),1.64-1.59(m,2h),1.39(s,9h)。
[0446]
lcms:(m+h)+:m/z:473.2
[0447][0448][0449]
步骤5:n-(4-(6,7-二甲氧基喹唑啉-4-基)硫代)丁基)磺胺盐酸盐
[0450][0451]
在室温下,向1,4-二氧六环(1.0ml)中的叔丁基(n-(4-((6,7-二甲氧基喹唑啉-4
‑ꢀ
基)硫代)丁基)氨基甲酸酯(6)(100mg,0.211mmol)在1,4-二氧六环(1.0ml)中的搅拌溶液中添加4m hcl到二氧六环(2ml)中。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗品化合物通过制备型hplc法纯化,得到的纯化合物n-(4-((6,7
‑ꢀ
二甲氧基喹唑啉-4-基)硫代)丁基)磺酰胺盐酸盐(30mg,0.08mmol,25%产率)为白色固体。
[0452]
分析数据:1h nmr(400mhz,dmso)δ8.83(s,1h),7.30(s,1h),7.18(s, 1h),6.53-6.47(m,3h),3.95(s,3h),3.93(s,3h),3.37-3.32(m,2h),2.93-2.88(m, 2h),1.77-1.72(m,2h),1.66-1.60(m,2h)。
[0453]
lcms:(m+h)+:m/z:373.23
[0454]
通过上述一般程序合成以下化合物
[0455][0456][0457]
化合物058也通过上述一般程序合成。
[0458][0459]
1h nmr(400mhz,dmso)δ8.83(s,1h),7.30(s,1h),7.18(s,1h), 6.53-6.47(m,3h),3.95(s,3h),3.93(s,3h),3.37-3.32(m,2h),2.93-2.88(m,2h), 1.77-1.72(m,2h),1.66-1.60(m,2h)。lcms 373.23。mw.408.92
[0460]
化合物059也通过上述一般程序合成。
[0461][0462]
1h nmr(400mhz,dmso)δ8.82(s,1h),7.30(s,1h),7.18(s,1h),6.45(s, 3h),3.95(s,3h),3.93(s,3h),3.34(t,2h),2.86(d,2h),1.72(t,2h),1.48(brs,4h)。 lcms 387.1.mw.422.9
[0463]
化合物013和014的合成方案:
[0464][0465]
步骤1:4-巯基-6,7-二甲氧基喹啉-3-甲腈2的合成:
[0466][0467]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(2000mg,8.06mmol)在乙醇(30ml)中的搅拌溶液中添加硫脲(920mg,12.08mmol),然后回流6小时。通过tlc监测反应进程。反应完成后,将反应混合物完全蒸馏掉并吸附在硅胶上,使用甲醇/dcm 进行grace柱色谱分析,得到的4-巯基-6,7-二甲氧基喹啉-3-腈2(1300mg)为淡粉色固体。
[0468]
分析数据:1h nmr(400mhz,dmso):δ13.51(brs,1h),8.57(s,1h),8.05(s, 1h),7.09(s,1h),3.91-3.88(m,6h)。
[0469]
lcms:(m+h)
+
:m/z:247.1
[0470]
步骤2:4-((4-(1,3-二氧代异吲哚啉-2-基)丁基)硫代)-6,7-二甲氧基喹啉-3-甲
腈4的合成:
[0471][0472]
在室温下,向dmf(10ml)中的4-巯基-6,7-二甲氧基喹啉-3-碳腈2(450mg, 1.8mmol)的搅拌溶液中缓慢添加2-(4-溴丁基)异吲哚啉-1,3-二酮3(513mg,1.8 mmol),然后添加k2co3(277mg,2.01mmol)。添加后,将反应混合物加热至90℃保持6小时。通过tlc监测反应进程。反应完成后,将反应混合物直接倒入冰冷的水中并搅拌。将沉淀出的固体过滤并再次用水洗涤,无需任何进一步纯化即可干燥,得到的4-((4-(1,3-二氧代异吲哚啉-2-基)丁基)硫代)-6,7-二甲氧基喹啉
ꢀ‑
3-甲腈4(600mg)为浅棕色固体。
[0473]
分析数据:1h nmr(400mhz,dmso)δ:8.86(s,1h),7.81-7.75(m,4h),7.66 (s,1h),7.41(s,1h),3.97-3.96(m,6h),3.49(t,2h),3.21(t,2h),1.72-1.65(m,2h), 1.50-1.43(m,2h)。
[0474]
lcms:(m+h)
+
:m/z:448.26
[0475]
步骤3:4-((4-氨基丁基)硫代)-6,7-二甲氧基喹啉-3-甲腈5的合成:
[0476][0477]
向4-(4-(1,3-二氧异辛醇-2-基)丁基)硫代-6,7-二甲氧基喹啉-3-碳腈4(550mg, 1.2mmol)在etoh(10ml)中的搅拌溶液中添加水合肼(0.19ml,3.7mmol),然后回流2小时。通过tlc监测反应进程。完成后,将反应混合物直接吸收到硅藻土上并转化为浆液。粗品通过反相grace柱色谱纯化,洗脱40%acn/水系统,得到的4-((4-氨基丁基)硫代)-6,7-二甲氧基喹啉-3-腈5(80mg)为淡黄色液体。
[0478]
分析数据:1h nmr(400mhz,dmso)δ:8.91(s,1h),7.71(s,1h),7.50(s, 1h),3.99-3.96(m,6h),3.20-3.15(m,2h),2.45-2.44(m,2h),1.53-1.41(m,4h)。
[0479]
lcms:(m+h)
+
:m/z:318.2
[0480]
步骤4:叔丁基(n-(4-((3-氰基-6,7-二甲氧基喹啉-4-基)硫代)丁基)氨磺酰基) 氨基甲酸7的合成:
[0481][0482]
向dcm(10ml)中的4-(4-氨基丁基)硫代)-6,7-二甲氧基喹啉-3-碳腈5(80mg, 0.25mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)
‑ꢀ
亚基)-n-甲基甲酰胺氯化物4(85mg,0.25mmol),然后在相同温度下添加 dipea(0.07ml,0.375mmol)。将反应混合物在室温下搅拌16小时。通过tlc 监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。粗品通过 combi-flash色谱法纯化,通过在己烷中洗脱70%etoac,得到的叔丁基(n-(4-(3
‑ꢀ
氰基-6,7-二甲氧基喹啉-4-基)硫代)氨磺酰)氨基甲酸酯(90mg)为白色固体。
[0483]
分析数据:1h nmr(400mhz,dmso)δ:10.73(s,1h),8.92(s,1h),7.71(s, 1h),7.55-7.50(m,2h),3.99-3.98(m,6h),3.19-3.17(m,2h),2.82-2.81(m,2h), 1.53-1.52(m,4h),1.37(s,9h)
[0484]
lcms:(m+h)
+
:m/z:497.2
[0485]
步骤5:化合物013的合成:
[0486][0487]
在0摄氏度下,向二氯甲烷(3ml)中的叔丁基(n-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)硫代)丁基)氨磺酰)氨基甲酸酯7(90mg,0.18mmol)的搅拌溶液中添加 4m hcl到二氧六环(1ml),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc纯化,得到的化合物013(25mg)为灰白色蓬松固体。
[0488]
分析数据:1h nmr(400mhz,dmso)δ:8.92(s,1h),7.72(s,1h),7.51(s, 1h),6.45-6.42(m,3h),6.45(t,1h)3.99-3.98(m,6h),3.21-3.17(m,2h),2.82-2.77 (m,2h),1.55-1.53(m,4h)。
[0489]
lcms:(m+h)
+
:m/z:397.1。
[0490]
步骤6:4-((5-(1,3-二氧代异吲哚啉-2-基)戊基)硫基)-6,7-二甲氧基喹啉-3-甲腈9的合成:
[0491][0492]
在室温下,向dmf(10ml)中的4-巯基-6,7-二甲氧基喹啉-3-碳腈2(450mg, 1.8mmol)的搅拌溶液中缓慢添加2-(5-溴戊基)异吲哚-1,3-二酮8(540mg,1.8 mmol),然后添加k2co3(273mg,1.98mmol)。添加后,将反应混合物加热至90℃保持6小时。通过tlc监测反应进程。反应完成后,将反应混合物直接倒入冰冷的水中并搅拌。将沉淀出的固体过滤并再次用水洗涤并干燥而无需任何进一步纯化,得到的4-((5-(1,3-二氧代异吲哚啉-2-基)戊基)硫代)-6,7-二甲氧基喹啉-3
‑ꢀ
腈9(600mg)为浅棕色固体。
[0493]
分析数据:1h nmr(400mhz,dmso)δ:8.89(s,1h),7.81-7.75(m,4h),7.69 (s,1h),7.48(s,1h),3.98-3.96(m,6h),3.49(t,2h),3.17(t,2h),1.56-1.46(m,4h), 1.40-1.36(m,2h)。
[0494]
lcms:(m+h)
+
:m/z:462.1
[0495]
步骤7:4-((5-氨基戊基)硫代)-6,7-二甲氧基喹啉-3-甲腈10的合成:
[0496][0497]
向dcm:meoh(1:1)(10ml)中的4-(5-(1,3-二氧异喹啉-2-基)戊基)硫代)-6,7
‑ꢀ
二甲氧基喹啉-3-碳腈9(600mg,1.3mmol)的搅拌溶液中:添加1,2二乙胺(0.43 ml,6.5mmol),然后在40℃下加热16小时。通过tlc监测反应进程。完成后,将反应混合物直接吸收到硅藻土上并转化为浆液。粗品通过反相grace柱色谱纯化,洗脱30-40%acn/水系统,得到的4-((5-氨基戊基)硫代)-6,7-二甲氧基喹啉-3-腈10(200mg)为淡黄色液体。
[0498]
分析数据:lcms:(m+h)
+
:m/z:332.2
[0499]
步骤8:叔丁基(n-(5-((3-氰基-6,7-二甲氧基喹啉-4-基)硫代)戊基)氨磺酰基) 氨基甲酸11的合成:
[0500][0501]
向dcm(10ml)中的4-(5-氨基戊基)硫代-6,7-二甲氧基喹啉-3-碳腈10(200 mg,0.60mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶
ꢀ‑
4(1h)-亚乙基)-n-甲基甲酰胺氯化物4(338mg,0.6mmol),然后在相同温度下添加dipea(0.16ml,0.9mmol)。将反应混合物在室温下搅拌16小时。通过 tlc监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。通过在己烷中洗脱70-80%etoac,通过combi-flash色谱法纯化粗产物,得到的叔丁基 (n-(5-((3-氰基-6,7-二甲氧基喹啉-4-基)硫代)戊基)氨磺酰基)氨基甲酸酯11(90 mg)为白色固体。
[0502]
分析数据:1h nmr(400mhz,dmso)δ:10.73(s,1h),8.92(s,1h),7.71(s, 1h),7.55-7.50(m,2h),4.00-3.98(m,6h),3.18-3.14(m,2h),2.80-2.79(m,2h), 1.45-1.41(m,2h),1.37(m,13h)。
[0503]
lcms:(m+h)
+
:m/z:511.2
[0504]
步骤9:化合物014的合成:
[0505][0506]
在0摄氏度下,向二氯甲烷(2ml)中的叔丁基(n-(5-(3-氰基-6,7-二甲氧基喹啉-4-基)硫代)戊基)氨磺酰基)氨基甲酸酯11(90mg,0.176mmol)的搅拌溶液中添加4m hcl(1ml)到二氧六环(1ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc纯化,得到的化合物014(29mg)为灰白色蓬松固体。
[0507]
分析数据:1h nmr(400mhz,dmso)δ:8.93(s,1h),7.73(s,1h),7.51(s, 1h),6.41-6.39(m,3h),4.09-3.99(m,6h),3.19(t,2h),2.80-2.78(m,2h),1.51-1.49 (m,2h),1.48-1.40(m,4h)。
[0508]
lcms:(m+h)
+
:m/z:411.1。
[0509]
总体方案4:
[0510][0511]
实施例4:n-(5-((6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)磺酰胺
[0512]
步骤1:叔丁基(5-(1,3-二氧异吲哚-2-基)戊基)氨基甲酸酯
[0513]
[0514]
向甲苯(10ml)中的叔丁基(5-氨基戊基)氨基甲酸酯1(500mg,2.47mmol)的搅拌溶液中添加异苯并呋喃-1,3-二酮2(366mg,2.47mmol),然后回流搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。通过用石油醚中的20%乙酸乙酯洗脱,通过 combi-flash柱色谱法纯化粗品,得到的(5-(1,3-二氧代异吲哚啉-2-基)戊基)氨基甲酸叔丁基(500mg,1.506mmol,61%产率)为白色固体。
[0515]
分析数据:1h nmr(400mhz,dmso)δ7.86-7.80(m,4h),6.74(t,1h), 3.56-3.52(t,2h),2.88-2.83(m,2h),1.58-1.54(m,2h),1.38-1.32(m,11h), 1.23-1.20(m,2h)。
[0516]
lcms:(m+na)+:m/z:355.41
[0517]
步骤2:叔丁基(5-(1,3-二氧代异吲哚啉-2-基)戊基)(甲基)氨基甲酸酯
[0518][0519]
向n,n
’‑
二甲基甲酰胺(20ml)中的叔丁基(5-(1,3-二氧异吲哚-2-基)戊基)氨基甲酸酯3(2g,6024mmol)的搅拌溶液中,在0℃下缓慢添加60%nah(723mg, 30.12mmol),然后在相同温度下添加碘甲烷(8.5g,60.24mmol)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。将反应混合物倒入冰冷的水(500 ml)中并用乙酸乙酯(2x400ml)萃取。用盐水溶液(400ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。。通过在石油醚中洗脱20%乙酸乙酯通过combi-flash 色谱法纯化粗品,得到的叔丁基(5-(1,3-二氧代异吲哚啉-2-基)戊基)(甲基)氨基甲酸酯4的混合物(1.44g,4.161mmol,69%产率)为白色固体。
[0520]
分析数据:1h nmr(400mhz,dmso)δ7.86-7.80(m,4h),3.57-3.54(t,2h), 3.12-3.08(t,2h),2.71(s,3h),1.63-1.56(m,2h),1.48-1.43(m,2h),1.32(s,9h), 1.20-1.17(m,2h)。
[0521]
lcms:(m-boc)+:m/z:247.2
[0522]
步骤3:2-(5-(甲基氨基)戊基)异吲哚啉-1,3-二酮盐酸盐
[0523][0524]
在0℃下,向二氯甲烷(15ml)中的叔丁基4-(2-(n-(叔丁氧羰基)氨磺酰基)乙基)-3,4-二氢喹啉-1(2h)-羧酸盐4(1.8g,5.202mmol)的搅拌溶液中添加4m hcl 到二氧六环(6.75ml),然后在室温下搅拌2小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。通过与乙醚(100ml)一起研磨纯化粗化合物,得到的2-(5-(甲基氨基)戊基)异二氢吲哚-1,3-二酮盐酸盐5(1.3g,4.609 mmol,89%产率)为白色固体。
[0525]
分析数据:1h nmr(400mhz,dmso)δ8.32(brs,2h),7.87-7.82(m,4h), 3.58-3.55(t,2h),2.83(m,2h),1.63-1.53(m,4h),1.33-1.28(m,2h)。
[0526]
lcms:(m+h)+:m/z:247.2
[0527]
步骤4:2-(5-(6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)异吲哚啉-1,3-二酮
[0528][0529]
向2-(5-(甲氨基)戊基)异吲哚啉-1,3-二酮盐酸盐5(1.2g,4.25mmol)在乙腈 (15ml)中的搅拌溶液中添加碳酸钾(1.76g,13.5mmol)和4-氯-6,7-二甲氧基喹唑啉6(953mg,4.25mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,加入水(200ml)并用乙酸乙酯(2x150ml)萃取。用盐水溶液(100ml) 清洗合并的有机层,用硫酸钠干燥,减压浓缩。通过在己烷中洗脱40%乙酸乙酯,通过combi-flash柱色谱纯化粗品,得到的2-(5-((6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)异二氢吲哚-1,3-二酮7(650mg,1.497mmol,44%产率)为白色固体。
[0530]
分析数据:1h nmr(400mhz,dmso)δ8.35(s,1h),7.84-7.79(m,4h),7.21 (s,1h),7.11(s,1h),3.89(s,3h),3.82(s,3h),3.60-3.54(m,2h),3.21(s,3h), 1.78-1.75(m,2h),1.65-1.59(m,2h),1.34-1.28(m,2h)。
[0531]
lcms:(m+h)+:m/z:435.2
[0532]
步骤5:n1-(6,7-二甲氧基喹唑啉-4-基)-n1-甲基戊烷-1,5-二胺
[0533][0534]
向2-(5-(6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)异吲哚啉-1,3-二酮7(545 mg,1.126mmol)在乙醇(15ml)中的搅拌溶液中添加水合肼(0.18ml,3.378mmol),然后在80℃下搅拌反应混合物2小时。通过tlc监测反应进程。反应完成后,滤出沉淀的固体,用乙醇(20ml)洗涤残基并浓缩滤液,得到粗化合物。通过grace 反相法纯化粗化合物,通过在水中的0.1%甲酸中洗脱14%乙腈,得到的n1-(6,7
‑ꢀ
二甲氧基喹唑啉-4-基)-n1-甲基戊烷-1,5-二胺8(330mg,1.085mmol,86%产率) 为无色胶状液体。
[0535]
分析数据:1h nmr(400mhz,dmso)δ8.38(s,1h),7.25(s,1h),7.14(s, 1h),3.90(s,3h),3.90(s,3h),3.60-3.56(t,2h),3.22-3.21(s,3h),1.76-1.72(m, 2h),1.38-1.30(m,4h)。
[0536]
lcms:(m+h)+:m/z:305.2
[0537]
步骤6:叔丁基(n-(5-((6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)氨磺酰基) 氨基甲酸
[0538][0539]
在0℃下,向n1-(6,7-二甲氧基喹唑啉-4-基)-n1-甲基戊烷-1,5-二胺8(360mg, 1.2mmol)在二氯甲烷(10ml)中的搅拌溶液中添加二异丙基乙胺(0.3ml,1.81 mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物 9(491mg,1.45mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗品通过60-120 硅胶柱色谱纯化,通过在二氯甲烷中的2%甲醇洗脱,得到的叔丁基(n-(5-((6,7
‑ꢀ
二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)氨磺酰基)氨基甲酸酯10(200mg,0.414 mmol,35%产率)为棕色固体。
[0540]
分析数据:1h nmr(400mhz,dmso)δ11.0-10.0(brs,1h),8.38(s,1h), 7.25(s,1h),7.22(m,1h),7.14(s,1h),3.90(s,3h),3.87(s,3h),3.59-3.55(t,2h), 3.22-3.21(s,3h),1.75-1.71(m,2h),1.50-1.45(m,2h),1.38(s,9h),1.31-1.24(m, 1h)。lcms:(m+h)+:m/z:484.2
[0541]
步骤7:n-(5-((6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)磺酰胺(化合物 061)
[0542][0543]
在0℃下,向二氯甲烷(6ml)中的叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)(甲基)氨基)戊基)氨磺酰)氨基甲酸酯10(200mg,0.414mmol)的搅拌溶液中添加4mhcl到二氧六环(4ml),然后在室温下搅拌3小时。通过tlc监测反应进程。完成后,在减压下完全蒸馏掉有机溶剂,得到粗化合物。粗品通过制备型hplc 法纯化,得到的n-(5-((6,7-二甲氧基喹唑
啉-4-基)(甲基)氨基)戊基)磺酰胺(90mg, 0.235mmol,57%产率)(化合物061)为灰白色固体。
[0544]
分析数据:1h nmr(400mhz,dmso)δ8.39(s,1h),8.14(s,1h),7.26(s, 1h),7.14(s,1h),6.44(m,3h),3.90(s,3h),3.88(s,3h),3.60-3.56(t,2h), 2.88-2.83(m,2h),1.77-1.71(m,2h),1.52-1.46(m,2h),1.37-1.31(m,2h)。 lcms:(m+h)+:m/z:384.2
[0545]
总体方案5:
[0546][0547]
实施例5:4-(6,7-二甲氧基喹唑啉-4-基)-1,4二氮杂环庚烷
‑‑
1-磺酰胺盐酸盐 (化合物015)
[0548]
步骤1:叔丁基4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-羧酸
[0549][0550]
向4-氯-6,7-二甲氧基喹唑啉1(2g,8.904mmol)在乙腈(25ml)中的搅拌溶液中添加碳酸钾(2.4g,17.809mmol)和1,4-二氮杂环庚烷-1-羧酸叔丁酯2(1.96g, 9.795mmol),然后在80℃下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉。通过combi-flash色谱法纯化粗品,通过在二氯甲烷中洗脱5%甲醇,得到的叔丁基4-(6,7-二甲氧基喹唑啉-4-基)-1,4
‑ꢀ
二氮杂环庚烷-1-羧酸(2.7g,6.958mmol),78%产率)为淡黄色固体。
[0551]
分析数据:1h nmr(400mhz,dmso)δ8.38(s,1h),7.14(s,1h),7.25(s, 1h),3.97-3.94(t,2h),3.89-3.84(m,8h),3.59(d,2h),3.41(s,2h),1.98(s,2h), 1.15(d,9h)。
[0552]
步骤2:4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉盐酸盐
[0553][0554]
在0℃下,在二氧六环(2ml)中的叔丁基4-(6,7-二甲氧基喹唑啉-4-基)-1,4
‑ꢀ
二氮杂环庚烷-1-羧酸盐3(200mg,0.742mmol)的搅拌溶液中将4m hcl添加到二氧六环(8ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过与乙醚(20ml)一起研磨纯化,得到的4-(1,4-二氮杂环庚烷-1-yl)-6,7-二甲氧基喹唑啉盐酸盐4(115mg,0.355 mmol,68%产率)为黄色固体。
[0555]
分析数据:1h nmr(400mhz,dmso)δ9.33(s,2h),8.79(s,1h),7.43(s, 1h),7.35(s,1h),4.19(s,2h),4.29(s,2h),3.97-3.93(m,6h),3.17(d,2h), 2.77-2.31(m,2h)。
[0556]
步骤3:叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯
[0557][0558]
在0℃下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉盐酸盐4(500 mg,1.508mmol)在二氯甲烷(10ml)中的搅拌溶液中添加二异丙基乙胺(0.5ml, 2.262mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺 5(508mg,1.508mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过 100-200硅胶柱色谱通过在二氯甲烷中的5%甲醇洗脱来纯化,得到半纯化合物。将该半纯品通过与石油醚中的50%乙酸乙酯一起研磨再次纯化,得到的叔丁基 ((4-(6,7-二甲氧基喹唑啉-4-基)-1,4二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯6(350 mg,0.686mmol,44%产率),为灰白色固体。
[0559]
分析数据:1h nmr(400mhz,dmso)δ11.07(brs,1h),8.18(s,1h),7.21(s, 1h),3.88-3.95(m,10h),3.65-3.68(t,2h),3.42-3.45(t,2h),2.06(d,2h),1.33-1.36 (s,9h)。lcms:(m+h+):m/z:468.15
[0560]
步骤4:4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐(化合物015-hcl)
[0561][0562]
在0℃下,向二氧六环(2ml)中的叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-1,4
‑ꢀ
二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯6(300mg,0.646mmol)的搅拌溶液中添加4m hcl到二氧六环(8ml)中,然后在室温下搅拌6小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。通过用5%甲醇的二氯甲烷 (50ml)研磨纯化粗产物,得到的4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷
ꢀ‑
1-磺酰胺盐酸盐(120mg,0.327mmol,51%产率)为灰白色固体。
[0563]
分析数据:1h nmr(400mhz,dmso)δ8.75(s,1h),7.43(s,1h),7.34(s, 1h),6.84(s,1h),4.18-4.22(m,4h),3.94(s,3h),3.96(s,3h),3.59(m,2h), 3.28-3.31(t,2h),2.08(brs,2h)。
[0564]
lcms:(m+h+):m/z:368.1
[0565]
化合物015-mes的合成方案
[0566]
4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺甲烷磺酸盐 (015-mes)
[0567][0568]
向4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(100mg,0.272 mmol)(通过与三乙胺搅拌两小时从hcl盐制备化合物015游离碱)在乙腈(2ml) 中的搅拌溶液中添加水甲烷磺酸(26mg,0.272mmol),然后将反应混合物在冻干下保持16小时,得到的4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷环庚烷环庚烷-1-磺酰胺甲烷磺酸盐(化合物015-mes)(115mg,0.248mmol,91%产率) 为灰白色固体。
[0569]
分析数据:1h nmr(400mhz,dmso)δ14.150(bs,1h),8.699(s,1h),7.401 (s,1h),7.183(s,1h),6.819(s,1h),4.141-4.166(m,4h),3.961(s,3h),3.930(s, 3h),3.559-3.591(m,2h),3.320(m,2h),2.279(s,3h),2.061-2.103(m,2h)。
[0570]
lcms:(m+h
+
):m/z:368.16.。
[0571]
化合物016的合成方案
[0572][0573]
叔丁基4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-羧酸(3)的合成
[0574][0575]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(750mg,3.0mmol)在乙腈(15ml)中的搅拌溶液中添加碳酸钾(834mg,6.0mmol)和1,4-二氮杂环庚烷-1-羧酸叔丁酯2(904 mg,4.5mmol),然后在80℃下搅拌16小时。通过tlc监测反应进程。反应完成后,向反应混合物中加入水(100ml)并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗化合物通过组合快速色谱法纯化,得到的纯化合物叔丁基4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-羧酸(450mg,1.09mmol,38%产率)为浅黄色固体。
[0576]
分析数据:1h nmr(400mhz,dmso)δ8.67(s,1h),7.39(s,1h),7.31(s,1h), 3.94(s,6h),3.59-3.62(m,6h),3.46-3.3.53(m,2h),2.05(s,2h),1.43(s,9h)。
[0577]
lcms:(m+h)
+
:m/z:413.2
[0578]
4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲腈盐酸盐(4)的合成
[0579][0580]
在0℃下,向二氧六环(2ml)中的叔丁基4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-羧酸盐3(450mg,1.09mmol)的搅拌溶液中添加4m hcl 到二氧六环(3ml)中,然后在室温下搅拌4小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。将粗残基用乙醚洗涤,得到的4-(1,4
‑ꢀ
二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲腈盐酸盐4(400mg,1.28mmol,92%产率)为黄色固体.
[0581]
lcms:(m+h)
+
:m/z:313.31
[0582]
叔丁基((4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基) 氨基甲酸酯(6)的合成-7-羧酸甲酯(2)的合成
[0595][0596]
向4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉
ꢀ‑
7-基三氟甲基磺酸盐1(200mg,0.342mmol)在n,n
’‑
二甲基甲酰胺(2ml)和甲醇 (10ml)中的搅拌溶液中添加三乙胺(103.6mg,1.026mmol),然后将反应混合物脱气30分钟。然后再次加入乙酸钯(ii)(3.8mg,0.017mmol)和xantphos(10mg, 0.017mmol),脱气5分钟,并在80℃的co气球压力下搅拌反应混合物6小时。通过tlc监测反应进程。反应完成后,将反应混合物减压蒸馏完全,向粗品中加入乙酸乙酯(50ml)并通过硅藻土过滤。用过量乙酸乙酯(50ml)洗涤硅藻土床。然后加入水(100ml)并萃取。有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥并减压浓缩。粗品经制备型hplc方法纯化,得到的4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-甲酸甲酯(2)(70g,0.141mol,41%) 为棕色固体。
[0597]
分析数据:1h nmr(400mhz,dmso)δ8.493(s,1h),7.952(s,1h),7.392(s, 1h),4.008-4.024(m,4h),3.938(s,3h),3.865(s,3h),3.691-3.718(t,2h), 3.446-3.476(t,2h),2.099(m,2h),1.363(s,9h)。
[0598]
甲基6-甲氧基-4-(4-氨磺酰-1,4二氮杂环庚烷-1-基)喹唑啉-7-羧酸盐酸盐 (int-4)的合成
[0599][0600]
在室温下将4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-羧酸盐2(70mg,0.545mmol)和4m hcl在二氧六环(4ml)中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过用5%甲醇的二氯甲烷(5ml)研磨纯化,得到的甲基6-甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷-1-基)喹唑啉-7-羧酸盐酸盐int-4(55mg,0.127 mmol,90%产率)为灰白色固体。
[0601]
分析数据:1h nmr(400mhz,dmso)δ8.486(s,1h),7.948(s,1h),7.406(s, 1h),3.990-4.040(m,4h),3.937(s,3h),3.865(s,3h),3.523-3.548(t,2h), 3.274-3.293(t,2h),2.103(m,2h)。
[0602]
lcms:(m+h
+
):m/z:396.1
[0603]
6-甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基)喹唑啉-7-羧酸(化合物017) 的合成
[0604][0605]
向甲基6-甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷-1-基)喹唑啉-7-羧酸盐酸盐 (int-4)(55mg,0.139mmol)在四氢呋喃(3ml)和水(1ml)中的搅拌溶液中添加0℃下的一水氢氧化锂(29mg,0.696mmol),然后在室温下搅拌16小时。反应完成后减压蒸馏除去有机溶剂。向粗残基中加入水(20ml)并用30%的柠檬酸溶液(10 ml)酸化。然后用二氯甲烷(50ml)中的10%甲醇萃取,减压浓缩,得到粗化合物。粗化合物通过制备型hplc方法纯化,得到的纯化合物6-甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷-1-基)喹唑啉-7-羧酸化合物017(10mg,0.03mmol,11%产率)为灰白色固体。
[0606]
分析数据:1h nmr(400mhz,dmso)δ13.237(bs,1h),8.470(s,1h),7.848 (bs,1h),7.363(s,1h),6.787(s,1h),3.980-4.033(m,4h),3.923(s,3h), 3.522-3.547(t,2h),3.280(t,2h),2.072-2.102(m,2h)。
[0607]
lcms:(m+h
+
):m/z:382
[0608]
化合物018的合成方案
[0609]
mg,0.668mmol)在乙腈(5ml)中的搅拌溶液中添加碳酸钾(276mg,2.0mmol) 和2-溴乙酰胺5(184mg,1.33mmol),然后在80℃下搅拌16小时。通过tlc 监测反应进程。反应完成后,向反应混合物中加入水(100ml)并用乙酸乙酯 (2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗化合物通过组合快速色谱法纯化,得到的纯化合物叔丁基4-(7-(2-氨基
ꢀ‑
2-氧代乙氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-羧酸6(200mg,0.462 mmol,71%产率)为浅棕色糖浆。
[0621]
lcms:(m+h
+
):m/z:432.3
[0622]
2-(4-(1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-基)氧基)乙酰胺盐酸盐(7) 的合成
[0623][0624]
在0℃下,向二氧六环(1ml)中的4-(7-(2-氨基-2-氧乙氧基)-6-甲氧基喹唑啉
ꢀ‑
4-基)-1,4-二氮杂环庚烷-1-羧酸叔丁酯6(200mg,0.462mmol)的搅拌溶液中添加4m hcl,然后在室温下搅拌2小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗残基用乙醚洗涤,得到的2-((4-(1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-基)氧基)乙酰胺盐酸盐7(150mg,0.451mmol,88%产率)为黄色固体。
[0625]
分析数据:1h nmr(400mhz,dmso)δ9.23(br s,1h),8.77(s,1h), 7.46-7.47(m,1h),7.01-7.26(m,2h),4.74(s,3h),4.19-4.26(m,4h),3.94(s,3h), 3.71(d,2h),3.45(m,2h),3.18-3.3.19(m,2h),2.24(m,2h).
[0626]
叔丁基((4-(7-(2-氨基-2-氧乙氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷
ꢀ‑
1-基)磺酰基)氨基甲酸酯(8)的合成
[0627][0628]
在室温下,向二氯甲烷(3ml)中的2-(4-(1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-基)氧基)乙酰胺盐酸盐(7)(150mg,0.451mmol)的搅拌溶液中加入二异丙基乙胺(0.24ml,1.36mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)-亚基)-n-甲基甲胺5(168mg,0.49mmol),并在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在石油醚中洗脱60%乙酸乙酯来纯化粗化合
物,通过组合快速柱色谱法得到的叔丁基((4-(7-(2-氨基-2-氧乙氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷
ꢀ‑
1-基)磺酰基)氨基甲酸酯(9)(150mg,0.294mmol,65%产率)为黄色固体。
[0629]
lcms:(m+h)
+
:m/z:511.2
[0630]
化合物018的合成
[0631][0632]
在室温下,向1,4-二氧六环(1.0ml)中的叔丁基((4-(7-(2-氨基-2-氧乙氧基)-6
‑ꢀ
甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(9)(150mg, 0.294mmol)的搅拌溶液中添加4m hcl到二氧六环(2.0ml)中。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的化合物018的纯化合物(15mg,0.036mmol,12%产率)为灰白色固体。
[0633]
分析数据:1h nmr(400mhz,dmso)δ8.39(s,1h),7.42-7.47(dd,2h),7.26 (s,1h),7.03(s,1h),6.77(s,1h),4.63(s,2h),3.91-3.97(m,7h),3.48-3.51(m,2h), 3.24-3.27(m,3h),2.05-2.08(m,2h)。
[0634]
lcms:(m+h)
+
:m/z:411.1
[0635]
化合物019、020、021和022的合成方案
[0636][0637]
7-(苄氧基)-4-(1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉盐酸盐(2)的合成
[0638][0639]
在室温下,将4-(7-(苄基氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1
‑ꢀ
羧酸酯1(1g,2.155mmol)和4m hcl在二氧六环(10ml)中的搅拌溶液搅拌1小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过与戊烷(50ml)一起研磨纯化,得到的7-(苄氧基)-4-(1,4-二氮杂环庚烷-1
‑ꢀ
基)-6-甲氧基喹唑啉盐酸盐2(600mg,1.5mmol,70%产率)为灰白色固体。
[0640]
分析数据:
[0641]
lcms:(m+h
+
):m/z:365.2
[0642]
叔丁基((4-(7-(苄氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基) 氨基甲酸叔(6)的合成
[0643][0644]
在0℃下,向7-(苄氧基)-4-(1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉盐酸盐 2(1g,2.497mmol)在二氯甲烷(20ml)中的搅拌溶液中添加二异丙基乙胺(805mg, 6.242mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺 3(841mg,2.497mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过 100-200硅胶柱色谱通过在二氯甲烷中的5%甲醇洗脱来纯化,得到半纯化合物。将该半纯品通过与石油醚中的50%乙酸乙酯一起研磨再次纯化,得到的叔丁基 ((4-(7-(苄氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基))磺酰基)氨基甲酸酯4(1.2g,2.21mmol,89%产率)为灰白色固体。
[0645]
分析数据:lcms:(m+h
+
):m/z:544.15
[0646]
叔丁基((4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(5)的合成
[0647][0648]
向叔丁基((4-(7-(苄基氧基)-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯4(1.2g,2.21mmol)在乙醇(30ml)中的搅拌溶液中添加10%钯/碳(200mg),并在室温下在气球氢气氛下搅拌反应混合物16小时。通过tlc监测反应进程。完成后,反应混合物通过硅藻土过滤并用含5%甲醇的二氯甲烷(100 ml)洗涤硅藻土床。减压浓缩滤液,得到的半纯化合物((4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸叔丁基(5)(1.1g,粗品)为灰白色固体。
[0649]
分析数据:1h nmr(400mhz,dmso)δ10.341(bs,1h),8.345(s,1h),7.205 (s,1h),7.027(s,1h),4.330-4.356(t,2h),3.890-3.924(m,5h),3.661(t,2h), 2.054-2.061(m,1h),1.247-1.366(m,9h)。
[0650]
4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7
‑ꢀ
基三氟甲基磺酸盐(7)的合成
[0651][0652]
在0℃下,向二氯甲烷(15mg)中的叔丁基((4-(7-羟基-6-甲氧基喹唑啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯5(1.1g,2428mmol)搅拌溶液中加入三乙胺(0.85ml,6.07mmol)和1,1,1-三氟-n-苯基-n-(三氟甲基)磺酰基)甲烷磺酰胺6(1.3g,3.642mmol),然后在室温下搅拌4小时。通过tlc监测反应进程。反应完成后,在减压下完全蒸馏掉有机溶剂,将水(200ml)加入粗品中并用二氯甲烷(2
×
200ml)分配。用盐水溶液(200ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。通过combi-flash色谱法纯化粗品,通过在石油醚中洗脱70%乙酸乙酯,得到的4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-基三氟甲基磺酸盐7(750mg,1.282mmol,58%两步产率)为灰白色固体。
[0653]
分析数据:1h nmr(400mhz,dmso)δ11.021(s,1h),8.514(s,1h),7.847(s, 1h),7.566(s,1h),3.990-4.031(m,8h),3.707(s,2h),3.443(s,2h),2.080(bs,2h), 1.342(s,9h)。
[0654]
4-(6-甲氧基-7-(1h-吡咯-3-基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物019)的合成
[0655][0656]
在密封管中,向4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6
‑ꢀ
甲氧基喹唑啉-7-基三氟甲基磺酸盐7(200mg,0.342mmol)在二氧六环(7ml)水 (2ml)中的搅拌溶液中添加(1-(三异丙基丙基硅基)-1h-吡咯-3-基)硼酸(119mg, 0.446mmol)和氟化铯(104mg,0.684mmol),然后将反应混合物脱气30分钟。然后再次脱气5分钟加入四(三苯基膦)钯(0)(20mg,0.0017mmol)并在65℃搅拌反应混合物3小时。通过tlc监测反应进程。反应
完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。粗品通过制备型hplc方法纯化得到的4-(6-甲氧基-7-(1h-吡咯-3-基)喹唑啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物019)(30mg,0.074mmol,22%)为棕色固体。
[0657]
分析数据:1h nmr(400mhz,dmso)δ10.984(s,1h),8.332(s,1h),8.180(s, 1h),7.832(s,1h),7.493(s,1h),7.288(s,1h),6.833(s,1h),6.650(s,1h),3.838 (m,8h),3.499(t,2h),3.251-3.277(t,2h),2.068(m,2h)。
[0658]
lcms:(m+h
+
):m/z:403.1
[0659]
化合物023、024和025的合成方案:
[0660][0661]
步骤1:4-(4-(叔丁氧基羰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3
‑ꢀ
羧酸乙酯3的合成:
[0662][0663]
向4-氯-6,7-二甲氧基喹啉-3-羧酸乙酯1(4.2g,4.2mmol)在dmf(40ml)中的搅拌溶液中添加1,4-二氮杂环庚烷-1-羧酸叔丁酯(4.2ml,4.2mmol)和k2co3(3.9g,28mmol),然后加热至80℃回流16小时。通过tlc监测反应进程。反应完成后,将反应混合物直接倒入冰
冷的水中并搅拌。将沉淀出的固体过滤并再次用水洗涤并干燥,无需任何进一步纯化,得到的乙基4-(4-(叔丁氧基羰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-羧酸盐3(5.5g)为淡黄色固体。
[0664]
分析数据:1h nmr(400mhz,dmso):8.68(s,1h),7.43(s,1h),7.37(s, 1h),4.34(q,2h),3.93(s,6h),3.59-3.54(m,4h),3.26-3.19(m,4h),1.97-1.92(m, 2h),1.43-1.32(m,11h)。
[0665]
lcms:(m+h)
+
:m/z:247.1
[0666]
步骤2:4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲酸乙酯盐酸盐4 的合成:
[0667][0668]
在0℃下,向1,4-二氧六环(50ml)中的4-(4-(叔丁氧羰基)-1,4-二氮杂环庚烷
ꢀ‑
1-基)-6,7-二甲氧基喹啉-3-羧酸盐3(5.5g,1,8mmol)搅拌溶液中缓慢添加4.0m 小时cl到1,4-二氧六环(50ml),并缓慢地使其到室温并搅拌2小时。反应完成后,减压除去挥发性有机物,与dcm共蒸馏三次并与乙醚一起研磨,得到的乙基4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-羧酸盐酸盐4(4.2g)为灰白色固体。通过tlc监测反应进程。
[0669]
分析数据:lcms:(m+h)
+
:m/z:360
[0670]
步骤3:4-(4-(n-(叔丁氧基羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-羧酸乙酯6:
[0671][0672]
向dcm(30ml)中的4-(4-氨基丁基)硫代-6,7-二甲氧基喹啉-3-碳腈4(2g, 5.56mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)
‑ꢀ
亚基)-n-甲基甲酰胺氯化物5(2.06g,6.1mmol),然后在相同温度下添加 dipea(2.68ml,0.375mmol)。将反应混合物在室温下搅拌16小时。通过tlc 监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。粗品通过 combi-flash色谱法纯化,通过在己烷中洗脱90%etoac,得到的乙基4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-羧酸盐6(1.1g) 为白色固体。
[0673]
分析数据:1h nmr(400mhz,dmso):8.72(s,1h),7.49(s,1h),7.37(s, 1h),4.36(q,2h),3.93(s,6h),3.59-3.52(m,4h),3.22-3.09(m,4h),1.97-1.96(m, 2h),1.47(s,
9h),1.36(t,3h)。
[0674]
lcms:(m+h)
+
:m/z:539.2
[0675]
步骤4:6,7-二甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基)喹啉-3-羧酸乙酯7(化合物023)的合成
[0676][0677]
在0℃下,向4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6,7
‑ꢀ
二甲氧基喹啉-3-羧酸乙酯7(300mg,0.56mmol)在二氯甲烷(3ml)中的搅拌溶液中添加tfa(3ml),然后在相同温度下搅拌4小时。通过tlc监测反应进程。反应完成后,用aq.nahco3中和tfa,用10%meoh/dcm萃取,干燥并浓缩。将获得的固体研磨,得到的6,7-二甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基) 喹啉-3-羧酸乙酯7化合物023(250mg)为淡黄色固体。
[0678]
分析数据:1h nmr(400mhz,dmso)δ:8.72(s,1h),7.54(s,1h),7.37(s, 1h),6.79(s,2h),4.36(q,2h),3.93(s,6h),3.44-3.43(m,4h),3.42-3.33(m,4h), 1.97-1.96(m,2h),1.36(t,3h)。
[0679]
lcms:(m+h)
+
:m/z:439.2
[0680]
步骤5:6,7-二甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基)喹啉-3-羧酸化合物024的合成:
[0681][0682]
在室温下,向thf:h2o(3:1)中的乙基6,7-二甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷-1-基)喹啉-3-羧酸酯7(250mg,0,57mmol)搅拌溶液中添加lioh(119mg, 2.85mmol)。添加后,使反应混合物在室温下搅拌16h。通过tlc监测反应进程。反应完成后,蒸发挥发性有机物并用乙醚研制,得到169mg的6,7-二甲氧基-4-(4
‑ꢀ
氨磺酰基-1,4-二氮杂环庚烷-1-基)喹啉-3-羧酸7。将69mg的7提交用于制备型 hplc。经hplc纯化后,获得的6,7-二甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷
ꢀ‑
1-基)喹啉-3-羧酸化合物024(26mg)为浅黄色固体。
[0683]
分析数据:1h nmr(400mhz,dmso)δ:13.36(brs,1h),8.74(s,1h),7.53(s, 1h),7.35(s,1h),6.79(s.1h),3.93(s,6h),3.45-3.38(m,8h),1.95(brs,2h)。
[0684]
lcms:(m+h)
+
:m/z:411.2
[0685]
步骤6:6,7-二甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基)喹啉-3-甲酰胺化合物025的合成:
[0686][0687]
在0℃下,向6,7-二甲氧基-4-(4-氨磺酰-1,4-二氮杂环庚烷-1-基)喹啉-3-羧酸 7(100mg,0.24mmol)在thf(3ml)中的搅拌溶液中添加socl2(0.026ml,0.36 mmol)。1小时后,反应混合物在相同温度下用nh3(气体)吹扫10分钟,并在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,反应混合物中的沉淀用10%meoh/dcm洗涤,滤液干燥并浓缩,得到约85mg粗品。hplc纯化后,得到的6,7-二甲氧基-4-(4-氨磺酰基-1,4-二氮杂环庚烷-1-基)喹啉-3-甲酰胺化合物025(9mg)为淡黄色固体。
[0688]
分析数据:1h nmr(400mhz,dmso)δ:8.50(s,1h),7.99(brs,1h),7.57(brs, 1h),7.46(s,1h),7.33(s,1h),6.77(s,2h),3.93-3.91(m,6h),3.45-3.42(m,4h), 3.37-3.35(m,4h),1.95(brs,2h)。
[0689]
4-(6-甲氧基-7-(1h-吡唑-4-基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物020)的合成
[0690][0691]
在密封管中,加入4-(4-(n-(叔丁氧羰基)氨磺酰基)-1的搅拌溶液,将4-二氮杂环庚烷-1-基)-6-甲氧基喹唑啉-7-基三氟甲基磺酸盐7(100mg,0.171mmol)加入二氧六环(5ml)和水(1.5ml)中的叔丁基4-(4,4,5,5-四甲基-1,3,2-二氧苯甲醛-2-基)-1h-吡唑-1-羧酸盐-1-羧酸盐9(65mg,0.222mmol)和氟化铯(78mg,0.513 mmol)然后将反应混合物脱气30分钟。然后再次脱气5分钟加入四(三苯基膦) 钯(0)(20mg,0.0017mmol)并在90℃搅拌反应混合物6小时。通过tlc监测反应进程。反应完成后,反应混合物通过硅藻土过滤。用乙酸乙酯(100ml)洗涤硅藻土床。然后加入水(100ml)并用过量乙酸乙酯(100ml)萃取。有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥并减压浓缩。粗品经制备型hplc方法纯化,得到的4-(6-甲氧基-7-(1h-吡唑-4-基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物020)
(10mg,0.024mmol,15%)为棕色固体。
[0692]
分析数据:1h nmr(400mhz,dmso)δ13.134(s,1h),8.457(s,1h),8.273(s, 1h),8.233(s,1h),7.751(bs,1h),7.405(s,1h),6.916(s,1h),6.799(s,1h), 3.996-4.042(m,8h),3.534-3.555(t,2h),2.097-2.141(t,2h),2.068(m,2h)。
[0693]
lcms:(m+h
+
):m/z:404.2.
[0694]
4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐(化合物 021)的合成
[0695][0696]
在室温下,将叔丁基((4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1
‑ꢀ
基)磺酰基)氨基甲酸酯5(100mg,0.221mmol)和4m hcl在二氧六环(3ml)中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过制备型hplc法纯化,得到的4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐(化合物021)(600mg,1.5mmol,70%产率)为灰白色固体。
[0697]
分析数据:1h nmr(400mhz,dmso)δ14.348(bs,1h),11.608(s,1h),8.693 (s,1h),7.415(s,1h),7.245(s,1h),6.842(s,2h),4.176-4.200(m,4h),3.933(s, 3h),3.555-3.580(m,2h),3.275-3.301(t,2h),2.078(m,2h)。
[0698]
lcms:(m+h
+
):m/z:354.1。
[0699]
4-(6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物022)的合成
[0700][0701]
在密封管中,向4-(4-(n-(叔丁氧羰基)氨磺酰基)-1,4-二氮杂环庚烷-1-基)-6
‑ꢀ
甲氧基喹唑啉-7-基三氟甲基磺酸7(100mg,0.171mmol)在n,n
’‑
二甲基甲酰胺(2 ml)中的搅拌溶液中添加甲酸9(0.064ml,1.196mmol),然后将三乙胺(34mg, 0.342mmol)从反应混合物脱气30分钟。然后再次加入乙酸钯(ii)(2mg,0.0085 mmol)和xantphos(5mg,0.0085mmol),脱气5分钟并在100℃搅拌反应混合物 16小时。通过tlc监测反应进程。反应完成后,反应混合物通过硅藻土过滤。用乙酸乙酯(100ml)洗涤硅藻土床。然后加入水(100ml)并用过量乙酸乙酯(100 ml)萃取。有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥
并减压浓缩。粗品经制备型hplc法纯化,得到的4-(6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物022)(10mg,0.024mmol,15%)为棕色固体。
[0702]
分析数据:1h nmr(400mhz,dmso)δ8.444(s,1h),7.704-7.727(d,1h), 7.447-7.477(dd,1h),7.310-7.316(d,1h),6.789(s,2h),3.953-4.013(m,4h),3.891 (s,3h),3.521-3.534(t,2h),3.268-3.296(t,2h),2.088-2.096(m,2h)。
[0703]
lcms:(m+h
+
):m/z:338
[0704]
化合物026和027的合成方案
[0705][0706]
4-(3,6-二氮杂二环[3.2.1]辛烷-3-基)-6,7-二甲氧基喹唑啉与4-(3,6-二氮杂二环[3.2.1]辛烷-6-基)-6,7-二甲氧基喹唑啉(3和3a)的化合物的合成
[0707][0708]
将碳酸铯(5.6g,17.119mmol)和3,6-二氮杂二环[3.2.1]辛烷2(900mg,4.891 mmol)添加到t-buoh(120ml)中的4-氯-6,7-二甲氧基喹唑啉1(1g,4.891mmol) 的搅拌溶液中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下完全蒸馏出反应混合物。粗品通过用乙醚研制纯化,得到的4-(3,6
‑ꢀ
二氮杂二环[3.2.1]辛烷-3-基)-6,7-二甲氧基喹唑啉与与4-(3,6-二氮杂二环[3.2.1] 辛烷-6-基)-6,7-二甲氧基喹唑啉(3和3a)的化合物(1.1g粗品)为白色固体。
[0709]
lcms:(m+h
+
):m/z:301.2
[0710]
叔丁基((3-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]辛烷-6-基)磺酰基)氨基甲酸酯(5)和叔丁基((6-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1] 辛烷-3-基)磺酰基)氨基甲酸酯(5a)的合成
[0711][0712]
在0℃下,向4-(3,6-二氮杂二环[3.2.1]辛烷-3-基)-6,7-二甲氧基喹唑啉化合物与4-(3,6-二氮杂二环[3.2.1]辛烷-6-基)-6,7-二甲氧基喹唑啉(3和3a)(1.1g, 3.666mmol)在二氯甲烷(20ml)中的搅拌溶液中添加二异丙基乙胺(0.95ml, 5.499mmol)和n-(1-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基。e)-n-甲基甲酰胺 4(1.23g,3.66mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过100-200 硅胶柱色谱纯化,通过在二氯甲烷中的3%甲醇洗脱,得到的异构体叔丁基 ((3-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]辛烷-6-基)磺酰基)氨基甲酸酯(5)(500mg,1.041mmol,28%产率)和叔丁基((6-(6,7-二甲氧基喹唑啉-4-基)-3,6
‑ꢀ
二氮杂二环[3.2.1]辛烷-3-基)磺酰基)氨基甲酸酯(5a)(150mg,0.312mmol,8%产率)纯化合物为灰白色固体。
[0713]
分析数据
[0714]
cpd-5:1h nmr(400mhz,dmso)δ8.324(s,1h),8.144(s,1h),6.732-7.616 (m,3h),4.853-4.920(dt,1h),4.287-4.351(m,1h),4.127-4.155(d,1h),3.961-3.989 (d,1h),3.896(s,7h),3.588-3.616(d,1h),3.413-3.439(d,1h),3.174-3.199(d,1h), 2.886-3.012(dd,1h),2.713-2.771(m,2h),2.004(m,2h),1.650-1.785(dd,1h), 1.117-1.287(d,8h)。
[0715]
lcms:(m+h
+
):m/z:480.2
[0716]
cpd-5b:1h nmr(400mhz,dmso)δ10.965-10.971(brs,1h),8.700-8.718(d, 1h),7.680-7.725(d,1h),7.211(s,1h),6.793(s,1h),5.027-5.102(d,1h), 4.515-4.526(m,1h),4.026-4.120(d,1h),3.944-3.959(d,6h),3.439-3.575(d,1h), 3.102-3.251(m,3h),2.844-2.942(m,2h),2.045-2.072(m,1h),1.757-1.912(s,1h), 1.232(s,5h)。
[0717]
lcms:(m+h
+
):m/z:480.2
[0718]
3-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]辛烷-6-磺酰胺盐酸盐(化合物026)的合成
[0719][0720]
在室温下,将叔丁基((3-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]
辛烷-6-基)磺酰基)氨基甲酸酯5(100mg,0.208mmol)和4m hcl在二氧六环(4ml) 中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过在二氯甲烷(50ml)中与5%甲醇一起研磨纯化,得到的3-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂双环[3.2.1]辛烷-6-磺酰胺盐酸盐化合物026(70mg,0.168mmol,81%产率)为灰白色固体。
[0721]
分析数据:1h nmr(400mhz,dmso)δ14.287(bs,1h),8.743(s,1h),7.740 (s,1h),7.26(s,1h),6.812(s,2h),5.118(s,1h),4.483-4.536(bs,1h),4.148(s,1h), 3.966(s,3h),3.971(s,3h),3.826-3.847(d,1h),3.441-3.470(d,1h),2.919-2.947(d, 1h),2.856(brs,2h),2.050-2.077(m,1h),1.768-1.797(d,1h)。
[0722]
lcms:(m+h
+
):m/z:380.2
[0723]
6-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]辛烷-3-磺酰胺盐酸盐(化合物027)的合成
[0724][0725]
在室温下,将叔丁基((6-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂二环[3.2.1]辛烷-3-基)磺酰基)氨基甲酸酯5a(100mg,0.208mmol)和4m hcl在二氧六环(4ml) 中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过在二氯甲烷(50ml)中与5%甲醇一起研磨纯化,得到的6-(6,7-二甲氧基喹唑啉-4-基)-3,6-二氮杂双环[3.2.1]辛烷-3-磺酰胺盐酸盐化合物027(70mg,0.168mmol,81%产率)为灰白色固体。
[0726]
分析数据:1h nmr(400mhz,dmso)δ14.229(bs,1h),8.724(s,1h),7.733 (s,1h),7.243(s,1h),6.802(s,2h),5.111(s,1h),4.498(bs,1h),4.113-4.116(d, 1h),3.971(s,6h),3.832-3.854(d,1h),3.444-3.469(d,1h),2.919-2.946(d,1h), 2.825-2.853(brs,2h),2.046-2.074(m,1h),1.764-1.793(d,1h)。
[0727]
lcms:(m+h
+
):m/z:380.1
[0728]
化合物028的合成方案
[0729]
4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物028)的合成
[0730][0731]
将2-氯-2,2-二氟乙酸、钠盐(335mg,2.207mmol)、碳酸铯(719mg,2.205 mmol)和碳酸铯(719mg,2.205mmol)添加到n,n
’‑
二甲基甲酰胺(5ml)和水(5 ml)中的叔丁基(4-(7-羟基-6-甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰基)氨基甲酸酯1(200mg,0.441mmol)的搅拌溶液中,然后在100℃下将反应混合物搅拌16小时。通过tlc监测反应进程。反应完成后,向反应混合物中加入水(100 ml),并用乙酸乙酯(2
×
50ml)萃取。将合并的有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥并在减压下浓缩以得到粗产物。粗品经制备型hplc方法纯化,得到的4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物028)(10 mg,0.027mmol,5%)为灰白色固体.
[0732]
分析数据:1h nmr(400mhz,dmso)δ8.460(s,1h),7.425-7.470(m,3h), 6.796(s,2h),3.979-4.001(m,4h),3.959(s,3h),3.509-3.535(t,2h),3.261-3.289(t, 2h),2.084(m,2h)。
[0733]
lcms:(m+h
+
):m/z:404.1
[0734]
化合物029的合成方案
[0735]
[0736]
4-(6,6-二氟-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉(3)的合成
[0737][0738]
向4-氯-6、7-二甲氧基喹唑啉1(160mg,0.695mmol)在叔丁醇(25ml)中的搅拌溶液中添加碳酸钾(288mg,2.085mmol)和6,6-二氟-1,4-二氮杂环庚烷2(218 mg,1.043mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉。向粗品中加入在二氯甲烷中的10%甲醇并过滤。减压浓缩滤液,得到的4-(6,6-二氟-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉(3)(180mg,粗品)为灰白色固体。
[0739]
lcms:(m+h
+
):m/z:325.2
[0740]
叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-6,6-二氟-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(5)的合成
[0741][0742]
在0℃下,将二异丙基乙胺(90mg,0.694mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺4(171mg,0.509mmol)添加到二氯甲烷(5 ml)中的4-(6,6-二氟-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉(3)(150mg, 0.463mmol)的搅拌溶液中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过100-200combi-flash色谱纯化,在二氯甲烷中的3%甲醇洗脱,得到的叔丁基 ((4-(6,7-二甲氧基喹唑啉-4-基)-6,6-二氟-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(5)(200mg,0.397mmol,86%产率)为灰白色固体。
[0743]
lcms:(m+h
+
):m/z:504.2
[0744]
4-(6,7-二甲氧基喹唑啉-4-基)-6,6-二氟-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐 (化合物029)的合成
[0745][0746]
在室温下,将叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-6,6-二氟-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯5(170mg,0338mmol)和4m hcl在二氧六环(10ml) 中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过用5%甲醇的二氯甲烷(5ml)研磨纯化,得到的 4-(6,7-二甲氧基喹唑啉-4-基)-6,6-二氟-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐化合物029(20mg,0.045mmol,13%产率)为灰白色固体。
[0747]
分析数据:1h nmr(400mhz,dmso)δ8.558(s,1h),7.251(s,1h),7.181(s, 1h),7.098(s,2h),4.388-4.456(t,2h),3.935(s,6h),3.878-3.903(t,3h), 3.789-3.822(d,2h),3.720-3.755(m,2h)。
[0748]
lcms:(m+h
+
):m/z:404.22
[0749]
化合物030的合成方案
[0750][0751]
4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉(3)的合成
[0752][0753]
向4-氯-6,7-二甲氧基喹啉1(2g,8.9686mmol)在乙醇(20ml)中的搅拌溶液中添加碳酸钾(2.4g,17.9372mmol)和1,4-二氮杂环庚烷2(2.7g,26.9058mmol),然后在90℃温度下搅拌4天。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉。向粗品中加入在二氯甲烷中的10%甲醇并过滤。减压浓缩滤液,得到灰白色固体形式的4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉(3)(1g)。
[0754]
分析数据:
[0755]
lcms:(m+h
+
):m/z:288.2。
[0756]
叔丁基((4-(6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(5)的合成
[0757][0758]
在0℃下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉(3)(150mg,0.0522 mmol)在二氯甲烷(5ml)中的搅拌溶液中添加二异丙基乙胺(0.13ml,0.7839 mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺4(176mg, 0.0522mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过 100-200combi-flash色谱纯化,在二氯甲烷中洗脱3%甲醇,得到的叔丁基((4-(6,7
‑ꢀ
二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(5)(100mg,41%产率)为灰白色固体。
[0759]
分析数据:
[0760]
lcms:(m+h
+
):m/z:466.13
[0761]
4-(6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺(化合物030)的合成
[0762][0763]
在室温下,将叔丁基((4-(6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯5(90mg,0.1931mmol)和4m hcl在二氧六环(5ml)中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过在二氯甲烷(5ml)中的5%甲醇研磨纯化,得到的4-(6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺化合物030(40mg,57%产率)为灰白色固体。
[0764]
分析数据:1h nmr(400mhz,dmso)δ8.42(d,1h),7.40(s,1h),7.35(s, 1h),6.98(d,1h),6.86(s,2h),3.94-3.99(m,10h),3.56(t,2h),2.13(s,2h)。
[0765]
lcms:(m+h
+
):m/z:367.28
[0766]
化合物031的合成方案
[0767][0768]
4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基-2-(三氟甲基)喹唑啉(3)的合成
[0769][0770]
向4-氯-6,7-二甲氧基-2-(三氟甲基)喹唑啉1(150mg,0.512mmol)在叔丁醇 (10ml)中的搅拌溶液中添加碳酸钾(71mg,0.512mmol)和1,4-二氮杂环庚烷 2(102mg,1.025mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉。向粗品中加入在二氯甲烷中的10%甲醇并过滤。减压浓缩滤液,得到的4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基-2-(三氟甲基)喹唑啉(3)(170mg,粗品)为灰白色固体。
[0771]
分析数据:1h nmr(400mhz,dmso)δ7.380(s,1h),7.312(s,1h), 3.903-3.969(m,10h),3.044-3.069(t,2h),2.793-2.820(t,2h),1.947(bs,2h)。
[0772]
叔丁基((4-(6,7-二甲氧基-2-(三氟甲基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基) 磺酰基)氨基甲酸酯(5)的合成
[0773][0774]
在0℃下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基-2-(三氟甲基)喹唑啉(3)(150mg,0.421mmol)在二氯甲烷(5ml)中的搅拌溶液中添加二异丙基乙胺(81 mg,0.632mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺4(142mg,0.421mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过100-200combi-flash色谱纯化,通过在二氯甲烷中洗脱3%甲醇,得到的叔丁基((4-(6,7-二甲氧基-2-(三氟甲基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基) 氨基甲酸酯(5)(190mg,0.355mmol,84%产率)为灰白色固体。
[0775]
分析数据:1h nmr (400mhz,dmso)δ11.094(bs,1h),7.330(d,2h), 4.009-4.019(m,4h),3.940(s,3h),3.924(s,3h),3.699-3.712(t,3h),3.435(t,2h), 2.072(bs,2h),1.343(s,9h)。
[0776]
4-(6,7-二甲氧基-2-(三氟甲基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺盐
酸盐(化合物031)的合成
[0777][0778]
在室温下,将叔丁基((4-(6,7-二甲氧基-2-(三氟甲基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯5(160mg,0299mmol)和4m hcl在二氧六环(10 ml)中的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过与在二氯甲烷(5ml)中的5%甲醇一起研磨而纯化,得到的4-(6,7-二甲氧基-2-(三氟甲基)喹唑啉-4-基)-1,4-二氮杂环庚烷-1-磺酰胺盐酸盐化合物031(100mg,0.212mmol,71%产率)为灰白色固体。
[0779]
分析数据:1h nmr(400mhz,dmso)δ7.340(s,1h),6.802(bs,2h), 3.992-4.040(m,4h),3.939(s,3h),3.924(s,3h),3.516-3.556(t,2h),3.261-3.289(t, 2h),2.063-2.090(m,2h)。
[0780]
lcms:(m+h
+
):m/z:436.33
[0781]
总体方案6:
[0782][0783]
实施例6:(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙基) 磺酰胺盐酸盐
[0784]
步骤1a:2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙腈
2752mmol)在1,4-二氧六环(18ml)和水(10ml)中的搅拌溶液中添加氢氧化锂一水合物(231mg,5504mmol)、雷尼镍(936mg)和10%钯/碳(295mg),并在室温下在气球氢气氛下搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,反应混合物通过硅藻土过滤并用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床。减压浓缩滤液,得到粗化合物。粗品通过grace反相柱色谱纯化,通过在水中的0.1%甲酸中洗脱20%乙腈,得到的2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙烷-1-胺3(100mg,0.302,11%)为红棕色胶状液体。
[0795]
分析数据:lcms:(m+h+):m/z:332.24
[0796]
通过上述一般程序合成以下化合物:
[0797][0798]
步骤3:叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基) 乙基)氨磺酰基)氨基甲酸酯
[0799][0800]
在0℃下,向2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基乙烷-1
‑ꢀ
乙烷-1-胺3(100mg,0.302mmol)在二氯甲烷(5ml)中的搅拌溶液中添加二异丙基乙胺(60mg,0.453mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物4(102mg,0.302mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过combi-flash柱色谱纯化,在二氯甲烷中洗脱5%甲醇,得到的叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙基)氨磺酰基)氨基甲酸酯5(90mg,0.176mmol,58%产率)为棕色固体。
[0801]
分析数据:1h nmr(400mhz,dmso)δ8.37(s,1h),7.26(s,1h),7.18(m, 1h),7.14(s,1h),3.89-3.87(d,10h),3.00-2.97(m,4h),2.75-2.68(m,2h), 2.66-2.62(m,2h),2.04-2.01(m,2h),1.39(s,9h)。lcms:(m+h+):m/z:511.21
[0802]
通过上述一般程序合成以下化合物
[0803][0804]
步骤4:(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙基) 磺胺盐酸盐(化合物063)
[0805][0806]
在0℃下,向二氧六环(2ml)中的叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)乙基)氨磺酰)氨基甲酸酯5(90mg,0.176mmol)的搅拌溶液中将4m hcl添加到二氧六环(8ml)中,然后在室温下搅拌6小时。通过 tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过制备型hplc法纯化,得到的(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙基)磺胺盐酸盐(15mg,0.036mmol,72%产率)为灰白色固体。
[0807]
分析数据:1h nmr(400mhz,dmso)δ8.38(s,1h),7.26(s,1h),7.14(s, 1h),6.56(brs,2h),6.26-6.27(brs,1h),3.90-3.87(m,10h),2.99-96(m,4h),2.03 (m,2h)。lcms:(m+h+):m/z:411.2
[0808][0809]
化合物062也基于上述一般程序制备:
[0810][0811]
1h nmr(400mhz,dmso)δ8.38(s,1h),7.26(s,1h),7.14(s,1h),6.56(brs, 2h),6.26-6.27(brs,1h),3.90-3.87(m,10h),2.99-96(m,4h),2.03(m,2h)。lcms 411.2。mw 446.95。
[0812]
化合物032的合成方案
[0813][0814]
4-(4-(2-(1,3-二氧异喹啉-2-基)乙基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈(3)的合成
[0815][0816]
将碳酸钾(662mg,4.8mmol)和2-(2-溴乙基)异吲哚啉-1,3-二酮2(610mg, 1.76mmol)添加到dmf(5ml)中的4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉
ꢀ‑
3-碳腈
1.9mmol)添加到dmf(5ml)中的4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉
ꢀ‑
3-碳腈盐酸盐1(500mg,1.6mmol)的搅拌溶液中,然后在90℃下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分离有机层并用水洗涤,然后将有机层减压浓缩以获得粗品。粗残基通过 combi-flash色谱法纯化,得到的纯化合物4-(4-(3-(1,3-二氧异喹啉-2-基)丙基)-1,4
‑ꢀ
二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈3(150mg,0.30mmol,19%产率) 为棕色糖浆。
[0836]
lcms:(m+h)
+
:m/z:500.34
[0837]
4-(4-(3-氨基丙基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈(4)的合成
[0838][0839]
在室温下,向4-(4-(3-(1,3-二氧异喹啉-2-基)丙基)-1,4-二氮杂环庚烷-1
‑ꢀ
基)-6,7-二甲氧基喹啉-3-碳腈3(150mg,0.3mmol)在etoh(3ml)中的搅拌溶液中添加90%的水合肼(0.03ml,0.6mmol),然后回流搅拌反应混合物4小时。通过tlc监测反应进程。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分离有机层并用水洗涤,将有机层减压浓缩以获得粗品。粗化合物通过 combi-flash色谱法纯化,得到的纯化合物4-(4-(3-氨基丙基)-1,4-二氮杂环庚烷-1
‑ꢀ
基)-6,7-二甲氧基喹啉-3-腈(4)(100mg,0.271mmol,90%产率)为棕色糖浆。
[0840]
lcms:(m+h)
+
:m/z:370.2
[0841]
叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)丙基)氨磺酰氨基甲酸酯(6)的合成
[0842][0843]
在室温下,在二氯甲烷(2ml)中的4-(4-(3-(3-氨基丙基)-1,4-二氮杂环庚烷氮
ꢀ‑
1-基)-6,7-二甲氧基喹啉-3-碳腈(4)(100mg,0.27mmol)的搅拌溶液中添加二异丙基乙胺(0.14ml,0.81mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)氨磺酰)吡啶-4(1h)
‑ꢀ
亚基)-n-甲基甲酰胺5(91mg,0.27mmol),然后在室温下搅拌16小时。通过tlc 监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过在dcm中洗脱5%meoh的
组合快速柱色谱法纯化,得到的叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)丙基)氨磺酰氨基甲酸酯(6)(100mg,0.182mmol,67%产率)为棕色固体。
[0844]
lcms:(m+h)
+
:m/z:549.31
[0845]
化合物033的合成
[0846][0847]
在室温下,向1,4-二氧六环(2.0ml)中的叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)丙基)氨磺酰氨基甲酸酯(6)(100mg,0.182 mmol)的搅拌溶液中添加4m hcl到二氧六环(2ml)。将反应混合物在室温下搅拌6小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的化合物033 的纯化合物(10mg,0.022mmol,12%产率)为灰白色固体。
[0848]
分析数据:1h nmr(400mhz,dmso)δ8.60(s,1h),7.30(s,1h),7.36(s,2h), 6.47-6.53(m,3h),3.90(d,6h),3.70-3.72(m,4h),2.90-2.95(m,2h),2.78-2.81(m, 4h),2.54-2.57(m,2h),1.98(m,2h),1.61-1.68(m,2h)。
[0849]
lcms:(m+h)
+
:m/z:449.2
[0850]
总体方案7:
[0851][0852][0853]
实施例7:(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)磺胺盐酸盐
[0854]
步骤1:叔丁基(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2
‑ꢀ
氧乙基)氨基甲酸酯的合成
[0855][0856]
在室温下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹唑啉(400mg,1.38 mmol)在dmf(5ml)中的搅拌溶液中添加二苯并[unk](0.85ml,4.83mmol)、 tbtu(531mg,1.65mmol)和(叔丁氧羰基)甘氨酸(267mg,1.52mmol)。将反应混合物搅拌16小时。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分离有机层,水洗,减压浓缩有机层,得到的纯叔丁基(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨基甲酸酯20(410mg,0.921mmol, 66%产率)的化合物为棕色固体。1h nmr(400mhz,dmso)δ8.41(d,1h),7.21 (d,1h),7.16(d,1h),6.72-6.69(m,1h),3.96-3.87(m,10h),3.80-3.76(m,4h), 3.56-3.55(m,2h),2.05-1.93(m,2h),1.36-1.33(m,9h)。lcms:(m+h)+:m/z: 446.26
[0857]
通过上述一般程序合成以下化合物:
[0858][0859][0860]
步骤2:2-氨基-1-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙-1
‑ꢀ
酮盐酸盐
[0861][0862]
在室温下,向二氧六环(1ml)中的叔丁基(2-(4-(6,7-二甲氧基喹唑啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨基甲酸酯(3)(300mg,0.674mmol)的搅拌溶液中加入4m盐酸(3ml),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,减压蒸馏出有机溶剂,得到的2-氨基-1-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)乙烷-1-一种盐酸盐(4)(250mg,0.656mmol, 91%产率)为棕色固体。
[0863]
分析数据:1h nmr(400mhz,dmso)δ15.07(brs,1h),8.77-8.78(d,1h), 8.10(brs,
3h),7.47-7.41(m,2h),4.28-4.19(m,4h),4.00-3.84(m,13h),3.66-3.64 (m,1h),2.00-2.10(m,2h)。
[0864][0865]
步骤3:叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷环丙烷-1-基)-2-氧乙基)氨磺酰基)氨基甲酸酯
[0866][0867]
在室温下,向2-氨基-1-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷环丙烷-1-基)乙-1-酮盐酸盐(4)(250mg,0.724mmol)在二氯甲烷(20ml)中的搅拌溶液添加二异丙基乙胺(0.631ml,3.62mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物4(293mg,0.869mmol),然后在室温下搅拌 16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在dcm中洗脱5%甲醇来纯化粗化合物,得到的叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨磺酰) 氨基甲酸酯6(200mg,0.381mmol,52%产率)为棕色固体。lcms:(m+h)+:m/z: 525.2
[0868][0869]
步骤4:(n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)磺胺盐酸盐(化合物064)
[0870][0871]
在室温下,向1,4-二氧六环(1.0ml)中的叔丁基(n-(2-(4-(6,7-二甲氧基喹唑啉
ꢀ‑
4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨磺酰)氨基甲酸酯6(200mg,0.381 mmol)的搅拌溶液中添加4m hcl到二氧六环(3ml)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的纯化合物 (n-(2-(4-(6,7-二甲氧基喹唑啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)磺胺盐酸盐(50mg,0.117mmol,31%产率)为灰白色固体。
[0872]
分析数据:1h nmr(400mhz,dmso)δ8.42(d,1h),7.22-7.21(d,1h),7.16 (d,1h),6.59-6.55(m,2h),6.15-6.14(m,1h),3.98-3.97(m,1h),3.90-3.88(m,10h), 3.82-3.78(m,3h),3.76-3.75(m,1h),3.57-3.56(m,2h),2.10-1.95(m,2h)。lcms: (m+h)+:m/z:425.2
[0873][0874]
化合物065也是基于上述一般合成方法制备的:
[0875][0876]
1h nmr(400mhz,dmso)δ15.07(brs,1h),8.77-8.78(d,1h),8.10(brs, 3h),7.47-7.41(m,2h),4.28-4.19(m,4h),4.00-3.84(m,13h),3.66-3.64(m,1h), 2.00-2.10(m,2h)。lcms 425.2.mw.460.93
[0877]
化合物034的合成方案
[0878][0879]
叔丁基(2-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨基甲酸酯(3)的合成
[0880][0881]
在室温下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐 1(200mg,0.641mmol)在dmf(4ml)中的搅拌溶液中添加dipea(0.335ml, 1.923mmol)、tbtu(247mg,0.769mmol)和(叔丁氧羰基)甘氨酸(123mg,0.705 mmol)。将反应混合物搅拌16小时。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分离有机层并用水洗涤,然后将有机层减压浓缩以获得粗品。粗化合物通过combi-flash色谱法纯化,得到的叔丁基(2-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨基甲酸酯(3)(200mg,0.426mmol,66%产率)为黄色固体。
[0882]
分析数据:1h nmr(400mhz,dmso)δ8.69(s,1h),7.94(s,1h),7.4(d,1h), 7.26(s,1h),6.73-6.77(m,1h),4.02-4.00(m,8h),3.80-3.81(m,2h),3.71(m,2h), 3.57(m,2h),3.47-3.48(m,1h),2.8(s,2h),2.1(m,2h),1.38(s,9h)。
[0883]
4-(4-甘氨酰-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐(4)的合成
[0884][0885]
在0℃下,向二氧六环(2ml)中的叔丁基(2-(4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨基甲酸酯3(300mg,0.639mmol)的搅拌溶液中将4m hcl添加到二氧六环(3ml)中,然后在室温下搅拌6小时。通过tlc 监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗残基用乙醚洗涤,得到的4-(4-甘氨酰-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲腈盐酸盐 4(250mg,0.677mmol,96%产率)为黄色固体。
[0886]
lcms:(m+h)
+
:m/z:370.2
[0887]
叔丁基(n-(2-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-2
‑ꢀ
氧乙基)氨磺酰基)氨基甲酸酯(6))的合成
[0888][0889]
在室温下,向二氯甲烷(20vol)中的4-(4-甘氨酰-1,4-二氮杂环庚烷-1
‑ꢀ
基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐(4)(250mg,0.677mmol)的搅拌溶液中添加二异丙基乙胺(0.354ml,2.03mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶
ꢀ‑
4(1h)-亚基)-n-甲基甲酰胺5(251mg,0.745mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在石油醚中洗脱60%乙酸乙酯来纯化粗化合物,得到的叔丁基 (n-(2-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-2-氧乙基)氨磺酰基)氨基甲酸酯(6)(200mg,0.364mmol,54%产率)为淡黄色固体。
[0890]
lcms:(m+h)
+
:m/z:549.34
[0891]
化合物034的制备
[0892][0893]
在室温下,向1,4-二氧六环(2.0ml)中的叔丁基((4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)磺酰基)氨基甲酸酯(6)(100mg,0.203mmol)的搅拌溶液中添加4m hcl到二氧六环(2.0ml)。将反应混合物在室温下搅拌16 小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的纯化合物034(35mg, 0.089mmol,41%产率)为淡黄色固体。
[0894]
分析数据:1h nmr(400mhz,dmso)δ8.67-8.7(d,1h),7.39-7.40(d,1h), 7.26(s,1h),6.62(d,2h),6.14-6.15(m,1h),3.92-3.94(s,6h),3.83(m,2h), 3.67-3.77(m,3h),3.50-3.59(m,3h),2.06-2.08(m,2h)。
[0895]
lcms:(m+h)
+
:m/z:449.2
[0896]
化合物035的合成方案
[0897][0898]
叔丁基4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-羧酸(3)的合成
[0899][0900]
向dmf(26ml)中的4-氯-6,7-二甲氧基喹啉-3-碳腈1(1.3g,5.22mmol)的搅拌溶液中添加碳酸钾(1.45g,10.44mmol)和1,4-二氮杂环庚烷-1-羧酸叔丁酯 2(1.57g,7.84mmol),然后在80℃下搅拌16小时。通过tlc监测反应进程。反应完成后,向反应混合物中加入水(100ml)并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)洗涤合并的有机层,用硫酸钠干燥并减压浓缩,得到的纯4-(3
‑ꢀ
氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-羧酸叔丁酯(1.5g,3.64mmol, 69%产率)的化合物为白色固体。
[0901]
lcms:(m+h)+:m/z:413.2
[0902]
4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐(4)的合成
[0903][0904]
在0℃下,向二氧六环(2ml)中的叔丁基4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-羧酸盐3(450mg,1.09mmol)的搅拌溶液中添加4m hcl 到二氧六环(3ml)中,然后在室温下搅拌4小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。将粗残基用乙醚洗涤,得到的4-(1,4
‑ꢀ
二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲腈盐酸盐4(400mg,1.28mmol,92%产率)为黄色固体。
[0905]
lcms:(m+h)
+
:m/z:313.31
[0906]
叔丁基(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-3-氧丙基)氨基甲酸酯(6)的合成
[0907][0908]
在室温下,向4-(1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐 4(100mg,0.32mmol)在dmf(2ml)中的搅拌溶液中添加dipea(0.16ml,0.96 mmol)、tbtu(124mg,0.38mmol)和3-(叔丁氧羰基)氨基)丙酸(66mg,0.35mmol)。将反应混合物搅拌16小时。反应完成后,将反应混合物倒在水上并用乙酸乙酯萃取。分离有机层并用水洗涤,然后将有机层减压浓缩以获得粗品。粗化合物通过combi-flash色谱法纯化,得到的叔丁基(3-(4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)-3-氧代丙基)氨基甲酸酯(6)(100mg,0.154mmol,66%产率)为浅棕色固体。
[0909]
lcms:(m+h)
+
:m/z:484.3
[0910]
4-(4-(3-氨基丙酰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐(7)的合成
[0911][0912]
在0℃下,向二氧六环(1ml)中的叔丁基(3-(4-(3-氰基-6,7-二甲氧基喹啉-4
‑ꢀ
基)-1,4-二氮杂环庚烷-1-基)-3-氧丙基)氨基甲酸酯7(200mg,0.308mmol)的搅拌溶液中将4m hcl添加到二氧六环(2ml)中,然后在室温下搅拌4小时。通过 tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。将粗残基用乙醚洗涤,得到的4-(4-(3-氨基丙酰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-甲腈盐酸盐7(150mg,0.391mmol,91%产率)为棕色固体。
[0913]
lcms:(m+h)
+
:m/z:384.2
[0914]
叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-3
‑ꢀ
氧丙基)氨磺酰氨基甲酸酯(8)的合成
[0915][0916]
在室温下,将二异丙基乙胺(0.2ml,1.17mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺(145mg,0.43mmol)添加到4-(4-(3-(3-(3-氨基丙酰基)-1,4-二氮杂环庚烷-1-基)-6,7-二甲氧基喹啉-3-碳腈盐酸盐(7)(150mg, 0.39mmol)在二氯甲烷(3ml)中的搅拌溶液中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在dcm中洗脱5%甲醇,通过组合快速柱色谱法纯化粗化合物,得到的叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1
‑ꢀ
基)-3-氧丙基)氨磺酰氨基甲酸酯(8)(150mg,0.266mmol,68%产率)为棕色固体。
[0917]
lcms:(m+h)
+
:m/z:563.3
[0918]
化合物035的合成
[0919][0920]
在室温下,向1,4-二氧六环(1.0ml)中的叔丁基(n-(3-(4-(3-氰基-6,7-二甲氧基喹啉-4-基)-1,4-二氮杂环庚烷-1-基)-3-氧丙基)氨基甲酸酯(8)(150mg,0.266 mmol)的搅拌溶液中添加4m hcl到二氧六环(2.0ml)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的化合物035 的纯化合物(30mg,0.064mmol,24%产率)为灰白色固体。
[0921]
分析数据:1h nmr(400mhz,dmso)δ8.71(d,1h),7.41(d,2h),7.27(s, 1h),6.56(d,2h),6.34-6.40(m,1h),3.92-3.94(m,6h),3.78-3.81(m,1h), 3.67-3.70(m,4h),3.50-3.59(m,4h),3.10-3.17(m,2h),2.65-2.70(m,2h), 2.06-2.07(m,2h)。lcms:(m+h)+:m/z:463.2
[0922]
总体方案8
[0923][0924]
实施例8:n-(2-(1-(6,7-二甲氧基喹唑啉-4-基)氮杂环庚-4-基)乙基)磺酰胺
[0925]
步骤1a:叔丁基4-(氰基甲基)氮杂环庚烷-1-羧酸
[0926][0927]
在0℃下,向四氢呋喃(10ml)和三乙胺(475mg,4694mmol)中的4-氧代烷
ꢀ‑
1-羧酸叔丁酯[unk](500mg,2347mmol)的搅拌溶液中添加二乙基(氰甲基)膦酸盐[unk](436mg,2464mmol)和溴化锂(245mg,2816mmol)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。完成后,将反应混合物倒入冰冷的水(100ml)中并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过100-200硅胶柱色谱纯化,通过在石油醚中的15%乙酸乙酯洗脱,得到的4-(氰亚甲基)氮杂环庚烷-1-甲酸叔丁基(510mg,2.161mmol,92%产率)为无色油状液体。1h nmr(400mhz,dmso) δ5.57
–
5.42(m,1h),3.43(m,2h),3.32(m,1h),3.29(m,1h),2.72(m,1h),2.59
–ꢀ
2.50(m,2h),2.40(d,1h),1.61(m,2h),1.38(s,9h)。
[0928]
步骤1b:叔丁基4-氰基氮杂烷-1-羧酸
[0929][0930]
在0℃下,向n,n
’‑
二甲基甲酰胺(1ml)中的4-氧代烷-1-羧酸叔丁酯1(250g, 1.173mmol)的搅拌溶液中添加1-(异氰甲基)磺酰基)-4-甲苯2(286mg,1.467 mmol)。在0℃下,向反应混合物中添加叔丁醇钾(262mg,2.346mmol)在0℃时在叔丁醇(1ml)和1,2-二甲氧基乙烷(1ml)中的溶液,并在室温下搅拌反应混合物3小时。通过tlc监测反应进程。完成后,将反应混合物倒入冰冷的水 (50ml)中并用乙酸乙酯(2x30ml)萃取。用盐水溶液(50ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过100-200硅胶柱色谱纯化,通过在石油醚中的15%乙酸乙酯洗脱,得到的叔丁基4-氰基氮杂烷-1-羧酸3(150mg,0.669mmol, 57%产率)为淡蓝色胶状液体。
[0931]
分析数据:1h nmr(400mhz,dmso)δ3.43-3.37(m,2h),3.27-3.16(m,2h), 3.07(brs,1h),1.88-1.85(m,2h),1.73(brs,4h),1.38(s,9h)。
[0932]
步骤2:叔丁基4-(2-氨基乙基)氮杂环庚烷-1-羧酸
[0933][0934]
向1,4-二氧六环(15ml)中的4-(氰甲基)氮杂环烷-1-羧酸叔丁酯3(510mg, 2.161mmol)和水(5ml)的搅拌溶液中添加氢氧化锂一水合物(200mg,4.754 mmol)、雷尼镍(500mg)和10%钯/碳(150mg),并在室温下在气球氢气氛下搅拌反应混合物16小时。通过tlc监测反应进程。完成后,反应混合物通过硅藻土过滤并用含5%甲醇的二氯甲烷(100ml)
洗涤硅藻土床。减压浓缩滤液,得到的半纯的4-(2-氨基乙基)氮杂环庚烷-1-羧酸叔丁基化合物4(500mg,粗品)为无色胶状液体。
[0935]
分析数据:1h nmr(400mhz,dmso)δ3.46
–
3.07(m,8h),2.55
–
2.50(m, 2h),1.76
–
1.66(m,3h),1.60(m,1h),1.43(m,3h),1.27
–
1.14(m,4h),1.30
–ꢀ
1.01(m,1h)。
[0936][0937]
步骤3:叔丁基4-(2-(n-(叔丁氧羰基)氨磺酰基)氨基)乙基)氮杂环庚烷-1-羧酸
[0938][0939]
在0℃下,将二异丙基乙胺(400mg,3.099mmol)和n-(1-(n-(叔丁氧羰基) 氨磺酰基)吡啶-4(1h)-亚叶状)-n-甲基甲酰胺5(696mg,2.066mmol)在0℃下添加到二氯甲烷(10ml)中的4-(2-氨基乙基)氮杂环戊烷-1-羧酸叔丁酯4(500mg, 2.066mmol)的搅拌溶液中,然后在室温下搅拌16小时。通过tlc监测反应进程。完成后,向反应混合物中加入水(100ml)并用二氯甲烷(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩,得到粗化合物。粗品通过100-200硅胶柱色谱法纯化,通过在二氯甲烷中的2%甲醇洗脱,得到半纯化合物。用石油醚中的50%乙酸乙酯洗涤该半纯品,得到的叔丁基 4-(2-(n-(叔丁氧羰基)氨磺酰)氨基)乙基)氮杂环庚烷-1-羧酸酯6(600mg,1.425 mmol,69%产率)为无色胶状液体。
[0940]
分析数据:1h nmr(400mhz,dmso)δ10.76(s,1h),7.50
–
7.45(m,1h), 3.41(m,1h),3.24
–
3.19(m,2h),3.12
–
3.03(m,1h),2.87(d,2h),1.70(m,2h), 1.57(m,1h),1.39(m,25h)。
[0941][0942]
步骤4:(n-(2-(氮杂环丙烷-4-基)乙基)磺酰胺
[0943][0944]
在0℃下,向二氧六环(5ml)中的叔丁基4-(2-(n-(叔丁氧羰基)氨磺酰基)乙基)氮杂环戊-1-甲酸酯6(600mg,1.425mmol)的搅拌溶液中将4m hcl添加到二氧六环(15ml)中,然后在室温下搅拌3小时。通过tlc监测反应进程。完成后,在减压下完全蒸馏掉有机溶剂,得到的粗品(n-(2-(氮杂环丙烷-4-基)乙基) 磺酰胺(420mg,粗品)为浅棕色胶状固体。
[0945]
分析数据:1h nmr(400mhz,dmso)δ8.94(d,2h),6.34(broad s,2h),3.07 (m,2h),2.96(m,2h),2.86(t,2h),1.76(m,3h),1.64(m,2h),1.52
–
1.44(m,1h), 1.41
–
1.32(m,2h),1.22(m,1h)。
[0946][0947]
步骤5:n-(2-(1-(6,7-二甲氧基喹唑啉-4-基)氮杂环丙烷-4-基)乙基)磺酰胺(化合物060)
[0948][0949]
向4-氯-6,7-二甲氧基喹唑啉8(285mg,1273mmol)在乙腈(15ml)中的搅拌溶液中添加碳酸钾(263mg,1909mmol)和化合物7(360mg,1,4mmol),然后在 90℃下搅拌16小时。通过tlc监测反应进程。反应完成后,加入水(100ml) 并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过制备型hplc法纯化,得到的n-(2-(1-(6,7-二甲氧基喹唑啉-4-基)氮杂环-4-基)乙基)磺酰胺(52mg,0.127mmol,10%产率)为淡橙色固体。
[0950]
分析数据:1h nmr(400mhz,dmso)δ8.35(s,1h),7.29(s,1h),7.12(s, 1h),6.43(m,3h),3.97(d,2h),3.88(m,6h),3.68(m,2h),2.89(m,2h),1.98(m, 2h),1.87(m,1h),1.74(m,1h),1.63(m,2h),1.44(m,2h),1.22(m,1h)。
[0951]
[0952][0953]
基于上述一般程序制备化合物049:
[0954][0955]
m.w.409.51
[0956]
1h nmr(400mhz,dmso)δ8.35(s,1h),7.29(s,1h),7.12(s,1h),6.43(m, 3h),3.97(d,2h),3.88(m,6h),3.68(m,2h),2.89(m,2h),1.98(m,2h),1.87(m, 1h),1.74(m,1h),1.63(m,2h),1.44(m,2h),1.22(m,1h)。lcms 409.9
[0957]
化合物036的合成方案:
[0958]
[0959]
步骤1:4-((2-(2-氨基乙氧基)乙基)氨基)-6,7-二甲氧基喹啉-3-腈3的合成:
[0960][0961]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(150mg,0.68mmol)在thf(15ml)中的搅拌溶液中添加2,2
’‑
氧双(乙烷-1-胺)2(314mg,3.4mmol),然后在50℃下搅拌反应混合物20小时。通过tlc监测反应进程。反应完成后,将反应混合物完全蒸馏出并吸附在硅藻土上,使用acn/水系统进行反相grace处理,得到的4-((2-(2-氨基乙氧基)乙基)氨基)-6,7-二甲氧基喹啉-3-甲腈(170mg)为白色固体。
[0962]
分析数据:1h nmr(400mhz,dmso):δ8.36-8.33(m,3h),8.09(brs,1h), 7.75(s,1h),7.21(s,1h),3.95-3.94(m,2h),3.90(s,6h),3.75(t,2h),3.60(t,2h), 2.89(t,2h)。
[0963]
lcms:(m+h)+:m/z:317.2
[0964]
步骤2:氨基甲酸叔丁基(n-(2-(2-((3-氰基-6,7-二甲氧基喹啉-4-基)氨基)乙氧基)乙基)氨磺酰基)氨基甲酸酯5的合成:
[0965][0966]
向dcm(10ml)中的4-(2-(2-氨基乙氧基)乙基)氨基)-6,7-二甲氧基喹啉-3-碳腈3(170mg,0.54mmol)的搅拌溶液中缓慢添加n-(1-(n-(叔丁氧羰基)氨磺酰基) 吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物4(163mg,0.48mmol),然后在相同温度下添加dipea(0.3ml,1.6mmol)。将反应混合物在室温下搅拌16小时。通过 tlc监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。通过在 dcm中洗脱2-3%meoh,通过combi-flash色谱法纯化粗产物,得到的叔丁基 (n-(2-(2-((3-氰基-6,7-二甲氧基喹啉-4-基)氨基)乙氧基))乙基)氨磺酰基)氨基甲酸酯5(90mg)为白色固体。
[0967]
分析数据:1h nmr(400mhz,dmso)δ:10.84(s,1h),8.34(s,1h),7.81(brs, 1h),7.64(s,1h),7.51(t,1h),7.21(s,1h),3.93-3.89(m,8h),3.72(t,2h),3.51(t, 2h),3.06-3.01(m,2h),1.35(s,9h)。
[0968]
lcms:(m+h)+:m/z:396
[0969]
步骤3:化合物036的合成:
[0970][0971]
在0℃下,向二氧六环(3ml)中的叔丁基(n-(2-(2-((3-氰基-6,7-二甲氧基喹啉
ꢀ‑
4-基)氨基)乙氧基)乙基)氨磺酰)氨基甲酸酯5(90mg,0.18mmol)搅拌溶液中添加4m hcl到二氧六环(1ml),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物通过制备型hplc 纯化,得到的化合物036(10mg)为白色固体。
[0972]
分析数据:1h nmr(400mhz,dmso)δ:8.34(s,1h),7.84(t,1h),7.64(s, 1h),7.22(s,1h),6.52(brs,2h),6.45(t,1h)3.94-3.89(m,8h),3.72(t,2h),3.54(t, 2h),3.06(q,2h)。
[0973]
lcms:(m+h)+:m/z:396.25。
[0974]
化合物037的合成方案
[0975][0976]
4-((4-((n-(叔丁氧基羰基)氨磺酰基)氨基)丁基)氨基)-6-甲氧基喹唑啉-7-基三氟甲磺酸酯(int-5)的合成
[0977][0978]
在0℃下,向int-6(500mg,1.13mmol)在二氯甲烷(20ml)中的搅拌溶液中添加三乙胺(0.475ml,3.39mmol)和1,1,1-三氟-n-苯基-n-(三氟甲基)磺酰基)甲磺酰胺2(445mg,1.24mmol),然后在室温下搅拌4小时。通过tlc监测反应进程。反应完成后,在减压下完全蒸
馏掉有机溶剂,将水(200ml)加入粗品中并用二氯甲烷(2
×
200ml)分配。用盐水溶液(200ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过combi-flash色谱法纯化,用石油醚中的70%乙酸乙酯洗脱,得到的4-((4-((n-(叔丁氧基羰基)氨磺酰基)氨基)丁基)氨基)-6-甲氧基喹唑啉-7-基三氟甲磺酸盐int-5(450mg,0.785mmol,69%两步产率)为淡黄色固体。
[0979]
lcms:(m+h
+
):m/z:574。
[0980]
化合物037的制备
[0981][0982]
在密封管中,向4-(4-(叔丁氧羰基)氨磺酰基)丁基)丁基)-6-甲氧基喹唑啉-7
‑ꢀ
基三氟甲基磺酸int-5(200mg,0.349mmol)在二氧六环(8ml)和水(2ml)中的搅拌溶液中添加3-(4,4,5,5-四甲基-1,3,2-二恶英-2-基)-1-(三异丙基硅烷基)-1h吡咯 (121mg,0.453mmol)和氟化铯(159mg,1047mmol),然后脱气反应混合物30 分钟。然后再次脱气5分钟加入四(三苯基膦)钯(0)(40mg,0.034mmol)并在100℃搅拌反应混合物5小时。通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。粗品通过制备型hplc法纯化,得到的(化合物037)(30mg,0.052mmol,23%) 为浅黄色固体。
[0983]
分析数据:1h nmr(400mhz,dmso)δ11.13(s,1h),8.625(brs,1h),8.49(s, 1h),7.8(s,1h),7.7(s,1h),7.51(s,1h),6.86-6.87(m,1h),6.62-63(m,1h), 6.46-6.52(m,3h),4.0(s,3h),3.59-3.61(q,2h),2.92-2.95(q,2h),1.55-1.72(m, 4h)。
[0984]
lcms:(m+h
+
):m/z:391.1
[0985]
化合物038的合成方案
[0986][0987]
向4-氯-6,7-二甲氧基喹啉-3-碳腈1(100mg,0.403mmol)在n,n
’‑
二甲基甲酰胺
(5ml)中的搅拌溶液中添加碳酸钾(83mg,0.443mmol)和化合物2(114mg, 0.443mmol),然后在90℃下搅拌3小时。通过tlc监测反应进程。反应完成后,加入水(100ml)并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过制备型hplc法纯化,得到化合物038(29mg,0.067mmol,16%产率)为灰白色固体。
[0988]
分析数据:1h nmr(400mhz,dmso)δ8.618(s,1h),7.365(s,1h),7.330(s, 1h),6.450 6.467(d,3h),3.94(s,3h),3.931(s,3h),3.671-3.689(m,2h), 3.554-3.587(m,2h),2.903-2.953(m,2h),1.820-1.926(m,5h),1.437-1.582(m, 4h)。
[0989]
lcms:(m+h+):m/z:434.2
[0990]
化合物038提交sfc并分离成两种对映异构体,得到038-ent-1(17mg,0.039 mmol)和038-ent-2(17mg,0.039mmol)。
[0991]
038-ent-1的分析数据:1h nmr(400mhz,dmso)δ8.628(s,1h),7.376(s, 1h),7.343(s,1h),6.456(bs,3h),3.951(s,3h),3.942(s,3h),3.679-3.722(t,2h), 3.580-3.624(m,2h),2.925-2.958(t,2h),1.835-1.935(m,5h),1.423-1.591(m,4h)。
[0992]
lcms:(m+h+):m/z:434.2
[0993]
038-ent-2的分析数据:1h nmr(400mhz,dmso)δ8.627(s,1h),7.376(s, 1h),7.342(s,1h),6.462(bs,3h),3.950(s,3h),3.941(s,3h),3.665-3.678(m,2h), 3.596-3.615(m,2h),2.940-2.957(t,2h),1.836-2.060(m,5h),1.507-1.523(m,4h)。
[0994]
lcms:(m+h+):m/z:434.2
[0995]
化合物039的合成方案
[0996][0997]
化合物039的制备的合成
[0998][0999]
向n,n
’‑
二甲基甲酰胺(3ml)中的4-氯-6,7-二甲氧基喹啉-3-碳腈8(150mg, 0.605mmol)的搅拌溶液中添加碳酸钾(250mg,1.814mmol)和化合物-7(220mg, 0.907mmol),然后在90℃下搅拌6小时。通过tlc监测反应进程。反应完成后,加入水(100ml)并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过制备型hplc法纯化,得到化合物039(170mg,0.405mmol,67%产率)为灰白色固体。
[1000]
分析数据:1h nmr(400mhz,dmso)δ8.625(s,1h),7.368(s,1h),7.331(s, 1h),6.613-6.644(t,1h),6.483(s,2h),3.94(s,3h),3.931(s,3h),3.544-3.3.688(m, 4h),2.788-2.848(m,2h),1.937-2.045(m,4h),1.740-1.793(m,1h),1.511-1.589 (m,1h),1.368-1.424(m,1h)。
[1001]
lcms:(m+h+):m/z:420.2
[1002]
化合物039提交sfc并分离成两种对映异构体,得到039-ent-1(25mg,0.059 mmol)和039-ent-2(17mg,0.04mmol)。
[1003]
039-ent-1的分析数据:1h nmr(400mhz,dmso)δ8.635(s,1h),7.379(s, 1h),7.343(s,1h),6.618-6.644(t,1h),6.487(s,2h),3.941(s,3h),3.951(s,3h), 3.645-3.672(m,4h),2.801-2.843(m,2h),1.952-2.053(m,4h),1.785-1.825(m, 1h),1.551-1.593(m,1h),1.390-1.456(m,1h)。
[1004]
lcms:(m+h+):m/z:420.2
[1005]
039-ent-2的分析数据:1h nmr(400mhz,dmso)δ8.636(s,1h),7.379(s, 1h),7.343(s,1h),6.634(bs,1h),6.488(t,1h),6.487(s,2h),3.941(s,3h),3.951 (s,3h),3.645-3.672(m,4h),2.801-2.843(m,2h),1.952-2.055(m,4h),1.765-1.825 (m,1h),1.553-1.573(m,1h),1.386-1.456(m,1h)。
[1006]
lcms:(m+h
+
):m/z:420
[1007]
化合物040-ent-1的合成方案
[1008][1009]
1-(6,7-二甲氧基喹唑啉-4-基)氮杂环烷-4-磺酰胺(化合物040-ent-1)的合成
[1010]
向4-氯-6,7-二甲氧基喹唑啉1(120mg,0.5357mmol)在acn(2ml)和 k2co3(222mg,1.6071mmol)中的搅拌溶液,然后在90℃下搅拌16小时。反应完成后,粗残基加入水(10ml)。然后用二氯甲烷(30ml)中的10%甲醇萃取,减压浓缩,得到粗化合物。粗化合物通过制备型hplc方法纯化,得到的纯化合物1-(6,7-二甲氧基喹唑啉-4-基)氮杂环烷-4-磺酰胺(t-116-ent-1)(10mg,5%产率)为白色固体。
[1011]
分析数据:1h nmr(400mhz,dmso)δ8.40(s,1h),7.26(s,1h),7.15(s, 1h),6.74(s,2h),4.09(m,2h),3.90(s,3h),3.88(s,3h),3.69-3.80(m,2h),3.69(m, 1h),3.01(p,2h),2.30(m,1h),2.08(p,2h),1.91(m,1h),1.60(m,1h)。
[1012]
lcms:(m+h
+
):m/z:367.1
[1013]
化合物040-ent-2的合成方案
[1014][1015]
1-(6,7-二甲氧基喹唑啉-4-基)氮杂环烷-4-磺酰胺(化合物040-ent-2)的合成
[1016]
向4-氯-6,7-二甲氧基喹唑啉1(120mg,0.5357mmol)在acn(2ml)和 k2co3(222mg,1.6071mmol)中的搅拌溶液,然后在90℃下搅拌16小时。反应完成后,粗残基加入水(10ml)。然后用二氯甲烷(30ml)中的10%甲醇萃取,减压浓缩,得到粗化合物。粗化合物通过制备型hplc方法纯化,得到的纯化合物1-(6,7-二甲氧基喹唑啉-4-基)氮杂环烷-4-磺酰胺(t-116-ent-2)(10mg,5%产率)为白色固体。
[1017]
分析数据:1h nmr(400mhz,dmso)δ8.50(s,1h),7.34(s,1h),7.18(s, 1h),6.78(s,2h),4.18(m,2h),3.93(s,3h),3.91(s,3h),3.76-3.84(m,2h),3.04(m, 1h),3.01(p,2h),2.92(m,1h),2.13(m,1h),1.98(m,1h),1.60(m,1h)lcms: (m+h+):m/z:367.1
[1018]
化合物041的合成方案
[1019][1020]
叔丁基4-亚甲基氮杂环丙烷-1-羧酸(2)的合成
[1021][1022]
向甲基三苯基膦酰亚胺2(227mg,0.563mmol)在乙醚(5ml)中的搅拌溶液中添加1m叔丁醇钾(63mg,0.563mmol),反应变为黄色。然后加入叔丁基4
‑ꢀ
氧乙酸乙酯-1-羧酸1(100mg,0.469mmol)并在50℃下搅拌3小时。通过tlc 监测反应进程。反应完成后,向反应混合物中加入水(30ml)并用乙酸乙酯(2
×
20 ml)萃取。用盐水溶液(40ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗化合物通过100-200硅胶柱色谱纯化,通过在石油醚中的5%乙酸乙酯洗脱,得到的4-亚甲基氮杂-1-羧酸叔丁基2(60mg,0.284mmol)为无色油状液体。
[1023]
分析数据:1h nmr(400mhz,dmso)δ4.732-4.786(m,4h),2.404-2.433(m, 2h),2.209-2.239(t,2h),1.655-1.706(m,2h),1.448(s,9h)。
[1024]
叔丁基4-(溴甲基)-4-氟氮杂烷-1-羧酸(3)的合成
[1025][1026]
在0℃下,向二氯甲烷(50ml)中的4-亚甲基氮杂环丙烷-1-羧酸叔丁酯2(1.9 g,
9.005mmol)的搅拌溶液中添加三乙胺三氢氟化物(3.6g,22.52mmol)和n-溴丁二酰亚胺(2.4g,13.507mmol),然后在室温下搅拌2小时。通过tlc监测反应进程。反应完成后,反应混合物用饱和nahco3溶液(100ml)淬灭并用过量二氯甲烷(2x150ml)萃取。用盐水溶液(150ml)洗涤合并的有机层,在na2so4 上干燥,并在减压下浓缩,得到粗化合物。粗品通过100-200combi-flash色谱纯化,通过在石油醚中洗脱5%乙酸乙酯,得到的叔丁基4-(溴甲基)-4-氟氮杂烷-1
‑ꢀ
羧酸3(1.7g,5.5mmol,61%产率)为无色油状液体。
[1027]
分析数据:1h nmr(400mhz,dmso)δ3.500-3.673(m,2h),3.434-3.477(d, 2h),3.162-3.269(m,4h),1.980-2.114(m,4h),1.652-1.913(m,2h),1.465(s,9h)。
[1028]
叔丁基4-(叠氮基甲基)-4-氟氮杂烷-1-羧酸(4)的合成
[1029][1030]
将叠氮化钠(473mg,7.281mmol)和碘化钠(1g,7.281mmol)添加到4-(溴甲基)-4-氟氮杂环戊烷-1-羧酸叔丁酯3(1.5g,4.854mmol)在二甲基亚砜(20ml)中的搅拌溶液中,然后在130℃下搅拌16小时。通过tlc监测反应进程。反应完成后,向反应混合物中加入水(200ml)并用乙酸乙酯(2
×
150ml)萃取。用盐水溶液(200ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩,得到粗化合物。通过在石油醚中洗脱20%乙酸乙酯通过combi-flash色谱法纯化粗品,得到的叔丁基 4-(叠氮基甲基)-4-氟氮杂烷-1-羧酸4(600mg,2.205mmol,45%产率)为无色油状液体。
[1031]
分析数据:1h nmr(400mhz,dmso)δ3.508-3.797(m,2h),3.148-3.387(m, 4h),1.952-2.158(m,3h),1.648-1.790(m,2h),1.442(s,9h)。
[1032]
叔丁基4-(氨基甲基)-4-氟氮杂烷-1-羧酸(5)的合成
[1033][1034]
添加10%pd/c(60mg,10%w/w)的叔丁基4-(叠氮甲基)-4-氟氮杂环烷-1-羧酸5(600mg,2.206mmol)在甲醇(20ml)中的搅拌溶液,然后在气球氢气氛下搅拌16小时。通过tlc监测反应进程。反应完成后,反应混合物通过硅藻土过滤,用10%甲醇的二氯甲烷溶液(50ml)洗涤硅藻土床。减压浓缩滤液,得到粗化合物。粗品通过combi-flash色谱法纯化,通过在石油醚中洗脱30%乙酸乙酯,得到的叔丁基4-(氨基甲基)-4-氟氮杂烷-1-羧酸5(400mg,1.626mmol,74%产率) 为无色油状液体。
[1035]
分析数据:1h nmr(400mhz,dmso)δ3.106-3.503(m,6h),2.618-2.625(d, 2h),2.570-2.576(d,1h),1.490-1.912(m,6h),1.380(s,9h)。
[1036]
叔丁基4-(((n-(叔丁氧羰基)氨磺酰基)氨基)甲基)-4-氟氮杂-1-羧酸(7)的合成
[1037][1038]
在0℃下,将二异丙基乙胺(315mg,2.439mmol)和n-(1-(n-(叔丁氧羰基) 氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺6(548mg,1.626mmol)添加到二氯甲烷 (10ml)中的4-(氨基甲基)-4-氟氮杂环丁烷-1-羧酸叔丁酯5(400mg,1.626mmol) 的搅拌溶液中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过 100-200combi-flash色谱纯化,在二氯甲烷中洗脱3%甲醇,得到的叔丁基 4-(((n-(叔丁氧羰基)氨磺酰基)氨基)甲基)-4-氟氮杂烷-1-羧酸7(350mg,0.823 mmol,50%产率)为棕色固体。
[1039]
分析数据:1h nmr(400mhz,dmso)δ10.827(s,1h),7.858(bs,1h), 3.031-3.515(m,4h),1.506-1.977(m,6h),1.381(s,9h),1.406(s,9h),1.218-1.234 (m,1h)。
[1040]
化合物8的合成
[1041][1042]
在室温下将二恶英(10ml)中的叔丁基4-(n-(叔丁氧羰基)氨磺酰基)甲基)-4
‑ꢀ
氟氮杂环烷-1-羧酸盐7(350mg,0.823mmol)和4m hcl的搅拌溶液搅拌16小时。通过tlc监测反应进程。反应完成后,减压蒸馏除去有机溶剂,得到的化合物 8(250mg,0.958mmol,定量产率)为棕色胶状液体。
[1043]
分析数据:1h nmr(400mhz,dmso)δ9.088(bs,2h),7.147(t,1h),6.880 (bs,1h),6.583(bs,1h),2.994-3.151(m,6h),2.077-2.163(m,2h),1.689-1.945(m, 4h)。
[1044]
化合物041的合成
[1045][1046]
向4-氯-6,7-二甲氧基喹啉-3-碳腈9(80mg,0.332mmol)在n,n
’‑
二甲基甲酰胺(5ml)中的搅拌溶液中添加碳酸钾(137mg,0.996mmol)和化合物-8(130mg, 0.498mmol),然后在90℃下搅拌6小时。通过tlc监测反应进程。反应完成后,加入水(100ml)并用乙酸乙酯(2x100ml)萃取。用盐水溶液(100ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩。粗品通过制备型hplc方法纯化,得到的化合物041(30mg,0.068mmol,21%产率)为灰白色固体。
[1047]
分析数据:1h nmr(400mhz,dmso)δ8.651(s,1h),7.377(s,1h),7.319(s, 1h),6.860-6.895(t,1h),6.567(s,2h),3.945(s,3h),3.937(s,3h),3.811-3.856(m, 1h),3.549-3.639(m,2h),3.462-3.500(m,1h),3.073-3.3.137(dd,2h),2.030-2.217 (m,5h),1.831-1.862(bs,1h)。
[1048]
化合物042和043的合成方案
[1049][1050]
步骤1:叔丁基4-(苄基氨基)氮杂环庚烷-1-羧酸(2)的合成
[1051][1052]
在0℃下,将苄胺(2.1ml,19.2mmol)和stab(2.1g,9.9mmol)添加到 dmf(7.5ml)中的4-氧代烷-1-羧酸叔丁酯1(1g,4.69mmol)的搅拌溶液中,然后添加acoh(0.5ml)。然后让
反应混合物在室温下搅拌16h。通过tlc监测反应进程。反应完成后,将反应混合物直接倒入冰冷的水中并搅拌。有机物用etoac 萃取三次,合并的有机物用盐水洗涤,干燥并浓缩。将化合物直接吸附在二氧化硅和combi-flash色谱上,得到叔丁基4-(苄基氨基)氮杂环庚烷-1-羧酸2(1.2g, 3.947mmol,85%产率)
[1053]
分析数据:(m+h)+:m/z:305.2
[1054]
步骤2:叔丁基4-氨基氮杂环戊烷-1-羧酸(3)的合成
[1055][1056]
向4-(苄基氨基)氮杂环庚烷-1-羧酸叔丁酯2(1.1g,3.6mmol)在甲醇(20ml) 中的搅拌溶液中添加钯/碳(100mg),并在室温下搅拌16小时。反应完成后,通过硅藻土垫过滤反应混合物。减压浓缩滤液,得到的叔丁基4-氨基氮杂-1-羧酸 3(600mg,2.803mmol,71%产率)为淡黄色液体。
[1057]
分析数据:1h nmr(400mhz,dmso):3.48-3.41(m,2h),3.29-3.27(m, 1h),3.10-3.05(m,1h),2.97-2.94(m,1h),1.93-1.89(m,1h),1.85-1.77(m,3h), 1.53-1.48(m,2h),1.39(s,9h)。
[1058]
步骤3:叔丁基4-((n-(叔丁氧基羰基)氨磺酰基)氨基)氮杂-1-羧酸5:
[1059][1060]
将n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化铵 4(1.4g,3.08mmol)缓慢添加到dcm(30ml)中的4-氨基氮杂环丙烷-1-羧酸叔丁酯3(600mg,2.8mmol)的搅拌溶液中,然后在相同温度下添加dipea二乙酯(1.5 ml,8.4mmol)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。将反应混合物直接吸附到二氧化硅上,粗品通过combi-flash色谱法纯化,通过在己烷中洗脱80%etoac,得到的4-((n-(叔丁氧基羰基)氨磺酰基)氨基)氮杂-1
‑ꢀ
羧酸叔丁基5(650mg,1.65mmol,59%产率)为白色固体。
[1061]
分析数据:1h nmr(400mhz,dmso):10.77(s,1h),7.68-7.63(m,1h), 3.32-3.30(m,1h),3.20-3.10(m,4h),1.89-1.74(m,3h),1.58-1.48(m,3h), 1.41-1.38(m,18h)。
[1062]
lcms:(m-h)+:m/z:392.1
[1063]
步骤4:4-((n-氨磺酰基)氨基)氮杂环丙烷-盐酸盐(6)的合成
[1064][1065]
在0℃下,向二氯甲烷(10ml)中的4-(n-(叔丁氧羰基)氨磺酰基)氮杂环戊-1
‑ꢀ
甲酸叔丁酯5(650mg,1.6mmol)的搅拌溶液中添加4m hcl到二氧六环(0.6ml) 中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗化合物与乙醚一起研磨,得到的4-((n-氨磺酰基)氨基)氮杂环庚烷-盐酸盐(310mg)为白色固体。
[1066]
分析数据:1h nmr(400mhz,dmso)δ:8.92(brs,2h),6.72-6.70(brs,1h), 6.53(brs,1h),3.39-3.37(s,1h),3.16-3.14(m,1h),3.16-3.14(m,1h),3.08-3.05(m, 1h),3.05-2.98(m,2h),2.06-2.04(m,1h),1.95-1.90(m,1h),1.87-1.81(m,2h), 1.67-1.54(m,2h)
[1067]
步骤5:n-(1-(3-氰基-6,7-二甲氧基喹啉-4-基)氮杂环-4-基)氨磺酰胺(化合物 042)的合成
[1068][1069]
在室温下,向dmf(5ml)中的4-氯-6,7-二甲氧基喹啉-3-碳腈7(146mg,0.65 mmol)的搅拌溶液中添加4-(n-氨磺酰)氨基氮杂环戊烷盐酸盐(135mg,0.58 mmol),然后添加k2co3(0.270mg,1.96mmol)。添加后,将反应混合物加热至 90℃搅拌16小时。通过tlc监测反应进程。反应完成后,用水淬灭,有机物用etoac萃取三次,合并的有机物用盐水洗涤,干燥,减压浓缩,得到粗品。粗化合物通过制备型hplc纯化,得到的n-(1-(3-氰基-6,7-二甲氧基喹啉-4-基) 氮杂环-4-基)氨磺酰胺(化合物042)(22mg,0.054mmol,9%产率)为淡黄色蓬松固体。
[1070]
分析数据:1h nmr(400mhz,dmso)δ:8.62(s,1h),7.36(s,1h),7.32(s, 1h),6.72(d,1h),6.51(s,2h),3.94(s,6h),3.62-3.61(m,3h),3.54-3.51(m,2h), 2.21-2.10(m,2h),1.93-1.91(m,1h),1.87-1.74(m,3h)
[1071]
lcms:(m+h)
+
:m/z:406.31
[1072]
步骤6:n-(1-(6,7-二甲氧基喹唑啉-4-基)氮杂环-4-基)氨磺酰胺(化合物043) 的合成
[1073][1074]
在室温下,向4-氯-6、7-二甲氧基喹唑啉8(146mg,0.65mmol)在dmf(5ml) 中的搅拌溶液中添加4-(n-氨磺酰)氮杂环庚烷-盐酸盐(135mg,0.589mmol),然后添加k2co3(0.270mg,1.96mmol)。添加后,将反应混合物加热至90℃搅拌 16小时。通过tlc监测反应进程。反应完成后,将反应混合物倒在水上,用 etoac萃取三次,合并的有机层用盐水洗涤,减压干燥,得到粗品。粗化合物通过制备型hplc纯化,得到的n-(1-(6,7-二甲氧基喹唑啉-4-基)氮杂-4-基)氨磺酰胺化合物043(24mg,0.062mmol,9.6%产率)为灰白色固体。
[1075]
分析数据:1h nmr(400mhz,dmso)δ:8.36(s,1h),7.27(s,1h),7.13(s, 1h),6.62(d,1h),6.49(s,2h),3.87-3.96(m,8h),3.63-3.71(m,2h),3.31-3.37(m, 1h),2.2-2.25(m,1h),1.95-2.01(m,3h),1.82-1.85(m,1h),1.50-1.58(m,1h)
[1076]
lcms:(m+h)
+
:m/z:382.19
[1077]
化合物044和045的合成方案
[1078][1079]
步骤1:叔丁基4-((三氟甲基)磺酰基)氧基)-2,3,6,7-四氢-1h-氮卓-1-羧酸酯(2) 的合成
[1080][1081]
在-78℃下,向叔丁基4-氧代氮杂-1-羧酸(1.5g,7.04mmol,1eq.)的thf(20 ml)溶液中,在氮气下滴加1n lihmds(7.7ml,7.74mmol)。将混合物搅拌20 分钟,然后添加phntf2(2.75g,7.71mmol)在thf(10ml)中的溶液。将混合物加热至0℃并搅拌3小时。将反应浓缩并用dcm稀释,通过中性氧化铝过滤并用9:1己烷/etoac洗脱产物,得到4-(((三氟甲基)磺酰基)氧基)-2,3,6,7-叔丁基四氢-1h-氮杂-1-羧酸盐(2.1g,6.08mmol,87%产率)。
[1082]
分析数据:1h nmr(400mhz,cdcl3):5.90(m,1h),3.90-3.99(m,2h), 3.51-3.60(m,2h),2.56(m,1h),1.92-1.97(m,2h),1.45(s,9h)
[1083]
步骤2:叔丁基4-(4,4,5,5-四甲基-1,3,2-二氧苯甲醛-2-基)-2,3,6,7-四氢-1h
‑ꢀ
氮杂卓-1-羧酸酯(4)的合成
[1084][1085]
在室温下,向二氧六环中的叔丁基4-(三氟甲基磺酰基)氧基)-2,3,6,7-四氢
ꢀ‑
1h-氮杂吡啶-1-羧酸盐2(1.5g,4.34mmol)的搅拌溶液中添加双(吡那克拉通)二硼隆3(1.3g,4.9mmol)和乙酸钾(1.28g,12.9mmol)。将混合物在氮气下脱气 15分钟,然后在室温下加入pdcl2(pph3)2(300mg,0.43mmol)并将混合物再脱气5分钟。将反应在80℃搅拌一夜,浓缩,用乙酸乙酯稀释并通过硅藻土垫过滤,将滤液减压浓缩得到粗品(3g),并将其用于下一步。
[1086]
步骤3:叔丁基4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮卓-1-羧酸(5)
[1087][1088]
向4-氯-6,7-二甲氧基喹唑啉(208mg,0.9mmol)在二氧六环(7ml)和水(1ml) 中的
搅拌溶液中添加叔丁基4-(4,4,5,5-四甲基-1,3,2-二氧苯甲醛-2-基)-2,3,6,7-四氢-1h-氮杂吡啶-1-羧酸盐4(600mg粗品,1.8mmol),然后添加na2co3(300mg, 2.7mmol),并用氩脱气30分钟。然后添加pdcl2(dppf)。添加dcm(76mg,0.09 mmol),并用氩气再次吹扫5分钟。将反应混合物加热至80℃持续16小时。通过tlc监测反应进程。反应混合物通过硅藻土垫过滤,滤液用水淬灭,用etoac 萃取三次,合并的有机层用盐水和水洗涤。减压浓缩有机层,得到粗品。通过 combi-flash色谱法纯化粗化合物,通过在己烷中洗脱90%etoac,得到的叔丁基 4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮卓-1-羧酸5(250mg,0.649mmol, 70%产率)为浅棕色固体。
[1089]
分析数据:1h nmr(400mhz,dmso):9.06(s,1h),7.55(s,1h),7.30-7.30 (m,1h),6.19(t,1h),4.11-4.44(m,2h),4.00-4.05(m,6h),3.69-3.74(m,2h), 2.81-2.83(m,2h),2.07-2.10(m,2h),1.48(s,9h)
[1090]
lcms:(m-h)
+
:m/z:386.2
[1091]
步骤4:6,7-二甲氧基-4-(2,3,6,7-四氢-1h-氮杂吡啶-4-基)喹唑啉盐酸盐(6)
[1092][1093]
在0℃下,向4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-阿氮平-1-羧酸叔丁酯5(100mg,0.83mmol)在1,4-二氧六环(10ml)中的搅拌溶液中缓慢添加 4.0m小时cl到1,4-二氧六环(1ml)中,并缓慢使其到室温,并搅拌2小时。反应完成后,减压除去挥发性有机物,与dcm共蒸馏三次并与乙醚一起研磨,得到的6,7-二甲氧基-4-(2,3,6,7-四氢-1h-氮杂吡啶-4-基)喹唑啉盐酸盐6(88mg,0.24 mmol,95%产率)为灰白色固体。
[1094]
分析数据:lcms:(m-h)+:m/z:286.2
[1095]
步骤5:叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮杂吡啶-1
‑ꢀ
基)磺酰基)氨基甲酸酯(8)
[1096][1097]
在室温下,向dcm中的6,7-二甲氧基-4-(2,3,6,7-四氢-1h-氮杂吡啶-4-基)喹唑啉盐酸盐6(90mg,0.28mmol)的搅拌溶液中添加n-(1-(n-(叔丁氧羰基)氨磺酰基)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物4(95mg,0.28mmol)和dipea(0.146 ml,0.841mmol)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应混合物直接吸附在二氧化硅上并转化成浆液。粗品通过combi-flash色谱法纯化,通过在己烷中洗脱90%etoac,得到的叔
丁基((4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮杂吡啶-1-基)磺酰基)氨基甲酸酯8(120mg,0258 mmol,92%产率)为灰白色固体。
[1098]
分析数据:1h nmr(400mhz,dmso):11.03(s,1h),8.98(s,1h),7.47(s, 1h),7.34(s,1h),6.15(t,1h),4.17-4.16(m,2h),3.96(s,3h),3.90(s,3h),3.57(t, 2h),2.78-2.80(m,2h),2.01-2.03(m,2h),1.38(s,9h)
[1099]
lcms:(m-h)
+
:m/z:465.2
[1100]
步骤6:4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮卓-1-磺酰胺(化合物 044)的合成
[1101][1102]
在0℃下,向二氯甲烷(5ml)中的叔丁基((4-(6,7-二甲氧基喹唑啉-4
‑ꢀ
基)-2,3,6,7-四氢-1h-氮杂吡啶-1-基)磺酰基)氨基甲酸酯8(125mg,0.26mmol)的搅拌溶液中添加tfa(1.2ml),然后在相同温度下搅拌4小时。通过tlc监测反应进程。反应完成后,用aq.nahco3中和tfa,用10%meoh/dcm萃取,干燥,减压浓缩,得到粗品。将粗化合物进行制备型hplc,得到的4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮杂-1-磺酰胺化合物044(70mg,0.192mmol, 70%产率)为灰白色固体。
[1103]
分析数据:1h nmr(400mhz,dmso):8.97(s,1h),7.52(s,1h),7.32(s,1h), 6.82(s,2h),6.16(t,1h),4.02-4.00(m,2h),3.96(s,3h),3.98(s,6h),3.51(t,2h), 2.82-2.79(m,2h),2.02-1.98(m,2h)
[1104]
lcms:(m-h)
+
:m/z:365.1
[1105]
步骤7:叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)氮杂环-1-基)磺酰基)氨基甲酸酯(9)
[1106][1107]
向叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)-2,3,6,7-四氢-1h-氮杂吡啶-1-基)磺酰基)氨基甲酸酯8(250mg,0.53mmol)在甲醇(3ml)中的搅拌溶液中添加10%钯/碳(25mg),并在室温下搅拌16小时。反应完成后,将反应混合物通过硅藻土垫过滤。减压浓缩滤液,得到的叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)氮杂环-1
‑ꢀ
基)磺酰基)氨基甲酸9(220mg,0.472mmol,87%产率)为淡黄色液体。
[1108]
分析数据:1h nmr(400mhz,dmso)δ:11.13(s,1h),8.96(s,1h),7.45(s, 1h),7.32
(s,1h),6.97(d,2h),3.96-3.95(m,6h),3.89-3.81(m,1h),3.79-3.64(m, 1h),3.58-3.32(m,3h),2.04-1.85(m,6h)。
[1109]
lcms:(m+h)
+
:m/z:467.11
[1110]
步骤8:4-(6,7-二甲氧基喹唑啉-4-基)氮杂环烷-1-磺酰胺盐酸盐(化合物045) 的合成
[1111][1112]
在0℃下,向叔丁基((4-(6,7-二甲氧基喹唑啉-4-基)氮杂环-1-基)磺酰基)氨基甲酸酯9(250mg,0.53mmol)在二氯甲烷(2.5ml)中的搅拌溶液中添加4mhcl(2.5ml)到二氧六环(2.5ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。粗反应混合物通过制备型hplc纯化,得到的4-(6,7-二甲氧基喹唑啉-4-基)氮杂-1-磺酰胺盐酸盐化合物045(25mg,0.062mmol,11%产率)为灰白色固体。
[1113]
分析数据:1h nmr(400mhz,dmso)δ:8.96(s,1h),7.44(s,1h),7.32(s, 1h),6.71(s,2h),3.95-3.96(m,6h),3.81-3.83(m,1h),3.47-3.53(m,2h),3.17-3.23 (m,1h),2.00-2.04(m,2h),1.85-1.95(m,4h)
[1114]
lcms:(m+h)
+
:m/z:367.3
[1115]
总体方案9
[1116][1117]
实施例9:n-((5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲基)磺酰胺
[1118]
步骤1:5-(6,7-二甲氧基喹唑啉-4-基)吡啶腈
[1119][1120]
在密封管中,向二氧六环(50ml)中的4-氯-6,7-二甲氧基喹唑啉1(1.5g,6.67 mmol)和水(20ml)的搅拌溶液中添加(6-氰基吡啶-3-基)硼酸(1.08g,0.72mmol) 和碳酸钠(2.12g,20.0mmol),然后将反应混合物脱气30分钟。然后,再次加入[1,1'-双(二苯基膦基)二茂铁]二氯钯(ii)二氯甲烷络合物(544mg,0.66mmol),脱气5分钟,并在100℃搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。粗品使用combi-flash柱色谱法,在二氯甲烷中洗脱 3%甲醇来纯化,得到的5-(6,7-二甲氧基喹唑啉-4-基)吡啶甲腈2(700mg,2.39 mmol,37%)为棕色固体。
[1121]
分析数据:1h nmr(400mhz,dmso)9.18(d,2h),8.51(d,1h),8.27(d, 1h),7.48(s,1h),7.23(s,1h),4.01(s,3h),3.86(s,3h)。lcms:(m+h+):m/z: 292.9
[1122]
步骤2:(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲胺
[1123][1124]
向5-(6,7-二甲氧基喹唑啉-4-基)吡啶腈2(500mg,1.7mmol)在乙酸(30ml) 中的搅拌溶液中添加10%钯/碳(300mg),并在室温下在气球氢气氛下搅拌16小时。通过tlc监测反应进程。反应完成后,使反应混合物通过硅藻土并用5%甲醇的二氯甲烷溶液(100ml)洗涤硅藻土床。减压浓缩滤液,得到的(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲胺3(500mg,1.689mmol,98%产率)为黄色固体。
[1125]
分析数据:1h nmr(400mhz,dmso)9.15(s,1h),8.97(s,1h),8.29(d, 1h),7.70(d,1h),7.45(s,1h),7.25(s,1h),4.11(brs,2h),4.00(s,3h),3.87(s,3h)。 lcms:(m+h+):m/z:297.0
[1126]
步骤3:叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲基)氨磺酰氨基甲酸酯(int-5)
[1127][1128]
在室温下,向二氯甲烷(40ml)中的(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基) 甲酰胺3(500mg,1.689mmol)的搅拌溶液中添加二异丙基乙胺(1.65ml,10.134 mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚乙基)-n-甲基甲酰胺氯化物 4(569mg,1.689mmol),允许在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在二氯甲烷中洗脱2%甲醇,在组合快速柱色谱上纯化粗化合物,得到的叔丁基(n-((5-(6,7
‑ꢀ
二甲氧基喹唑啉-4-基)吡啶-2-基)甲基)氨磺酰基)氨基甲酸(300mg,0.631mmol, 37%产率)为黄色固体。
[1129]
分析数据:1h nmr(400mhz,dmso)9.15(s,1h),8.37(s,1h),8.29(d,1h), 7.67(d,1h),7.46(s,1h),7.26(s,1h),4.37(d,2h),4.01(s,3h),3.59(s,3h),1.39(s, 9h)。lcms:(m+h+):m/z:475.9
[1130]
步骤4:n-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲基)磺酰胺(化合物047)
[1131][1132]
在室温下,向叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)甲基)氨磺酰) 氨基甲酸酯int-5(100mg,0.210mmol)在1,4-二氧六环(1.0ml)中的搅拌溶液中添加4m hcl到二氧六环(2.5ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过制备纯化粗化合物。hplc得到的n-((5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基) 甲基)磺酰胺30mg,0.08mmol,38%产率)的纯化合物(化合物47)为灰白色固体。
[1133]
分析数据:1h nmr(400mhz,dmso)9.15(s,1h),8.93(s,1h),8.28(d, 1h),7.73(d,1h),7.46(s,1h),7.30-7.27(m,2h),6.75(s,2h),4.32(d,2h),4.01(s, 3h),3.85(s,3h)。lcms:(m+h+):m/z:375.9;m.w.411.86.
[1134]
化合物046的合成方案
[1135][1136][1137]
叔丁基(5-(3-氰基-6,7-二甲氧基喹啉-4-基)吡啶-2-基)甲氨基甲酸酯(2)的合成
[1138][1139]
向4-氯-6,7-二甲氧基喹啉-3-碳腈(500mg,2.01mmol)在3:1二氧六环(20ml) 中的搅拌溶液中:在室温下添加na2co3(641mg,6.04mmol)和叔丁基 ((5-(4,4,5,5-四甲基-1,3,2-二氧苯甲醛-2-基)吡啶-2-基)甲基)氨基甲酸酯int-9(1.3g, 4.03mmol),然后将反应混合物脱气30分钟。然后再次加入[1,1'-双(二苯基膦基) 二茂铁]二氯钯(ii)(165mg,0.2mmol),脱气5分钟,并在100℃搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml) 中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。粗品经制备型 hplc法纯化,得到的叔丁基((5-(3-氰基-6,7-二甲氧基喹啉-4-基)吡啶-2-基)甲基) 氨基甲酸(2)(250mg,0.127mmol,30%)为黄色固体。
[1140]
分析数据:1h nmr(400mhz,dmso)δ9.066(s,1h),8.72(s,1h),8.07-8.09 (dd,1h),7.52-7.59(m,4h),6.86(s,1h),4.38-4.41(m,2h),4.01(s,3h),3.74(s, 3h),1.43(s,
9h)。
[1141]
lcms:(m+h
+
):m/z:421.2
[1142]
4-(6-(氨基甲基)吡啶-3-基)-6,7-二甲氧基喹啉-3-腈(3)的合成
[1143][1144]
在0℃下,向二氧六环(2ml)中的叔丁基(5-(3-氰基-6,7-二甲氧基喹啉-4-基) 吡啶-2-基)甲氨基甲酸酯2(250mg,0.127mmol)的搅拌溶液中添加4m hcl到二氧六环(4ml),然后在室温下搅拌6小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。将粗残基用乙醚洗涤,得到的4-(6-(氨基甲基)吡啶-3-基)-6,7-二甲氧基喹啉-3-甲腈(3)(150mg,0.451mmol,88%产率)为淡褐色固体。
[1145]
分析数据:1h nmr(400mhz,dmso)δ9.1(s,1h),8.89(s,1h),8.45(brs, 2h),8.19-8.22(dd,1h),7.76-7.79(dd,1h),7.61(s,1h),6.82(s,1h),4.39-4.41(m, 2h),4.02(s,3h),3.74(s,3h)。
[1146]
lcms:(m+h
+
):m/z:321.1
[1147]
叔丁基(n-((5-(3-氰基-6,7-二甲氧基喹啉-4-基)吡啶-2-基)甲基)氨磺酰基)氨基甲酸(5)的合成
[1148][1149]
在室温下,向二氯甲烷(4ml)中的4-(6-(氨基甲基)吡啶-3-基)-6,7-二甲氧基喹啉-3-碳腈(3)(200mg,0.625mmol)的搅拌溶液中添加二异丙基乙胺(0.326ml, 1.87mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)氨磺酰)吡啶-4(1h)-亚叶立胺)-n-甲基甲酰胺4(210mg,0.625mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。通过在石油醚中洗脱60%乙酸乙酯来纯化粗化合物,得到的叔丁基(n-(5-(3-氰基
ꢀ‑
6,7-二甲氧基喹啉-4-基)吡啶-2-基)甲基)氨磺酰氨基甲酸酯(5)(150mg, 0.30mmol,48%产率)为黄色固体。
[1150]
lcms:(m+h)
+
:m/z:499.97
[1151]
化合物046的制备
[1152][1153]
在室温下,向1,4-二氧六环(1.0ml)中的叔丁基(n-(5-(3-氰基-6,7-二甲氧基喹啉-4-基)吡啶-2-基)甲基)氨磺酰)氨基甲酸酯(5)(150mg,0.294mmol)的搅拌溶液中添加4m hcl到二氧六环(2.0ml)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,在减压下将有机溶剂完全蒸馏掉,得到粗化合物。粗化合物通过制备型hplc法纯化,得到的化合物046的纯化合物(85mg, 0.213mmol,66%产率)为灰白色固体。
[1154]
分析数据:1h nmr(400mhz,dmso)δ9.06(s,1h),8.71-8.72(d,1h), 8.08-8.11(dd,1h),7.76-7.78(dd,1h),7.58(s,1h),7.29-7.31(t,1h),6.85(s,1h), 6.77(s,1h),4.35(d,2h),4.0(s,3h),3.73(s,3h)。
[1155]
lcms:(m+h)
+
:m/z:400.0
[1156]
叔丁基((5-溴吡啶-2-基)甲基)氨基甲酸(6)的合成
[1157][1158]
在0℃下,向二氯甲烷(20ml)中的(5-溴吡啶-2-基)甲胺6(1g,5.34mmol) 的搅拌溶液中添加二异丙基乙胺(2.8ml,16.04mmol)和二碳酸二叔丁酯(1.28 ml,5.88mmol)。将反应混合物在室温下搅拌16小时。通过tlc监测反应进程。完成后,将反应混合物倒入冰冷的水(500ml)中并用dcm(2x100ml)萃取。用盐水溶液(200ml)洗涤合并的有机层,用硫酸钠干燥并减压浓缩,得到的((5
‑ꢀ
溴吡啶-2-基)甲基)氨基甲酸叔丁基6(1.0g,3.49mmol,66%产率)为棕色固体。
[1159]
分析数据:1h nmr(400mhz,cdcl3)δ8.6(d,1h),8.00-8.03(dd,1h),7.45(t, 1h),7.23(d,1h),4.17(d,1h),1.39(s,9h)。
[1160]
lcms:(m-boc)
+
:m/z:287.0
[1161]
中间体9的制备
[1162][1163]
在室温下,将koac(1.02g,10.48mmol)和4,4,4',4',5,5,5',5'-八甲基-2,2'-双 (1,3,2-二氧苯甲醛)(1.77g,6.99mmol)添加到二氧六环(15ml)中的叔丁基((5-溴吡啶-2-基)甲基)氨基甲酸酯6(1g,3.49mmol)的搅拌溶液中,然后在室温下将反应混合物脱气30分钟。然后再次加入[1,1'-双(二苯基膦基)二茂铁]二氯钯(ii)(285 mg,0.34mmol),脱气5分钟,并在100℃搅拌反应混合物16小时。通过tlc 监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用乙酸乙酯(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(200ml)洗涤,经硫酸钠干燥并减压浓缩。未经纯化的粗品直接使用作为下一步的原料,得到的int-9(1.1g,粗品)为白色固体。
[1164]
总体方案10:
[1165][1166]
实施例10:(n-(2-((5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)氨基)乙基)磺酰胺盐酸盐
[1167]
步骤1:5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-醇
[1168][1169]
向4-氯-6,7-二甲氧基喹唑啉1(107mg,0.48mmol)在二氧六环(7ml)和水(3 ml)中的搅拌溶液中添加(6-羟基吡啶-3-基)硼酸2(100mg,0.72mmol)和碳酸钠 (0.15g,1.44mmol)。然后将反应混合物脱气30分钟。然后加入氯[1,1'-双(二苯基膦基)二茂铁]二
氯钯(ii)二氯甲烷络合物(38mg,0.048mmol),再次将反应混合物脱气5分钟,并在110℃搅拌反应混合物16小时.通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥并减压浓缩。粗品通过100-200硅胶柱层析通过100%乙酸乙酯洗脱,得到的5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-醇3(57mg,0.201mmol,45%) 为黄色固体。
[1170]
分析数据:1h nmr(400mhz,dmso)δ11.98(brs,1h),9.02(s,1h),7.97(s, 1h),7.35(s,1h),7.38(d,2h),6.52(d,1h),3.90(s,3h),3.98(s,3h)。lcms: (m+h+):m/z:283.9
[1171]
步骤2:4-(6-氯吡啶-3-基)-6,7-二甲氧基喹唑啉
[1172][1173]
将5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-醇3(500mg,1.766mmol)和氧氯化磷(16ml)的溶液在110℃下搅拌2小时。通过tlc监测反应进程。反应完成后,将反应混合物在冷却下缓慢倒入饱和nahco3溶液(100ml)中,并用5%甲醇的二氯甲烷溶液(2x50ml)萃取。用盐水溶液(100ml)洗涤合并的有机层,用硫酸钠干燥并减压浓缩,得到的4-(6-氯吡啶-3-基)-6,7-二甲氧基喹唑啉4(430mg, 0.305mmol,86%)为灰白色固体。
[1174]
分析数据:lcms:(m+h+):m/z:301.9
[1175]
步骤3:n1-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)乙烷-1,2-二胺
[1176][1177]
将4-(6-氯吡啶-3-基)-6,7-二甲氧基喹唑啉4(300mg,0.996mmol)和乙二胺(5 ml)的溶液在100℃下搅拌5小时。通过tlc监测反应进程。反应完成后,将反应混合物减压蒸馏完全,得到粗化合物。粗化合物通过combi-flash色谱法纯化,通过在二氯甲烷中洗脱10%甲醇,得到的纯n1-(5-(6,7-二甲氧基喹唑啉-4
‑ꢀ
基)吡啶-2-基)乙烷-1,2-二胺5(130mg,0.4mmol,40%产率)化合物为浅棕色固体。
[1178]
分析数据:1h nmr(400mhz,dmso)δ9.01(s,1h),8.51(s,1h),7.91(d, 1h),7.37(s,1h),7.38(s,1h),6.65(d,1h),3.87(s,3h),3.98(s,3h),2.69-2.72(m, 4h)。lcms:(m+h+):m/z:326.0
[1179]
步骤4:叔丁基(n-(2-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)氨基)乙基)氨磺酰氨基甲酸酯
[1180][1181]
在0℃下,向n1-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基乙烷-1,2-二胺5(100 mg,0.307mmol)在二氯甲烷(8ml)中的搅拌溶液中添加二异丙基乙胺(0.1ml, 0.461mmol)和n-(1-(n-(叔丁氧羰基)氨磺酰)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺氯化物6(156mg,0.461mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,将反应混合物在减压下完全蒸馏掉,得到粗化合物。粗品通过100-200硅胶柱色谱纯化,在二氯甲烷中的3%甲醇洗脱,得到的叔丁基(n-(2-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)氨基)乙基)氨磺酰氨基)甲酸酯 7(140mg,0.277mmol,90%产率)为淡黄色固体。
[1182]
分析数据:1h nmr (400mhz,dmso)δ10.92(bs,1h),9.02(s,1h),8.52(s, 1h),7.94(d,1h),7.70(t,1h),7.38(s,2h),7.19(t,1h),6.65(d,1h),3.87(s,3h), 3.98(s,3h),3.48-3.46(m,2h),3.09-3.08(m,2h),1.38(s,9h)。lcms:(m+h+): m/z:504.9
[1183]
步骤5:(n-(2-(5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)氨基)乙基)磺胺盐酸盐(化合物048)
[1184][1185]
在0摄氏度下,向二氧六环(2ml)中的叔丁基(n-(2-(5-(6,7-二甲氧基喹唑啉
ꢀ‑
4-基)吡啶-2-基)氨基)乙基)氨磺酰)氨基甲酸酯7(110mg,0.216mmol)的搅拌溶液中将4m hcl添加到二氧六环(8ml)中,然后在室温下搅拌6小时。通过tlc 监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过制备型 hplc法纯化,得到的(n-(2-((5-(6,7-二甲氧基喹唑啉-4-基)吡啶-2-基)氨基)乙基) 磺酰胺盐酸盐(化合物048)。
[1186]
(41mg,0.101mmol,46%产率)为黄色固体。
[1187]
分析数据:1h nmr(400mhz,dmso)δ9.02(s,1h),8.53(s,1h),7.94(d, 1h),7.38(s,2h),7.18-7.10(m,1h),6.67-6.63(m,2h),6.57(s,2h),3.98(s,3h), 3.88(s,3h),3.48-3.51(m,2h),3.11-3.06(m,2h)。lcms:(m+h+):m/z:405.1
[1188]
基于实施例10的一般程序制备化合物050。
[1189][1190]
(400mhz,dmso)δ8.94(s,1h),7.43(s,1h),7.31(s,1h),6.44(s,3h),3.96 (d,6h),3.18(t,2h),2.85(dd,2h),1.85
–
1.73(m,2h),1.56
–
1.46(m,2h),1.42(d, 2h)。lcms 355.1.mw 390.88
[1191]
总体方案11:
[1192][1193][1194]
实施例11:n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)磺酰胺
[1195]
步骤1:(e)-5-(4,4,5,5-四甲基-1,3,2-二氧杂环丙烷-2-基)戊-4-烯腈
二环己基膦基-2',4',6'-三异丙基-1,1'-联苯)[2-(2'-氨基-1,1'-联苯)]钯(ii)(35mg,0.044mmol)再次使反应混合物脱气5分钟,并在50℃下搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,将反应混合物倒入水(100ml)中并通过硅藻土过滤。用含10%甲醇的二氯甲烷(100ml)洗涤硅藻土床并分离两层。有机层用盐水溶液(100ml)洗涤,经硫酸钠干燥并减压浓缩。粗品通过100-200硅胶柱色谱纯化,通过在二氯甲烷中的2%甲醇洗脱,得到的(e)
ꢀ‑
5-(6,7-二甲氧基喹唑啉-4-基)戊-4-烯腈5(150mg,0.557mmol,62%)为棕色固体。
[1208]
分析数据:1h nmr(400mhz,dmso)δ8.97(s,1h),7.61(d,2h),7.32
–ꢀ
7.22(m,2h),3.98(d,6h),2.83(t,2h),2.72
–
2.63(m,2h)。
[1209]
与相应的频哪醇硼酸酯进行相同的反应,得到以下中间体
[1210][1211]
步骤4:5-(6,7-二甲氧基喹唑啉-4-基)戊烷-1-胺
[1212][1213]
向(e)-5-(6,7-二甲氧基喹唑啉-4-基)戊-4-烯腈5(670mg,2.49mmol)在1,4
‑ꢀ
二氧六环(25ml)和水(10ml)中的搅拌溶液中添加氢氧化锂一水合物(230mg, 5.48mmol)、雷尼镍(700mg)和10%钯/碳(220mg),并在室温下在气球氢气氛下搅拌反应混合物16小时。通过tlc监测反应进程。反应完成后,反应混合物通过硅藻土过滤并用含5%甲醇的二氯甲烷(100ml)洗涤硅藻土床。滤液在减压下浓缩。粗化合物通过grace反相法纯化,通过在水中的0.1%甲酸中洗脱40%乙腈,得到的5-(6,7-二甲氧基喹唑啉-4-基)戊烷-1-胺4(200mg,0.727mmol,29%产率)为红棕色胶状液体。
[1214]
分析数据:1h nmr(400mhz,dmso)δ8.94(s,1h),8.46(s,1h),7.43(s, 1h),7.31(s,1h),3.95(s,7h),3.23
–
3.17(t,2h),2.64(t,2h),1.79(m,2h),1.51 (m,2h),1.40(m,2h)。
[1215][1216]
步骤5:叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)氨磺酰)氨基甲酸酯
[1217][1218]
在0℃下,向二氯甲烷(5ml)中的5-(6,7-二甲氧基喹唑啉-4-基)戊烷-1-胺 6(200mg,0.727mmol)的搅拌溶液中添加二异丙基乙胺(140mg,1.091mmol)和 n-(1-(n-(叔丁氧羰基)氨磺酰)吡啶-4(1h)-亚基)-n-甲基甲酰胺7(269mg,0.8 mmol),然后在室温下搅拌16小时。通过tlc监测反应进程。完成后,向反应混合物中加入水(50ml)并用二氯甲烷(2x50ml)萃取。用盐水溶液(50ml)清洗合并的有机层,用硫酸钠干燥,减压浓缩,得到粗化合物。粗品通过100-200硅胶柱色谱纯化,在二氯甲烷中的2%甲醇洗脱,得到的叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)氨磺酰基)氨基甲酸酯(200mg,0.44mmol,60%产率)为浅棕色固体。
[1219]
分析数据:1h nmr(400mhz,dmso)δ10.76(s,1h),8.93(s,1h),7.53(bs, 1h),7.42(s,1h),7.31(s,1h),3.96(s,6h),3.18(t,2h),2.89
–
2.81(m,2h),1.83
–ꢀ
1.72(m,2h),1.51(m,2h),1.39(m,11h)。
[1220][1221]
步骤6:n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)磺酰胺(化合物051)
[1222][1223]
在0℃下,向二氧六环(2ml)中的叔丁基(n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)氨磺酰)氨基甲酸酯int-5(200mg,0.44mmol)的搅拌溶液中将4m hcl添加到二氧六环(7ml)中,然后在室温下搅拌16小时。通过tlc监测反应进程。反应完成后,有机溶剂在减压下完全蒸馏掉。粗品通过制备型hplc法纯化,得到的n-(5-(6,7-二甲氧基喹唑啉-4-基)戊基)磺酰胺(50mg,0.141mmol,29%产率) 为淡黄色固体。
[1224]
分析数据:1h nmr(400mhz,dmso)δ8.94(s,1h),7.43(s,1h),7.31(s, 1h),6.44(s,3h),3.96(d,6h),3.18(t,2h),2.85(dd,2h),1.85
–
1.73(m,2h),1.56
ꢀ–
1.46(m,2h),1.42(d,2h)。
[1225][1226][1227]
体外生物学
[1228]
实施例1:enpp1测定(tmp)
[1229]
材料:
[1230]
测定缓冲液:1mm cacl2,0.2mm zncl2,50mm tris,ph 9.0
[1231]
底物:1.5mm胸苷5'-单磷酸二钠水合物(西格玛公司:t4510)
–
测定浓度: 150μm
[1232]
酶:1ng/μl重组人enpp-1蛋白(内部纯化)-测定浓度:5ng/well
[1233]
dmso
[1234]
96孔透明测定板
[1235]
协议:
[1236]
在10倍的测定缓冲液中制备药物的十点连续稀释液,最终测定浓度从10 μm、3μm、1μm、0.3μm
…
0μm开始。包含dmso的稀释液作为对照。如下设置测定板,每个孔一式两份:75μl测定缓冲液+10μlenpp1抑制剂或dmso 稀释+10μl底物+5μl酶(5ng)。将酶和底物两者添加到孔的相对侧以确保不存在相互作用,直到所有孔均具有两种组分。然后将板轻轻离心10
秒,随后在37℃下孵育45分钟。通过使用envision读板仪在405nm下测量吸光度来量化反应。使用graphpad prism8.0分析数据。
[1237]
结果如下表1所示:
[1238]
表1
[1239][1240][1241][1242][1243]
实施例2:enpp1热位移测定材料:
[1244]
重组人enpp-1蛋白(内部纯化的)
[1245]
测定缓冲液(1mm cacl2、0.2mm zncl2、50mm tris、ph 9.0)
[1246]
5000倍sypro橙(赛默飞世尔科技公司目录号s6651)
[1247]
384孔pcr板
[1248]
协议:
[1249]
方法:将每种药物制备为在测定缓冲液中的10倍溶液,并且将sypro橙在水中稀释到10倍浓度。如下在384孔pcr板中一式两份地设置孔:14μl测定缓冲液、2μlenpp1抑制剂或dmso、2μl(0.5μg)enpp1蛋白。将每个孔混合并且在冰上温育5分钟。孵育后,将2μl的sypro橙混合到每个孔中,并且随后进行温和离心。使用viia7软件运行蛋白质熔融反应,温度从25℃开始,增加0.05℃/s,最高温度为99℃。
[1250][1251]
实施例3:enpp2测定
[1252]
材料:
[1253]
测定缓冲液:10mm cacl2、5mm mgcl2、50mm tris、0.02%brij-35、ph 8.5
[1254]
底物:20mm双(对硝基苯基)磷酸钠盐(bpnpp)(西格玛公司,目录号n3002)
[1255]
酶:0.01ng/μl重组人enpp-2/自噬毒素(rhenpp-2)(研发目录号5255-en)
[1256]
dmso
[1257]
pf8380(selleck s8218)
[1258]
96孔透明测定板
[1259]
协议:
[1260]
在10倍的分析缓冲液中制备药物的八点连续稀释液,最终测定浓度从10 μm、3μm、
1μm、0.3μm
…
0μm开始。包含dmso的稀释液作为对照。按如下方法设置测定板,每个孔一式两份:81μl测定缓冲液+10μl enpp1抑制剂或二甲基亚砜+5μl底物+5μl酶(0.05ng)。将酶和底物两者添加到孔的相对侧以确保不存在相互作用,直到所有孔均具有两种组分。然后将板轻轻离心10秒,随后在37℃下孵育10分钟。通过使用envision在400nm下测量吸光度来量化反应。pf8380用作该测定的阳性对照。使用graphpad prism8.0分析数据。
[1261][1262][1263]
实施例4:基于细胞的enpp选择性测定(tmp)
[1264]
材料:
[1265]
hek293t细胞
[1266]
培养基:89%dmem、10%fbs、1%青霉素/链霉素
[1267]
转染试剂:聚乙烯亚胺支链,1mg/ml(西格玛公司:408719)
[1268]
转染培养基:opti-mem低血清培养基(赛默飞世尔科技公司:31985088)
[1269]
质粒构造:
[1270]
pcmv6空构造(原产地:ps100001)
[1271]
henpp1(原产地:rc209222)
[1272]
henpp3(基因脚本:ohu19400d)
[1273]
menpp1(原产地:mr227498)
[1274]
测定缓冲液:1mm cacl2、0.2mm zncl2、50mm tris、ph9.0
[1275]
底物:8mm胸苷5'-一磷酸二钠盐水合物(西格玛公司编号t7004-1g)
[1276]
6孔组织培养处理板
[1277]
96孔透明测定板
[1278]
协议:
[1279]
hek293t细胞以每孔5x10
5个
细胞接种在6孔组织培养处理板中。将含有7 μl转染试剂、2μg质粒构建体和200μl转染培养基的转染混合物在室温下孵育20分钟。将转染混合物逐滴添加到每个孔中,并在37℃/5%co2下孵育48小时。通过胰蛋白酶消化收集转染的细胞,裂解并测定蛋白质浓度。药物在10倍的测定缓冲液中制备,并以1μm的最终分析浓度进行测试。在加入5μl底物之前,将裂解液(3μg)与10μlenpp1抑制剂和81μl测定缓冲液在4℃下孵育2小时。最终反应在37℃下孵育45分钟,并通过使用envision读板器测量405nm 处的吸光度进行量化。将数据标准化为空构造对照。
[1280]
结果如图1所示。
[1281]
实施例5:溶解度和稳定性测定
[1282]
材料:
[1283]
pbsph7.4(目录号10010-031;来自赛默飞世尔科技公司),
[1284]
fassif(ph 6.5)、fessif(ph 5.0)和fassgf(ph 1.6)水性缓冲液(来自 biorelevant.com的目录号fff01、fasbuf01、fesbuf01、fasbuf01)
[1285]
协议:
[1286]
将每种化合物的1mg粉末与1ml缓冲液混合,制成1mg/ml的混合物。将这些样品在带有珠子的磁力搅拌器中在室温下搅拌一夜。然后将样品通过0.45 μptfe注射器过滤器。滤液在分析前用相应的缓冲液稀释。所有样品均通过紫外-可见分光光度法(赛默飞世尔科技公司,紫外分光光度计8000)对照标准进行测定。将样品保持在室温(室温),并在相应的时间点对等分试样进行紫外-可见分光光度分析以测量稳定性。
[1287]
实施例6:免疫渗透测定
[1288]
材料:
[1289]
hpac(atcc目录号:crl-2119)
[1290]
基质凝胶生长因子降低(康宁目录号:354230)
[1291]
96孔球体微孔板:ula,圆底,黑壁板(康宁目录号:10185-094)
[1292]
康宁hts transwell 96孔渗透支架,5μm(康宁目录号:3387)
[1293]
dmem,高葡萄糖,hepes,无酚红(赛默飞世尔科技公司目录号:21063045)
[1294]
人pbmc外周血单核细胞,低温放大器(龙沙公司目录号:cc-2702)
[1295]
分子探针celltracker cm dii染料(赛默飞世尔科技公司目录号:c7000)
[1296]
10倍药物
[1297]
协议:
[1298]
根据atcc指南培养hpac细胞。在实验的第一天,在含有1.5%基质凝胶的50μl培养基中,将5000个细胞接种在96孔球形微孔板中。细胞在1800rpm 下离心2分钟,然后在37℃/5%co2的平板搅拌器上低速培养72小时,使每个孔形成单个球体。孵育后,向每个相应的孔中添加150μl含有载体(二甲基亚砜) 或药物的培养基,并在37℃/5%co2下培养1小时。在孵育过程中,根据制造商的方案,对人pbmc进行计数,并用分子探针celltracker cm dii染料进行荧光染色。与药物孵育1小时后,将transwell平板轻轻放入球形平板中。然后洗涤pbmc,并将其以400000个细胞/100μl的培养基添加到每个相应的孔中。实验在37℃/5%co2下渗透48小时,使免疫细胞渗透到球体中。孵育后,移除 transwell,使用biotek cytation5为每个球体拍摄rfp荧光和亮场z叠加图像。压缩图像并评估总rfp表达。使用graphpad prism8.0分析数据。
[1299]
预示性药物组合物实施例
[1300]
如贯穿这些实施例所使用的“活性成分”涉及本发明的化合物、或其药学上可接受的盐、溶剂化物、多晶型物、水合物和立体化学异构体中的一种或更多种。本发明的化合物在片剂、悬浮液、可注射剂和软膏剂中的制剂的以下实施例是预示的。
[1301]
本发明制剂的制剂的典型实施例如下所示。各种其它剂型可以在本文中应用,如填充的明胶胶囊、液体乳液/悬浮液、软膏剂、栓剂或咀嚼片形式,根据本发明以所期望的剂量使用所公开化合物。可以使用用于制备合适的剂型的各种常规技术来制备预示药物组合物,如本文中以及标准参考文本中公开的那些预示药物组合物,例如英国和美国药典、雷明顿氏药物科学(马克出版公司)以及马丁代尔大药典(伦敦制药出版社)。此参考文献的公开内容特此通过引用并入本文。
[1302]
用于口服施用的药物组合物
[1303]
可以如下制备片剂:
[1304][1305][1306]
可替代地,每片剂使用约100mg所公开化合物、50mg乳糖(一水合物)、 50mg玉米淀粉(天然)、10mg聚乙烯吡咯烷酮(pvp 25)(例如,来自德国路德维希港的巴斯夫(basf))和2mg硬脂酸镁。将活性组分、乳糖和淀粉的混合物与 pvp在水中的5%溶液(m/m)一起制成颗粒。干燥后,将颗粒与硬脂酸镁混合5 分钟。使用常规压片机(例如,片剂形式:直径8mm,曲
率半径12mm)模制这种混合物。所施加的模制力通常为约15kn。
[1307]
可替代地,所公开化合物可以以调配用于口服使用的悬浮液的形式施用。例如,在搅拌下将约100-5000mg所期望的所公开化合物、1000mg乙醇(96%)、 400mg黄原胶和99g水合并。可以通过10ml的口服悬浮液提供约10-500mg 的所期望的所公开化合物的单一剂量。
[1308]
在这些实施例中,活性成分可以被同一量的任何根据本发明的化合物,具体地同一量的任何例示化合物替代。在一些情况下,可能期望使用胶囊,例如填充的明胶胶囊代替片剂形式。片剂或胶囊的选择将部分地取决于所使用的特定的所公开化合物的物理化学特性。
[1309]
用于制备口服制剂的替代性有用载体的实施例是乳糖、蔗糖、淀粉、滑石粉、硬脂酸镁、结晶纤维素、甲基纤维素、羟丙基纤维素、羟丙基甲基纤维素、羧甲基纤维素、甘油、海藻酸钠、阿拉伯树胶等。这些替代性载体可以取代以上给出的那些载体,如所期望的溶解、吸收和制造特性所需的。
[1310]
根据在合适的动物模型,例如大鼠和至少一种非啮齿类动物物种中获得的毒理学和药代动力学数据两者确定每片剂用于人类使用的药物组合物中的所公开化合物的量,并且基于人类临床试验数据进行调整。例如,所公开化合物以每片剂剂量单位约10到1000mg的水平存在可能是适当的。
[1311]
注射用药物组合物
[1312]
可以如下制备肠胃外组合物:
[1313][1314]
*在活性成分的量和活性成分的形式,例如活性成分的特定盐形式的背景下,根据需要调节量以维持生理ph。
[1315]
可替代地,可以使用用于静脉内注射的药物组合物,其中组合物包括约 100-5000mg的所公开化合物、15g聚乙二醇400和250g盐水溶液,其中任选地高达约15%cremophorel、以及任选地高达15%乙醇以及任选地高达2当量的药学上合适的酸(如柠檬酸或盐酸)被使用。这种可注射组合物的制备可以如下完成:将所公开化合物和聚乙二醇400在搅拌下溶解于水中。将溶液无菌过滤(孔径0.22μm)并且在无菌条件下填充到加热灭菌的输注瓶中。输注瓶用橡胶密封件密封。
[1316]
在另外的实施例中,可以使用用于静脉内注射的药物组合物,其中组合物包括约10-500mg的所公开化合物、标准盐水溶液,任选地具有高达按重量计15%的cremophor el、
以及任选地高达按重量计15%的乙醇以及任选地高达2当量药学上合适的酸,如柠檬酸或盐酸。制备可以如下完成:将所期望的所公开化合物在搅拌下溶解于盐水溶液中。任选地添加cremophor el、乙醇或酸。将溶液无菌过滤(孔径0.22μm)并且在无菌条件下填充到加热灭菌的输注瓶中。输注瓶用橡胶密封件密封。
[1317]
在这个实施例中,活性成分可以被同一量的任何根据本发明的化合物,具体地同一量的任何例示化合物替代。
[1318]
根据在合适的动物模型,例如大鼠和至少一种非啮齿类动物物种中获得的毒理学和药代动力学数据两者确定每安瓿用于人类使用的药物组合物中的所公开化合物的量,并且基于人类临床试验数据进行调整。例如,所公开化合物以每片剂剂量单位约10到1000mg的水平存在可能是适当的。
[1319]
适用于肠胃外制剂的载体是例如水、生理盐水溶液等,其可以与用作增溶剂或ph调节剂的三(羟甲基)氨基甲烷、碳酸钠、氢氧化钠等一起使用。肠胃外制剂优选地含有50到1000mg的所公开化合物每剂量单位。
[1320]
实施例7
[1321]
体内方法
[1322]
研究i:测定雄性sprague-dawley大鼠静脉内和口服施用后015-hcl的生物利用度。
[1323]
通过静脉(iv)和口服(po)施用途径分别以2mg/kg和10mg/kg的剂量给药化合物015-hcl。在给药后24小时内采集血样,并通过lc-ms/ms测定015-hcl 的血液浓度。使用phoenix winnonlin(v8.0)软件确定药代动力学参数。
[1324]
研究ii:化合物015-hcl在c57bl/6小鼠pan02(小鼠胰腺导管腺癌模型) 同基因模型中的抗肿瘤作用
[1325]
实验设计:
[1326]
动物:雌性c57bl/6(查尔斯河实验室4-6周龄)。
[1327]
pan02细胞在含有10%胎牛血清的dmem细胞培养基中增殖。在对数生长期收获细胞并且将其皮下(1
×
106)植入小鼠的下腹中。每天监测肿瘤生长,肿瘤达到80至100mm3后,将小鼠随机分为每组10只动物的组,并按表2所示进行治疗。当肿瘤达到约2000mm3或治疗方案完成或20%体重减轻或发生溃疡和坏死时,对动物实施安乐死。终止后,收集肿瘤样本和血液,并分析其生物标志物。
[1328]
表2:研究设计、组数、途径和剂量
[1329]
[1330][1331]
研究iii:化合物015-hcl在c57bl/6小鼠mc38(结肠腺癌小鼠模型)同基因模型中的抗肿瘤作用
[1332]
实验设计:
[1333]
动物:雌性c57bl/6(查尔斯河实验室4-6周龄)。
[1334]
mc38细胞在含有10%胎牛血清的rpmi细胞培养基中增殖。在对数生长期收获细胞并皮下(2x105)植入小鼠侧腹。每天监测肿瘤生长,肿瘤达到约100mm3后,将小鼠随机分为每组10只动物。在第17天,用015-hcl化合物或载体处理小鼠,如表3所示。在第18天,第2、5和6组在肿瘤部位接受了单次10gy 的局灶辐射照射。当肿瘤达到2000mm3左右或治疗方案完成或体重减轻20%,或出现溃疡和坏死时,对动物实施安乐死。终止后,收集肿瘤样品和血液并分析生物标志物。
[1335]
表3:研究设计、组数、途径和剂量
[1336][1337][1338]
对于本领域的技术人员显而易见的是,在不脱离本发明的范围或精神的情况下,可以在本发明中进行各种修改和变化。本领域技术人员通过考虑在本文所公开的本发明的说明书和实践将明白本发明的其它实施方式。所打算的是说明书和各实施例旨在被认为仅是示例性的,而本发明的实际范围和精神由随附权利要求书来指示。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1