作为DHODH抑制剂的化合物的制作方法
本发明总体涉及作为二氢乳清酸脱氢酶(dhodh)活性的抑制剂的化合物。更具体地,本发明进一步涉及所述化合物的制备及其在用于治疗与dhodh活性相关的各种疾病、病症和障碍的药物组合物中的用途。
背景技术:
1、在细胞核和线粒体中,嘧啶是生物大分子(包括dna、rna、糖蛋白和磷脂)的生物合成所需的,并通过磷酸二酯桥连接到双链dna中的嘌呤核苷酸(loeffler,m.等人,encyc.biol.chem.,2004,3,600–605.)大多数生物体内嘧啶的合成有两种途径:补救途径和从小代谢物的从头合成。对于正常分化的细胞,补救途径是嘧啶核苷酸的主要来源。为了满足对核酸前体和其他细胞组分增长的需求,激活的t细胞和其他快速增殖的细胞很大程度上依赖于从头合成。(fairbanks,l.d.等人,j.biol.chem.,1995,270,29682-29689.)二氢乳清酸脱氢酶(dhodh)是一种位于线粒体中的黄素依赖性酶,并负责第4步嘧啶合成。dhodh催化dho转化为oro,这代表嘧啶从头生物合成中的限速步骤(loffler m.等人,molcell biochem.1997,174,125-129)。dhodh还催化黄素单核苷酸(fmn)还原为二氢黄素单核苷酸(fmnh2),这包括氧化还原对的两个半反应。dhodh使用的共底物电子受体在不同的生物体中有所不同。在人dhodh中,黄素辅因子是fmn,泛醌(coq)是第二底物。来自高等真核生物的dhodh展现出双位点乒乓机制,其中fmn作为电子转移的中间体。(hansen,m.,等人,protein sci.,2004,13,1031-1042.hurt,d.e.等人,acta crystallogr d biolcrystallogr.2006,62,312-323.)
2、由于dhodh参与嘧啶生物合成和线粒体电子传递链过程,并被视为这两个过程中的中心酶,抑制dhodh会减少细胞中的细胞内嘧啶核苷酸库。通过抑制dhodh而降低嘧啶核苷酸水平能阻止异常细胞增殖,因为快速细胞增殖通常依赖于嘧啶核苷酸的从头合成,这使得dhodh成为治疗癌症、关节炎和疟疾的生物学和临床应用的有吸引力的靶标。
3、dhodh抑制剂已被证明可有效治疗许多疾病,包括细菌和病毒感染、寄生虫病(即疟疾)、自身免疫病和癌症(reis,r,等人,arch.biochem.biophys.2017,632,175-191)。dhodh的抑制会耗尽细胞内嘧啶核苷酸库并导致细胞周期停滞在s期、对当前化学疗法敏感、神经嵴细胞分化和急性髓系白血病(aml)(koundinya,m.,等人,cell chem biol,2018,25,705-717)。因此,dhodh抑制剂具有作为单一疗法或组合疗法的一部分用于癌症治疗的潜力。
4、dhodh与癌症的相关性在近六十年前就得到了认可,当时smith等人指出dhodh在白血病细胞中活性升高(smith l.h.,等人,blood,1960,15,360-369;),最近的报道重新审视了dhodh抑制与细胞中的抗增殖作用之间的联系,发现dhodh抑制与大多数癌细胞系中的细胞生长减少相关(aguirre a.j.,等人,cancer discov,2016,6,914-929),所述细胞如来自结直肠癌的hct-116、来自白血病的jurkat和来自淋巴瘤的hut-78。
5、除了在癌症治疗中的应用外,dhodh抑制剂还表现出广谱抗病毒活性,这主要归因于病毒基因组复制所必需的核苷的耗尽(hoffmann h.h.,等人,proc natl acad sci usa2011,108,15366-15371;wachsman m,等人,antivir chem chemother 1996,40,434-466;chenung n.n.,等人,j gen virol.2017,98,946-954)。几项寻找宿主靶向抗病毒(hta)药物的独立研究共同得到靶向宿主嘧啶合成途径以抑制病毒感染的化合物,这表明病毒的复制广泛地依赖于宿主嘧啶合成(chung,d.h.,等人,antimicrob.agents chemother.2016,60,4552-4562)。已证实靶向dhodh的cmp1和fk778可抑制rag-/-小鼠中的dna病毒(cmv)复制(marschall,m.,等人,antiviral res.2013,100,640-648。zeng,h.,等人,transplantation2005,79,17-22)。最近发现,dhodh的两种代表性抑制剂s312和s416对多种rna病毒表现出广谱抗病毒作用,包括甲型流感病毒、寨卡病毒、埃博拉病毒和sars-cov-2(xiong r.等人,biorxiv preprint 2020,https://doi.org/10.1101/2020.03.11.983056)。
6、第一代dhodh抑制剂(如来氟米特)被开发为免疫调节剂,用于类风湿性关节炎的症状的治疗。然而,早期dhodh抑制剂的弱活性和非特异性被怀疑是在人中缺乏功效和临床挫败的原因。最近,更多的证据使得人们对dhodh机制研究和临床应用重新产生了兴趣。因此非常需要开发新一代dhodh抑制剂。
技术实现思路
1、本文描述了可用于抑制dhodh的化合物及其药学上可接受的盐、立体异构体、前药或溶剂化物。还提供了包括所述化合物的组合物,以及使用和制备所述化合物的方法。本文提供的化合物可用于治疗由dhodh介导的疾病、病症或障碍。
2、在第一方面,提供了式(i)的化合物:
3、
4、或其药学上可接受的盐、立体异构体、前药或溶剂化物,其中:
5、x和z独立地是n或c;
6、y选自n和cr7;
7、其中当x是n、z是c时,是单键,是双键;
8、当x是c、z是n时,是双键,是单键;
9、r1选自
10、c1-c8烷基;
11、c2-c8卤代烷基;
12、任选地被1-6个卤素原子或选自羟基和苯基的基团取代的c3-c8环烷基,其中所述苯基取代基任选地被1-4个卤素原子或选自c1-c3烷基、c1-c4卤代烷基、c1-c3烷氧基、cn和羟基的基团取代;
13、被单环或二环杂芳基取代的c3-c6烷基;
14、(c2-c6羟基烷基)-o-(c2-c6烷基);
15、(c3-c6烷基)-n(r7)(r8);
16、(c3-c8环烷基)-n(r7)(r8);
17、(c3-c6-烷基)-c(=o)n(r7)(r8);
18、4-7元杂环烷基,其中所述4-7元杂环烷基任选地被一个或两个独立地选自以下的取代基取代:c1-c3烷基、5至6元杂芳基、-c(=o)o(c1-c4烷基)、-c(=o)(c1-c3-烷基)、-c(=o)(c3-c6-环烷基)、-s(=o)2(c1-c6-烷基)和氧代基(=o);
19、任选地被一个、两个、三个、四个或五个取代基取代的苯基,其中每个取代基独立地选自卤素、c1-c6烷基、c3-c8环烷基、c1-c6卤代烷基、c2-c6-烯基、c2-c6炔基、芳基、-(c1-c6烷基)-芳基、-芳基-(c1-c6烷基)、羟基、氰基、c1-c6羟基烷基、c1-c4烷氧基、-o(c2-c6烯基)、c1-c6卤代烷氧基、c3-c8环烷氧基、芳基、-o-芳基、氰基、-c(=o)or6、-c(=o)n(r7)(r8)、-n(r7)(r8)、-(c1-c6烷基)-n(r7)(r8)、-(c1-c6烷基)-c(=o)or6、-(c1-c6烷基)-c(=o)n(r7)(r8)、-o-c(=o)-(c1-c6烷基)、-sh、-s-(c1-c6烷基)、-s-(c2-c6烯基)、-s(=o)2n(r7)(r8)、-s(=o)2(c1-c6烷基)、
20、-s(=o)2-(c2-c6烯基)、-s(=o)(=nr11)(c1-c3烷基)、-n(o)2、-p(=o)(c1-c3烷基)2;二环芳基和5-10元杂芳基,其中所述二环芳基和所述5-10元杂芳基任选地被一个、两个或三个取代基取代,其中每个取代基独立地是卤素原子或选自以下的基团:c1-c6烷基、c3-c8环烷基、c1-c6卤代烷基、c2-c6-烯基、c2-c6炔基、芳基、-(c1-c6烷基)-芳基、-芳基-(c1-c6烷基)、羟基、氰基、c1-c6羟基烷基、c1-c4-烷氧基、-o(c2-c6烯基)、c1-c6-卤代烷氧基、c3-c8-环烷氧基、芳基、-o-芳基、氰基、-c(=o)or6、-c(=o)n(r7)(r8)、-n(r7)(r8)、-(c1-c6-烷基)-n(r7)(r8)、-(c1-c6-烷基)-c(=o)or6、-(c1-c6-烷基)-c(=o)n(r7)(r8)、-o-c(=o)-(c1-c6-烷基)、-s-(c1-c6烷基)、-s-(c2-c6-烯基)、-s(=o)2n(r7)(r8)、-s(=o)2(c1-c6-烷基)、-s(=o)2-(c2-c6烯基)、-s(=o)(=nr11)(c1-c3烷基)、-n(o)2、-p(=o)(c1-c3-烷基)2;
21、r2选自氢、d、cn和卤素;
22、r3选自卤素、c1-c6烷基、c3-c8环烷基、c1-c6卤代烷基、c1-c6羟基烷基、(c1-c3烷氧基)-(c1-c6烷基)、c2-c6烯基、c2-c6炔基、c1-c6烷氧基、c1-c6烷基硫烷基、(c1-c6烷基)-n(r7)(r8)、-n(r7)(r8)、-c(=o)or6、-c(=o)n(r7)(r8)和s(=o)(=nr11)(c1-c3烷基);
23、r4是氢或选自c1-c6烷基、c2-c6亚烷基、c3-c8环烷基、c2-c6卤代烷基、c2-c6羟基烷基和(c2-c6烷基)-n(r7)(r8),其中所述c1-c6烷基任选地被选自c3-c8环烷基和苯基的基团取代,其中所述苯基任选地被一个、两个或三个取代基取代,其中每个取代基独立地选自卤素、c1-c3烷基、c1-c4卤代烷基、c1-c3烷氧基和羟基;
24、r5选自c1-c6烷基、c3-c8环烷基、c1-c6卤代烷基、c1-c6羟基烷基、c2-c6烯基、c2-c6炔基、c4-c8环烯基、(c1-c6烷基)-n(r7)(r8)、-(c1-c6烷基)-(4至7元含氮杂环烷基)和苯基,其中所述c1-c6烷基任选地被c3-c8环烷基或nr7r8取代,所述4至7元含氮杂环烷基任选地被经由所述杂环烷基的碳原子连接到所述4至7元含氮杂环烷基的c1-c3烷基取代,并且所述苯基被1-4个卤素原子或c1-c3烷基、c1-c4卤代烷基、c1-c3烷氧基和羟基取代;
25、r6是氢或选自c1-c6烷基和苄基;
26、r7和r8独立地是氢或选自c1-c6烷基、c2-c6羟基烷基、(c2-c6烷基)-n(r9)(r10)和c3-c6环烷基,或r7和r8连同它们所附接的氮一起表示含氮的4至7元杂环烷基,其中所述4至7元含氮杂环烷基任选地被c1-c3烷基、-s(=o)2(c1-c3烷基)和-c(=o)o(c1-c4烷基)取代;
27、r9和r10独立地是氢或c1-c3烷基,或r9和r10连同它们所附接的氮一起表示含氮的4至7元杂环烷基;
28、r11是氢、氰基或c(=o)(c1-c3卤代烷基)。
29、在一些实施方案中,提供了式(i)的化合物,或其药学上可接受的盐、立体异构体、前药或溶剂化物,其中y是n,x是c,z是n,是双键,是单键。
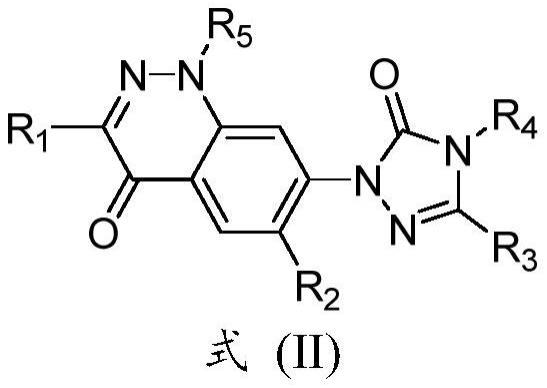
30、在第二和优选的方面,提供了一种式(ii)的化合物:
31、
32、或其药学上可接受的盐、立体异构体、前药或溶剂化物,其中r1、r2、r3、r4和r5是如本文对式(i)所公开的。
33、在另一方面,提供了一种用于治疗或预防dhodh介导的疾病、病症或障碍的方法,所述方法包括向有需要的受试者施用治疗有效量的式(i)或式(ii)的化合物或其药学上可接受的盐、立体异构体或溶剂化物。
34、还提供了药物组合物,所述药物组合物包含:(i)式(i)或式(ii)的化合物,或其药学上可接受的盐、立体异构体或溶剂化物,以及(ii)一种或多种药学上可接受的载体或赋形剂。还提供了包含式(i)或式(ii)的化合物或其药学上可接受的盐、立体异构体或溶剂化物以及任选地使用说明书的试剂盒。
35、还提供了式(i)或式(ii)的化合物或其药学上可接受的盐、立体异构体或溶剂化物作为药物的用途。还提供了如本文详述的化合物或其药学上可接受的盐、立体异构体或溶剂化物,用于制造用于治疗或预防dhodh介导的疾病、病症或障碍(如病毒感染、癌症、炎性障碍等)的药物。
- 还没有人留言评论。精彩留言会获得点赞!