用于核酸检测和疾病诊断的基于质谱的方法和试剂盒与流程
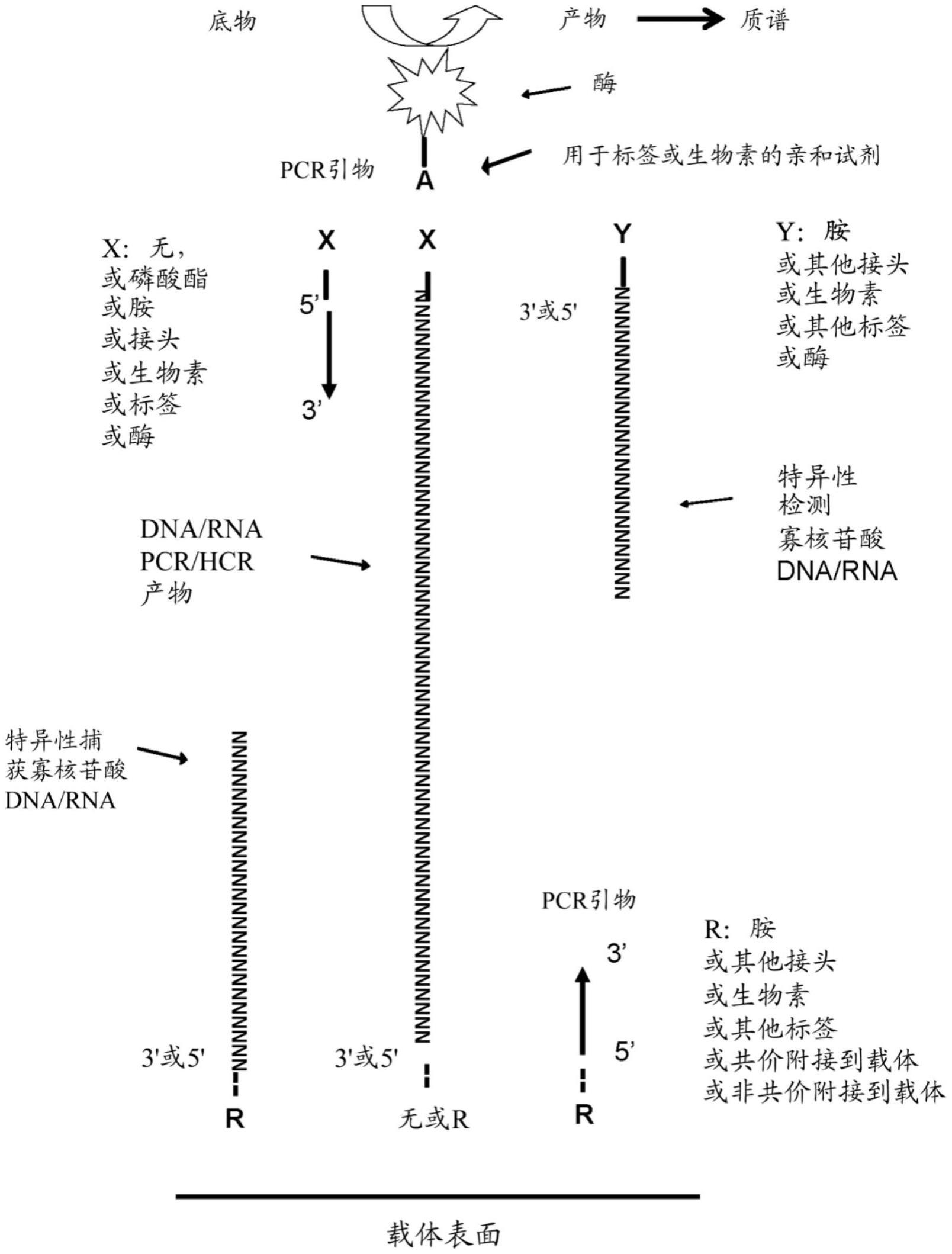
本公开涉及用于使用质谱来检测和测量靶核酸的方法和试剂盒。此外,本公开涉及用于疾病诊断的方法和试剂盒。引言准确检测和定量生物分子的能力在包括基础生物化学研究、诊断和治疗医学以及水和食品安全的多个领域中是非常重要的。处于目前方法检测的边缘处的许多潜在的诊断dna分子和治疗性蛋白质需要被绝对定量。通过半定量“计数”方法(诸如聚合酶链反应(pcr)扩增和聚苯乙烯寡聚合成微珠上的dna测序)发现的生物学上重要的核酸已揭示了重要的分子(consortium,2011),这些分子需要通过线性和高斯型杂交测定与标准品一起被绝对定量。目前的技术(诸如pcr)在测定时无法定量处于仄摩尔(10-21)至幺摩尔(10-24)量的这些水平的分子(rutledge,2003)。pcr(chin,2013)已被用于检测小至单个聚合酶模板,但这是非线性的,可能显示假阴性结果,具有较大的定量误差,并且从pcr反应中提取绝对定量的数学程序令人望而生畏(rutledge,2003)。通过pcr分析hiv和其他动物病毒具有显著的假阴性率(xie,2020;xiao,2020)。据报道,杂交和杂交链反应具有宽泛的灵敏度值范围(basiri,2020;santhanam,2020;doddapaneni,2020;jiao,2020;vermisoglou,2020)。基于定量dna的测定在固体载体上的近期应用可能已达到皮摩尔(pm)浓度范围,或者使用荧光(其使用宽吸收范围)、使用本质上不是线性和高斯型的电化学检测或tirf,或者使用通过pcr或hcr进行多轮扩增然后进行酶扩增的方案,该酶扩增可能显示误差倍增(xu,2016)shi,guo,xiong和/或超灵敏的参照物。相反,质谱更特定于单个质荷比而不是广谱,质谱本质上是线性和高斯型的,并且可用一轮酶扩增来扩增以达到pm或更低的浓度范围。荧光的全内反射(tirf)可用于dna序列中核苷酸的定性检测(vandamme,1995)。然而,该信号是非线性的,使得该校准可能输出1000倍(tobos,2019;tangemann,1995),并且依赖于定性数据的集合,这妨碍了安全检测限的计算(rissin,2010)。来自tirf的定量具有实际限制性,并且最近显示提供与使用辣根过氧化物酶(hrp)的酶扩增的那些结果类似的结果(li,2017)。质谱是一种线性和高斯型分析技术(razumienko,2008;bowden,2012),该技术检测100皮摩尔浓度(100pm)的腺苷,其中1微升注射(1μl)相当于在酶扩增之前柱上的100阿摩尔(100amol)(florentinus,2011;onisko,2007)。液相色谱电喷雾电离串联质谱(lc-esi-ms/ms)与其他方法相比具有一些有效优点:无需免疫或酶扩增即可直接检测血液中的蛋白质到ng/ml水平(munge,2005)。免疫基质辅助激光解吸/电离(maldi)直接分析蛋白质或肽的免疫复合物(li,2017),但对dna并不适用。此外,其信号不受益于酶扩增,并且仅达到ng/ml灵敏度。类似地,液相色谱电感耦合等离子体质谱(lc-icp-ms)通常可达到与elisa的现有检测限类似的ng/ml水平(shukla,2013)。据报道,现有的电化学方法达到幺摩尔范围。然而,该信号本质上不是线性或高斯型的(saiki,1985;rissin,2010)。uv/vis检测不如质谱分析法灵敏或特异;但酶扩增和uv/vis检测的组合有效地提高了uv/vis分析的灵敏度。通过碱性磷酸酶(ap)、dna聚合酶、辣根过氧化物酶或荧光素酶进行的酶扩增的使用已经提高了诸如uv-vis、ecl或荧光检测等方法的有用灵敏度(ronaghi,1996;chen,1994;florentinus-mefailoski,2014;walt,2013;munge,2005;saiki,1985;sun,2006;shukla,2013;chin,2013;tobos,2019;vandamme,1995;tangemann,1995;tucholska,2009;li,2017;razumienko,2008;bowden,2012;florentinus-mefailoski,2015;florentinus,2011;onisko,2007)。使用酶联免疫质谱测定(elimsa),蛋白质和抗体先前已在聚苯乙烯载体上使用含脱氧胆酸盐或n-辛基葡糖苷修饰的且lc-esi-ms兼容的蛋白质相互作用缓冲液的96孔板进行绝对定量(florentinus-mefailoski,2014;florentinus-mefailoski,2016;florentinus-mefailoski,2014;florentinus-mefailoski,2015)。elimsa测定已在美国专利号9,964,538中有所描述。与达到纳克量的蛋白质的传统比色酶联免疫吸附测定(elisa)的直接测量相比,elimsa使用碱性磷酸酶链霉亲和素(apsa)酶缀合物对蛋白质的检测已达到皮克灵敏度,可检测到50飞克(florentinus-mefailoski,2015)。使用apsa酶缀合物对前列腺特异性抗原(psa)和抗体的检测在正相二氧化硅固定相上达到高幺摩尔范围(florentinus-mefailoski,2014;florentinus-mefailoski,2015;florentinus-mefailoski,2016)。通过elimsa进行的蛋白检测是盲测的,以显示在高浓度下与商业荧光和ecl系统一致的结果,但是更加灵敏并且继续显示远低于1ng/ml(飞摩尔范围)的线性定量(florentinus-mefailoski,2015)。通过质谱对核酸进行定量可能是困难的。例如,通常用于核酸结合、杂交和反应的缓冲液含有盐,诸如nacl,以促进核酸相互作用。然而,无机盐诸如nacl不能容易地用于质谱测量。因此,需要用于对核酸进行检测和定量的线性和高斯型测定,这些测定在低浓度下是灵敏的,例如其中核酸以飞摩尔至阿摩尔浓度的范围存在,并且/或者优选与ms兼容。
背景技术:
技术实现思路
1、目前研究表明,来自例如生物样品或pcr反应产物的低浓度的靶核酸分子可被灵敏地且特异性地检测和定量。本文所述的方法包括:将选择性捕获和/或检测寡核苷酸探针的使用与报道酶(诸如碱性磷酸酶(ap))的酶活性的测量相结合进行扩增以通过质谱(ms)方法进行检测。此外,研究表明,当pcr反应的至少一个引物用二级靶部分诸如生物素进行官能化时,pcr产物可用报道酶检测探针直接检测和定量,该报道酶检测探针与该二级靶部分结合,并且该报道酶检测探针具有放大pcr产物的存在以通过ms检测的酶活性。
2、此外,研究表明,挥发性缓冲液可用于替代一种或多种缓冲液中的盐(诸如nacl),以使ms分析中的残余盐最小化。
3、本公开的方法可用作具有选择性的且灵敏的诊断方法。
4、因此,在一个方面,本公开包括一种检测靶核酸分子的方法,该方法包括a.
5、i.在第一结合溶液中孵育样品与捕获寡核苷酸探针,该样品假定包含该靶核酸分子,该捕获寡核苷酸探针包含与该靶核酸分子互补的序列,并且该捕获寡核苷酸探针附接到固相,任选地其中该固相通过接头附接到该捕获寡核苷酸探针;或者
6、ii.在第一结合溶液中孵育样品与固相,该样品假定包含该靶核酸分子,以将所述样品/靶核酸分子附接到所述固相,任选地其中该固相通过接头附接到该样品/靶核酸分子;
7、b.在形成靶:检测探针复合物的条件下,在第二结合溶液中使任何靶核酸分子与检测寡核苷酸探针结合;
8、c.在形成靶:检测探针:酶复合物的条件下,在第三挥发性结合溶液中孵育任何靶:检测探针复合物与报道酶检测探针,该第三挥发性结合溶液基本上不含无机盐,诸如nacl;
9、d.用洗涤溶液洗涤固相,以除去任何未结合的报道酶检测探针;
10、e.在底物反应溶液中孵育任何靶:检测探针:酶复合物与报道酶检测探针底物,以产生一种或多种可电离产物;以及
11、f.使用质谱(ms)检测该一种或多种可电离产物中的至少一种可电离产物,
12、其中
13、i.第一结合溶液、第二结合溶液和第三结合溶液中的至少第三结合溶液基本上不含无机盐;
14、ii.洗涤溶液基本上不含无机盐;
15、iii.该方法还包括在任选的步骤d)和步骤e)之前交联任何靶:检测探针:酶复合物的组分和捕获寡核苷酸探针;并且/或者
16、iv.该方法还包括在使用ms检测之前分离一种或多种可电离产物;并且
17、其中对一种或多种可电离产物中的至少一种可电离产物的检测指示样品包含靶核酸分子。
18、该检测寡核苷酸探针可以是检测寡核苷酸引物。在这种情况下,该步骤包括在扩增溶液中用检测寡核苷酸引物扩增靶核酸分子,并且在形成靶:检测探针复合物的条件下,在第二结合溶液中使任何经扩增的靶与该检测寡核苷酸探针结合。
19、在另一个方面,本公开包括一种定量样品中靶核酸分子的量的方法,该方法包括以下步骤:
20、a.根据本公开的方法检测靶核酸分子;以及
21、b.基于通过质谱检测的可电离产物中的一种或多种可电离产物的信号的强度来定量样品中靶核酸分子的量。
22、在另一个方面,本公开包括一种检测靶核酸分子的方法,该方法包括
23、用经修饰的引物和第二引物对推定包含靶核酸分子的测试样品进行核酸扩增,诸如聚合酶链反应(pcr)或杂交链反应(hcr)或滚环反应或其他核酸反应,以获得经扩增的核酸产物,即任选的pcr产物,该经扩增的核酸产物包含该经修饰的引物,该经修饰的引物用二级靶部分或报道酶进行官能化;
24、分离该经扩增的核酸产物与任何未反应的经修饰的引物;
25、当该经修饰的引物用该二级靶部分进行官能化时,在形成经扩增的核酸产物:报道酶复合物的条件下,在第一结合溶液中孵育该经扩增的核酸产物与报道酶检测探针,并用洗涤溶液除去任何未结合的报道酶检测探针,该报道酶检测探针包含二级靶结合部分和报道酶;
26、在底物反应溶液中孵育该经扩增的核酸产物或该经扩增的核酸产物:报道酶复合物与报道酶底物,以产生一种或多种可电离产物;以及
27、使用质谱(ms)检测该一种或多种可电离产物,
28、其中当经修饰的引物是正向引物时,第二引物是反向引物,并且其中当经修饰的引物是反向引物时,第二引物是正向引物。
29、在另一个方面,本公开包括一种定量测试样品中靶核酸分子的量的方法,该方法包括以下步骤:
30、a.根据检测本公开的靶核酸分子的方法检测靶核酸分子;以及
31、b.基于通过质谱检测的可电离产物中的一种或多种可电离产物的信号的强度来定量测试样品中靶核酸分子的量。
32、在另一个方面,本公开包括一种检测hiv的方法,该方法包括检测本公开的靶核酸分子的方法,其中该靶核酸分子是hiv核酸分子。
33、在另一个方面,本公开包括一种检测sars-cov2的方法,该方法包括检测本公开的靶核酸分子的方法,其中该靶核酸分子是sars-cov2核酸分子。
34、在另一个方面,本公开包括一种试剂盒,该试剂盒包括:
35、i.捕获寡核苷酸探针,该捕获寡核苷酸探针任选地通过接头与固相任选地结合;
36、ii.结合溶液,该结合溶液包含挥发性缓冲液并且基本上不含nacl,或者包含交联剂;
37、iii.检测寡核苷酸探针,该检测寡核苷酸探针包含寡核苷酸和二级靶部分;
38、iv.报道酶检测探针,该报道酶检测探针包含报道酶和能够结合该二级靶部分的二级靶结合部分;和/或
39、v.以下中的一者或多者:如本文所述的底物、固相、标准品,即任选的产物离子标准品,该标准品任选地用于制备标准曲线或调整校准物;第二结合溶液、第三结合溶液、底物反应溶液、电离溶液、淬灭溶液,即任选的第二结合溶液、检测探针溶液、底物反应溶液、淬灭溶液、电离溶液。
40、在另一个方面,本方面包括一种试剂盒,该试剂盒包括:
41、i.经修饰的引物,该经修饰的引物用二级靶部分或报道酶进行官能化;
42、ii.第二引物;
43、iii.报道酶检测探针,当该经修饰的引物用该二级靶部分进行官能化时,该报道酶检测探针包含报道酶和能够结合该二级靶部分的二级靶结合部分;和
44、iv.以下中的一者或多者:如本文所述的底物、固相、标准品,即任选的产物离子标准品,该标准品任选地用于制备标准曲线或调整校准物;结合溶液、第二结合溶液、洗涤溶液、底物反应溶液、电离溶液、淬灭溶液,即任选的结合溶液、第二结合溶液、检测探针溶液、底物反应溶液、淬灭溶液、电离溶液,
45、其中当经修饰的引物是正向引物时,第二引物是反向引物,并且当经修饰的引物是反向引物时,第二引物是正向引物。
46、在另一个方面,本公开包括一种序列选自seq id 2至37的核酸。
47、根据以下详细描述,本公开的其他特征和优点将变得显而易见。然而,应当理解,详细描述和具体实施例在指示本公开的优选实施方案时仅以举例说明的方式给出,因为根据该详细描述,在本公开的实质和范围内的各种变化和修改对于本领域技术人员来说将变得显而易见。
- 还没有人留言评论。精彩留言会获得点赞!