一种新型脂肪酶AjLip970及其应用
一种新型脂肪酶ajlip970及其应用
技术领域
1.本发明涉及基因工程和酶工程领域,涉及一种具有高催化活性脂肪酶功能的基因。
背景技术:
2.脂肪酶具有广泛的工业用途,在洗涤、制革、医药、功能性油脂生产、及生物柴油方面有极大的应用价值和广阔的前景。微生物脂肪酶因其ph和底物适应范围大等优点使得它占据了脂肪酶市场的绝大部分,2018年微生物脂肪酶市场使用量为4.25亿美元,到2023年预计将达到5.902亿美元,从2018年起以6.8%的复合年增长率增长。脂肪酶使用场景和市场的不断扩大和增长,促进了脂肪酶在菌株分离、脂肪酶异源高效表达以及脂肪酶固定化等方面的相关研究。
3.近年来关于不动杆菌脂肪酶的研究报道相对较少,特别是新型的、具有高效活性的不动杆菌脂肪酶的研究报道更是少见,而不动杆菌脂肪酶具有ph稳定性高,底物选择性较低的优点是工业微生物脂肪酶的重要来源。本发明发现的来源于菌株acinetobacter junii wco-9(gdmcc no:61851)的基因,其编码的脂肪酶ajlip970是一种新型、高效的细菌来源脂肪酶,具有广阔的应用前景。
技术实现要素:
4.本发明的一个目的是解决至少上述问题和/或缺陷,并提供至少后面将说明的优点。
5.为了实现根据本发明的这些目的和其它优点,提供了一种新型脂肪酶ajlip970,所述脂肪酶ajlip970的氨基酸序列如seq id no.2所示;所述脂肪酶ajlip970具有催化油脂降解的功能。
6.本发明还提供一种编码如上所述脂肪酶ajlip970的基因,所述基因的核苷酸序列如seq id no.1所示。
7.本发明还提供一种含上述的基因的重组载体。
8.本发明还提供一种如上所述的重组载体在培育产脂肪酶微生物中的用途。
9.本发明还提供一种由上所述的重组载体转化得到的重组工程菌株。
10.优选的是,将重组载体转入原核宿主细胞大肠杆菌中,获得重组工程菌株。
11.本发明还提供一种如上所述的重组工程菌株在培育产脂肪酶微生物中的用途。
12.优选的是,诱导表达发酵后产生脂肪酶,经亲和层析纯化获得纯蛋白,在催化不同链长对硝基苯酯中的应用。
13.优选的是,重组工程菌株经诱导,脂肪酶基因ajlip970在重组工程菌株中能够大量表达;经细胞破碎离心收集上清液,通过目的蛋白his标签与ni-nta树脂的特异性吸附纯化脂肪酶。
14.本发明还提供一种如上所述的新型脂肪酶ajlip970在催化油脂降解工业中的应
用。
15.本发明至少包括以下有益效果:本发明基因编码的脂肪酶ajlip970氨基酸序列在ncbi数据库中一致性最高为90.76%,鉴定为一种新型脂肪酶;本发明构建了含有ajlip970基因的重组载体pet22b-ajlip970,将其在原核宿主细胞大肠杆菌bl21(de3)中表达,实验证明,所述基因在原核宿主细胞中表达后,获得的纯化脂肪酶具有高效催化酯类底物水解的活性,在餐厨废油的无害化处理和资源化利用领域具有巨大的应用潜力。
16.本发明的其它优点、目标和特征将部分通过下面的说明体现,部分还将通过对本发明的研究和实践而为本领域的技术人员所理解。
附图说明:
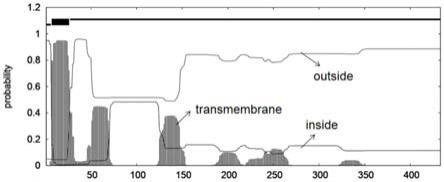
17.图1是脂肪酶ajlip970跨膜结构预测;
18.图2是脂肪酶ajlip970信号肽预测;
19.图3是pcr扩增并纯化的ajlip970基因片段(m为trans 2k plusii dna marker,泳道1为扩增并纯化的ajlip970基因片段);
20.图4是重组质粒pet22b-ajlip970的构建及验证,其中:
21.a是pet22b质粒和ajlip970基因片段连接后转化大肠杆菌top10的菌落pcr验证(m为trans 2k plusii dna marker,泳道1为空白对照,泳道2为wco-9基因组dna为模板pcr的阳性对照,泳道3为待测的含有重组质粒的菌落pcr结果);
22.b是提取的重组质粒pet22b-ajlip970及其pcr、酶切验证(m为trans 2k plusii dna marker,泳道1为重组质粒pet22b-ajlip970,泳道2为wco-9基因组dna为模板pcr的阳性对照,泳道3为空质粒对照,泳道4为重组质粒pet22b-ajlip970的pcr结果,泳道5为重组质粒pet22b-ajlip970的酶切验证)。
23.图5是脂肪酶ajlip970大量诱导及纯化的sds-page电泳分析图(m为预染的蛋白marker,泳道1为含有空载体菌株表达的蛋白对照,泳道2为诱导表达的pet22b-ajlip970/bl21菌株未纯化的蛋白上清,泳道3为纯化的脂肪酶ajlip970,方框为目标蛋白)。
24.图6是按照蛋白定量测定试剂盒说明书标准曲线绘制方法绘制的蛋白标准曲线。
25.图7是脂肪酶ajlip970底物特异性分析中绘制标准曲线所用试剂用量图。
26.图8是脂肪酶ajlip970底物特异性分析中绘制的标准曲线。
27.图9是脂肪酶ajlip970对不同链长底物水解活性差异分析。
具体实施方式:
28.下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
29.应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不配出一个或多个其它元件或其组合的存在或添加。
30.以下实施例中涉及的质粒、菌株等只是用于对本发明作进一步详细说明,并不对本发明的实质内容加以限制。凡未注明具体实验条件的,均为按照本领域技术人员熟知的常规条件或按照制造厂商所建议的条件进行的。
31.实施例中涉及的质粒、菌株来源及试剂:
32.菌株和质粒:acinetobacter junii wco-9由实验室自行分离并保藏于广东省微生物菌种保藏中心(gdmcc),保藏号gdmcc no:61851,大肠杆菌克隆菌株top 10、大肠杆菌表达菌株bl21(de3)由实验室保存;质粒pet22b为实验室保存,重组表达质粒pet22b-ajlip970和重组表达菌株pet22b-ajlip970/bl21由本发明自行构建。
33.生化试剂:限制性内切酶购自neb公司;dntps、高保真primestar hs dna polymerase、t4 dna连接酶等购自大连宝生物公司(takara);琼脂糖凝胶dna回收试剂盒、普通dna产物纯化试剂盒、普通质粒小提试剂盒、细菌基因组提取试剂盒均购自天根生化科技公司(tiangen),ni-nta树脂层析柱、bradford法蛋白定量测定试剂盒购自全式金公司;iptg、抗生素等购自阿拉丁(aladdin);对硝基苯酯底物(ρ-npc
10-18
)购自美国sigma公司;其余生化试剂均为分析纯级。实验中所用引物合成及测序由华大基因公司和北京百迈客生物科技有限公司完成。
34.lb培养基:胰蛋白胨10g/l,酵母提取物5g/l,nacl 10g/l,固体培养基中加入琼脂粉15g/l。高压蒸汽(121℃,1.034
×
105pa)灭菌30min。
35.氨苄青霉素(amp)(50mg/ml):称取0.5g氨苄青霉素粉末,溶于10ml双蒸水中,滤膜过滤除杂后分装,保存于-20℃冰箱,氯霉素(cm)(34mg/ml):称取0.34g氯霉素粉末,溶于乙醇中,分装保存于-20℃冰箱;
36.iptg(0.1mol/l):称取0.24g iptg,溶于10ml双蒸水中,滤膜过滤除菌后分装,保存于-20℃冰箱;
37.为了实现本发明,本发明通过了以下研究发现:
38.(1)acinetobacter junii wco-9菌株中含有多个脂肪酶基因,其中包含序列特异性较高的基因ajlip970,其核苷酸序列如seq no.1所示,该基因编码的脂肪酶具有较高的催化活性,ajlip970属于一种新型脂肪酶,其氨基酸序列如seq no.2所示。该脂肪酶基因在新型脂肪酶的挖掘研究和应用中具有重要意义,同时为培育产脂肪酶的工程微生物提供了基因来源。
39.(2)利用http://web.expasy.org/protparam/对ajlip970脂肪酶氨基酸序列进行在线预测,该蛋白由433个氨基酸组成,其中带负电氨基酸残基总数(asp+glu)为24,带正电氨基酸残基总数(arg+lys)为31,蛋白分子式c
2102h3294n542o605s12
,其分子量为46.2kda,理论等电点为9.12,不稳定指数30.88,属于稳定蛋白质;对ajlip970进行信号肽和跨膜结构分析,该脂肪酶是一种胞外蛋白(图1),前24位氨基酸为信号肽区域(图2);二级结构预测发现,该蛋白具有13个α螺旋,12个β折叠,以及24个其余结构。
40.(3)acinetobacter junii wco-9菌株基因组测序及ajlip970脂肪酶序列比对
41.菌株基因组测序委托北京百迈客生物科技有限公司完成,测序结果根据功能数据库注释发现,该菌株中含有一个特异性脂肪酶基因ajlip970,其所编码的蛋白ajlip970氨基酸序列比对一致性为90.76%,是一种新的脂肪酶编码基因。
42.(4)获得含有脂肪酶基因ajlip970的重组菌株
43.1)利用pcr从acinetobacter junii wco-9菌株(gdmcc no:61851)基因组扩增ajlip970基因(图3),其核苷酸序列如seq no.1所示,基因序列长度为1302bp,通过酶切连接,将其重组于载体pet22b上,构建了含有完整脂肪酶基因ajlip970的重组质粒pet22b-ajlip970(图4);
44.2)将含有ajlip970基因的重组质粒pet22b-ajlip970转入原核宿主细胞大肠杆菌bl21(de3)中,获得重组工程菌株pet22b-ajlip970/bl21。
45.(5)重组工程菌株pet22b-ajlip970/bl21脂肪酶ajlip970的诱导表达和蛋白纯化(图5)
46.1)重组菌株pet22b-ajlip970/bl21经0.5mm iptg诱导,以pet22b空载菌株为对照,经sds-page电泳和酶活性测定实验表明脂肪酶ajlip970在重组菌株中能够大量表达;
47.2)重组菌株使用iptg诱导大量表达后,经细胞破碎离心收集上清液,通过目的蛋白his标签与ni-nta树脂的特异性吸附纯化脂肪酶ajlip970;
48.(6)脂肪酶ajlip970活性测定及底物特异性分析
49.经过亲和层析纯化的脂肪酶ajlip970依据gb/t 23535—2009测定脂肪酶活性,测定结果显示脂肪酶ajlip970活性为131,000u/g;底物特异性分析显示脂肪酶ajlip970具有极高的水解活性,对不同链长脂肪酸底物的水解活性也具有较好的底物广谱性,但随着c10~c18脂肪酸底物链长的延长,其催化水解活性呈下降趋势(图9),总体而言,脂肪酶ajlip970在工业应用领域具有美好前景。
50.实施例1:
51.重组质粒pet22b-ajlip970的构建及转化至表达菌株的过程:
52.根据试剂盒说明书提取细菌wco-9基因组,根据菌株全基因测序结果设计扩增目的基因ajlip970的引物,如下:
[0053][0054]
以acinetobacter junii wco-9基因组为模板,使用上表中引物970-f/r扩增目的基因全长,扩增体系(50μl):2
×
phanta max master mix 25μl;模板0.5μl;引物970-f/r各1μl;灭菌ddh2o 22.5μl;加样后混匀离心。pcr条件:95℃10min;94℃30sec;57℃30sec;72℃1.5min;34个循环;72℃10min。纯化回收获得脂肪酶基因ajlip970片段(图3)。
[0055]
使用限制性内切酶(hindⅲ和xhoⅰ)消化目的基因片段和pet22b质粒,酶切体系20μl:10
×
cutsmart buffer 2μl;目的片段10μl;hindⅲ和xhoⅰ各1μl;灭菌ddh2o 6μl;混匀后37℃水浴酶切12h。酶切片段使用普通dna产物纯化试剂盒纯化。
[0056]
建立连接体系(20μl):10
×
t4 dna ligase buffer 2μl;t4 dna ligase 1μl;pet22b酶切片段10μl;目的基因酶切片段7μl;混匀于16℃连接4h。取连接产物10μl与50μl大肠杆菌top10感受态细胞于灭菌离心管中混匀,冰浴30min,42℃水浴1~2min后立即冰浴2~3min,向离心管中加入无抗生素的lb液体培养基800μl,37℃,200rpm摇床振荡培养1h,4000rpm离心5min,去掉多余上清,用剩余的150μl上清液重悬菌体,涂布于含有对应抗生素(amp)的lb固体培养基,37℃恒温培养箱培养12~16h,挑取单菌落验证并作阴性和阳性对照,结果从转化后的菌株中扩增到ajlip970片段(图4a),表明目的基因成功连接到pet22b载体上。
[0057]
挑取验证成功的菌落扩大培养,使用普通质粒小提试剂盒提取重组质粒pet22b-ajlip970,重组质粒经pcr和酶切验证成功(图4b)后送华大基因测序,测序结果经比对确认重组质粒构建成功。将重组质粒pet22b-ajlip970按上述转化大肠杆菌感受态的方法转入表达菌株bl21(de3)中获得重组表达菌株pet22b-ajlip970/bl21。
[0058]
实施例2:脂肪酶ajlip970的诱导表达和蛋白纯化:
[0059]
(1)不同浓度的iptg诱导脂肪酶ajlip970
[0060]
挑取重组表达菌株pet22b-ajlip970/bl21单菌落接种于20ml lb液体培养基(含amp+cm)中,37℃,200rpm振荡培养12~16h制备种子液,测定菌液od
600
并按初始od
600
=0.1接种于新的50ml lb液体培养基(含amp+cm)中,37℃,200rpm振荡培养至od
600
=0.5,分别向各培养瓶加入不同量的iptg,使各培养瓶中iptg终浓度分别为0.1mm、0.25mm、0.5mm、0.75mm、1.0mm,16℃,180rpm诱导48h,同时以0.1mm诱导的pet22b/bl21空载表达菌株作为对照。4℃,8000
×
g离心10min收集菌体,菌体使用50mm tris-hcl(ph=8.0)重悬洗涤2~3次,洗涤完毕的菌体使用2ml 50mm tris-hcl(ph=8.0)重悬,通过sds-page电泳检测脂肪酶ajlip970的表达差异,最终选择0.5mm浓度的iptg进行脂肪酶ajlip970的诱导表达。
[0061]
(2)脂肪酶ajlip970的大量诱导及蛋白纯化
[0062]
挑取重组表达菌株pet22b-ajlip970/bl21单菌落接种于20ml lb液体培养基(含amp+cm)中,37℃,200rpm振荡培养12~16h制备种子液,按初始od
600
=0.1将种子液接种于新的500ml lb液体培养基(含amp+cm)中,37℃,200rpm振荡培养至od
600
=0.5,按终浓度为0.5mm加入iptg,16℃,180rpm诱导20h。4℃,8000
×
g离心10min收集菌体,菌体使用50mm tris-hcl(ph=8.0)重悬洗涤2~3次,洗涤完毕的菌体使用20ml 50mm tris-hcl(ph=8.0)重悬菌体。使用超声破碎仪处理重悬液破碎细胞,破碎功率25%,超声开2s,超声关3s,冰浴破碎处理10min。4℃,12000
×
g离心20min收集上清液即为ajlip970脂肪酶粗酶液。
[0063]
利用带有6*his标签的脂肪酶ajlip970与ni-nta 树脂特异性吸附的原理纯化ajlip970脂肪酶,具体操作:重悬介质,根据待纯化蛋白量在层析柱中填入适量的介质(介质载量为10~20mg蛋白/ml wet gel),静置5min;用5~10倍柱体积平衡缓冲液平衡层析柱(本研究所使用的层析柱体积为6ml);将收集的ajlip970上清粗酶液分批加入层析柱中,静置5min(样品缓冲液尽可能与平衡缓冲液一致),收集上样流穿液,可重复上样提高回收率;上样完毕后,用5~10倍柱体积平衡缓冲液洗涤层析柱,收集流出液;使用200mm(ph=8.0)的咪唑洗脱目标蛋白,得到纯化的脂肪酶ajlip970。纯化后的脂肪酶ajlip970通过sds-page电泳检测纯化效果,电泳结果显示通过该方法纯化到了脂肪酶ajlip970(图5),脂肪酶ajlip970蛋白样品保存于-80℃冰箱。
[0064]
(3)蛋白浓度测定:
[0065]
按照蛋白定量测定试剂盒说明书标准曲线绘制方法绘制蛋白标准曲线,计算样品中的蛋白浓度,蛋白标准曲线绘制如图6所述:
[0066]
将适当体积的样品(100μl)加入到1.5ml离心管中,对于浓度过高的样品用h2o稀释,向管中加入1.0ml考马斯亮蓝染液,混匀,室温放置5-10分钟,测定595nm处的吸光值,以不含ajlip970蛋白样品的咪唑作为空白对照,根据绘制的标准曲线,计算样品中的蛋白浓度。
[0067]
实施例3:脂肪酶ajlip970的活性测定及底物特异性分析
[0068]
(1)脂肪酶ajlip970活性测定
[0069]
依据gb/t 23535—2009文件所示指示剂滴定法配制脂肪酶活性测定所需的所有试剂,指示剂滴定法测定脂肪酶活性具体操作:a)取两个100ml三角瓶,分别于空白瓶(a)和样品瓶(b)中各加人底物溶液4.0ml和磷酸缓冲液5.0ml,再于a瓶中加入95%乙醇15.0ml,于40℃
±
0.2℃水浴中预热5min,然后于a、b瓶中各加待测酶液1.0ml,立即混匀计时,准确反应15min后,于b瓶中立即补加95%乙醇15.0ml终止反应,取出;b)于空白和样品溶液中各加酚酞指示液两滴,用氢氧化钠标准溶液滴定,直至微红色并保持30s不褪色为滴定终点,记录消耗氢氧化钠标准溶液的体积,根据给定的脂肪酶活力计算公式并结合样品蛋白浓度计算脂肪酶ajlip970酶活性。
[0070]
(2)脂肪酶ajlip970底物特异性分析
[0071]
标准曲线的绘制:称取0.08346g对硝基苯酚,先用少量95%乙醇溶解,然后用水定容至l00ml,浓度为6mmol/l。按下表分别加入不同量的对硝基酚溶液(如图7所示)和50mmol/l tris-hcl(ph8.0)缓冲液,然后每管加入0.25ml 10%三氯乙酸,再加入0.25ml 10%na2co3溶液,总体积为1.5ml,410nm测定光吸收值,绘制标准曲线,如图8所示。每组3个重复。
[0072]
以异丙醇为溶剂,配制反应底物溶液(底物现配现用),分别称取对硝基苯癸酸、月桂酸、豆蔻酸、硬脂酸、棕榈酸酯底物45mg于15ml异丙醇,反应体系:首先加入900μl 50mmol/l tris-hcl(ph 8.0)缓冲液,90μl反应底物,混匀,然后加入10μl酶液,37℃水浴锅反应10min,快速加入250μl 10%三氯乙酸终止反应,再加入250μl 10%na2co3溶液显色,410nm测定光吸收值。空白对照为200mm的不含脂肪酶ajlip970的咪唑溶液,1个酶活单位(u)定义为该实验条件下,每分钟释放1μmol对硝基苯酚所需要的酶量,酶活计算公式:
[0073]
a=([a
1-a0]
×
k+c0)
×v1
×
n/(v2×
t)
[0074]
式中a
‑‑
样品酶活(u/ml)
[0075]a1-样品酶液的吸光度od值
[0076]a0-对应酶液的空白吸光度od值
[0077]k‑‑
对硝基苯酚标准曲线的斜率
[0078]
c0‑‑
对硝基苯酚标准曲线的截距
[0079]n‑‑
稀释倍数
[0080]v1
‑‑
反应液的体积/ml
[0081]v2
‑‑
酶液的体积/ml
[0082]
t
‑‑
反应时间/min
[0083]
根据蛋白浓度,将上述酶活计算结果换算为u/mg作图(见图9),结果表明脂肪酶ajlip970具有极高的酶活性并且拥有较好的底物广谱性。
[0084]
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1