一种索烃化的VAR2CSA重组蛋白及其制备方法和应用与流程
一种索烃化的var2csa重组蛋白及其制备方法和应用
技术领域
1.本发明属于细胞免疫治疗技术领域,涉及一种索烃化的var2csa重组蛋白及其制备方法和应用。
背景技术:
2.近年来,以嵌合抗原受体t细胞(car-t)技术为代表的免疫细胞疗法在血液肿瘤的临床治疗上取得了巨大的成功,对实体肿瘤治疗的也在探索之中(june et al., science. 2018, 359(6382): 1361-1365.)。随着临床研究的不断开展,越来越多的研究者发现仍然有10%~20%的b细胞淋巴瘤和b淋巴细胞白血病患者对anti-cd19 car-t治疗无反应(maude et al., n engl j med. 2018, 378(5): 439-448.),在部分临床试验中患者接受anti-cd19 car-t细胞治疗一年后的复发率最高超过50%(park et al., n engl j med. 2018, 378(5): 449-459.),出现这些现象的主要原因包括cd19阴性的肿瘤患者客观存在、car-t细胞的体内持久性不足和癌细胞cd19靶抗原突变导致其膜表达量下调或丢失等。
3.为了解决car-t细胞持久性以及b淋巴细胞瘤cd19抗原缺少或丢失的难题,研究者们采取的措施主要包括:1、阻断嵌合抗原受体(car)泛素化以增强内体car的信号传导和car-t细胞的持久性(li et al., immunity. 2020, 53(2):456-470.e6.);2、构建cd19抗原低亲和力的car以提高car-t细胞的增殖能力并增强其持久性(ghorashian et al., nat med. 2019, 25(9): 1408-1414.);3、构建双靶点car-t细胞,例如同时靶向cd19和cd20(zah et al., cancer immunol res. 2016, 4(6): 498-508.)两个抗原来减少b细胞肿瘤抗原逃逸的几率等。此外,car-t细胞治疗的毒副作用,例如细胞因子释放综合征(crs)或免疫效应细胞相关神经毒性综合征(icans)等威胁患者生存的安全性问题也不可忽视,除了加强医学分级和管理(neelapu ss. hematol oncol. 2019, 37 suppl 1: 48-52.)之外,从car-t细胞体系的源头上进行创新设计(jaspers and brentjens. pharmacol ther. 2017, 178: 83-91.)才有可能一劳永逸地解决问题。
4.综合上述,如何设计和制造一种广谱(多靶点)、安全性高、稳定性好且具备持久抗肿瘤活性的嵌合抗原受体细胞体系,是免疫细胞治疗领域取得更大突破的关键。
技术实现要素:
5.针对现有技术的不足和实际需求,本发明提供一种索烃化的var2csa重组蛋白及其制备方法和应用,所述索烃化的var2csa重组蛋白与普通var2csa重组蛋白(野生型)相比,具备更高的蛋白稳定性、与肿瘤特异性抗原胎盘样硫酸软骨素a(pl-csa)的亲和力更强,可应用于制备抗肿瘤药物如嵌合抗原受体细胞。
6.为达上述目的,本发明采用以下技术方案:第一方面,本发明提供一种索烃化的var2csa重组蛋白,所述索烃化的var2csa重组蛋白包括随机排列连接的结合域、spytag、p53dim domain和spycatcher,所述结合域包括var2csa蛋白中与胎盘样硫酸软骨素a结合的结构域。
7.本发明中,利用var2csa蛋白中能够识别并结合肿瘤特异性抗原胎盘样硫酸软骨素a(pl-csa)的结合域与spytag、p53dim domain和spycatcher随机组合排列连接形成融合蛋白,由于spytag短肽与其蛋白配体spycatcher的可自发酰胺键缩合形成异肽键,使得融合蛋白分子内(n-端和c端)或者融合蛋白分子之间发生共价偶联反应产生蛋白分子环化和索烃化,并最终形成“套环”多聚体重组蛋白,与单体var2csa重组蛋白(rvar2)相比,索烃化显著提高了蛋白稳定性及其与肿瘤特异性抗原pl-csa的亲和力,并且以索烃化的var2csa重组蛋白为导航系统的car-t细胞体系,其抗肿瘤效果得到了全面提升,且细胞因子分泌水平较低,推测其在临床上发生细胞因子释放综合征等毒副作用的风险也较低。因此,所述索烃化的var2csa重组蛋白可有效应用于肿瘤的免疫治疗领域,如免疫细胞疗法。
8.优选地,所述结合域的多肽序列包括seq id no.1所示的序列。
9.优选地,所述spytag的多肽序列包括seq id no.2所示的序列。
10.优选地,所述p53dim domain的多肽序列包括seq id no.3所示的序列。
11.优选地,所述spycatcher的多肽序列包括seq id no.4所示的序列。
12.seq id no.1:nyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddnicgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskld。
13.seq id no.2:ahivmvdaykptk。
14.seq id no.3:ggeyftlqirgrerfeefreknealelkdaqagkepgg。
15.seq id no.4:amvdtlsglsseqgqsgdmtieedsathikfskrdedgkelagatmelrdssgktistwisdgqvkdfylypgkytfvetaapdgyevataitftvneqgqvtvngkatkgdahi。
16.优选地,所述索烃化的var2csa重组蛋白还包括蛋白标签及空间链接linker。
17.优选地,所述蛋白标签包括pne-tag、人c-myc-tag、captureselect
™ꢀ
c-tag、flag-tag、3
×
flag-tag、twin-strep-tag、strep-tag、6
×
his-tag、v5 tag、s-tag、ha-tag、vsv-g-tag、gst-tag、halotag、xten-tag或huegfrt-tag中的任意一种或至少两种的组合。
18.优选地,所述twin-strep-tag的多肽序列包括seq id no.5所示的序列。
19.优选地,所述空间链接linker包括柔性linker和helix-forming peptide linker。
20.优选地,所述柔性linker的多肽序列包括seq id no.6所示的序列。
21.优选地,所述helix-forming peptide linker的多肽序列包括seq id no.7所示的序列。
22.seq id no.5:sawshpqfekgggsgggsggssawshpqfek。
23.seq id no.6:ggggs。
24.seq id no.7:lvgeaaakeaaaka。
25.本发明中,将所述结合域、spytag、p53dim domain、spycatcher和蛋白标签通过空间连接linker随机组合排列连接,可合成功能相似但序列和结构不同的索烃化var2csa重组蛋白。
26.优选地,所述柔性linker位于所述spytag与p53dim domain之间。
27.优选地,所述helix-forming peptide linker位于spycatcher与twin-strep-tag之间。
28.优选地,所述索烃化的var2csa重组蛋白的多肽序列包括seq id no.8、seq id no.9或seq id no.10所示的序列。
29.seq id no.8:mahivmvdaykptkggggsggeyftlqirgrerfeefreknealelkdaqagkepggvdnyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddnicgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskldgtamvdtlsglsseqgqsgdmtieedsathikfskrdedgkelagatmelrdssgktistwisdgqvkdfylypgkytfvetaapdgyevataitftvneqgqvtvngkatkgdahi。
30.seq id no.9:mnyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddnicgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskldgsahivmvdaykptkggggsggeyftlqirgrerfeefreknealelkdaqagkepggvdnyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddn
icgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskldgtamvdtlsglsseqgqsgdmtieedsathikfskrdedgkelagatmelrdssgktistwisdgqvkdfylypgkytfvetaapdgyevataitftvneqgqvtvngkatkgdahi。
31.seq id no.10:mahivmvdaykptknyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddnicgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskldgsggeyftlqirgrerfeefreknealelkdaqagkepggvdnyikgdpyfaeyatklsfilnssdannpsekiqknndevcncnesgiasveqeqisdpssnktcithssikankkkvckhvklgvrendkdlrvcviehtslsgvencccqdflrilqencsdnksgsssngscnnknqeaceknlekvlasltncykcdkckseqskknnknwiwkkssgkegglqkeyantiglpprtqslclvvcldekgkktqelknirtnsellkewiiaafhegknlkpshekknddngkklckaleysfadygdlikgtsiwdneytkdlelnlqkifgklfrkyikknntaeqdtsyssldelreswwntnkkyiwlamkhgagmnsttccgdgsvtgsgsscddiptidlipqylrflqewvehfckqrqekvkpviencksckesggtcngecktecknkcevykkfiedckggdgtagsswvkrwdqiykryskyiedakrnrkagtkncgpssttnaaenkcvqsdidsffkhlidiglttpssylsivlddnicgadkapwttyttytttekcnketdksklqqcntavvvnvpsplgntphgykyacqckiptneetcddrkeymnqwscgsartmkrgykndnyelckyngvdvkpttvrsnsskldgtamvdtlsglsseqgqsgdmtieedsathikfskrdedgkelagatmelrdssgktistwisdgqvkdfylypgkytfvetaapdgyevataitftvneqgqvtvngkatkgdahi。
32.第二方面,本发明提供第一方面所述的索烃化的var2csa重组蛋白的制备方法,所述制备方法包括:构建含有第一方面所述的索烃化的var2csa重组蛋白的编码基因的表达载体,将所述表达载体转入细胞中,培养细胞并进行蛋白纯化,得到所述索烃化的var2csa重组蛋白。
33.第三方面,本发明提供一种核酸分子,所述核酸分子包括权第一方面所述的索烃化的var2csa重组蛋白的编码基因。
34.优选地,所述核酸分子包括seq id no.11、seq id no.12或seq id no.13所示的脱氧核糖核酸序列或与其具有至少80%以上核苷酸同一性的变体。
35.seq id no.11:atggcgcacattgttatggtggacgcgtacaaaccgaccaagggtggcggtggcagcggtggcgagtatttcaccctgcagatccgtggccgtgaacgtttcgaggaatttcgtgagaaaaacgaagcgctggagctgaaagatgcgcaagcgggcaaggagccgggtggcgtcgacaactacatcaaaggcgatccgtatttcgcggaatacgcgaccaagctgagctttattctgaacagcagcgacgcgaacaacccgagcgagaaaatccagaagaacaacgatgaagtgtg
caactgcaacgagagcggtattgcgagcgttgagcaggaacaaatcagcgacccgagcagcaacaaaacctgcattacccacagcagcatcaaggcgaacaagaaaaaggtttgcaaacacgtgaagctgggcgttcgtgagaacgacaaggatctgcgtgtttgcgtgattgagcacaccagcctgagcggtgtggaaaactgctgctgccaggactttctgcgtatcctgcaagaaaactgcagcgataacaaaagcggtagcagcagcaacggcagctgcaacaacaagaaccaggaagcgtgcgagaaaaacctggagaaggttctggcgagcctgaccaactgctacaaatgcgacaaatgcaagagcgaacaaagcaaaaagaacaacaagaactggatttggaaaaagagcagcggcaaagaaggtggcctgcagaaggagtatgcgaacaccatcggtctgccgccgcgtacccaaagcctgtgcctggtggtttgcctggatgaaaaaggtaaaaagacccaggagctgaagaacatccgtaccaacagcgaactgctgaaagagtggatcattgcggcgttccacgagggcaaaaacctgaagccgagccacgagaagaagaacgacgataacggtaaaaagctgtgcaaggcgctggagtatagctttgcggactacggtgatctgattaaaggcaccagcatctgggacaacgaatacaccaaggatctggagctgaacctgcagaaaattttcggcaagctgttccgtaagtacatcaaaaagaacaacaccgcggaacaagacaccagctatagcagcctggatgaactgcgtgagtcctggtggaacaccaacaaaaagtacatctggctggcgatgaaacacggtgcgggcatgaacagcaccacctgctgcggtgatggcagcgtgaccggtagcggcagcagctgcgacgatatcccgaccattgatctgatcccgcagtatctgcgtttcctgcaagaatgggttgagcacttttgcaaacagcgtcaagaaaaagttaagccggtgattgagaactgcaaaagctgcaaggaaagcggtggcacctgcaacggtgaatgcaagaccgagtgcaaaaacaagtgcgaggtgtacaaaaagttcatcgaagactgcaaaggtggcgatggcaccgcgggcagcagctgggttaagcgttgggaccagatttacaagcgttatagcaaatacatcgaggatgcgaagcgtaaccgtaaagcgggcaccaagaactgcggtccgagcagcaccaccaacgcggcggaaaacaaatgcgtgcaaagcgacattgatagcttctttaagcacctgatcgacattggcctgaccaccccgagcagctacctgagcattgttctggacgataacatttgcggtgcggacaaggcgccgtggaccacctataccacctacaccaccaccgaaaaatgcaacaaggaaaccgataaaagcaagctgcagcaatgcaacaccgcggtggttgtgaacgttccgagcccgctgggtaacaccccgcacggctacaaatatgcgtgccagtgcaagatcccgaccaacgaggaaacctgcgacgatcgtaaagagtatatgaaccaatggagctgcggtagcgcgcgtaccatgaaacgtggctataagaacgacaactacgaactgtgcaaatataacggcgttgatgtgaagccgaccaccgtgcgtagcaacagcagcaagctggacggtaccgcgatggttgataccctgagcggtctgagcagcgagcagggtcaaagcggcgacatgaccattgaggaagatagcgcgacccacatcaaattcagcaagcgtgacgaagatggtaaagagctggcgggcgcgaccatggaactgcgtgacagcagcggcaagaccattagcacctggatcagcgacggccaggtgaaagatttctacctgtatccgggcaagtacacctttgttgaaaccgcggcgccggatggttatgaagtggcgaccgcgattacctttaccgttaacgagcagggtcaagttaccgtgaacggtaaagcgaccaagggcgatgcgcacatctaa。
36.seq id no.12:atgaactacatcaaaggcgatccgtatttcgcggaatacgcgaccaagctgagctttattctgaacagcagcgacgcgaacaacccgagcgagaaaatccagaagaacaacgatgaagtgtgcaactgcaacgagagcggtattgcgagcgttgagcaggaacaaatcagcgacccgagcagcaacaaaacctgcattacccacagcagcatcaaggcgaacaagaaaaaggtttgcaaacacgtgaagctgggcgttcgtgagaacgacaaggatctgcgtgtttgcgtgattgagcacaccagcctgagcggtgtggaaaactgctgctgccaggactttctgcgtatcctgcaagaaaactgcagcgataacaaaagcggtagcagcagcaacggcagctgcaacaacaagaaccaggaagcgtgcgagaaaaacctggagaaggttctggcgagcctgaccaactgctacaaatgcgacaaatgcaagagcgaacaaagcaaaaagaacaacaagaactggatttggaaaaagagcagcggcaaagaaggtggcctgcagaaggagtatgcgaacaccatcggtctgccgccgcgtacccaaagcctgtgcctggtggtttgcctggatgaaaaaggtaaaaagacccaggagctgaagaacatccgtacca
acagcgaactgctgaaagagtggatcattgcggcgttccacgagggcaaaaacctgaagccgagccacgagaagaagaacgacgataacggtaaaaagctgtgcaaggcgctggagtatagctttgcggactacggtgatctgattaaaggcaccagcatctgggacaacgaatacaccaaggatctggagctgaacctgcagaaaattttcggcaagctgttccgtaagtacatcaaaaagaacaacaccgcggaacaagacaccagctatagcagcctggatgaactgcgtgagtcctggtggaacaccaacaaaaagtacatctggctggcgatgaaacacggtgcgggcatgaacagcaccacctgctgcggtgatggcagcgtgaccggtagcggcagcagctgcgacgatatcccgaccattgatctgatcccgcagtatctgcgtttcctgcaagaatgggttgagcacttttgcaaacagcgtcaagaaaaagttaagccggtgattgagaactgcaaaagctgcaaggaaagcggtggcacctgcaacggtgaatgcaagaccgagtgcaaaaacaagtgcgaggtgtacaaaaagttcatcgaagactgcaaaggtggcgatggcaccgcgggcagcagctgggttaagcgttgggaccagatttacaagcgttatagcaaatacatcgaggatgcgaagcgtaaccgtaaagcgggcaccaagaactgcggtccgagcagcaccaccaacgcggcggaaaacaaatgcgtgcaaagcgacattgatagcttctttaagcacctgatcgacattggcctgaccaccccgagcagctacctgagcattgttctggacgataacatttgcggtgcggacaaggcgccgtggaccacctataccacctacaccaccaccgaaaaatgcaacaaggaaaccgataaaagcaagctgcagcaatgcaacaccgcggtggttgtgaacgttccgagcccgctgggtaacaccccgcacggctacaaatatgcgtgccagtgcaagatcccgaccaacgaggaaacctgcgacgatcgtaaagagtatatgaaccaatggagctgcggtagcgcgcgtaccatgaaacgtggctataagaacgacaactacgaactgtgcaaatataacggcgttgatgtgaagccgaccaccgtgcgtagcaacagcagcaagctggacggatccgcgcacattgttatggtggacgcgtacaaaccgaccaagggtggcggtggcagcggtggcgagtatttcaccctgcagatccgtggccgtgaacgtttcgaggaatttcgtgagaaaaacgaagcgctggagctgaaagatgcgcaagcgggcaaggagccgggtggcgtcgacaactacatcaaaggcgatccgtatttcgcggaatacgcgaccaagctgagctttattctgaacagcagcgacgcgaacaacccgagcgagaaaatccagaagaacaacgatgaagtgtgcaactgcaacgagagcggtattgcgagcgttgagcaggaacaaatcagcgacccgagcagcaacaaaacctgcattacccacagcagcatcaaggcgaacaagaaaaaggtttgcaaacacgtgaagctgggcgttcgtgagaacgacaaggatctgcgtgtttgcgtgattgagcacaccagcctgagcggtgtggaaaactgctgctgccaggactttctgcgtatcctgcaagaaaactgcagcgataacaaaagcggtagcagcagcaacggcagctgcaacaacaagaaccaggaagcgtgcgagaaaaacctggagaaggttctggcgagcctgaccaactgctacaaatgcgacaaatgcaagagcgaacaaagcaaaaagaacaacaagaactggatttggaaaaagagcagcggcaaagaaggtggcctgcagaaggagtatgcgaacaccatcggtctgccgccgcgtacccaaagcctgtgcctggtggtttgcctggatgaaaaaggtaaaaagacccaggagctgaagaacatccgtaccaacagcgaactgctgaaagagtggatcattgcggcgttccacgagggcaaaaacctgaagccgagccacgagaagaagaacgacgataacggtaaaaagctgtgcaaggcgctggagtatagctttgcggactacggtgatctgattaaaggcaccagcatctgggacaacgaatacaccaaggatctggagctgaacctgcagaaaattttcggcaagctgttccgtaagtacatcaaaaagaacaacaccgcggaacaagacaccagctatagcagcctggatgaactgcgtgagtcctggtggaacaccaacaaaaagtacatctggctggcgatgaaacacggtgcgggcatgaacagcaccacctgctgcggtgatggcagcgtgaccggtagcggcagcagctgcgacgatatcccgaccattgatctgatcccgcagtatctgcgtttcctgcaagaatgggttgagcacttttgcaaacagcgtcaagaaaaagttaagccggtgattgagaactgcaaaagctgcaaggaaagcggtggcacctgcaacggtgaatgcaagaccgagtgcaaaaacaagtgcgaggtgtacaaaaagttcatcgaagactgcaaaggtggcgatggcaccgcgggcagcagctgggttaagcgttgggaccagatttacaagcgttatagcaaatacatcgaggatgcgaagcgtaaccgtaaagcgggcaccaagaactgcggtccgagcagcaccaccaacgcggcggaaaacaaatgcgtgcaaagcgacattgatagcttctttaagcacctgatcgacattggcctgaccaccccgagcagctacctgagcattgttctggacgataacatttgcggtgcggaca
aggcgccgtggaccacctataccacctacaccaccaccgaaaaatgcaacaaggaaaccgataaaagcaagctgcagcaatgcaacaccgcggtggttgtgaacgttccgagcccgctgggtaacaccccgcacggctacaaatatgcgtgccagtgcaagatcccgaccaacgaggaaacctgcgacgatcgtaaagagtatatgaaccaatggagctgcggtagcgcgcgtaccatgaaacgtggctataagaacgacaactacgaactgtgcaaatataacggcgttgatgtgaagccgaccaccgtgcgtagcaacagcagcaagctggacggtaccgcgatggttgataccctgagcggtctgagcagcgagcagggtcaaagcggcgacatgaccattgaggaagatagcgcgacccacatcaaattcagcaagcgtgacgaagatggtaaagagctggcgggcgcgaccatggaactgcgtgacagcagcggcaagaccattagcacctggatcagcgacggccaggtgaaagatttctacctgtatccgggcaagtacacctttgttgaaaccgcggcgccggatggttatgaagtggcgaccgcgattacctttaccgttaacgagcagggtcaagttaccgtgaacggtaaagcgaccaagggcgatgcgcacatctaa。
37.seq id no.13:atggcgcacattgttatggtggacgcgtacaaaccgaccaagaactacatcaaaggcgatccgtatttcgcggaatacgcgaccaagctgagctttattctgaacagcagcgacgcgaacaacccgagcgagaaaatccagaagaacaacgatgaagtgtgcaactgcaacgagagcggtattgcgagcgttgagcaggaacaaatcagcgacccgagcagcaacaaaacctgcattacccacagcagcatcaaggcgaacaagaaaaaggtttgcaaacacgtgaagctgggcgttcgtgagaacgacaaggatctgcgtgtttgcgtgattgagcacaccagcctgagcggtgtggaaaactgctgctgccaggactttctgcgtatcctgcaagaaaactgcagcgataacaaaagcggtagcagcagcaacggcagctgcaacaacaagaaccaggaagcgtgcgagaaaaacctggagaaggttctggcgagcctgaccaactgctacaaatgcgacaaatgcaagagcgaacaaagcaaaaagaacaacaagaactggatttggaaaaagagcagcggcaaagaaggtggcctgcagaaggagtatgcgaacaccatcggtctgccgccgcgtacccaaagcctgtgcctggtggtttgcctggatgaaaaaggtaaaaagacccaggagctgaagaacatccgtaccaacagcgaactgctgaaagagtggatcattgcggcgttccacgagggcaaaaacctgaagccgagccacgagaagaagaacgacgataacggtaaaaagctgtgcaaggcgctggagtatagctttgcggactacggtgatctgattaaaggcaccagcatctgggacaacgaatacaccaaggatctggagctgaacctgcagaaaattttcggcaagctgttccgtaagtacatcaaaaagaacaacaccgcggaacaagacaccagctatagcagcctggatgaactgcgtgagtcctggtggaacaccaacaaaaagtacatctggctggcgatgaaacacggtgcgggcatgaacagcaccacctgctgcggtgatggcagcgtgaccggtagcggcagcagctgcgacgatatcccgaccattgatctgatcccgcagtatctgcgtttcctgcaagaatgggttgagcacttttgcaaacagcgtcaagaaaaagttaagccggtgattgagaactgcaaaagctgcaaggaaagcggtggcacctgcaacggtgaatgcaagaccgagtgcaaaaacaagtgcgaggtgtacaaaaagttcatcgaagactgcaaaggtggcgatggcaccgcgggcagcagctgggttaagcgttgggaccagatttacaagcgttatagcaaatacatcgaggatgcgaagcgtaaccgtaaagcgggcaccaagaactgcggtccgagcagcaccaccaacgcggcggaaaacaaatgcgtgcaaagcgacattgatagcttctttaagcacctgatcgacattggcctgaccaccccgagcagctacctgagcattgttctggacgataacatttgcggtgcggacaaggcgccgtggaccacctataccacctacaccaccaccgaaaaatgcaacaaggaaaccgataaaagcaagctgcagcaatgcaacaccgcggtggttgtgaacgttccgagcccgctgggtaacaccccgcacggctacaaatatgcgtgccagtgcaagatcccgaccaacgaggaaacctgcgacgatcgtaaagagtatatgaaccaatggagctgcggtagcgcgcgtaccatgaaacgtggctataagaacgacaactacgaactgtgcaaatataacggcgttgatgtgaagccgaccaccgtgcgtagcaacagcagcaagctggacggatccggtggcgagtatttcaccctgcagatccgtggccgtgaacgtttcgaggaatttcgtgagaaaaacgaagcgctggagctgaaagatgcgcaagcgggcaaggagccgggtggcgtcgacaactacatcaaaggcgatccgtatttcgcggaatacgcgaccaagctgagctttat
tctgaacagcagcgacgcgaacaacccgagcgagaaaatccagaagaacaacgatgaagtgtgcaactgcaacgagagcggtattgcgagcgttgagcaggaacaaatcagcgacccgagcagcaacaaaacctgcattacccacagcagcatcaaggcgaacaagaaaaaggtttgcaaacacgtgaagctgggcgttcgtgagaacgacaaggatctgcgtgtttgcgtgattgagcacaccagcctgagcggtgtggaaaactgctgctgccaggactttctgcgtatcctgcaagaaaactgcagcgataacaaaagcggtagcagcagcaacggcagctgcaacaacaagaaccaggaagcgtgcgagaaaaacctggagaaggttctggcgagcctgaccaactgctacaaatgcgacaaatgcaagagcgaacaaagcaaaaagaacaacaagaactggatttggaaaaagagcagcggcaaagaaggtggcctgcagaaggagtatgcgaacaccatcggtctgccgccgcgtacccaaagcctgtgcctggtggtttgcctggatgaaaaaggtaaaaagacccaggagctgaagaacatccgtaccaacagcgaactgctgaaagagtggatcattgcggcgttccacgagggcaaaaacctgaagccgagccacgagaagaagaacgacgataacggtaaaaagctgtgcaaggcgctggagtatagctttgcggactacggtgatctgattaaaggcaccagcatctgggacaacgaatacaccaaggatctggagctgaacctgcagaaaattttcggcaagctgttccgtaagtacatcaaaaagaacaacaccgcggaacaagacaccagctatagcagcctggatgaactgcgtgagtcctggtggaacaccaacaaaaagtacatctggctggcgatgaaacacggtgcgggcatgaacagcaccacctgctgcggtgatggcagcgtgaccggtagcggcagcagctgcgacgatatcccgaccattgatctgatcccgcagtatctgcgtttcctgcaagaatgggttgagcacttttgcaaacagcgtcaagaaaaagttaagccggtgattgagaactgcaaaagctgcaaggaaagcggtggcacctgcaacggtgaatgcaagaccgagtgcaaaaacaagtgcgaggtgtacaaaaagttcatcgaagactgcaaaggtggcgatggcaccgcgggcagcagctgggttaagcgttgggaccagatttacaagcgttatagcaaatacatcgaggatgcgaagcgtaaccgtaaagcgggcaccaagaactgcggtccgagcagcaccaccaacgcggcggaaaacaaatgcgtgcaaagcgacattgatagcttctttaagcacctgatcgacattggcctgaccaccccgagcagctacctgagcattgttctggacgataacatttgcggtgcggacaaggcgccgtggaccacctataccacctacaccaccaccgaaaaatgcaacaaggaaaccgataaaagcaagctgcagcaatgcaacaccgcggtggttgtgaacgttccgagcccgctgggtaacaccccgcacggctacaaatatgcgtgccagtgcaagatcccgaccaacgaggaaacctgcgacgatcgtaaagagtatatgaaccaatggagctgcggtagcgcgcgtaccatgaaacgtggctataagaacgacaactacgaactgtgcaaatataacggcgttgatgtgaagccgaccaccgtgcgtagcaacagcagcaagctggacggtaccgcgatggttgataccctgagcggtctgagcagcgagcagggtcaaagcggcgacatgaccattgaggaagatagcgcgacccacatcaaattcagcaagcgtgacgaagatggtaaagagctggcgggcgcgaccatggaactgcgtgacagcagcggcaagaccattagcacctggatcagcgacggccaggtgaaagatttctacctgtatccgggcaagtacacctttgttgaaaccgcggcgccggatggttatgaagtggcgaccgcgattacctttaccgttaacgagcagggtcaagttaccgtgaacggtaaagcgaccaagggcgatgcgcacatctaa。
38.第四方面,本发明提供一种嵌合抗原受体细胞体系,所述嵌合抗原受体细胞体系包括第一方面所述的索烃化的var2csa重组蛋白和嵌合抗原受体细胞,所述嵌合抗原受体细胞表达识别所述索烃化的var2csa重组蛋白的嵌合抗原受体。
39.本发明的嵌合抗原受体细胞体系中,所述嵌合抗原受体细胞能够识别并结合所述索烃化的var2csa重组蛋白,从而具备了识别并结合pl-csa的能力,即嵌合抗原受体细胞以索烃化的var2csa重组蛋白为导航系统,二者进入体内后可自动“组装”并捕获和杀伤肿瘤细胞,由于索烃化的var2csa重组蛋白具备更高的稳定性和亲和力,使得嵌合抗原受体细胞的抗肿瘤活性更强、更持久,此外,索烃化的var2csa重组蛋白游离于嵌合抗原受体细胞外,既是嵌合抗原受体细胞的导航系统也是“安全开关”,可以通过调控体系中索烃化的var2csa重组蛋白的含量来间接调控嵌合抗原受体细胞的功能,一旦出现诸如细胞因子释
放综合征(crs)或免疫效应细胞相关神经毒性综合征(icans)等严重毒副作用,通过切断体系中索烃化的var2csa重组蛋白的供应就能够使得依赖索烃化的var2csa重组蛋白起作用的嵌合抗原受体细胞失去活性,从而使得体系具备可调控性,增强了体系的安全性。
40.优选地,所述细胞为免疫效应细胞,优选为t细胞、b细胞、nk细胞、nkt细胞、树突状细胞或巨噬细胞中的任意一种或至少两种的组合。
41.本发明中,其他任何能够直接或者间接识别所述索烃化的var2csa重组蛋白的嵌合抗原受体细胞也可达到本发明所述的效果,落在本发明的保护范围之内。
42.优选地,所述嵌合抗原受体包括识别所述索烃化的var2csa重组蛋白的结构域。
43.优选地,所述嵌合抗原受体还包括铰链区、跨膜区和胞内共刺激信号区。
44.优选地,所述识别所述索烃化的var2csa重组蛋白的结构域包含由重链可变区和轻链可变区组成的单链抗体。
45.优选地,编码所述单链抗体重链可变区的基因为如seq id no.14所示的脱氧核糖核酸序列或与其具有至少80%以上核苷酸同一性的变体。
46.优选地,编码所述单链抗体轻链可变区的基因为如seq id no.15所示的脱氧核糖核酸序列或与其具有至少80%以上核苷酸同一性的变体。
47.seq id no.14:gaggtgaagctggtggaaagcggcggcggactggtgaaacctggaggcagcctgaagctcagctgcgccgctagcggatttacatttagcaactacgccatgagctgggtgcggcagagccccgagaggcgcctggaatgggtcgctgagatcagcatcaccggcagatacacctactaccccgacaccgttacaggccggttcaccatcagccgggacaacgccaagaacaccctgtacctggagatgagttctctgagatctgaagataccgccatgtactactgcaccagagagggctacgactacgccccttcttggttcgcctactggggacagggaaccctggtcaccgtgtccgcc。
48.seq id no.15:gacgtggtgatgacccagacacctctgagcctgcctgtgtctctgggcgaccaggccagcatcagctgtagaagcggccagaccctggtgcacagaaatggcatcacatacctggaatggtatctgcagaagcctggccaatctccaaagctgctgatctacaaggtgtccaaccggttcagcggcgtgcccgatagattcagcggcagcggctccggcaccgacttcaccctgaaaatctccagagtggaagccgaggatctgggaatctactattgcttccagggctctcacgtgcctagaacattcggcggaggtacaaagctggagattaag。
49.优选地,所述铰链区为人cd8α铰链区。
50.优选地,所述跨膜区为人cd28跨膜区。
51.优选地,所述胞内共刺激信号区为人cd27胞内信号区、人cd134胞内信号区、人cd28胞内信号区或人4-1bb胞内信号区中的任意一种或至少两种的组合。
52.优选地,所述嵌合抗原受体的氨基末端含有一个cd8α信号肽。
53.优选地,所述嵌合抗原受体的羧基末端还包含一个人cd3ζ胞内信号区。
54.优选地,所述嵌合抗原受体包含多功能域依次串联的cd8α信号肽、识别所述索烃化的var2csa重组蛋白的单链抗体、人cd8α铰链区、人cd28跨膜区、人cd28胞内信号区、人4-1bb胞内信号区和人cd3ζ胞内信号区;优选地,所述嵌合抗原受体包含如seq id no.16所示的多肽序列。
55.seq id no.16:malpvtalllplalllhaarpdvvmtqtplslpvslgdqasiscrsgqtlvhrngitylewylqkpgq
spklliykvsnrfsgvpdrfsgsgsgtdftlkisrveaedlgiyycfqgshvprtfgggtkleikggggsggggsggggsevklvesggglvkpggslklscaasgftfsnyamswvrqsperrlewvaeisitgrytyypdtvtgrftisrdnakntlylemsslrsedtamyyctregydyapswfaywgqgtlvtvsatttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrskrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr。
56.第五方面,本发明提供一种嵌合抗原受体细胞,所述嵌合抗原受体细胞表达如第一方面所述的索烃化的var2csa重组蛋白,和识别所述索烃化的var2csa重组蛋白的嵌合抗原受体。
57.第六方面,本发明提供一种药物组合物,所述药物组合物包括第一方面所述的索烃化的var2csa重组蛋白、如第三方面所述的核酸分子、如第四方面所述的嵌合抗原受体细胞体系或如第五方面所述的嵌合抗原受体细胞中任意一种或至少两种的组合。
58.优选地,所述药物组合物还包括药学上可接受的辅料。
59.第七方面,本发明提供如第一方面所述的索烃化的var2csa重组蛋白、第三方面所述的核酸分子、第四方面所述的嵌合抗原受体细胞体系、第五方面所述的嵌合抗原受体细胞或第六方面所述的药物组合物在制备治疗肿瘤的药物中的应用。
60.优选地,所述肿瘤为实体肿瘤和/或血液肿瘤。
61.所述肿瘤可以是能够被var2csa蛋白或者var2csa蛋白中能够与胎盘样硫酸软骨素a(pl-csa)结合的结构域特异性识别和结合的任意肿瘤组织和细胞,可以是人实体肿瘤细胞系,例如肺癌细胞系,包括nci-h460(大细胞肺癌细胞系,atcc#htb177)、nci-h520(鳞状细胞肺癌细胞系,atcc#htb182)以及a549(肺腺癌细胞系,atcc#ccl185)等;人黑色素瘤细胞系,包括mp38(葡萄膜黑色素瘤细胞系,atcc# crl-3296)等;还可以是人血液肿瘤细胞系,包括raji(b细胞淋巴瘤细胞系,atcc# ccl86)、k562(人慢性髓性白血病细胞系,atcc# ccl-243)等。
62.与现有技术相比,本发明具备以下有益效果:(1)本发明设计并成功制备索烃化的var2csa重组蛋白,显著提高了蛋白稳定性和对肿瘤特异性抗原胎盘样硫酸软骨素a的亲和力;(2)本发明的嵌合抗原受体细胞体系中嵌合抗原受体细胞以索烃化的var2csa重组蛋白为导航系统,抗肿瘤活性更强、更持久,具备良好的体内肿瘤治疗效果,能够通过调节体系中索烃化的var2csa重组蛋白的含量来调控嵌合抗原受体细胞的功能,预示着可以在临床治疗中通过调控导航蛋白的给药剂量来避免发生细胞因子释放综合征(crs)或免疫效应细胞相关神经毒性综合征(icans)等由于car-t细胞功能激活而导致的毒副作用,安全性更好。
附图说明
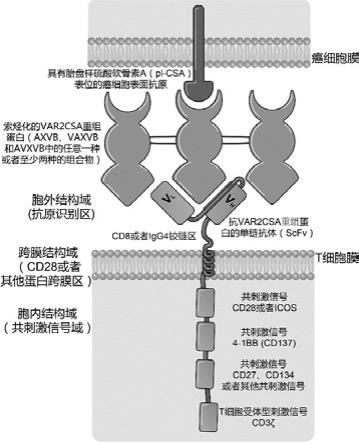
63.图1为索烃化var2csa重组蛋白的基因表达载体示意图;图2为以索烃化的疟原虫var2csa重组蛋白为导航系统的car-t细胞体系的抗肿瘤原理示意图;
图3为索烃化var2csa重组蛋白的细胞内合成路线图;图4为索烃化var2csa重组蛋白的诱导型原核表达载体质粒图谱;图5为聚丙烯酰胺凝胶电泳检测采用strep-tactin树脂纯化的var2csa重组蛋白结果图;图6为聚丙烯酰胺凝胶电泳检测采用strep-tactin树脂和阴离子交换树脂联用纯化的var2csa重组蛋白结果图;图7为anti-cd19 car和anti-rvar2 car的模块组成示意图;图8为流式细胞术分析普通t细胞组、cd19-car t细胞组和anti-rvar2-car t细胞组中表达car的阳性t细胞的比例图;图9为western-blot检测car的表达图;图10为axvb与5h4 mab的亲和力检测结果图;图11为rvar2与5h4 mab的亲和力检测结果图;图12为avxvb与5h4 mab的亲和力检测结果图;图13为vaxvb与5h4 mab的亲和力检测结果图;图14为axvb和rvar2与不同类型肿瘤细胞系靶向结合的相对平均荧光强度分析图;图15为不同温度和时间处理条件下,axvb和rvar2与raji细胞的结合比例对比分析图;图16为不同温度和时间处理条件下,axvb和rvar2与k562细胞的结合比例对比分析图;图17为不同温度和时间处理条件下,axvb与rvar2蛋白与raji细胞结合的相对剩余活性比较分析图;图18为不同温度和时间处理条件下,axvb与rvar2蛋白与k562细胞结合的相对剩余活性比较分析图;图19为流式细胞术分析raji、k562和h460细胞膜表面cd19抗原分子的表达情况图;图20为导航蛋白(axvb和rvar2)或以之为导航系统的car-t细胞体系与cd19-car t细胞对raji细胞的体外细胞毒性比较图;图21为导航蛋白(axvb和rvar2)或以之为导航系统的car-t细胞体系与cd19-car t细胞对k562细胞的体外细胞毒性比较图;图22为导航蛋白(axvb和rvar2)或以之为导航系统的car-t细胞体系与cd19-car t细胞对h460细胞的体外细胞毒性比较图;图23为以raji细胞为靶细胞,比较普通t细胞、cd19-car t细胞和以axvb或rvar2为导航系统的car-t细胞体系的体外细胞因子分泌水平图;图24为以k562细胞为靶细胞,比较普通t细胞、cd19-car t细胞和以axvb或rvar2为导航系统的car-t细胞体系的体外细胞因子分泌水平图;图25为索烃化var2csa重组蛋白axvb调控axvb-[switch]-car t细胞体系中il-2的分泌水平图;图26为索烃化var2csa重组蛋白axvb调控axvb-[switch]-car t细胞体系中tnf-α
的分泌水平图;图27为索烃化var2csa重组蛋白axvb调控axvb-[switch]-car t细胞体系中ifn-γ的分泌水平图;图28为索烃化var2csa重组蛋白axvb调控axvb-[switch]-car t细胞体系的抗肿瘤活性图;图29为car-t细胞疗法动物模型实验分组和基本流程示意图;图30为raji细胞荷瘤小鼠经car-t细胞治疗的活体成像检测结果图,肿瘤负荷显示为量化的萤火虫荧光素酶催化d-荧光素底物发光信号,5只小鼠一组;图31为raji细胞荷瘤小鼠的生存期曲线图,*为p 《 0.05,**为p 《 0.01,ns为p 》 0.05;图32为k562细胞荷瘤小鼠经car-t细胞治疗的活体成像检测结果图,肿瘤负荷显示为量化的萤火虫荧光素酶催化d-荧光素底物发光信号,5只小鼠一组;图33为k562细胞荷瘤小鼠的生存期曲线图,*为p 《 0.05,**为p 《 0.01,ns为p 》 0.05;图34为pbs对照组raji细胞荷瘤小鼠体内的肿瘤转移灶图,黑色箭头所指为肿瘤转移灶部位。
具体实施方式
[0064]
为进一步阐述本发明所采取的技术手段及其效果,以下结合实施例和附图对本发明作进一步地说明。可以理解的是,此处所描述的具体实施方式仅仅用于解释本发明,而非对本发明的限定。
[0065]
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购买获得的常规产品。
[0066]
实施例1本实施例设计索烃化的var2csa重组蛋白及嵌合抗原受体t细胞体系。
[0067]
本实施中设计3种包含var2csa蛋白中与胎盘样硫酸软骨素a结合的结构域(v)、spytag(a)、p53dim domain(x)、spycatcher(b)、twin-strep-tag (t)及helix-forming peptide linker(l)的索烃化的var2csa重组蛋白,分别命名为axvb、vaxvb和avxvb,结构排列示意图如图1所示,多肽序列分别如seq id no.8(axvb)、seq id no.9(vaxvb)和seq id no.10(avxvb)所示。
[0068]
本实施例的嵌合抗原受体细胞体系中,所述嵌合抗原受体细胞为嵌合抗原受体t细胞(car-t),其表达的嵌合抗原受体的多肽序列如seq id no.16所示,car-t细胞体系的抗肿瘤原理示意图如图2所示,car-t细胞能够识别并结合索烃化的var2csa重组蛋白,进而能够识别肿瘤组织并发挥杀伤作用。
[0069]
实施例2本实施例制备实施例1所述的索烃化的var2csa重组蛋白(axvb、vaxvb和avxvb)和野生型var2csa重组蛋白(rvar2,除了蛋白标签以外,其蛋白结构域的多肽序列与野生型疟原虫var2csa蛋白中的相关结构域的多肽序列完全相同,并且不存在蛋白分子内或蛋白分
industries, cat.# 04-001-1acs)、2 mm l-谷氨酰胺(gibco, cat.# 25030-081)和210 iu/ml重组人白介素-2(rhil-2, r&d system, cat.# 202-il-050))中刺激过夜;刺激后的t细胞采用cn110325551b中所描述的编码anti-rvar2-car的慢病毒表达载体(plenticart-anti-rvar2(5h4 scfv))包装的慢病毒,并按照其中描述的实验步骤进行t细胞转染;在随后的分析之前,对照组(普通t细胞组、anti-cd19-car t细胞组)和实验组(anti-rvar2-car t细胞组,表达如seq id no.16所示的嵌合抗原受体)的t细胞每周用x-vivo-15完全培养基换液3次,持续培养14天,以上所述anti-cd19-car t(熟称cd19-car t)细胞组和anti-rvar2-car t细胞组中嵌合抗原受体(car)的模块组成示意图如图7所示,其中cd8 leader为膜表达信号肽,αcd19 v
l
为抗cd19单链抗体的轻链,l为柔性链接(linker)序列,αcd19 vh为抗cd19单链抗体的重链,cd8 hinge为胞外cd8铰链区,cd28 tm为cd28跨膜区,cd28和4-1bb为t细胞共刺激信号,cd3ζ为t细胞激活信号,f2a为自剪切“2a”多肽,egfp为增强型绿色荧光蛋白作为报告基因;αrvar2 v
l
为抗var2csa重组蛋白单链抗体的轻链,αrvar2 vh为抗var2csa重组蛋白单链抗体的重链。
[0075]
car-t细胞输注前进行流式细胞术检测car
+-t细胞的比例(阳性率)(图8),约为70%,随后利用留样的t细胞样品,进一步采用辣根过氧化物酶(hrp)标记的cd3ζ抗体(6b10.2,santa cruz, cat.# sc-1239 hrp)进行western-blot检测car的表达情况,如图9所示,其中1为普通t细胞;2为anti-rvar2-car t细胞;3为cd19-car t细胞,anti-rvar2-car的平均分子量大小约为75 kda,而cd19-car的平均分子量大小约为73 kda,所有t细胞中都表达的组成型cd3ζ的平均分子量大小约为16 kda,结果显示所有蛋白杂交印迹的分子量大小都符合预期,表明car的表达正常。
[0076]
所述anti-cd19-car t(以下简称cd19-car t)细胞中的嵌合抗原受体(car)除了单链抗体(anti-cd19 scfv)序列不同以外,其他元件与seq id no.16所示的anti-rvar2-car的多肽序列和功能域组合顺序一致,所述anti-cd19 scfv的轻链和重链都来自靶向人cd19的鼠源单克隆抗体fmc63(nicholson et al. mol immunol. 1997, 34(16-17):1157-65.)并且具有如seq id no.18所示的多肽序列。
[0077]
seq id no.18:qvqlqqsgaelvrpgssvkisckasgyafssywmnwvkqrpgqglewigqiwpgdgdtnyngkfkgkatltadessstaymqlsslasedsavyfcarretttvgryyyamdywgqgttvtvssggggsggggsggggsdiqltqspaslavslgqratisckasqsvdydgdsylnwyqqipgqppklliydasnlvsgipprfsgsgsgtdftlnihpvekvdaatyhcqqstedpwtfgggtkleik。
[0078]
实施例4本实施例比较索烃化的var2csa重组蛋白(axvb、vaxvb和avxvb)与野生型var2csa重组蛋白(rvar2)对car-t细胞的胞外识别结构域单链抗体的亲和力。
[0079]
本发明中所述的car-t细胞的胞外识别结构域单链抗体为5h4 scfv(pct/cn2017/113661, zl201780001820.4),它由识别索烃化的var2csa重组蛋白(axvb、vaxvb和avxvb)与野生型var2csa重组蛋白(rvar2)结构域中id2α表位的单克隆抗体5h4(5h4 mab)中的vh链以及5h4的v
l
链以及两者之间的连接序列(ggggsggggsggggs)组成。采用elisa法(syedbasha et al., j vis exp. 2016, (109): 53575.)测定单克隆抗体5h4(5h4 mab)与索烃化的var2csa重组蛋白(axvb、vaxvb和avxvb)与野生型var2csa重组蛋白(rvar2)的
fluor
®ꢀ
488标记的山羊抗小鼠igg(h&l)二抗(abcam, cat.# ab150113),且以上所有的蛋白和抗体都采用抗体稀释液(含有0.1% fbs的1
×
pbs)稀释;每个蛋白或抗体孵育45分钟后,在孵育下一个蛋白或抗体之前或二抗孵育完成之后,均采用4℃预冷的pbs-f(含0.02% nan3、2% fbs)洗涤3次,每次间隔2分钟,最后通过bd accuri
™ꢀ
c6 plus流式细胞仪检测所示肿瘤细胞系与重组蛋白axvb和rvar2孵育后的相对平均荧光强度(mfi),比较二者的细胞结合亲和力强弱,经统计分析发现,结果如图14所示,axvb蛋白对肿瘤细胞的结合亲和力显著强于rvar2蛋白(p 《 0.05或 p 《 0.01)。
[0085]
实施例6本实施例比较axvb与rvar2蛋白的热稳定性。
[0086]
细胞因子释放综合征(crs)是car-t细胞疗法最常见的副作用(neelapu ss. hematol oncol. 2019;37(s1):48-52.),即便最低等级的crs,也会伴随身体发烧≥38℃,甚至身体持续高烧(≥39℃)超过10小时,这大大超过了人体的正常体温(36.1~37.2℃);因此,蛋白的热稳定性可能会直接影响以之为导航系统的car-t细胞体系在人体临床肿瘤治疗中的疗效,在本发明中,采用与肿瘤细胞结合活性的动态监测法来评估导航蛋白的热稳定性,包括以下步骤:(1)自-80℃冰箱中取出冻存的纯度≥98%的axvb或rvar2蛋白,冰上解冻后用冰预冷的pbs缓冲液将蛋白浓度分别调至200 nm并按照500 μl/管分装4管,然后将样品各自分别在30℃,37℃,和42℃条件下温育30分钟,2小时,24小时和48小时;定期采集温育后的样品,以储存于-80℃的同批次纯化的axvb和rvar2蛋白在冰上融解后作为阳性对照组蛋白,继续进一步的实验;(2)为每个温度条件和不同时间点收集的蛋白样品分别准备2
×
105个raji 细胞(人b细胞淋巴瘤细胞系,atcc# ccl86)或k562细胞(人慢性髓性白血病细胞系,atcc# ccl-243),依次加入200 μl步骤(1)中收集的不同温度和处理时间的浓度为200 nm的axvb或rvar2重组蛋白,1 μg/ml小鼠抗rvar2蛋白单克隆抗体5h4 mab,以及1 μg/ml alexa fluor
®ꢀ
488标记的山羊抗小鼠igg (h&l)二抗(abcam, cat.# ab150113),且以上所有的蛋白和抗体都采用抗体稀释液(含0.1% fbs的1
×
pbs)稀释;每个蛋白或抗体孵育45分钟后,在孵育下一个蛋白或抗体之前或二抗孵育完成之后,均采用4℃预冷的pbs-f(含0.02% nan3、2% fbs)洗涤3次,每次间隔2分钟;以不加重组蛋白孵育的等量细胞作为阴性对照组;(3)通过cytek aurora流式细胞仪检测重组蛋白axvb和rvar2与raji(图15)或k562(图16)结合后的阳性率和相应的平均荧光强度(mean fluorescence intensity, mfi),如图15所示,随着处理温度的升高和处理时间的延长,axvb与raji细胞的结合比例明显高于rvar2蛋白与raji细胞的结合比例,rvar2蛋白在42℃处理48小时后,完全丧失了与肿瘤细胞的结合活性;如图16所示,随着处理温度的升高和处理时间的延长,axvb与k562细胞的结合比例显著高于rvar2蛋白与raji细胞的结合比例,rvar2蛋白在达到或超过30℃处理24小时后,几乎完全丧失了与肿瘤细胞的结合活性;我们进一步分析了蛋白在不同温度条件处理后时间依赖性的与肿瘤细胞raji(表1,图17)或k562(表1,图18)结合的相对剩余活性差异,其中,相对剩余活性(relative residual activity, %)=(实验组样品的mfi/阳性对照组样品的mfi)
×
100,通过比较与肿瘤细胞结合的相对剩余活性的差异,可以间接比较axvb和rvar2蛋白的热稳定性。
[0087]
表1
上述结果表明,axvb蛋白比rvar2蛋白的热稳定性更好,可能有助于增强其在人体内的持久活性,进而提高以之为导航系统的car-t细胞体系的抗肿瘤疗效。
[0088]
实施例7本实施例比较不同car-t细胞体系对肿瘤细胞的体外细胞毒性。
[0089]
通过标准的荧光素酶活性测定试验(eyquem et al., nature. 2017, 543(7643): 113-117.)来验证以axvb蛋白为导航系统的car-t细胞体系(axvb-[switch]-car t)的细胞毒性。简而言之,以稳定表达红色荧光蛋白(mcherry)和萤火虫荧光素酶(firefly luciferase, ffluc)融合蛋白的稳转细胞系raji/mcherry-ffluc(cd19阳性血液肿瘤细胞)、k562/mcherry-ffluc(cd19阴性血液肿瘤细胞)以及h460/mcherry-ffluc(人大细胞肺癌细胞系,atcc# htb177,cd19阴性实体肿瘤细胞)作为靶细胞,各靶细胞的流式细胞术分析结果如图19所示,取一个96-孔的黑壁细胞培养板,细胞培养液总体积保持100 μl,按照
效应细胞(effector, e)与靶细胞(tumor target, t)的比例为e/t = 4:1,使用1640完全培养基(含10%灭活的fbs(biological industries, cat.# 04-001-1acs)的无酚红rpmi-1640培养基(gibco, cat.# 11875093))将1
×
105个靶细胞和相应的效应细胞体系(cart-anti-rvar2细胞以及100 nm axvb蛋白)共培养,每个样品做3个复孔,单独的靶细胞用相同的细胞密度铺板以确定最大荧光素酶表达强度(相对发光单位;rlumax),24小时后,将100 μl荧光素酶底物(bright-glo,promega, cat.# e2650)直接加入每个细胞培养孔中,在biotek synergy h1系统中检测发射光,并使用graphpad prism软件进行数据分析,细胞裂解率(%)计算公式为(1
ꢀ‑
(rlusample)/(rlumax))
×
100,针对不同靶细胞系的体外细胞毒性试验结果如图20(raji/mcherry-ffluc)、图21(k562/mcherry-ffluc)和图22(h460/mcherry-ffluc)所示,可见axvb-[switch]-car t对多种不同类型的肿瘤细胞都有体外细胞毒性,对cd19阳性细胞raji/mcherry-ffluc而言,与普通t细胞组(normal t)相比较,cd19-car t的细胞毒性更高,但axvb-[switch]-car t与rvar2-[switch]-car t也存在显著的细胞毒性(图20),且axvb-[switch]-car t体系的细胞毒性更高;与普通t细胞组(normal t)相比较,axvb-[switch]-car t与rvar2-[switch]-car t都具有显著较高的体外细胞毒性(图20,p值分别为p 《 0.05和p 《 0.05),有趣的是,cd19-car t对cd19阴性的k562/mcherry-ffluc细胞也有一定的体外细胞毒性(p 《 0.05,图21),这可能是car-t制造过程中激活所导致的非特异性杀伤效应;对于非小细胞肺癌细胞系h460/mcherry-ffluc,与普通t细胞组(normal t)相比较,axvb-[switch]-car t与rvar2-[switch]-car t都具有显著的细胞毒性(p 《 0.001,图22),并且axvb-[switch]-car t体系的细胞毒性稍弱于rvar2-[switch]-car t体系,这预示着axvb-[switch]-car t体系对血液肿瘤肿瘤和实体肿瘤的治疗效果可能会有区别,综合以上数据(图20-图22),说明:(1)与cd19-car t相比较,axvb-[switch]-car t与rvar2-[switch]-car t的具备更广谱的抗肿瘤效果;(2)无论是rvar2还是axvb蛋白,单独使用都不具备体外细胞毒性;(3)在本试验条件下,axvb-[switch]-car t体系与rvar2-[switch]-car t体系对肿瘤细胞的体外细胞毒性相当,可能是由于体系中axvb蛋白和rvar2蛋白均过量,故而不能完全体现出axvb与肿瘤细胞的结合表位较多、亲和力较高的优势。
[0090]
实施例8本实施例采用cba法检测car-t细胞的体外细胞因子分泌水平。
[0091]
采用“bd
™ꢀ
cytometric bead array (cba) human th1/th2/th17 cytokine kit”试剂盒(bd, cat.# 560484),该试剂盒可以在单个axvb-[switch]-car t或“scart-anti-rvar2”(即rvar2-[switch]-car t)的处理样品中同时检测interleukin-2 (il-2)、interleukin-4(il-4)、interleukin-6 (il-6)、interleukin-10 (il-10)、tumor necrosis factor (tnf)、interferon-γ (ifn-γ)和interleukin-17a (il-17a)共7个细胞因子的分泌水平,其主要实验步骤如下:(1)取一个96-孔细胞培养板,分别将培养好的raji(atcc# ccl86)和k562(atcc# ccl-243)细胞作为靶细胞,用一定量的1640完全培养基重悬并轻柔混合均匀,按照“5000个细胞/100 μl培养基/孔”的密度和体积铺板,随后在普通t细胞组(normal t)和anti-rvar2-car t组中分别加入终浓度为100 nm的rvar2或者axvb蛋白,于5% co2培养箱中,37℃孵育培养;
(2)3小时后,按照效靶比(e/t = 4:1)按加入相应数量的“car+-t细胞/100 μl培养基/孔”于5% co2培养箱中,37℃孵育共培养24小时,单独的普通t细胞对照组,加入100 μl rpmi-1640完全培养基重悬的同等数量的普通t细胞进行培养;(3)按照cba法细胞因子检测试剂盒(bd, cat.# 560484)说明书的指导,分别制备好标准品和细胞培养上清的流式检测上机样本,采用cytek aurora流式细胞仪上机检测后用其自带的spectroflo软件解析后,再结合microsoft excel和graphpad prism软件进行数据分析,结论如下:(1)与cd19-car t相比,axvb-[switch]-car t与rvar2-[switch]-car t分泌较低水平的细胞因子(图23和图24),尤其il-6、tnf和ifn-γ等促炎性细胞因子的分泌处于显著低水平(p 《 0.01),并且除了cd19-car t细胞组以外,其他实验组几乎不分泌抗炎细胞因子il-10,抗炎细胞因子il-4也处于较低水平,预示着发生细胞因子释放综合征(crs)的风险较低;(2)il-2,ifn-γ,il-6等效应细胞因子的分泌依赖于体系中是否存在一定浓度的导航蛋白(图23,图24),这预示着通过调控导航蛋白的浓度可以有效调节car-t细胞的细胞因子分泌水平及其对肿瘤细胞的细胞毒性,使得axvb-[switch]-car t与rvar2-[switch]-car t细胞体系一样,具备功能可调控性;(3)所有对照组与实验组的t细胞皆分泌th17细胞因子il-17a,且il-17a的分泌水平无显著差异(图23,图24;p 》0.05),预示制造的car-t细胞能够在肿瘤微环境中存活更久;(4)对于特定类型的肿瘤细胞(例如k562),与rvar2-[switch]-car t细胞体系相比(图24),axvb-[switch]-car t分泌相对显著低水平的系统性促炎细胞因子tnf(p 《 0.001),还分泌相对显著高水平的抗炎细胞因子il-4(p 《 0.001),推测其在体内发生细胞因子释放综合征的几率更低,安全性更好。
[0092]
实施例9本实施例测试以索烃化的var2csa重组蛋白作为导航系统的car-t细胞体系的功能可调控性。
[0093]
为了验证索烃化的var2csa重组蛋白作为car-t细胞体系的导航系统能否起到调控car-t细胞功能的作用,我们从car-t细胞体系的细胞因子分泌水平和car-t细胞体系的细胞毒性两方面分析了导航蛋白“开关”在体系中的调控作用。首先,我们采用elisa法测试了axvb导航蛋白对axvb-[switch]-car t细胞体系中细胞因子分泌水平的调控,具体步骤如下:(1)样品制备:将培养的细胞用含有不同摩尔浓度梯度的导航蛋白的rpmi-1640(gibco, cat.# 11875093)完全培养基(含3%灭活的胎牛血清)重悬,随后按照肿瘤细胞h460(mcherry-ffluc)密度为1.25
×
105个/250 μl/孔接种在48孔细胞培养板(costar, product# 3548)中,每个不同的导航蛋白浓度分别做3个复孔,在37℃,5% co2培养箱中培养3小时后,室温条件下300
×
g离心5分钟去掉培养基上清,用移液枪加入250 μl新的rpmi-1640完全培养基;按照t细胞(效应细胞,e)与肿瘤细胞(靶细胞,t)的比例为e:t=1:1,分别加入体积为250 μl且细胞总数一致的普通t细胞和car-t细胞共培养,且靶细胞与效应细胞的总和不超过1
×
106个/500μl/孔;以单独的anti-rvar2-car t细胞组代表实验组细胞因子分泌的本底水平,该组只取250 μl anti-rvar2-car t加250 μl含有不同摩尔浓度梯度的导航蛋白的rpmi-1640完全培养基;最后将所有试验样品在37℃,5% co2培养箱中共培养;(2)样品收集:24小时后,将试验样品转到干净无菌的1.5 ml ep管中,500
×
g室温
离心5分钟,用移液枪吸取细胞培养上清300 μl转移到一个新的干净无菌的1.5 ml ep管中以备后续的elisa检测;(3)按照r&d elisa kit试剂盒的使用说明分别检测收集的细胞培养上清中的细胞因子il-2(r&d systems,cat.# d2050)、tnf-α(r&d systems,cat.# dta00d)和ifn-γ(r&d systems,cat.# dif50)的含量,并采用graphpad prism软件进行数据分析。其中il-2的检测结果如图25所示,与普通t细胞对照组以及cd19-car t细胞组相比,axvb-[switch]-car t细胞体系中il-2的分泌水平高低与体系中索烃化蛋白axvb的浓度成正比;tnf-α与ifn-γ的检测结果分别如图26和图27所示,同样,与普通t细胞对照组以及cd19-car t细胞组相比,axvb-[switch]-car t细胞体系中il-2的分泌水平高低与体系中索烃化蛋白axvb的浓度同样成正比;说明可以通过调控索烃化的var2csa重组蛋白axvb的含量来调控axvb-[switch]-car t细胞体系中的细胞因子分泌水平。
[0094]
其次,采用与实施例7中同样的方法,我们比较了不同摩尔浓度梯度的导航蛋白介导car-t细胞对人非小细胞肺癌细胞系h460/mcherry-ffluc细胞毒性的差异,间接分析axvb导航蛋白对axvb-[switch]-car t细胞体系抗肿瘤活性的调控作用。实验结果如图28所示,与普通t细胞对照组以及cd19-car t细胞组相比,axvb-[switch]-car t细胞体系对肿瘤细胞的细胞毒性高低与体系中索烃化蛋白axvb的浓度成正比;说明可以通过调控索烃化的var2csa重组蛋白axvb的含量来调控axvb-[switch]-car t细胞体系对肿瘤细胞的杀伤活性。
[0095]
根据图25-图28的结果表明,可以通过增减体系中导航蛋白的含量来调控以索烃化var2csa重组蛋白为导航系统的car t细胞体系(例如axvb-[switch]-car t)的功能。其中,索烃化var2csa重组蛋白不仅具备导航功能而且还起到“安全开关”的作用。
[0096]
实施例10本实施例采用动物模型试验测试car-t细胞体系的体内抗肿瘤活性。
[0097]
为了验证和比较axvb-[switch]-car t细胞体系的体内抗肿瘤活性,我们设计并实施了动物模型体内实验,实施流程如图29所示,首先将稳转细胞系raji/mcherry-ffluc和k562/mcherry-ffluc分别按照5
×
105个肿瘤细胞/只小鼠,尾静脉注射接种至8-10周龄大小的雌性nsg(nod.cg-prkdcscid il2rgtm1wjl/szj,购自beijing biocytogen co., ltd)小鼠体内建立荷瘤小鼠模型;接种后第三天(day
ꢀ‑
3)通过活体成像分别检测raji/mcherry-ffluc和k562/mcherry-ffluc荷瘤小鼠肿瘤的荧光素酶表达水平,将表达水平接近的小鼠混合并随机分组到不同的组别;在第0,8和14天(day 0,day 8,和day 14 )分别单次尾静脉输注总数不超过2
×
107个car-t细胞(60%-80% car
+
阳性率),3小时后,向anti-rvar2-car t细胞治疗组每只小鼠再输注100 nmol/kg的rvar2或axvb导航蛋白“开关”,之后每隔一天输注一次导航蛋白,共输注10次;自car-t细胞输注前一天开始,采用ivis-spectrum 成像系统(caliper life sciences, hopkinton, ma, usa)分别对小鼠进行活体成像,并且平均间隔约7天检测一次,共检测5次。所有待活体成像检测的小鼠都用异氟醚(2%)麻醉,并按照150 mg/kg(d-荧光素质量/体重)浓度进行腹腔注射(i.p.),其中d-荧光素(d-luciferin,购自yeasen biotechnology (shanghai) co., ltd),注射入体内12分钟后进行成像分析,荧光素酶活性以每秒每平方厘米每球面度 (p/s-1
cm-2
sr-1
) 的光子数为单位;采用living image软件(caliper life sciences, hopkinton, ma, usa)用于图像
分析;自car-t输注的前一天(day
ꢀ‑
1)开始监测小鼠体重,每周测定2次,若实验过程中荷瘤小鼠的体重相比“药物”输注前的体重减轻≥20%,或者短期内体重急剧降低≥15%,将被视为不良反应,荷瘤小鼠将被安乐死,患有溃疡肿瘤的小鼠也将被安乐死。所有的动物实验都严格遵照动物福利的“3r”原则,并得到研究单位实验动物伦理审查委员会的批准。
[0098]
荷瘤小鼠活体成像实验结果表明,对于cd19阳性细胞raji,自car-t细胞输注后第8天开始,与未经治疗的对照组(仅输注等体积用于重悬t细胞的1
×
pbs)相比,axvb-[switch]-car t和rvar2-[switch]-car t与cd19-car t一样,都能够持续降低肿瘤负荷(图30),并且小鼠的生存期显著延长(图31),其中axvb-[switch]-car t治疗的小鼠中位生存期最长,达到79天,其他几组荷瘤小鼠的中位生存期分别为44天(pbs)、49天(cd19-car t)和56天(rvar2-[switch]-car t)。
[0099]
对于cd19阴性细胞k562,自car-t细胞输注后第8天,与未经治疗的对照组(pbs,用于重悬t细胞的1
×
pbs缓冲液)相比,axvb-[switch]-car t和rvar2-[switch]-car t与cd19-car t一样,都能够有效降低肿瘤负荷,但是随着时间的延长,到治疗后第14天,cd19-car t治疗组的小鼠肿瘤生长开始反弹,后期肿瘤的负荷与未经治疗的对照组几乎一致(图32);axvb-[switch]-car t治疗的小鼠生存期最长并且与pbs对照组存在显著性差异(p 《 0.05,图33),中位生存期达到76天,其他几组荷瘤小鼠的中位生存期分别为38天(pbs)、47天(cd19-car t)和61天(rvar2-[switch]-car t)。说明axvb-[switch]-car t和rvar2-[switch]-car t比cd19-car t的抗肿瘤谱更广,并且axvb-[switch]-car t的体内抗肿瘤效果更好。
[0100]
此外,对部分raji细胞荷瘤小鼠安乐死之后的解剖观察发现,只在pbs对照组部分小鼠的肝脏、脾脏和卵巢组织中发现肿瘤的转移灶(图34),而在其他car-t细胞治疗组中未发现,说明car-t细胞治疗组可以有效抑制肿瘤细胞通过血液和淋巴循环转移到重要的器官。
[0101]
综上所述,本发明设计并成功制备索烃化的var2csa重组蛋白,与普通var2csa重组蛋白(野生型)相比,显著提高了蛋白稳定性和对肿瘤特异性抗原胎盘样硫酸软骨素a的亲和力;并且创造性组合设计嵌合抗原受体细胞体系,将索烃化的var2csa重组蛋白应用于免疫细胞疗法,所述嵌合抗原受体细胞体系中,嵌合抗原受体细胞以索烃化的var2csa重组蛋白为导航系统(例如axvb-[switch]-car t),与野生型var2csa重组蛋白为导航系统(例如rvar2-[switch]-car t)的嵌合抗原受体细胞体系相比较,抗肿瘤活性更强、更持久,具备更好的体内肿瘤治疗效果;此外,通过供应或切断体系中索烃化的var2csa重组蛋白的就能够使得以之为导航系统的嵌合抗原受体细胞体系得到或失去抗肿瘤活性,还可以通过调控体系中索烃化的var2csa重组蛋白的含量多少来调控嵌合抗原受体细胞体系的功能强弱,其中索烃化的var2csa重组蛋白就如同一个可调控的“安全开关”,使得整个嵌合抗原受体细胞体系不仅具备可调控性还增强了体系的安全性。
[0102]
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1