一种由三苯胺制备三(4-乙炔基苯基)胺的方法
技术领域
1.本发明涉及有机化学技术,尤其涉及一种由三苯胺制备三(4-乙炔基苯基)胺的方法。
背景技术:2.三(4-乙炔基苯基)胺中n原子存在着孤对电子,是优良的电子给体,且共轭的苯乙炔结构提供稳定的电荷传输通道,对聚合物的光电性能带来显著影响。因此,三(4-乙炔基苯基)胺常被用于光电材料领域。另外其非平面的空间结构可以有效抑制分子聚集,形成多维网状结构,是合成共轭有机多孔材料理想单体。合成的微孔材料已在气体吸附,催化和传感器等领域被广泛应用。虽然三(4-乙炔基苯基)胺市场需求大,但由于末端炔基合成难度较大,所需试剂较贵,限制了其的应用范围。
3.目前公开的文献和专利报道合成端炔基的方法,主要有以下几种:
4.1)以卤代芳烃为原料,在金属钯催化下和三甲基硅基乙炔或2-甲基-3-丁炔基-2-醇经sonogashira偶联反应,最后再脱除保护基得到目标产物。中国专利cn 102898315 a公开一种3-乙炔基-4-氟苯胺的制备方法。该方法是以3-溴-4-氟硝基苯为原料,在pd(pph3)4催化下和三甲基硅基乙炔反应,得到3-三甲基硅基乙炔基-4-氟硝基苯,最后在碱性条件下消除三甲基硅基,得到3-乙炔基-4-氟硝基苯。中国专利cn 104177209 a公开了一种芳基末端炔的制备方法,首先芳卤与2-甲基-3-丁炔基-2-醇sonogashira交叉偶联反应得到带2-羟基-2-丙基保护基团的芳炔化合物4-芳基-2-甲基-3-丁炔基-2-醇,再脱除保护基团得到芳基末端炔产物。
5.2)以苯乙烯为原料,溴代得二乙烯溴代产物,再消除得目标产物。中国专利cn 102001902 a公开了一种1,1-二溴代乙烯基化合物合成端炔的方法。该方法以苯乙烯为原料,将苯乙烯溴代后得到1,1-二溴代乙烯基化合物,在碱性条件下脱溴制得端炔化合物。
6.3)以苯乙烷为原料,溴代得二溴代乙烷产物,再消除得目标产物。中国专利cn 112645826 a公开了一种以4-硝基乙苯为原料,通过自由基溴代反应制备得到1,1-二溴-1-(硝基苯基)乙烷,再在碱的作用下进行消除反应得到硝基苯乙炔。
7.4)以3-芳基丙烯酸为原料,溴代得3-芳基-2,3-二溴丙酸,再脱溴和脱羧得苯乙炔衍生物。中国专利cn 101967075 a公开了一种用3-苯基-2,3-二溴丙酸合成端炔化合物的方法。该方法溴代3-苯基-1-丙烯酸得到3-苯基-2,3-二溴丙酸,再在碱性条件下脱羧和卤素得到苯乙炔。
8.尽管文献报道制备苯乙炔及其衍生物的方法较多,但主要以2种方法为主,一是以乙炔基衍生物在氯化钯或醋酸钯做催化剂下,经sonogashira偶联反应,再脱保护得目标产物。此方法采用贵金属催化,且需无水无氧的操作条件,导致合成苯乙炔的工艺条件复杂,生产成本较高,难以规模化应用。另一种是由苯乙烯或苯乙烷等衍生物经溴代,再脱溴得到苯乙炔产物。此方法主要问题是高活性的溴代试剂不易获得,过量的溴代试剂对环境危害大,且对底物结构有要求。
技术实现要素:9.本发明的目的在于,针对现有三(4-乙炔基苯基)胺的制备方法存在工艺条件复杂、生产成本较高、环境危害大等问题,提出一种由三苯胺制备三(4-乙炔基苯基)胺的方法,该方法操作简单安全、原料价廉易得、生产成本低、三废排放少、易于实现三(4-乙炔基苯基)胺的产业化。
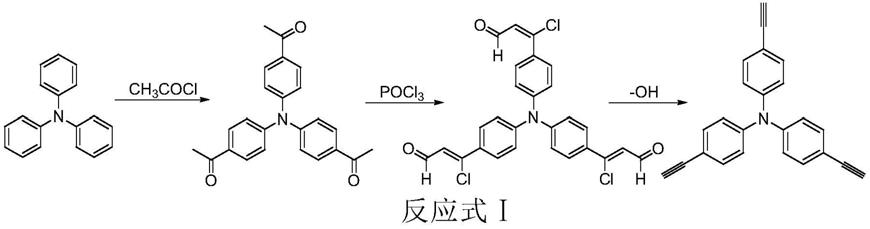
10.为实现上述目的,本发明采用的技术方案是:一种由三苯胺制备三(4-乙炔基苯基)胺的方法,包括以下步骤:
11.(1)以三苯胺为原料,在lewis催化剂的催化下,滴入乙酰氯,酰基化反应后过滤除去固体催化剂,得到三(4-乙酰基苯基)胺;
12.(2)将三(4-乙酰基苯基)胺溶解在非极性溶剂中,在0~30℃下滴加vilsmeier试剂,升温反应后,倒入冰水静置10~24h,过滤得三(4-(3-氯烯丙基醛基)苯基)胺;
13.(3)三(4-(3-氯烯丙基醛基)苯基)胺在碱性条件下消除得到三(4-乙炔基苯基)胺。
14.反应路线如下:
[0015][0016]
三(4-乙炔基苯基)胺的结构如结构式1所示,其特征是与n原子连接的苯环上对位有乙炔基基团:
[0017][0018]
进一步地,步骤(1)的具体步骤为将三苯胺、lewis催化剂和有机溶剂加入装有机械搅拌,回流冷凝管和温度计的容器(如三口烧瓶)中,搅拌下滴入乙酰氯;控制温度0~30℃温度,搅拌反应10-24h,过滤除去固体催化剂,有机层水洗至中性,无水硫酸钠干燥,减压蒸出溶剂即得淡黄色的三(4-乙酰基苯基)胺。
[0019]
进一步地,所述lewis催化剂为三氯化铝、三氯化铁、氯化铜、氯化亚铜、四氯化锡、氯化锌和三氯化硼中的一种或多种的混合。优选的lewis催化剂为三氯化铝。
[0020]
进一步地,所述有机溶剂为二氯甲烷、1,2-二氯乙烷、三氯甲烷和四氯化碳中的一种或几种的混合。
[0021]
进一步地,步骤(1)所述三苯胺、lewis催化剂、乙酰氯的物质量比为1:3~3.6:3~3.3;所述有机溶剂用量为三苯胺的物质量为0.5~1ml/mol。
[0022]
进一步地,步骤(2)的具体步骤为:室温下将三(4-乙酰基苯基)胺溶于非极性溶剂中,搅拌溶解后,冰水浴冷却15min以上,在0~30℃下滴加vilsmeier试剂,滴加完后升温至40~80℃,反应5~10h,倒入冰水中静置10~24h,过滤,烘干后得黄色三(4-(3-氯烯丙基醛基)苯基)胺。
[0023]
进一步地,所述非极性溶剂为二甲基亚砜、n,n
’‑
二甲基甲酰胺、n,n
’‑
二甲基乙酰胺和n-甲基吡喏烷酮中的一种或多种的混合。优选的溶剂为二甲基亚砜和/或n,n
’‑
二甲基甲酰胺。
[0024]
进一步地,步骤(3)的具体步骤为:在容器(如三口烧瓶)中加入三(4-(3-氯烯丙基醛基)苯基)胺、有机溶剂和碱,升温至回流,搅拌反应2~10h,反应完成后倒入去离子水中,用乙醚萃取三次;有机层经饱和食盐水洗涤,无水硫酸钠干燥,过滤,蒸出溶剂得粗产品;以石油醚/乙酸乙酯=10:1为淋洗液进行柱层析分离提取,制备得到三(4-乙炔基苯基)胺。
[0025]
进一步地,步骤(3)所述有机溶剂为甲醇、乙醇、丙醇、异丙醇和叔丁醇中的一种或几种的混合;所述碱为无机碱axby。其中a为li
+
、na
+
、k
+
、cs
+
等中任一种;b=co
32-、hco
3-、hso
3-、hcoo-、ch3coo-、(ch3)3co-、f-等中任一种。优选的碱为naoh、koh、cs2co3或(ch3)3cok。
[0026]
进一步地,所述三(4-(3-氯烯丙基醛基)苯基)胺与碱的摩尔比为1:3~5;所述有机溶剂的用量以三(4-(3-氯烯丙基醛基)苯基)胺物质的量计为1~4ml/mmol。
[0027]
本发明由三苯胺制备三(4-乙炔基苯基)胺的方法,与现有技术相比较具有以下优点:
[0028]
本发明以廉价易得的三苯胺化合物为原料,使用化学性质稳定的无机碱做消除试剂,与现有合成方法相比,本发明所用原料和试剂都很容易获得,无需使用价格昂贵的炔基化试剂、金属催化剂和对环境有危害的溴代试剂。本发明方法工艺路线简单,反应条件温和,易于控制,三废排放少、易于实现三(4-乙炔基苯基)胺的产业化。
附图说明
[0029]
图1为实施例1三(4-乙酰基苯基)胺的核磁谱图;
[0030]
图2为实施例1三(4-(3-氯烯丙基醛基)苯基)胺的核磁谱图;
[0031]
图3为实施例1三(4-乙炔基苯基)胺的核磁谱图。
具体实施方式
[0032]
以下结合实施例对本发明进一步说明:
[0033]
实施例1
[0034]
在装有机械搅拌,回流冷凝管和温度计的100ml三口烧瓶中依次加入2.45g(0.01mol)三苯胺,4g(0.03mol)三氯化铝和20ml二氯甲烷,搅拌下滴入2.59g(0.033mol)乙酰氯。滴加过程中控制温度小于30℃温度,搅拌反应10-24h。反应完成后,过滤除去固体催化剂,有机层水洗至中性,无水硫酸钠干燥,减压蒸出溶剂即得淡黄色的三(4-乙酰基苯基)胺,产率86%。
[0035]
室温下,将3.71g(0.01mol)三(4-乙酰基苯基)胺溶于20mln,n
’‑
二甲基甲酰胺中,
搅拌溶解后,冰水浴冷却15min以上,于0℃滴加4.2g(0.045mol)vilsmeier试剂,滴加完后升温至40~80℃,反应5~10h,倒入冰水中,调节ph至中性,过滤,烘干后得黄色三(4-(3-氯烯丙基醛基)苯基)胺。
[0036]
在100ml三口烧瓶中加入5.1g(0.03mol)三(4-(3-氯烯丙基醛基)苯基)胺,30ml乙醇和1.2g(0.03mol)naoh,升温至回流,搅拌反应2~10h,反应完成后倒入去离子水中,用乙醚萃取。有机层经饱和食盐水洗涤,无水硫酸钠干燥,过滤,蒸出溶剂得粗产品。以石油醚/乙酸乙酯=10:1为淋洗液进行柱层析分离提取即得三(4-乙炔基苯基)胺,收率60%。
[0037]
图1为实施例1三(4-乙酰基苯基)胺的核磁谱图;图2为实施例1三(4-(3-氯烯丙基醛基)苯基)胺的核磁谱图;图3为实施例1三(4-乙炔基苯基)胺的核磁谱图。由图1-3所示,在图1的核磁氢谱中可以发现在2.78ppm处出现了乙酰基上甲基氢的化学位移,表明酰基化成功。图2中在10.2ppm处出现了醛基氢的化学位移,6.82ppm处为烯丙基中氢的化学位移,说明乙酰基已经转变成3-氯烯丙基醛基。图3中,10.2ppm处的醛基氢和6.82ppm处烯丙基的氢峰都消失不见了,而在3.05ppm处出现了端炔基氢的峰,证明三苯胺上3-氯烯丙基醛基在碱性条件下消除得到了端炔基。
[0038]
实施例2
[0039]
在装有机械搅拌,回流冷凝管和温度计的100ml三口烧瓶中依次加入4g(0.03mol)三氯化铝、2.59g(0.033mol)乙酰氯和10ml二氯甲烷,将2.45g(0.01mol)三苯胺溶于10ml二氯甲烷,搅拌下滴入三苯胺溶液。滴加过程中控制温度小于30℃温度,搅拌反应10-24h。反应完成后,过滤除去固体催化剂,有机层水洗至中性,无水硫酸钠干燥,减压蒸出溶剂即得淡黄色的三(4-乙酰基苯基)胺,产率80%。
[0040]
室温下,3.71g(0.01mol)三(4-乙酰基苯基)胺溶于20mln,n
’‑
二甲基甲酰胺中,搅拌溶解后,冰水浴冷却15min以上,于0℃滴加4.2g(0.045mol)vilsmeier试剂,滴加完后升温至40~80℃,反应5~10h,倒入冰水中,调节ph至中性,过滤,烘干后得黄色三(4-(3-氯烯丙基醛基)苯基)胺。
[0041]
在100ml三口烧瓶中加入5.1g(0.03mol)三(4-(3-氯烯丙基醛基)苯基)胺,30ml乙醇和1.2g(0.03mol)naoh,升温至回流,搅拌反应2~10h,反应完成后倒入去离子水中,用乙醚萃取。有机层经饱和食盐水洗涤,无水硫酸钠干燥,过滤,蒸出溶剂得粗产品。以石油醚/乙酸乙酯=10:1为淋洗液进行柱层析分离提取即得目标产物,收率60%。
[0042]
实施例3
[0043]
在装有机械搅拌,回流冷凝管和温度计的100ml三口烧瓶中依次加入2.45g(0.01mol)三苯胺,4.08g(0.03mol)氯化锌和20ml二氯甲烷,搅拌下滴入2.59g(0.033mol)乙酰氯。滴加过程中控制温度小于30℃温度,搅拌反应10-24h。反应完成后,过滤除去固体催化剂,有机层水洗至中性,无水硫酸钠干燥,减压蒸出溶剂即得淡黄色的三(4-乙酰基苯基)胺,产率88%。
[0044]
室温下,3.71g(0.01mol)三(4-乙酰基苯基)胺溶于20mln,n
’‑
二甲基甲酰胺中,搅拌溶解后,冰水浴冷却15min以上,于0℃滴加4.2g(0.045mol)vilsmeier试剂,滴加完后升温至40~80℃,反应5~10h,倒入冰水中,调节ph至中性,过滤,烘干后得黄色三(4-(3-氯烯丙基醛基)苯基)胺。
[0045]
在100ml三口烧瓶中加入5.1g(0.03mol)三(4-(3-氯烯丙基醛基)苯基)胺,30ml乙
醇和1.68g(0.03mol)koh,升温至回流,搅拌反应2~10h,反应完成后倒入去离子水中,用乙醚萃取。有机层经饱和食盐水洗涤,无水硫酸钠干燥,过滤,蒸出溶剂得粗产品。以石油醚/乙酸乙酯=10:1为淋洗液进行柱层析分离提取即得目标产物,收率66%。
[0046]
实施例4
[0047]
在装有机械搅拌,回流冷凝管和温度计的100ml三口烧瓶中依次加入2.45g(0.01mol)三苯胺,2g(0.015mol)三氯化铝、2.04g(0.015mol)氯化锌和20ml二氯甲烷,搅拌下滴入2.59g(0.033mol)乙酰氯。滴加过程中控制温度小于30℃温度,搅拌反应10-24h。反应完成后,过滤除去固体催化剂,有机层水洗至中性,无水硫酸钠干燥,减压蒸出溶剂即得淡黄色的三(4-乙酰基苯基)胺,产率80%。
[0048]
室温下,3.71g(0.01mol)三(4-乙酰基苯基)胺溶于20mln,n
’‑
二甲基甲酰胺中,搅拌溶解后,冰水浴冷却15min以上,于0℃滴加4.2g(0.045mol)vilsmeier试剂,滴加完后升温至40~80℃,反应5~10h,倒入冰水中,调节ph至中性,过滤,烘干后得黄色三(4-(3-氯烯丙基醛基)苯基)胺。
[0049]
在100ml三口烧瓶中加入5.1g(0.03mol)三(4-(3-氯烯丙基醛基)苯基)胺,30ml甲醇和9.78g(0.03mol)cs2co3,升温至回流,搅拌反应2~10h,反应完成后倒入去离子水中,用乙醚萃取。有机层经饱和食盐水洗涤,无水硫酸钠干燥,过滤,蒸出溶剂得粗产品。以石油醚/乙酸乙酯=10:1为淋洗液进行柱层析分离提取即得目标产物,收率46%。
[0050]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
